
О зависимости коэффициента активности от концентрации
.pdf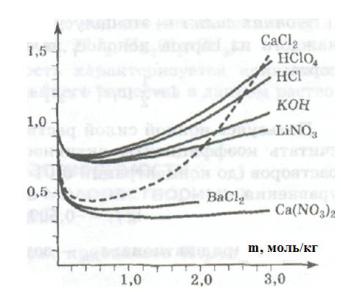
В бесконечно разбавленных водных растворах неэлектролитов коэффициент активности равен единице. Опыт показывает, что по мере увеличения концентрации электролита величины ± уменьшаются, проходят через минимум, а затем снова увеличиваются и становятся существенно больше единицы в крепких растворах.
±
Такой ход зависимости ± от концентрации определяется двумя физическими явлениями.
Первое особенно сильно проявляется при малых концентрациях и обусловлено электростатическим притяжением между противоположно заряженными ионами. Силы притяжения между ионами преобладают над силами отталкивания, т.е. в растворе устанавливается ближний порядок, при котором каждый ион окружен ионами противоположного знака. Следствием этого является усиление связи с раствором, что находит отражение в уменьшении коэффициента активности.
Естественно, что взаимодействие между ионами возрастает при увеличении их зарядов. При возрастании концентрации все большее влияние на активность электролитов оказывает второе явление, которое обусловлено взаимодействием между ионами и молекулами воды (гидратацией). При этом в относительно концентрированных растворах количество воды становится недостаточным для всех ионов и начинается постепенная дегидратация, т.е. связь ионов с раствором уменьшается, следовательно, увеличиваются коэффициенты активности. Стоит отметить, что при некоторой концентрации силы притяжения и силы отталкивания уравновешивают друг друга, и можно сказать, что приблизительно отсутствуют взаимодействия между ионами и коэффициент активности снова становится равным единицы.
