
к экзамену последний семестр / ответики
.docxУксусная кислота при температуре 700С разлагается одновременно по двум направлениям: Период полураспада кислоты не зависит от начальной концентрации и равен 0,087с. Отношение числа молей обр метана и кетена в любой момент времени равно 0,8. Рассчитайте значение конст скорости первой стадии.
Ответ: К1=3,5; К2=4,5
Выберите выражение для полной акт сильного электролита Na2SO4 как компонента водного раствора с моляльностью m.
Ответ: 4m^3y^3
Константа скорости некоторой реакции при 9,4С равно 2,37 л*моль-1*мин-1, а при 14,4С равно с*моль-1*мин-1. Найдите Еа реакции.
Ответ: 41 кДж/моль
Пользуясь справочными данными, рассчитайте средний ионный коэффициент активности в децимоляльном водном растворе CdCl2,
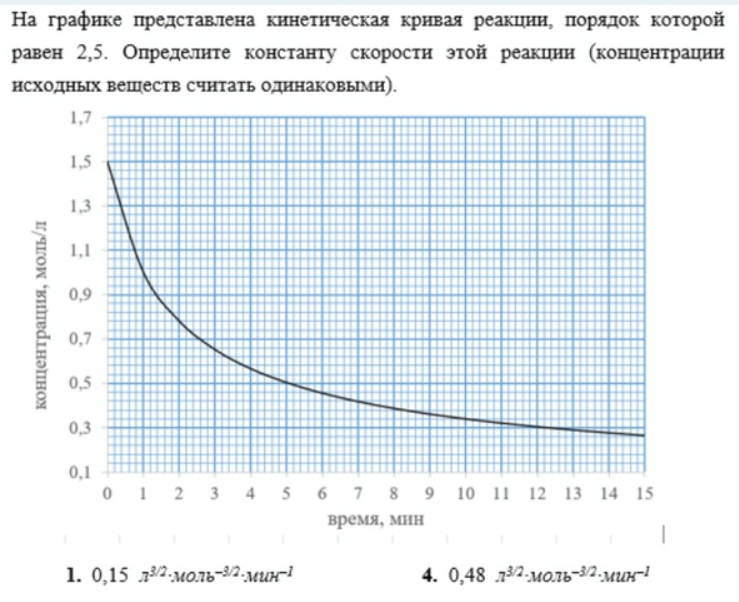
На графике представлена кинетическая кривая реакции, порядок которой равен 2,5. Определите константу скорости этой реакции (конц исх в-в считать одинаковыми). Ответ: 0,3
Выразите в общем виде константу диссоциации слабой кислоты Н2А через степень диссоциации а и молярную концентрацию электролита с.
Ответ: Кд= (4а^3c^2)/(1-а)
Может ли квантовый выход фотохимической реакции быть >1? И, если да, то при каких условиях протекания реакции?
Ответ: Может, если в первичном ф/х процессе возникают частицы со свободной валентностью (атомы или радикалы).
При 293К измена удельная электрическая проводимость водных растворов сильного бинарного электролита при следующих конц:
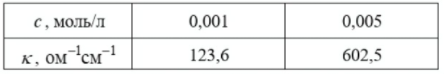
Определите морярную электрическую проводимость электролита при бесконечном разведени.
Ответ: 126,2*10^(-4)
Укажите правильную схему записи электрохимической цепи без переноса с учетом правила знаков ЭДС и электронных потенциалов.

Вычислите
ЭДС элемента при 25С, используя справочные
данные:
![]()
Ответ: 0,0146В
Какой электрод можно использовать в качестве электрода сравнения при измерении ЭДС электрохимической цепи?
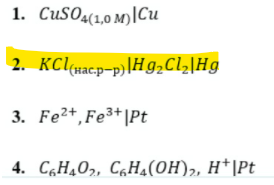
Сравнивания ряд реакций с различными величинами энергии активации Еа и температурного коэффициента Вант-Гоффа y. Для каких реакций скорость изменяется более резко с повышением температуры?
Ответ: для реакций, у которых Еа меньше
Радиус ионной атмосферы зависит от ионной силы раствора, температуры, диэлектричекой проницаемости среды, и не зависит от степени диссоциации.
В обратимой реакции скорости прямой и обратной реакции соответственно равны 4,5мин-1 и 1,5мин-1. В момент начала реакции система содержит только вещество А. За какое время его конц уменьшится в 2 раза.
Ответ: 0,183 мин
Для некоторой реакции первого порядка период полупревращения при 25С равен 104ч, а при 35С равен 39ч. Определите температурный коэффициент Вант-Гоффа.
Ответ: 2,7
Пользуясь справочными данными, определить ля раствора FeCl2 с концентрацией 1,0 моль/кг среднюю ионную активность при 298К.
Ответ: 0,810
При 504С ацетон разлагается в газовой фазе по реакции
CH3COCH3=C2H4 +CO+H2
Констана скорости этой реакции равна 4,27*10^(-4)с-1. Рассчитайте, чему будет равно парциальное давление ацетона через 1200с от начала опыта, если начальное давление было равно 1 атм.
Ответ: 0,6атм
Какова должна быть площадь электродов, расположенных на расстоянии 1см друг от друга, чтобы электрическая проводимость раствора электролита с концентрацией 0,2 моль/л, помещенного в измерительную электрохимическую ячейку, отвечала молярной электрической проводимости этого электролита.
Ответ: 5*10^(-3) м^2
При
изучении зависимости начальной скорости
распада ацетальдегида от начального
давления быи получены данные, представленные
в виде графика. Найдите порядок реакции.
 Ответ:
1,5
Ответ:
1,5
Температурный коэффициент Вант-Гоффа некоторой реакции равен 3. При 20С реакция заканчивается за два часа. При какой температуре она закончится за 25 минут?
Ответ: 34С
Определите средний ионный коэффициент активности сульфата меди (m=0,0005моль/кг), если в растворе также присутствует нитрат калия (m=0,0025моль/кг). Температура составляет 298К.
Ответ: 0,73
Удельная электропроводность водного раствора некоторой одноосновной кислоты с разведением 1024 л/моль составляет 4,23 мСм/м. Определите константу диссоциации данной кислоты, если ее электропроводность при бесконечном разведении составляет 385,6 См*см2/моль.
Ответ: 1,4*10^(-5) моль/л
