
семинары / Семинар 4
.docОХТ, семинар 4
Кинетика химических превращений
Скорость превращения вещества (Wi) - количество i-го вещества, которое превращается в единице реакционного пространства в единицу времени. Для закрытой системы, концентрации веществ изменяются во времени, можно написать:
 если
V= const,
тогда
если
V= const,
тогда
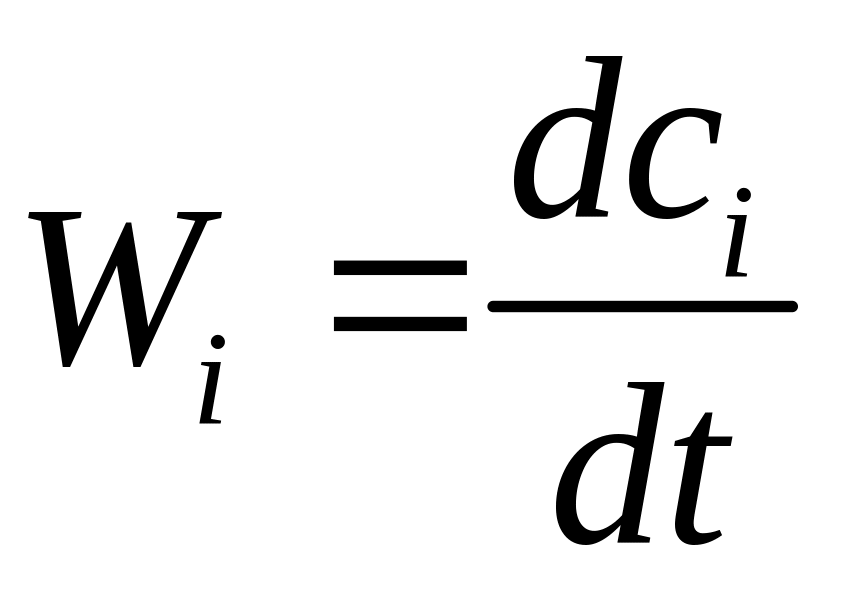 ,
,
Если вещество расходуется, то Wi<0, если образуется Wi>0.
Так как количества веществ, участвующих в реакции
nAA + nBB + ... ® nRR + nSS + ...
связаны между собой стехиометрическими соотношениями, то скорости их превращения находятся в зависимости:
WA/n A = WB/nB = WR/nR = WS/nS = const = r,
где r определим как скорость химической реакции.
Скорость превращения i-го вещества в простой реакции Wi = i r
в сложной реакции Wi = Snij rj , где rj - скорость j-й частной реакции.
Кинетическое уравнение - функциональная зависимость скорости реакции или скорости превращения вещества от условий ее протекания (концентрации реагентов, температуры, давления)
r = r (T, с) = k (T) f (с)
где k - константа скорости реакции, зависящая только от температуры.
Зависимость k = f(T) определяется уравнением Аррениуса:
k =
k0×![]()
Вид зависимости r(T,с) зависит от типа и механизма реакции. Размерность k определяется видом функциональной зависимости f(c) и размерностью r.
Скорость обратимой реакции
nАА
+ nВВ![]() nRR
+ nSS
nRR
+ nSS
записывается в виде разности скоростей прямой r1 и обратной реакций r-1:
r = r1 - r-1 = k1(T) × f1(c) – k-1(T)× f2 (c) = k1(T)× f1 (c)×[1 - j (c)/ Kр],
где
j
(c)=
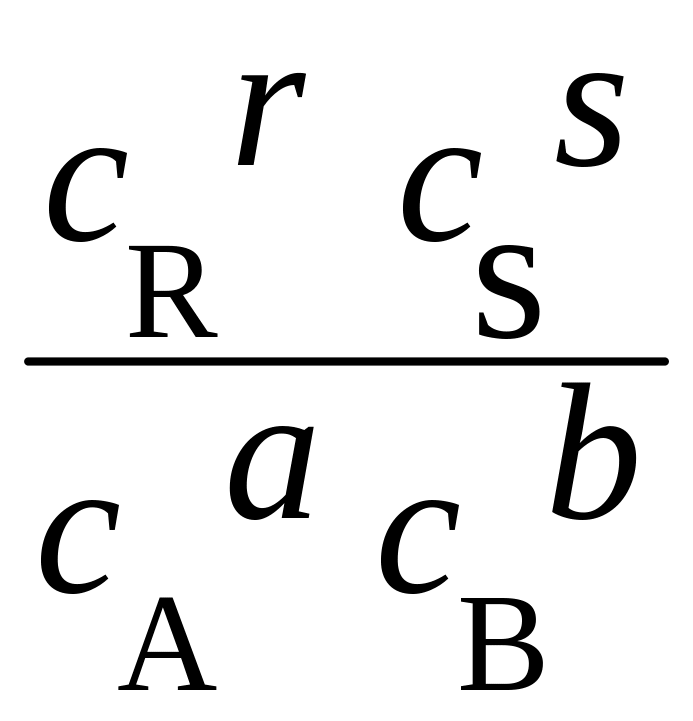 ,
Kр
=
,
Kр
=
![]()
Показатели степеней a, b, r и s при концентрациях исходных веществ и продуктов называются порядками реакции по отношению к данному реагенту. Обычно порядок реакции определяют экспериментально, поэтому он может не совпадать со стехиометрическим коэффициентом.
В частном случае,
для обратимой реакции первого порядка
А
![]() R скорость
реакции r
= k1сА
-
k-1сR
и скорость
превращения, например,
для вещества А:
R скорость
реакции r
= k1сА
-
k-1сR
и скорость
превращения, например,
для вещества А:

где сА= сА0(1-х) и сR= сА0х.
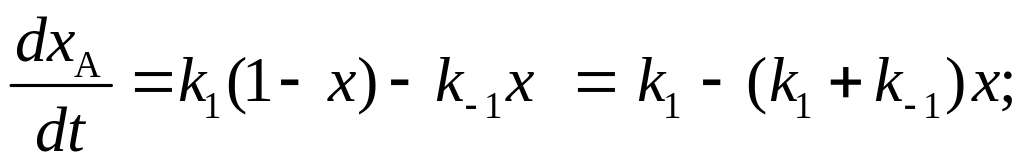
п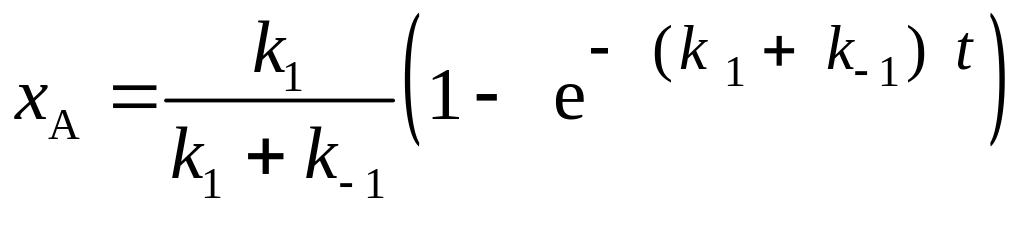 ри
t =
0 х =
0. После интегрирования получим:
ри
t =
0 х =
0. После интегрирования получим:
Параллельные реакции:
k1 k2
А ® R; A ® S;
Скорости превращения веществ (пусть обе реакции 1-го порядка):
WA = dсA/dt = -(k1+ k2 )сA, WR = dсR/dt = k1сA, WS= dсS/dt = k2сA
п
П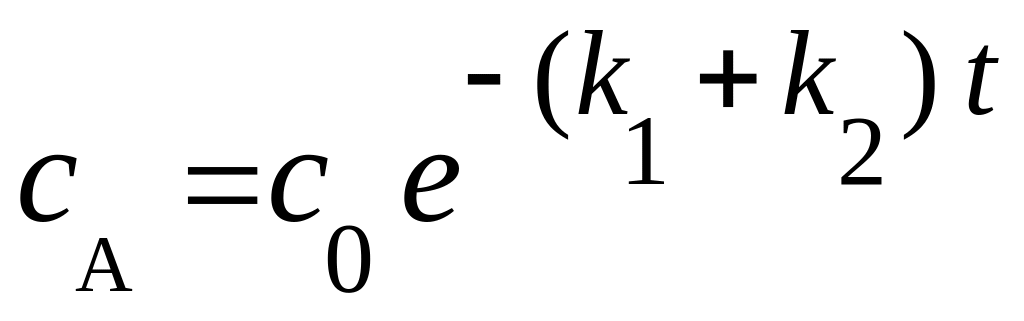
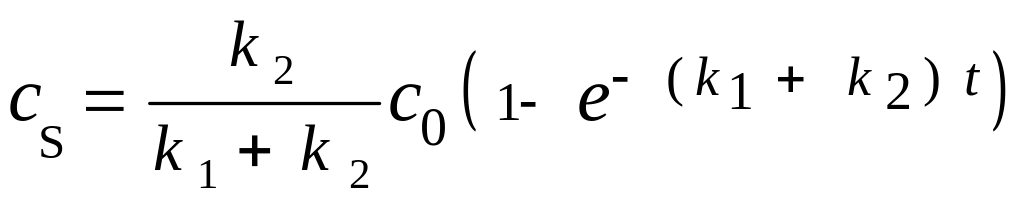
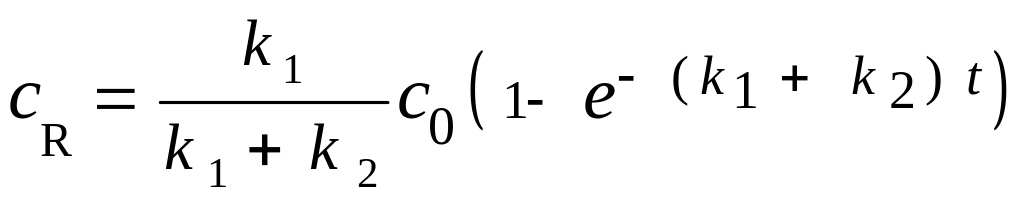 оследовательные
реакции 1-го порядка:
оследовательные
реакции 1-го порядка:
k1 k2
А ® R; R ® S;
Скорости превращения: WA= dсA/dt= -k1сA ,
WR= dсR/dt=k1сA - k2сR, WS = dсS/dt = k2сR; при t = 0: сA = со и сR = сS = 0.
П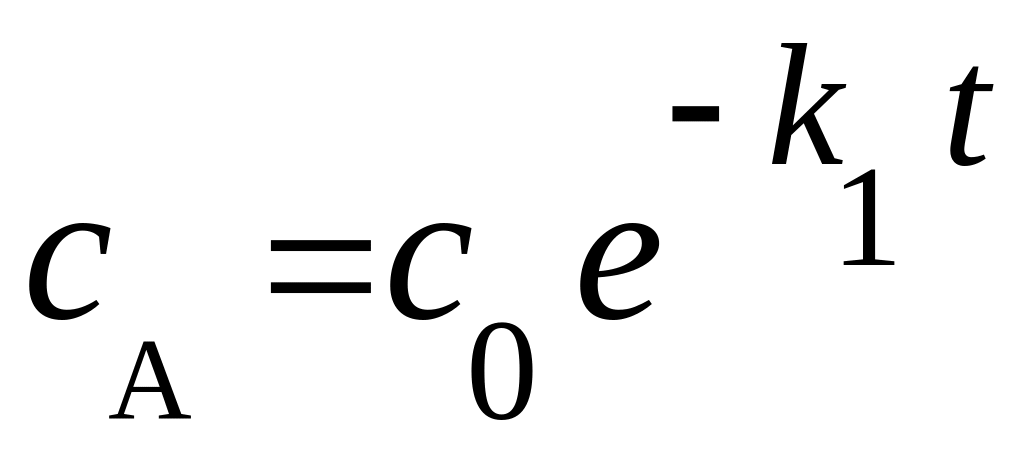 осле
интегрирования уравнений найдем:
осле
интегрирования уравнений найдем:
сS
=
с0
-
сA
-
сR
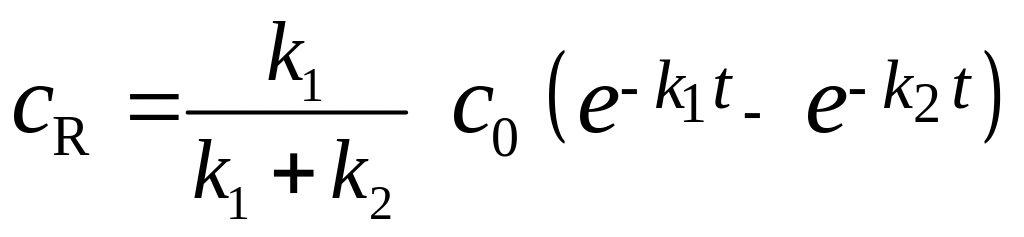
Для определения максимальной концентрации целевого продукта R необходимо взять производную dсR/dt и приравнять её 0.
Получим координаты точки максимума:
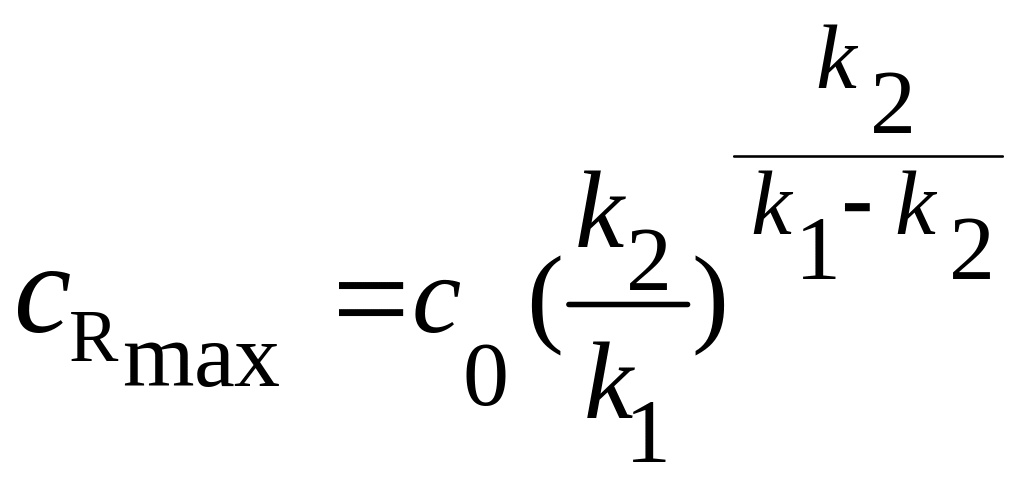

Дифференциальная селективность по продукту (SR¢) - отношение скорости превращения исходного вещества в заданный продукт (WA→R) к общей скорости превращения исходного вещества по всем направлениям (WA):
SR'
=
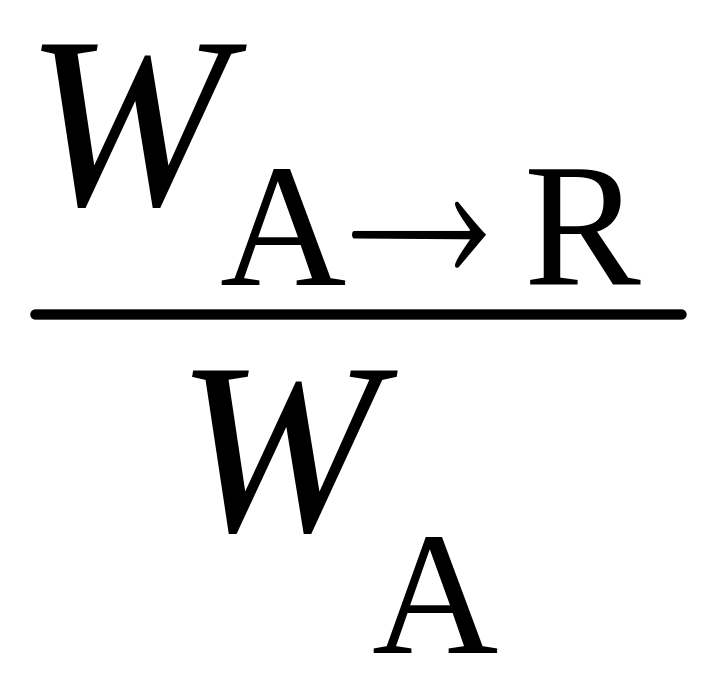 или SR'
=
или SR'
=
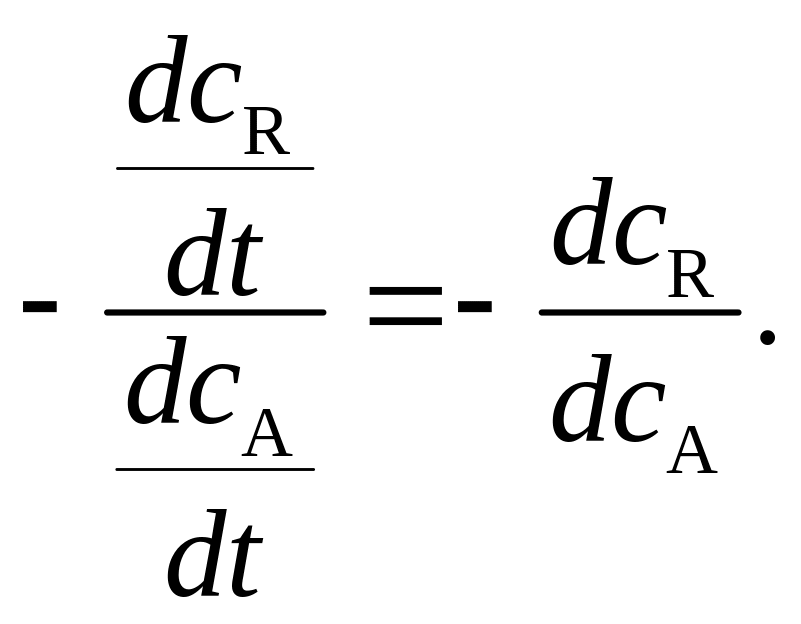
откуда
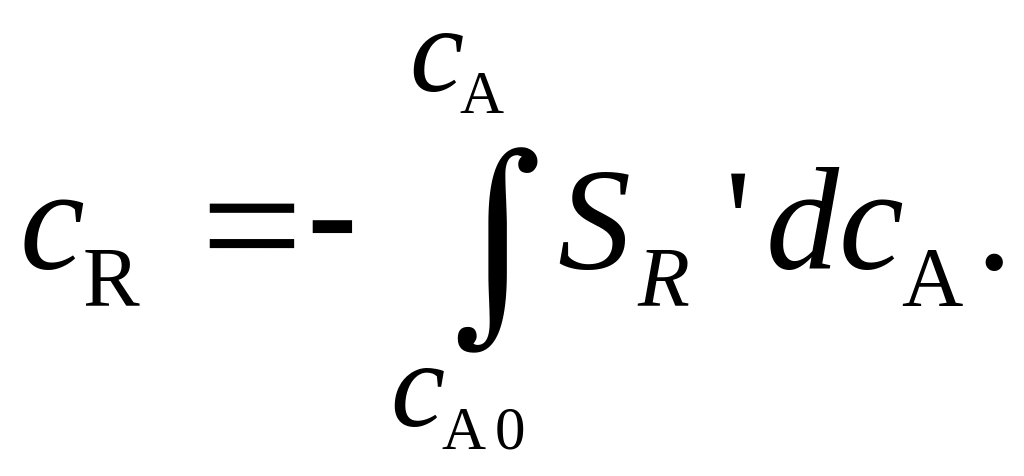
Связь между интегральной и дифференциальной селективностями:
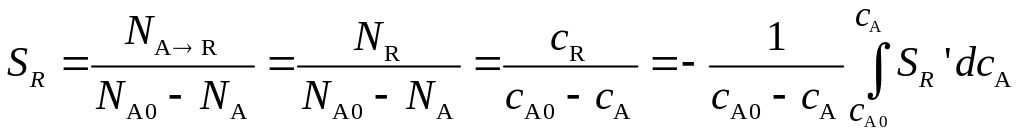
Для простой реакции SR = SR¢= 1.
Пример 1. Протекает химическая реакция вида 2А + 3В → S + 4R + 2F. Известно, что скорость по компоненту А составляет 5 моль/(л∙с). Определить скорости по остальным компонентам.
Wi= ir
WA = -2r = -5; r = 2,5 моль/(л∙с);
WB = -3r = -3 2,5 = -7,5 моль/(л∙с);
WR = 4r = 4∙2,5 = 10 моль/(л∙с);
WS = r = 2,5 моль/(л∙с);
WF = 2r = 2∙2,5 =5 моль/(л∙с).
Пример 2. Константа скорости реакции А → R равна 0,025 с-1. Исходная концентрация реагента составляет 1 кмоль/м3. Определить значения скорости реакции, протекающей в замкнутом объеме через 10, 30, 50 c.
Решение.
Размерность константы скорости «обратное
время» указывает на то, что реакция 1-го
порядка: WA
=
![]() = Аr
= –kсА
или
= Аr
= –kсА
или
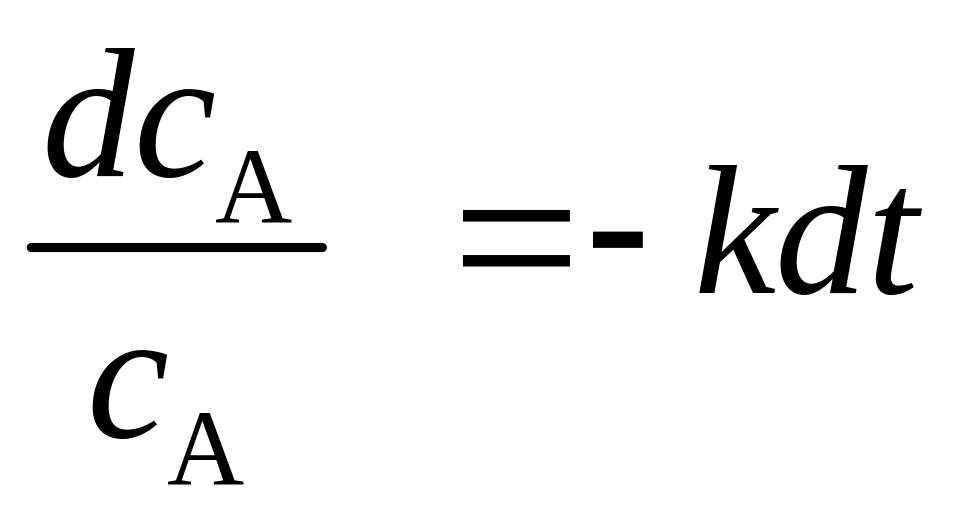
и далее сА= сА,0 е-kt.
t, с |
10 |
30 |
50 |
сА, кмоль/м3 |
0,78 |
0,47 |
0,29 |
102 r, кмоль/(м3с) |
1,95 |
1,18 |
0,73 |
Пример 3. В реакторе протекает сложная реакция в жидкой фазе: А = R,
R + 2B = S. сАо =1,8; сВо =1,5; сRо= сSо = 0; Текущие концентрации сА = 0,40;
сs = 0,3 кмоль/м3. Константы скоростей отдельных реакций равны k1 =3,8·10-2 с-1, k2 = 2,2·10-2 л/(моль.с). Определить скорости превращения по всем компонентам для текущих концентраций
Решение. WA = –k1сА ; WB = –2k2сR сВ; WR = k1сА – k2сRсВ; WS= k2сR сB.
сВ и сR? При переходе к более удобной для расчета системе двух уравнений:
А = R и А + 2В = S легко видно, что сАо– сА = сR + сS тогда сR= 1,8– 04 – 0,3 = 1,1 кмоль/м3. cВо– сВ= 2сS и сВ= 1,2 кмоль/м3. WA = ?WB =? WR =? WS=?
Пример 4. При постоянной температуре протекают две параллельные реакции:
k1 k2
А ® R; A ® S;
с константами скоростей k1 = 10– 2 c–1 и k2 = 10-1 c–1. Перед началом реакции
сА,0 = 3 кмоль/м3, сR,0= сS,0 = 0. Определить скорость и степень превращения реагента А, а также селективность по продукту R в момент времени, равный
30 с.
Решение. Скорость превращения А:
WA = –dсA/dt = (k1+ k2 )сA = (k1+ k2 )сA,0e – (k1+ k2) t = 0,32 кмоль/(м3.с);
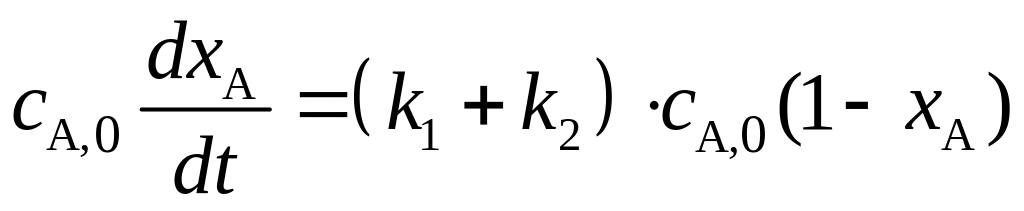
![]() =
0,28.
=
0,28.
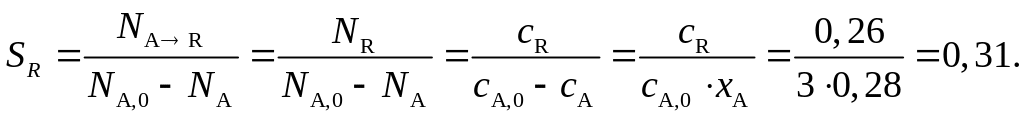
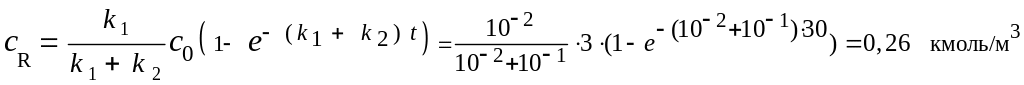
Пример 5. При какой температуре должны протекать реакции А = 2R(1) и
A = 3S(2), чтобы на образование 2 молей продукта R получить 1 моль S, если
к1 = 106 ехр (–45000/RT) c-1, к2 = 105 ехр (–20000/RT) c-1.

ДЗ
1) Для двух параллельных реакций
k1 k2
А ® 2R и A ® S
с константами скоростей к1 =0,01 с-1 и к2 = 0,03 с-1 определить время, при котором в продуктах будет содержаться 0,7 кмоль/м3 вещества S. Перед началом реакции концентрация вещества А была 2,2 кмоль/м3, а вещества R и S отсутствовали. Найти также селективность по веществу R.
2)
Для двух параллельных реакций А®R(1)
и А®2D(2),
константы скоростей
к1 =
6.
1013×exp
(–![]() )
с-1
и к2
= 3,7.
1013×exp
(–
)
с-1
и к2
= 3,7.
1013×exp
(–![]() )
с-1.
Какова должна быть температура, при
которой на образование двух молей R
образуется 0,5 моля продукта D.
Перед началом реакции вещества R
и D
отсутствовали.
)
с-1.
Какова должна быть температура, при
которой на образование двух молей R
образуется 0,5 моля продукта D.
Перед началом реакции вещества R
и D
отсутствовали.
