
лекции / Лекция-15 Аммиак
.pdfОХТ лекция 15
ХТС производства аммиака
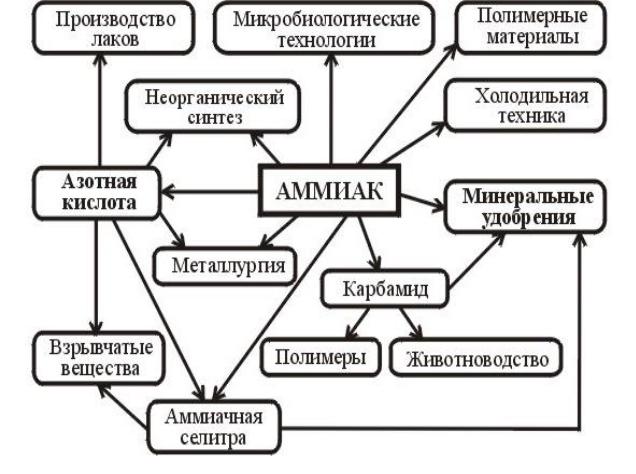
Применение NH3

ПРОИЗВОДСТВО АММИАКА
Химическая схема
включает следующие реакции:
•паровая конверсия метана CH4 + H2O CO + 3H2-Qр;
•воздушная конверсия метана СН4 +1/2О2 →СО + Н2+ Qp
•конверсия оксида углерода СО + H2O |
CO2 + H2 +Qр; |
|
•синтез аммиака |
N2 + 3H2 |
2NH3 +Qр . |
Все реакции каталитические.
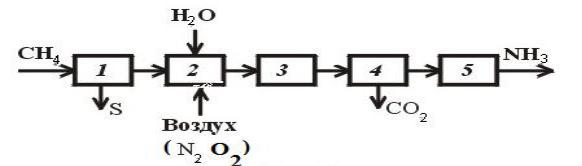
Функциональная схема производства
1- очистка природного газа от серосодержащих соединений, которые являются каталитическими ядами, 2-паровая и воздушная конверсия природного газа, 3-конверсия СО,
4-очистка азотоводородной смеси от оксидов углерода,
5-синтез аммиака.
Очистка природного газа от серосодержащих соединений
Природный газ содержит примеси серосодержащих соединений - меркаптаны (RSH), сероуглерод (CS2), сульфиды (R2S), сероводород (H2S) и др. Кроме того, газ одорируют - добавляют этилмеркаптан, обладающий сильным запахом- в целях безопасности. Содержание серы не велико, в среднем - несколько десятков мг/м3. Но сера в любом виде отравляет катализаторы, используемые в производстве аммиака. Ее содержание не должно превышать 0,5 мг S/м3.
Есть эффективный способ очистки –сорбционной, сорбент на основе оксида цинка. Но он поглощает в основном сероводород. Поэтому все серосодержащие соединения сначала "приводят" в одно состояние - их гидрируют до сероводорода:
RSH + H2 = H2S + RH; C4H4S + 4H2 = H2S + C4H10; CS2 + 4H2 = 2H2S + CH4 и т.д.
Водород для гидрирования в составе азотоводородной смеси имеется в производстве аммиака.
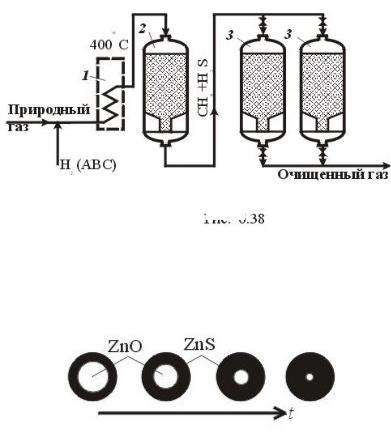
Выходящий из реактора гидрирования 2 газ содержит серу только в виде H2S и направляется в адсорбер, в котором и происходит собственно очистка газа. Технологическая схема сероочистки
показана на рис.1. 1
Поглотитель сероводорода - оксид цинка
ZnO:
ZnO + H2S = ZnS + H2O.
Процесс описывается моделью «сжимающееся» ядро. Лимитирующая стадия –внутренняя диффузия. Форма сорбента – полые цилиндры с тонкими стенками.

Конверсия природного газа
Физико-химические основы
Взаимодействие метана с водой протекает на катализаторе и представлено двумя обратимыми реакциями:
СН4 + Н2О СО + 3Н2 Q1; (1)
СО + Н2О СО2 + Н2 + Q2. (2)
Надо обеспечить наиболее полное превращение метана и температуру процесса целесообразно повышать. При этом равновесие второй реакции (1) сдвигается влево. При этом также возрастает скорость реакции. Доля реакции конверсии СО в общем процессе очень малая.
Вспомним : r (k1+k-1)С0(xp-x). Конверсия метана протекает с
увеличением объема, и поэтому низкое давление будет способствовать более полному превращению метана (с т.з. термодинамики). Однако для системы в целом выгоднее работать при повышенном давлении.
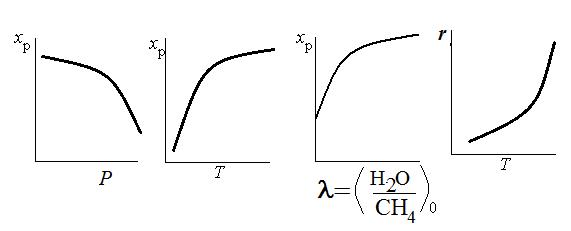
состав реакционной смеси
Негативное влияние давления на равновесие компенсируют избытком пара по отношению к стехиометрии. При давлении до 4
МПа избыток водяного пара ( = 4:1) позволит достичь почти
полного превращения: xр = 99%. Избыток H2O также предотвращает образование углерода на катализаторе.
Аппаратурное оформление конверсии метана
Конверсия метана - реакция эндотермическая: Необходимое подвести тепло так, чтобы разогреть слой катализатора. Вопрос, какой реактор взять как его расположить в реакторе, чтобы он прогревался всем объемом? Для этого используют трубчатый реактор или печь. Обогрев ведут через стенки реакционных труб, в которых находится катализатор. Чем обогревать, пара с такой температурой 900оС нет. Обогрев осуществляется с помощью дымовых газов путем сжигания природного газа в факельных инжекционных горелках. Температура, необходимая для полного превращения метана 1300 К, а металл, из которого сделаны трубки, допускает нагрев не выше 1180-1200 К. Максимальная температура в слое (на выходе) будет, естественно, ниже 1080-1100 К. Превращение метана не превышает 75% .
Необходима вторая ступень конверсии.
Она представлена адиабатическим реактором - шахтным конвертором. Стенки его внутри футерованы огнеупорным керамическим материалом - для предохранения корпуса от перегрева.
Необходимую температуру создают тем, что в реактор подают воздух. Часть метана сгорает в кислороде воздуха, и при этом температура повышается до 1230-1280 К.
Если в трубчатом реакторе тепло подводится за счет внешнего теплообмена, то в шахтном реакторе за счет внутреннего тепловыделения (экзотермической реакции).
