
- •Рас. 23. Схема почечного клубочка (Bargmann).
- •Воточного поворотного множителя
- •Состав некоторых веществ в плазме крови и в моче в процентах
- •Яичком и надпочечником (Nelson).
- •Количество микробов, обнаруживаемое в 1 и 10 полях зрения микроскопа
- •Зависимость количества колоний в различных секторах чашки Петри от интенсивности бактериурии
- •Артериографическая фаза в норме.
- •Метастазы рака мочевого пузыря в лимфатические узлы по ходу подвздошных сосудов (Alberti).
- •Жизни плода (Kelly- Burnam).
- •Транслюмбальная почечная ангиограмма. Артериографическая фаза.
- •Двусторонняя пиелограмма. Снимок сделан на одной пленке при вдохе и выдохе.
- •Почечная ангиограмма по Сельдингеру.
- •Рас. 149. Разрезы для вне-брюшного обнажения почки.
- •II. Опухоли почечной лоханки и мочеточника
- •Селективная почечная ангиограмма. Нефрографическая фаза.
- •Рас. 205. Этапы трансабдоминальной нефрэктомии.
- •Puс. 210. Рак стенки солитарной кисты почки.
- •Обзорная рентгенограмма (наблюдение в. Д. Грунд).
- •Нефрогенной гипертонии (см. Рис. 239).
- •Оглавление
- •Для заметок
Рас. 149. Разрезы для вне-брюшного обнажения почки.
а — Симона; б — Черни; в — Бергмана—Израэля; г — Пеана; 9 — Федорова.
Косые поясничные и косопоперечный пояснично-брюшной разрезы Федорова имеют следующие недостатки.
1. В процессе рассечения мышц можно легко пересечь XII межреберный нерв (п. intercostalis), который бывает виден у нижнего края XII ребра, и подвздошно-подчревный нерв (п. hypogastricus), идущий параллельно наружному краю квадратной поясничной мышцы. Перерезка этих нервов влечет за собой парезы косых и поперечной мышц живота с последующим образованием послеоперационных грыж. При разрезе Федорова опасность ранения подвздошно-подчревного нерва меньше. Возникновению послеоперационных грыж способствует также рассечение мышц передней брюшной стенки.
2. Имеется опасность вскрытия плевры при рассечении мышц в верхнезаднем участке, при пересечении подвздошно-реберной связки и резекции XII ребра, особенно если оно коротко.
3. Не виден верхний полюс почки при ее нормальном расположении и его приходится выделять на большой глубине без контроля глазом.
Для устранения первого недостатка при косых поясничных разрезах и разрезе Федорова вместо рассечения мышц применяют тупое разделение их по ходу волокон, избегая тем самым ранения крупных нервов и сосудов, по принципу перемежающегося межмышечного разреза (в „клетку"), предложенного еще в 1894 г. Н. М. Волковичем для аппендэктомии. При этом методе косые мышцы живота расслаивают в продольном, а поперечную — в поперечном направлении. Брюшину отодвигают тупо в медиальном направлении и вверх, после чего удается проникнуть в забрюшинное пространство к мочеточнику и почке. Послеоперационные грыжи наблюдаются при этом доступе очень редко. В различных модификациях межмышечный доступ к почке и мочеточнику нашел применение при операциях пиелолитотомии и главным образом уретеролитотомии.
Впервые межмышечный доступ к мочеточнику для удаления камня предложил в 1926 г. С. И. Спасокукоцкий. За последние годы (1949—1963) использовали этот разрез для удаления камней мочеточника С. А. Апа-кова, X. П. Блатной, П. И. Гельфер, А. Я. Пытель, М. Д. Джавад-Заде и др.
А. П. Фрумкин применил межмышечный доступ не только при уретеролитотомии, но и при пиелотомии для удаления одиночных камней лоханки. Использовали этот метод оперирования для доступа к почке И. И. Сабельников и В. В. Ившин, Lurz при pyelolithotomia in situ, Bosenstein и др. Для нефрэктомии и нефролитотомии, для удаления отростчатых и множественных камней почек этот доступ тесен и создает неоправданные трудности для хирурга. Вывести почку в рану при межмышечном разрезе в „клетку" невозможно. Пиелолитотомию производят in situ.
Используют межмышечный доступ к почке также через треугольник Грюнфельда—Лесгафта. Основоположником этой операции надо считать Simon, который еще в 1869 г. впервые в мире произвел 2 нефрэктомии через треугольник Грюнфельда—Лесгафта, произведя вертикальный разрез по наружному краю спинно-крестцовой мышцы. Различные варианты этого разреза сохранились и по настоящее время.
Г. С. Гребенщиков, Н. В. Куренной и В. Л. Ямпольский (1963) применили межмышечный доступ к почке через треугольник Грюнфельда—Лесгафта для удаления одиночных камней почечных лоханок. Они указывают на малую травматичность этого вида оперативного вмешательства, поскольку мышечные, нервные волокна и сосуды не пересекаются, почка в рану не вывихивается, вскрывается только позадипочечная жировая клетчатка и манипуляции на почке производятся вдали от брюшины.
Техника операции. Больного укладывают на живот. Верхняя половина живота находится на валике. Разрез длиной 8—10 см проводят от середины XII ребра косо книзу и медиально по направлению к углублению между гребешком подвздошной кости и разгибателем спины. После обнажения широкой мышцы спины, ее апоневроза и пояснично-спинной фасции волокна широкой мышцы спины расслаивают продольно, отодвигают в стороны и обнажают треугольник Грюнфельда—Лесгафта. Косые мышцы живота отодвигают латерально, а длинный разгибатель спины и задневерхнюю зубчатую мышцу (если она попадает в разрез) — медиально к позвоночнику, после чего в глубине виден апоневроз поперечной мышцы живота. Его расслаивают по ходу волокон, после чего открывают забрюшинное пространство, рассекая ретроренальную фасцию. Околопочечную жировую клетчатку отодвигают кверху и книзу и при обычном расположении почки обнажают ее нижний полюс и верхнюю часть мочеточника.
Описанный доступ также тесен и через него можно удалить только одиночные камни почек и фиксированные камни верхней трети мочеточника.
И. П. Погорелко (1957—1959) предложил следующие межмышечные доступы к почке: 1) задне-латеральный, 2) задне-медиальный, 3) задний косопоперечный с пересечением широкой мышцы спины, 4) передний.
При задне-латеральном доступе больной находится в положении на здоровом боку. Разрез кожи производят от конца XII ребра книзу по направлению к треугольнику Пти. Широкую мышцу спины и наружную косую мышцу живота тупо раздвигают в стороны. Образуется широкая межмышечная щель, в глубине которой видны волокна внутренней косой мышцы живота, отделяющей треугольник Грюнфельда — Лесгафта от треугольника Пти. Для проникновения в забрюшинное пространство раздвигают внутреннюю косую и затем в глубине поперечную мышцы живота. Тупо расширяют рану крючками. По вскрытии околопочечной жировой клетчатки и ретроренальной фасции обнажается наружный край почки.
При очевидных положительных сторонах задне-латеральный доступ, как это отмечает и сам автор, имеет крупный недостаток, заключающийся в узости операционной раны. Почка при этом доступе лежит глубоко и труднодостижима.
Большего внимания заслуживает задне-медиальный доступ. Больного укладывают на живот, подложив валик под верхнюю половину живота. Разрез кожи длиной 8—10 см проводят от середины XII ребра косо книзу и медиально по направлению к углублению между гребешком подвздошной кости и позвоночником. Обнажают широкую мышцу спины с ее апоневрозом и пояснично-спинной фасцией. Волокна широкой мышцы спины расслаивают продольно, отодвигают в стороны, обнажая место соприкосновения косых мышц живота и длинного сгибателя спины. Косые мышцы отодвигают латерально, длинный сгибатель спины и задневерхнюю зубчатую мышцы — медиально к позвоночнику. Показавшуюся поперечную мышцу живота с ее апоневрозом расслаивают тупо по ходу волокон, после чего становится доступным забрюшинное пространство. По вскрытии ретроренальной фасции под жировую капсулу почки подводят тупые крючки. Околопочечную клетчатку отодвигают вверх и вниз, после чего обнажается задняя поверхность почки с лоханкой и верхним отрезком мочеточника. При пиелолитотомии фиксируют мочеточник на резиновой держалке и освобождают лоханку от прилоханочной жировой ткани. После операции больной лежит на спине, и дренаж от почки выводят между двумя поперечно положенными матрацами, на которые укладывают больного.
Преимущества этой операции: малая травматичность, отсутствие послеоперационных грыж, хороший отток мочи по дренажу после операции.
И. П. Погорелко подчеркивает, что этот доступ предназначен главным образом для удаления одиночных камней почечных лоханок, но с его помощью можно произвести одномоментное удаление двусторонних камней почек и мочеточников, а также нефростомию, нефропексию и декапсуля-цию почек.
Для производства нефрэктомии и других оперативных вмешательств на почке у тучных больных И. П. Погорелко рекомендует задний косо-поперечный доступ с пересечением мышц при положении больного на животе. Как отмечает и сам автор способа, этот доступ в принципе ничем не отличается от обычных косых доступов с пересечением мышц. Поэтому мы этот доступ описывать не будем. Преимущество косопоперечного доступа в том, что благодаря положению больного на животе почка ближе подходит к ране, это облегчает извлечение из почки камня.
Задний косопоперечный доступ к почке с пересечением мышц при положении больного на животе уступает обычным пояснично-косым доступам или доступу по Федорову и заменить их не может. Само положение больного на животе на валике в течение операции менее выгодно для больного и для ведения наркоза. Это тяжело отражается на сердечной и легочной деятельности, поскольку полностью выключается брюшной пресс и значительно ограничивается экскурсия легких в процессе дыхания. Широта доступа меньше, чем при обычных косых и косопоперечных разрезах.
Передний межмышечный доступ И. П. Погорелко рекомендует при почечных аномалиях, в частности при подковообразной почке. Производят его следующим образом: кожу разрезают от конца XII ребра косо вниз кпереди длиной 8—10 см. Волокна наружной косой мышцы живота тупо расслаивают вдоль. Также расслаивают и раздвигают волокна внутренней косой мышцы живота на протяжении 6—7 см, после чего видны волокна поперечной мышцы живота. Последнюю расслаивают по ходу волокон. Брюшину и жировую клетчатку отодвигают медиально. Вскрывают листок почечной фасции и обнажают лоханку спереди. Мобилиьуют мочеточник вблизи лоханки. По освобождении лоханки от прилоханочной жировой ткани производят пиелолитотомию. Этот способ удобен, так как обеспечивает хороший доступ к передней стенке лоханки при наименьшей травматизации мышц передней брюшной стенки.
Чрезбрюшинный путь для операций на почке по поводу нефролитиаза, как правило, не применяется в связи с опасностью инфицирования брюшной полости мочой и большими трудностями при обнажении почки чрез-брюшинным путем по сравнению с внебрюшинным. Поясиично-брюшной внебрюшиныый разрез является наиболее удобным при всех операциях по поводу камней почек, включая и нефрэктомию.
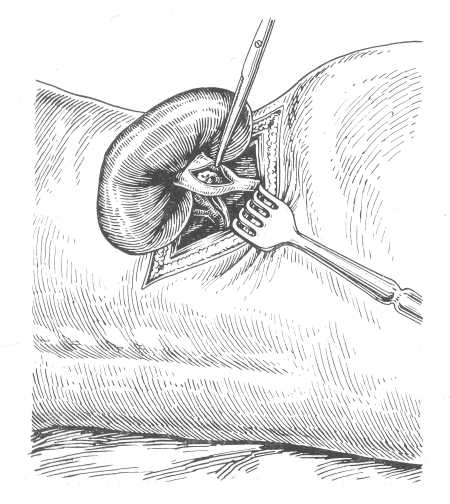
Рис. 150. Задняя пиелоли-тотомия. Лоханка рассечена, в ней виден камень.
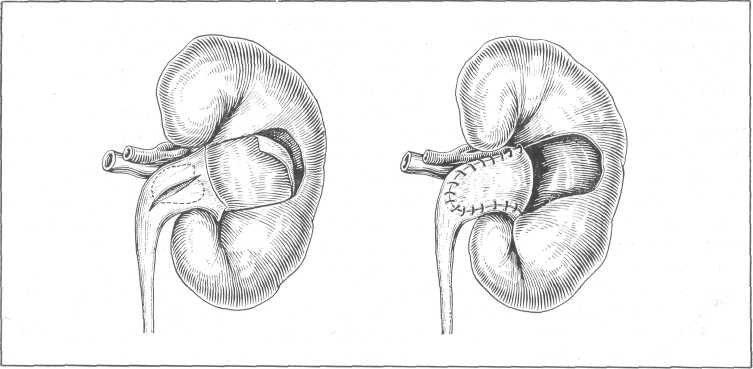
Рис. 151. Задняя пиелолитотомия. Прикрытие раны лоханки лоскутом фиброзной капсулы (Рауг).
По поводу нефролитиаза предпринимают следующие оперативные вмешательства: 1) пиелотомия (пиелолитотомия), нефротомия (нефроли-тотомия), 3) нефростомия и пиелостомия, 4) резекция почки, 5) нефрэктомия.
Каждая из этих операций имеет различные варианты, которые зависят от локализации, формы, величины и числа камней, состояния почечной паренхимы, формы и расположения почечной лоханки, ветвления сосудов почки.
В. Ф. Хоменко, изучая хирургическую анатомию артериальных сосудов почки у людей и животных, пришел к выводу, что попытки создать какую-либо единую схему расположения сосудов и малососудистых зон почки следует признать несостоятельными.
С практической точки зрения можно выделить 2 основные формы перед-нелоханочной и заднелоханочной половины почки: бобовидную (реже грибовидную) и форму запятой.
Бобовидной и грибовидной формам почки соответствует рассыпной тип ветвления передней и задней почечных артерий и тогда разрез можно вести через всю ширину той или другой половины почки, вплоть до пересечения соответствующей губы. Почке в форме запятой соответствует магистральная форма ветвления артерий. В этих случаях основной ствол артерий прикрыт губой и идет под ней сверху вниз. В таких случаях разрез лоханки надо заканчивать не доходя 1—1,5 см до края губы.
Пиелолитотомия (pyelolithotomia) впервые была произведена в 1880 г. Czerny и получила быстрое распространение.
Применяют заднюю, нижнюю и переднюю пиелолитотомию.
При передней пиелолитотомии (pyelolithotomia anter.) производят рассечение лоханки по ее передней поверхности. Эта операция имеет очень узкие показания, так как впереди лоханки расположены крупные сосуды почки, доступ к лоханке затруднен и опасен (возможность ранения сосудов). Разрез лоханки производят вблизи брюшины, прикрывающей лоханку спереди, дренирование раны затруднено, и создаются благоприятные условия для мочевой инфильтрации. Эта операция показана только при аномалиях почки, когда лоханка расположена спереди, при подковообразной и дистопированной почке.
Операцией выбора для удаления камней лоханки является задняя пие-лолитотомия (рис. 150, 151) (pyelolithotomia posterior), так как задняя поверхность лоханки наиболее доступна, нет опасности ранений сосудов почечной ножки и брюшины, обеспечивается хорошее дренирование раны. Камни лоханки, имеющие отростки без значительных утолщений на концах, также могут быть извлечены путем пиелотомии. Задняя пиелолито-томия невыполнима при внутрипочечной лоханке. В таких случаях показана нижняя пиелолитотомия или нефролитотомия.
Техника операции — почку обнажают косым поясничным внебрюшин-ным разрезом, выделяют из жировой капсулы, выводят в рану и поворачивают по длинной оси кпереди с тем, чтобы облегчить доступ к задней поверхности лоханки. Задняя поверхность лоханки и прилегающая часть мочеточника освобождаются от окололоханочной жировой ткани. Последняя при наличии камня в лоханке значительно развита, склерозирована. Разрез лоханки производят по задней ее поверхности, над камнем, который помощник или сам хирург подводит к линии разреза. Направление разреза обычно продольное, но может меняться в зависимости от расположения сосудов на задней поверхности лоханки, которые отодвигают или предварительно лигируют.
Размер разреза зависит от величины камня. Не надо делать разрез меньше диаметра камня, так как при этом камень извлекается с трудом, возможны разрывы лоханки. В то же время не следует для поисков камня и облегчения его удаления продолжать разрез на почечную паренхиму, например при внутрипочечном расположении лоханки или при больших отрост-чатых камнях, о чем справедливо предупреждает С. П. Федоров. При этом легко может быть ранена крупная ветвь почечной артерии (задняя лоханочная артерия), скрытая под задним краем почечных ворот (рис. 152). Тогда наступает значительное, подчас угрожающее, кровотечение, требующее обкалывания сосуда, а иногда даже нефрэктомии. Во избежание ранения задней лоханочной артерии Michalowski предпочитает поперечную пиелотомию, проводя поперечный разрез по задней стенке лоханки, параллельно задней губе почки, особенно в случаях длинной почки. Конкремент удаляют пинцетом, зажимом Пеана, Кохера или специальными окончатыми щипцами. Иногда камень легко выводится в рану при незначительном давлении на лоханку. Когда камень лоханки мало подвижен,, вколочен, замурован в склерозированной ткани, его надо осторожно выделить концом введенного в полость лоханки зонда Кохера, узкими сомкнутыми ножницами или специальным камнеэкстрактором. Так же поступают при выделении камня с отростками, вклинившимися в чашечки. В случаях, когда сообщение между чашечкой и лоханкой узкое, надо пальцем, введенным в лоханку, расширить ущемляющее камень кольцо. Этим приемом можно предупредить дробление камня с образованием осколков, чаще всего остающихся в чашечках.
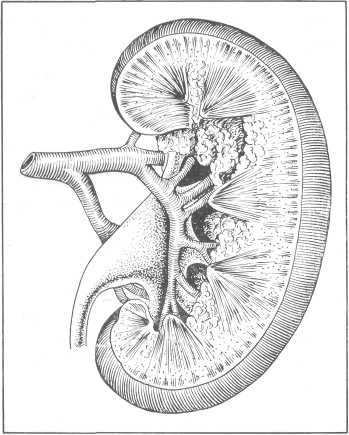
Рис. 152. Задняя лоханочная артерия (Б. Н. Хольцов).
Извлечение камня надо производить осторожно, чтобы не дробить его и не оставлять осколков. Особенно легко разрушаются фосфатные камни. Встречаются затруднения при удалении через лоханку оставшихся в чашечках осколков камня. В таких случаях не надо травмировать чашечки щипцами. Необходимо сделать нефротомию непосредственно над камнем, подавая его пальцем к поверхности почки, и извлечь камень из чашечки через почечный разрез. Иногда для этого требуется несколько небольших не-фротомических разрезов.
После удаления камней надо убедиться в том, что не осталось незамеченного камня или его осколка в лоханке, чашечке или в мочеточнике, для чего производят ревизию полостей почки пальпацией и зондированием. При обнаружении камня (или осколка) в почке его удаляют описанными выше приемами. Камень мочеточника надо попытаться поднять в лоханку и извлечь через имеющийся в ней разрез. Если выведение камня из мочеточника в лоханку затруднено, то лучше сделать уретеротомию.
После удаления камня рану лоханки ушивают узловыми тонкими кет-гутовыми швами, проходящими через серозно-мышечный слой и не захватывающими слизистой оболочки. Линию шва прикрывают окололоханочным жиром, ушивая его над раной лоханки. В тех случаях, когда рану лоханки ушить не удается, можно ограничиться сближением краев раны ушиванием окололоханочного жира. Разрез лоханки и мочеточника быстро закрывается и без ушивания, если отток мочи в мочевой пузырь не нарушен, что подтверждают клинические наблюдения и экспериментальные исследования.
Большинство авторов (В. И. Воробцов, Н. Ф. Лежнев, И. П. Погорелко, А. П. Фрумкин, А. П. Цулукидзе, Kasper, Israel и др.) предпочитает, когда это возможно, производить зашивание лоханки и мочеточника после извлечения камней, так как это способствует более быстрому заживлению раны и уменьшает опасность мочевой инфильтрации околопочечной и забрюшинной жировой клетчатки.
Удобный прием для вскрытия лоханки и ушивания ее после извлечения камня предложил Н. Ф. Горкун. После обнажения задней поверхности лоханки на нее накладывают в продольном направлении по обеим сторонам будущего разреза лоханки по одному предварительному кет-гутовому шву, не захватывая ими слизистой оболочки. Расстояние между вколом и выколом на каждой стороне определяется длиной предполагаемого разреза. Продольно вскрывают лоханку между этими швами. В процессе извлечения камня предварительные швы служат держалками, при помощи которых раскрывают рану и тем облегчают извлечение камня. После извлечения камня лоханку можно закрыть упомянутыми предварительными швами. Для этого надо соединить снизу и сверху оба шва двойным узлом. При необходимости можно наложить дополнительные швы на лоханку.
После этого почку помещают в ложе. К разрезу лоханки, подводят резиновый дренаж. Рану послойно ушивают. Дренаж извлекают на 7—8-й день. При промокании повязки мочой или нагноении раны дренаж удаляют позднее.
Для извлечения камней из почечной лоханки С. П. Федоров предложил получившую общее признание пиелолитомию in situ. Сущность этого метода заключается в том, что всю почку не выделяют из жировой капсулы и в рану не выводят. Разрез делают до жировой капсулы. Освобождают от нее только выпуклый край и заднюю поверхность почки. Ассистент удерживает почку треугольным зажимом, наложенным на переднюю часть жировой капсулы, не отделенной от почки. При необходимости выделяют и нижний полюс почки. Когда через жировую клетчатку удается ясно ощупать камень, помощник крючками или рукой отклоняет почку кнутри и оттягивает кверху. Лоханка тогда становится доступной глазу. Дальше операция принимает ход, обычный для задней пиелотомии. Пие-лолитотомия in situ особенно показана при фиксированных почках, короткой ножке и у тучных людей. Преимущество этой операции очевидно: не нарушаются связи почки с окружающими тканями, почка не травмируется, сохраняется нервно-сосудистый аппарат, кровотечение минимальное.
Внутрипочечное расположение лоханки является противопоказанием для задней пиелотомии ввиду технических трудностей операции в этих условиях и опасности ранения задней лоханочной артерии.
Babies для извлечения отростчатых камней при внутрипочечном типе лоханки предложил каликотомию. Сущность этой операции заключается в том, что для получения доступа к чашечке отсепаровывают и оттягивают заднюю губу почечных ворот от лоханки и чашечки, после чего вскрывают чашечку и извлекают камень. Эта операция сложна и травматична, так как трудно на большой глубине отсепаровать лоханку и чашечку от коркового слоя задней губы почки.
И. П. Погорелко внес изменение в технику операции, предложенной Babies, он тупо освобождает почечную лоханку от почечной паренхимы, проделывая с помощью тупого инструмента (зонд Кохера) или пальца тоннель между задней почечной губой и наружной стенкой лоханки сзади.
Наличие хорошо развитой жировой клетчатки между паренхимой почки и лоханкой в случае внутрипочечного ее расположения облегчает создание тупым путем указанного тоннеля. Заднюю почечную губу отодвигают специальным крючком, йонажают почечную лоханку сзади, вскрывают ее по задней стороне и извлекают камень. Почечную губу после этого опускают и прикрывают ею место разреза. Ушивать в таких случаях разрез лоханки нет необходимости. Описанная операция названа И. П. Погорелко субкортикальной пиелотомией.
При этой операции исключается ранение позадилоханочной артерии, так как тоннель проделывают тупым путем в обильно развитой жировой клетчатке.
Не являясь операцией выбора, так как доступ к лоханке и камню при этой операции ограничен, она имеет свои преимущества (возможность применения при внутрипочечной лоханке без повреждения паренхимы почки и задней почечной артерии) и заслуживает распространения по определенным показателям (при небольших и средних размеров камнях лоханки, чашечки при внутрипочечной лоханке).
Если большой размер камней лоханки и их форма (коралловидные и ветвистые камни) являются препятствием к их свободному извлечению, то за последние годы некоторые авторы (К. А. Великанов, Dorsey) рекомендуют имеющий уже 50-летнюю давность метод пиелотомии с раздроблением в полости лоханки камней на несколько частей, используя для этой цели стальной зажим, камнедробитель и им подобные инструменты. После удаления крупных осколков для извлечения мелких осколков производят обильное промывание почечной лоханки физиологическим раствором. Подобная методика описана И. X. Дзирне в 1914 г. Этот метод мы считаем нецелесообразным по следующим причинам.
1. Хирург никогда не может быть уверенным, что удастся извлечь все отломки, особенно неровные, шиловидные, вклиненные и фиксированные в чашечках. Подобные отломки камней с трудом извлекаются щипцами или камнеэкстракторами и их нельзя отмыть.
2. Дробление камней в лоханке любыми инструментами сопряжено со значительной травмой не только лоханки, но и почечной паренхимы, что может способствовать развитию пиелонефрита и рецидивам камней.
3. Обильное промывание в процессе операции вскрытой лоханки физиологическим или другим раствором способствует заносу вместе с промывной жидкостью мочевой инфекции; от этого не избавляет прибавление к промывной жидкости антибиотиков (в частности пенициллина, как это делает К. А. Великанов).
Для удаления из почечных полостей небольших камней и их мелких отломков Stoll рекомендует предложенный в 1943 г. Dees способ, называемый коагулопиелолитотомией. Сущность способа заключается в следующем: в раскрытую в процессе пиелотомии лоханку вводят катетер № 16 по Шарьеру. Этот катетер прикрепляют к лоханке и по нему вводят после пережатия мочеточника ниже лоханки смесь фибриногена и тромбина (90% раствор фибриногена, 10% раствор фибриногена и 10% раствор тромбина). Эта смесь обволакивает камни чашечек и лоханки и через 5 минут застывает с образованием вокруг камней коагуляционной массы (сгустка). Этот сгусток извлекают вместе с заключенными в нем камушками (или мелкими их осколками). Однако рассчитывать на удаление указанным приемом застрявших в чашечках камней и осколков нельзя. Частичная нефротомия при этом является наиболее надежным способом.
Нижнюю пиелолитотомию (pyelolithotomia inferior) производят как при внутрипочечной, так и при внепочечной лоханке. Особенно она показана при камнях внутрипочечной лоханки, при наличии больших рубцов и спаек вокруг почки и лоханки, при короткой почечной ножке, т. е. когда задняя пиелотомия вообще неосуществима. Хороший доступ дает нижняя пиелолитотомия к нижнему рогу лоханки. Значение этой операции вытекает из того факта, что внутрипочечная лоханка встречается, по данным В. В. Москаленко, у 28% больных, а по данным В. Ф. Хоменко — даже у 35,1%. Большим преимуществом нижней пиелолитотомии является возможность производить ее in situ, что впервые было выполнено С. П. Федоровым в 1908 г. В последующие годы этот метод усовершенствовал А. П. Фрумкин. Сущность операции заключается в том, что разрез проходит по нижнему краю лоханки, где нет крупных сосудов.
Техника нижней пиелолитотомии. После подхода к почке выделяют только ее нижний полюс, который отодвигают кверху и кнаружи, чем достигается натяжение мочеточника и лоханки. Отделяют осторожно окололоханочный жир. После этого между губами почки заводят два маленьких крючка, которыми губы почечной паренхимы раздвигают в стороны. В дальнейшем тщательно и осторожно продолжают отделение прилоханочного жира и обнажают нижний рог лоханки. Продольным разрезом рассекают нижний рог лоханки и извлекают камень, после чего разрез лоханки ушивают несколькими парамукозными узловыми кетгутовыми швами.
Известно, насколько тяжелыми и опасными для больного и трудными для хирурга являются вторичные пиело- и нефролитотомии. После первой операции на почке образуются плотные рубцовые спайки, фиксирующие ее к окружающим тканям и соседним органам. Воспалительный процесс в околопочечной клетчатке создает плотный рубцовый панцирь вокруг почки. При этом имеется опасность повреждения брюшины, плевры, ранения двенадцатиперстной, восходящей и нисходящей кишок и нижней полой вены. У некоторых больных доступ к лоханке для извлечения из нее камня вообще осуществить невозможно. Для таких случаев весьма полезной является предложенная А. П. Фрумкиным субкапсулярная нижняя пиелолитотомия. Эту операцию производят следующим образом.
Обнажают почку косопоперечным разрезом типа разреза Федорова. Пальпацией и ощупыванием устанавливают внутренний край и нижний полюс почки. После этого рассекают собственную капсулу почки по передней ее поверхности примерно на 2 поперечных пальца кнаружи от внутреннего края почки (рис. 153). Затем собственную капсулу, прикрывающую внутренний край почки, отслаивают и отодвигают кнутри (рис. 153,6). Этот прием облегчает доступ к воротам почки. Крючком, введенным за внутренний край, нижний полюс почки отодвигают кнаружи, обнажают область почечной лоханки. Нижний полюс почки удерживают в указанном положении в течение всей операции. Рассекают продольно собственную капсулу почки по направлению нижнего края почечной лоханки и обнажают последнюю. После этого для лучшего доступа к лоханке раздвигают края рассеченной капсулы почки. Вскрывают лоханку по ее нижнему краю и извлекают камень (рис. 153, б, г). Резиновый дренаж вводят в нижний угол операционной раны, после чего на почку надвигают отвернутую собственную капсулу. Разрез лоханки не ушивают. Таким образом, повторная субкапсулярная пиелолитотомия является, как это подчеркивает А. П. Фрумкин, нижней пиелотомией, произведенной in situ. Она осуществляется без травмы соседних органов, не нарушает васкуляризации почки и обеспечивает оптимальные условия для удаления камня лоханки независимо от типа строения почечной лоханки.
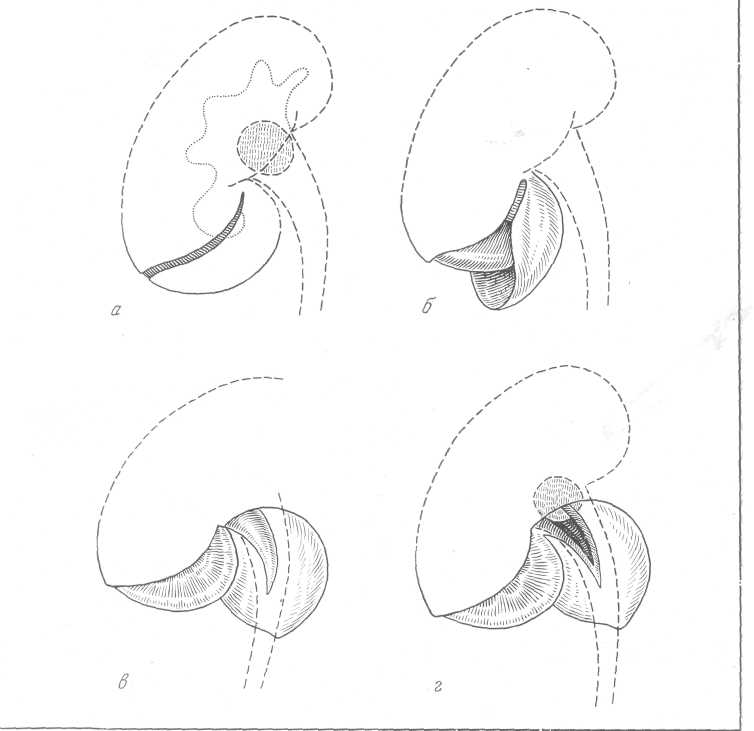
Рис. 153. Повторная субкапсулярная пиелолитотомия по А. П. Фрумкину.
а — разрез собственной капсулы почки; б — отведение кнутри собственной капсулы; в — сечение по внутренней поверхности собственной капсулы; г — рассечение лоханки по нижнему ее краю, извлечение конкремента.
Помимо А. П. Фрумкина, об успешном применении описанной операции сообщил А. М. Гаспарян. Надо считать, что субкапсулярная пиелолитотомия в методике, предложенной А. П. Фрумкиным, является лучшим оперативным методом при рецидивных камнях лоханки, подобному тому как задняя пиелотомия в тех или иных вариантах, а также нижняя пиелотомия in situ при соответствующих, описанных выше, показаниях остаются лучшими операциями для удаления первичных камней лоханки. Осложнения после этих операций редки, летальность незначительна (ниже 1%), количество рецидивов меньше, чем при нефротомии.
Нефролитотомия (nephrolithotomia). He все почечные камни возможно извлечь пиелотомией. Коралловидные, отростчатые камни, ветви которых, вклиненные в чашечки, расширены на концах, а также камни, заложенные глубоко в почечных чашечках (или паренхиме), подлежат удалению путем нефротомии.
Применяют также нефролитотомию при внутрипочечной лоханке и при невозможности освободить лоханку от сращений с прилегающими тканями.
Расширенные показания к нефротомии при коралловидных камнях ставят М. М. Ковалев, К. Т. Овнатанян, М. Н. Энфеджиев, Hiensch. Они считают, что хронический пиелонефрит, приводящий в конечном счете к гибели почки, не может быть излечен без удаления из нее камней. Большинство авторов все же полагает, что оперативное вмешательство при коралловидных камнях должно производиться только по абсолютным показаниям (анурия, тяжелые формы пиелонефрита, макрогематурия). Сторонники ограничения показаний к операции удаления коралловидных камней справедливо указывают, что в этих случаях никогда нельзя рассчитывать на полное удаление всех камней и их осколков. У таких больных быстро возникают послеоперационные рецидивы камней и операция часто только ухудшает состояние больного. Большие разрезы паренхимы почки, которые необходимы для удаления коралловидных камней, вызывают опасные операционные и вторичные почечные кровотечения (инфаркт почки), а рубцевание раны почки приводит к нарушению кровоснабжения, склерозу и атрофии почечной паренхимы. Эти соображения побудили Fey и Truck заявить на 58-м Конгрессе французских урологов в 1956 г., что полная нефротомия должна быть совершенно оставлена.
Множественные небольшие камни паренхимы, чашечек удаляют с помощью нескольких частичных нефротомии, производимых непосредственно над камнем. Часто это облегчается тем, что паренхима почки над камнем чашечки истончена. Конкременты, находящиеся одновременно в лоханке, извлекают путем добавочной пиелотомии. Этот комбинированный метод удаления камней безопаснее и выгоднее пиелонефротомии, при которой разрез лоханки продолжается на почку. При этом разрезе, при любых его вариантах всегда остается опасность ранения крупных сосудов, заложенных в паренхиме почки и под ее губой, прикрывающей лоханку. Если имеется сочетание камней лоханки и чашечек и удалить камни чашечек путем пиелотомии не представляется возможным, то можно начинать с частичной нефротомии и не делать дополнительной пиелотомии, удалив камень из лоханки через уже существующий разрез почечной паренхимы.
Существуют большие (полные) и малые (частичные) нефротомии. Большие нефротомии, предназначенные для удаления коралловидных и крупных множественных камней, производят путем секционного разреза почки, т. е. разреза, проводимого продольно через выпуклый край почки и разделяющего ее на две равные половины.
Применяют разрез Цондека, проходящий примерно на 1 см кзади от середины выпуклого края почки через плоскость естественной делимости почечных сосудов, или поперечный (радиарный) разрез Марведеля, проходящий по передней или задней поверхности почки.
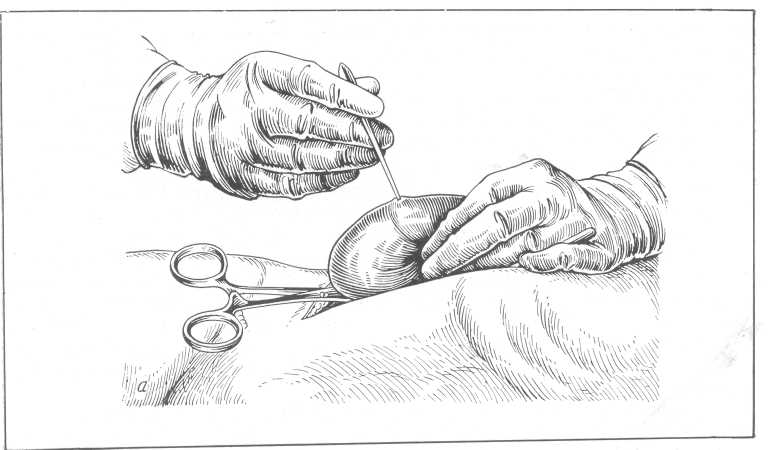
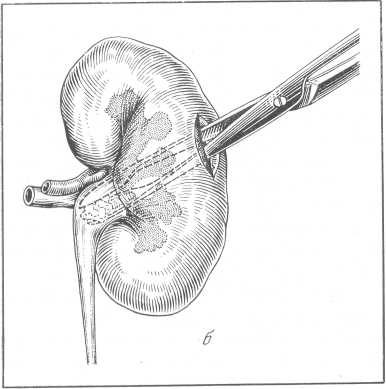
Рис. 154. Нефролитотомия. а — нащупывание конкремента: б — извлечение камня.
Этот разрез рассчитан на меньшую травму почечных сосудов, так как последние идут спереди назад и разветвляются в паренхиме почки веерообразно.
Но ни один из указанных способов полной нефротомии не избавляет от сильного кровотечения, которое в случае мощного слоя почечной паренхимы принимает угрожающий характер.
Полная нефротомия безопасна лишь при гидронефрозе и пионефрозе, так как почечная паренхима в этих случаях атрофирована, истончена и кровотечение из нее вследствие этого незначительно.
Сторонниками поперечной нефротомии при коралловидных камнях являются Hienzsch, Hasselbacher. Они видят преимущество поперечного разреза почки в хорошем доступе к лоханке, в меньшем ранении почечной ткани и в сравнительно ограниченном кровотечении по сравнению с продольным разрезом почки. Hasselbacher предложил поперечный разрез, пересекающий паренхиму почки на две равные части в центральном ее отделе вплоть до лоханки (как бы по экватору). Раздвиганием обеих половин хорошо обнажается лоханка, но труднее извлечение камней из верхней и нижней чашечек.
Значительно безопаснее малая (частичная) нефротомия, поскольку почечная ткань рассекается над камнем на небольшом протяжении и кровотечение из раны почки бывает умеренным или незначительным.
Техника нефротомии (рис. 154, а, б). При нефротомии необходимо хорошо мобилизовать почку и ее ножку. До разреза почечной паренхимы почечную ножку для предупреждения кровотечения зажимают между пальцами или мягким зажимом (кишечным зажимом, на бранши которого надевают резиновые трубки). Можно, как это рекомендует А. П. Цулукидзе, вокруг почечной ножки обвести тонкий резиновый катетер, который закручивается, и в таком виде его удерживает ассистент.
Сохранение почечной капсулы при нефротомии — обязательное условие, так как фиброзная капсула является опорой для швов, накладываемых на рану почки после удаления камней.
При полной нефротомии, применяемой только для извлечения коралловидных камней, мы применяем продольный разрез Цондека, дающий больше возможности для удаления осколков камней из верхней и нижней чашечек. Для доступа к лоханке надо рассечь шейки чашечек. Кровотечение останавливают перевязкой сосудов почечной паренхимы или обкалыванием больших сосудов тонким кетгутом. Для выявления кровоточащих сосудов ассистент постепенно ослабляет наложенный на почечную ножку зажим. Нет необходимости лигировать все мелкие кровоточащие сосуды почки, так как после сближения краев раны почки и помещения почки в ее ложе эти сосуды перестают кровоточить.
После удаления камня и перевязки сосудов обе половины почки сближают и сшивают кетгутовыми нитями средней толщины. Швы накладывают в два ряда — сначала узловатые глубокие на расстояния 1,5—2 см друг от друга, проникающие через мозговое вещество и выходящие над капсулой почки, а второй ряд—поверхностные, также узловатые, но более частые, на расстоянии 1 см друг от друга, проникающие через капсулу и корковое вещество почки. Отдельно ушивают капсулу почки непрерывным или узловатым кетгутовым швом. Некоторые хирурги, в том числе и С. П. Федоров, А. П. Цулукидзе, рекомендуют для первого ряда матрацные швы. М. Н. Эфенджиев, применяющий для извлечения коралловидных камней разрез Цондека или 2—3 меньших продольных разреза паренхимы почки, производит ушивание раны почки следующим образом.
Круглой сильно изогнутой иглой, вкалываемой глубоко в почечную паренхиму с одной стороны разреза и выводимой с другой стороны, проводят через почку двойную кетгутовую нитку. Когда концы нитки показываются, освобождают их из ушка иглы и в петлю нитки вкладывают кусочек жировой клетчатки. С другой стороны почки между обоими концами ниток также кладут кусочек жировой клетчатки и на нее завязывают нитку так, чтобы две части почки плотно прилегали друг к другу. Количество таких швов определяется величиной разреза почки. Затем ушивают фиброзную капсулу почки узловыми швами или непрерывным кетгутовым швом. М. Н. Эфенджиев, а также Rosenstein подчеркивают, что прижатие друг к другу обеих плоскостей почечного разреза вызывает остановку кровотечения. Поэтому М. Н. Эфенджиев после полной нефротомии не оставляет дренажа в ране почки.
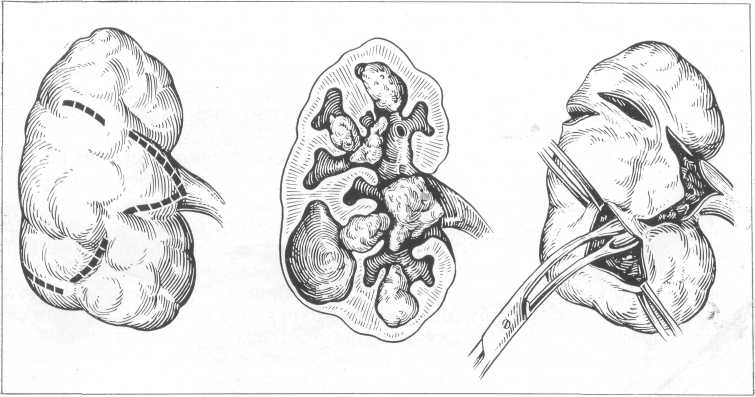
Рис. 155. Парциальная нефротомия и нефролитотомия при множественных камнях
почки.
Ни при каких методах ушивания раны почки не следует сильно затягивать швы, так как после снятия зажима с ножки (это делают после наложения швов) наступают прилив крови к почке, ее гиперемия, набухание, вследствие чего края почки плотно соприкасаются друг с другом. Сильное затягивание швов будет способствовать их напряжению, прорезанию и нарушению почечного кровообращения.
Глухой шов на рану почки накладывают только при отсутствии или маловыраженной инфекции в почке, при условии достаточного гемостаза. В противном случае через рану почечной паренхимы в лоханку вводят резиновый дренаж с ушиванием почки до дренажа.
При частичной нефротомии определяют локализацию камня ощупыванием или проколом иглой, ориентируясь по рентгеновским снимкам. Над камнем на протяжении 1,5—2 см рассекают фиброзную капсулу почки и через этот разрез по ходу иглы в глубь почечной паренхимы по направлению к камню тупо вводят зажим Кохера, которым захватывают и извлекают камень (рис. 155).
Благодаря тупому расслоению почечной паренхимы кровотечение из нее при описанной методике частичной нефротомии бывает незначительным. Если зажимом Кохера инкапсулированный отростчатый камень не удается извлечь, его надо выделить с помощью экстрактора или же удалить под контролем пальца,-чтобы избежать дробления. При частичной нефротомии вводить дренажную трубку в лоханку почки не следует, так как кровотечение бывает небольшим и легко останавливается после наложения на рану почки швов и помещения почки в ее ложе. Ушивание почечной раны производят круглыми иглами, узловыми швами, кетгутом средней толщины по описанным выше правилам. Швы проводят через почку с таким расчетом, чтобы не проникать в лоханку и чашечки во избежание образования мочевых свищей.
Хорошее гемостатическое действие оказывает тампонада почечной раны куском мышцы, взятой у больного и предварительно размозженной. Мышцу укрепляют в ране теми же кетгутовыми швами, которыми ушивают почку. С этой же целью с успехом применяют также тампонаду почечной раны жировой клетчаткой.
Если, несмотря на принятые меры, кровотечение из почки значительно операцию следует закончить нефрэктомией. На тампонаду раны почки в таких случаях рассчитывать нельзя, но при сложной обстановке (единственная почка, недостаточность другой почки) можно прибегнуть к тугому сдавлению почки с обеих сторон до плотного сближения краев кровоточащей раны. Почечную лоханку в таких случаях необходимо дренировать.
По окончании нефротомии к почке в область раны подводят резиновый дренаж. Дренаж оставляется, пока не прекратится промокание раны мочой или кровью.
Больной после операции должен быть под неуклонным наблюдением врача, так как после нефротомии иногда наблюдаются вторичные кровотечения.
Причинами их являются: 1) инфекция раны почки, расплавление тромба, 2) ишемические инфаркты, 3) венозный застой в почке, 4) кровотечение из сосудов вследствие расхождения краев раны после рассасывания кет-гутовых швов и распирания почки скапливающимися в лоханке кровяными сгустками.
Профилактика вторичных кровотечений: 1) борьба с инфекцией, 2) оставление нефростомического дренажа в почке, когда нет уверенности, что после нефротомии кровотечение остановилось.
Если после нефротомии кровотечение носит умеренный характер, то можно рассчитывать на его прекращение под влиянием гемостатических препаратов.
Летальность после нефролитотомии значительно больше, чем после пиелолитотомии, и составляет в среднем 5—7%. Рецидивы камней также наблюдаются чаще.
Резекция почки (resectio renis)
В 1930 г. В. А. Гораш предложил резекцию почки как один из методов лечения камней почек. Он обосновывал данную операцию тем, что в случае гидрокаликса после удаления камня остается полость, в которой имеется застой мочи и развивается инфекция. Это благоприятствует быстрому рецидиву камнеобразования, во избежание чего необходимо резецировать пораженную часть почки.
Эта операция получила распространение за последнее десятилетие.
В 1960 г. Thelen сообщил о 76 случаях резекции почки по поводу нефро-литиаза. Рецидивы наблюдались у 3 оперированных; у 3 возникли вторичные почечные кровотечения, потребовавшие нефрзктомии, и один умер от послеоперационного осложнения со стороны сердца.
Показания к резекции почки при нефролитиазе следующие: 1) камни в гидрокаликсе, 2) фиксированные камни в чашечках (так называемые „каменные гнезда"), 3) воспалительные стенозы шеек чашечек, 4) рецидивы камней в одном из сегментов почки.
Thelen и Kuhlo расширяют показания к этой операции, считая, что ее нужно производить и в тех случаях нефролитиаза, когда имеются воспалительные изменения в сосочках и чашечках почки и когда камнеобразование связано с нарушением оттока мочи на почве добавочного сосуда. Мы согласны с мнением тех авторов, которые ограничивают показания к резекции почки. Надо учитывать тот факт, что после удаления камней из чашечки во многих случаях полость ее подвергается сморщиванию, рубцеванию, а на инфекцию после удаления камня можно воздействовать различными лекарственными средствами, если отток мочи из почки хороший. Бесспорно, что резекция почки является более сложной операцией, чем пиелотомия и нефротомия, почечные кровотечения в процессе операции и вторичные кровотечения после нее также встречаются чаще.
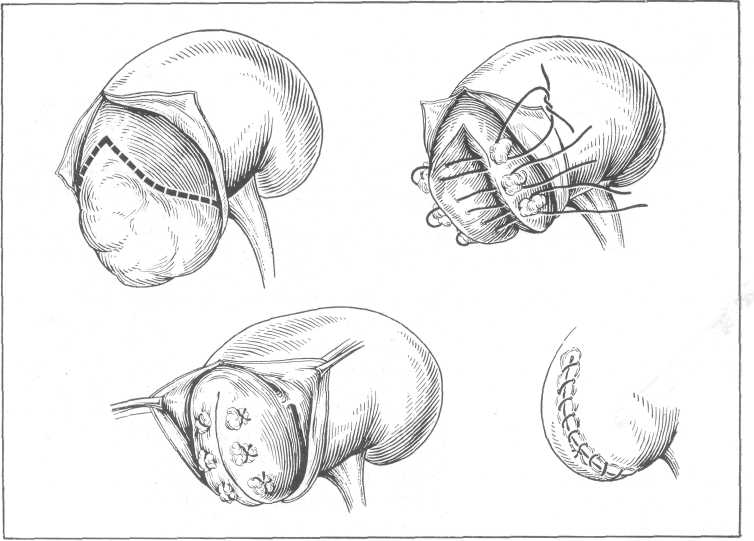
Рис. 156. Резекция почки при камнях.
В большинстве случаев производят резекцию нижнего полюса почки, так как камни в нижних чашечках встречаются чаще, что объясняется затруднением оттока мочи из нижней чашечки при вертикальном положении тела. Bibus указывает, что в 75% „каменные гнезда" наблюдаются в нижних чашечках.
Техника резекции почки. До резекции почки мобилизуют ее и почечную ножку. Почку выводят в рану. Boeminghaus производит резекцию нижнего полюса почки in situ и доступ к почке осуществляет поясничным межмышечным разрезом. Почечную ножку осторожно сдавливают мягким зажимом или тонкой резиновой трубкой (как это описано выше для операции нефротомии). Некоторые хирурги не накладывают зажима, а предварительный гемостаз осуществляют сдавлением почки между большим и указательным пальцами левой руки в зоне рассечения почки. При такой методике сохраняется свободным кровообращение в почке вне области операции. Этот прием неосуществим при резекции центральной части почки. Уменьшая сдавление почки, легко обнаружить те мелкие артериальные сосуды, которые остались нелигированными.
Разрез производят по выпуклому краю почки над намеченной зоной резекции. После рассечения фиброзной капсулы ее отделяют от зоны резекции с тем, чтобы после резекции этой же частью капсулы прикрыть почечную рану.
Резекцию полюса почки одни клиницисты производят плоскостным, перпендикулярным к длинной оси почки сечением (А. П. Фрумкин, Г. Д. Сперанский, А. А. Бухман), другие же (С. П. Федоров, А. П. Цулукидзе, Н. В. Боброва, Bibus) предпочитают клиновидную резекцию, при которой лучше адаптируются края раны (рис. 156, 157).
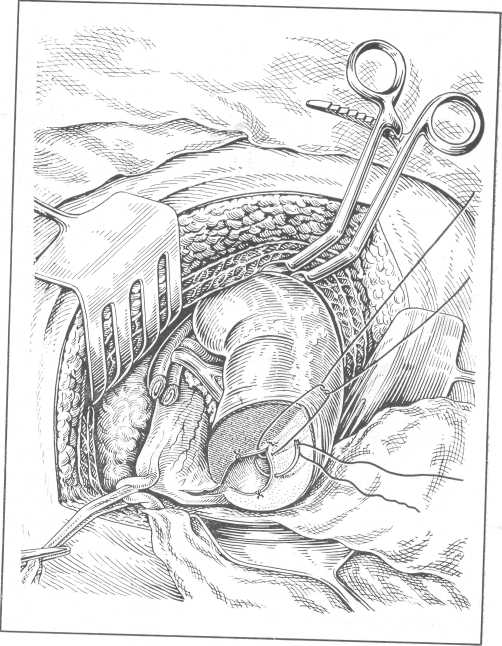
Рис. 157. Резекция нижнего полюса почки. Наложение швов на чашечку и лоханку (Bischoff).
Остановку кровотечения из артерий производят кетгутовыми лигатурами и при необходимости обкалыванием кровоточащего сосуда. Резецированные стенки чашечек, а также и лоханку, если она попадает в разрез, ушивают тонким кетгутом. Все же после гемостаза имеется капиллярное кровотечение из паренхимы почки, которое останавливают биологической тампонадой — кусочком мышцы, взятой из операционной раны. Вместо мышцы для тампонады раны почки можно использовать жировую ткань, взятую из околопочечной жировой клетчатки. Кусочек мышцы или жировую клетчатку фиксируют к ране почки тем же швом, которым ушивают ранее отсепарованную фиброзную капсулу. Прикрытие раны почки фиброзной капсулой улучшает гемостаз. Небольшое застойное венозное кровотечение в почке прекращается быстро после того, как почка помещена в свое ложе. Операцию заканчивают укрытием почки околопочечной жировой капсулой.
Kaminaga экспериментально показал, что простое сшивание капсулы над раной почки без ее тампонады кусочком мышцы или жировой ткани является достаточным как для гемостаза, так и для хорошего заживления раны. Все же имеющиеся клинические наблюдения, описанные в литературе, и наш личный опыт говорят в пользу биологической тампонады раны почки.
Операцию резекции почки заканчивают подведением резинового дренажа к области сечения почки и марлевого тампона под ее нижний полюс. Летальность после резекции почки при нефролитиазе, по данным разных авторов, колеблется от 1,3 до 5%. Рецидивы камней после нее наблюдаются реже, чем после нефротомии.
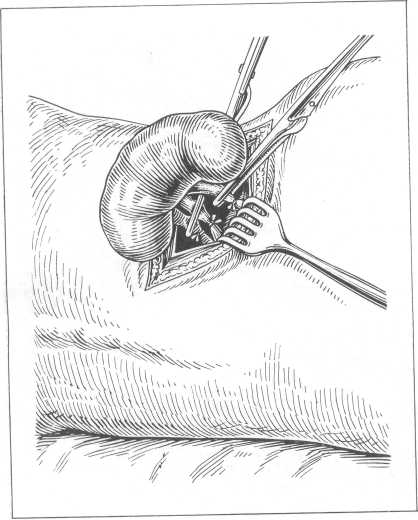
Рис. 158. Нефрэктомия.
Нефрэктомия (nephreetomia)
Несмотря на стремление к сохраняющим почку хирургическим вмешательствам, нефрэктомия все же занимает видное место среди операций, производимых по поводу нефролитиаза, хотя благодаря расширению показаний к раннему хирургическому лечению и применению антибиотиков и химиопрепара-тов широкого спектра действия число нефрэктомий снизилось с 30—40 до 13—25% всех операций по поводу нефролитиаза (В. М. Борисова, П. И. Гельфер и X. П. Блатной, М. Н. Ефенд-жиев, М. Ф. Мурадов и Р. А. Шахбазов, М.Б. Пластунов и др.). Можно думать, что дальнейшее совершенствование различных методов лечения уролитиаза и пиелонефрита позволит прибегать к нефрэктомий
значительно реже.
Необходимо стремиться сохранить почку не только при гидронефрозе, но и при пионефрозе, поскольку имеется ряд наблюдений, что даже при пионефрозе почка сохраняет известную функциональную способность, обеспечивающую возможность длительной жизни больного и его работоспособность. Кроме того, имеется опасность рецидива камня в другой
почке.
У подавляющего большинства больных калъкулезным пионефрозом мы вынуждены производить нефрэктомию. При пионефрозах, протекающих с высокой температурой и интоксикацией, при тяжело протекающих пиелонефритах показана срочная нефрэктомия. Она показана также при тяжелой профузной почечной гематурии, которую не удается остановить консервативными мероприятиями.
Нефрэктомия не представляет особых трудностей в обычных случаях нефролитиаза. Но она становится исключительно тяжелой и сложной операцией при наличии пери- и паранефральных спаек, интимных сращений почки с окружающими органами и тканями, при явлениях хронического склерозирующего пери- и паранефрита, что часто наблюдается при многолетнем калькулезном пионефрозе. Особенно трудна бывает вторичная нефрэктомия.
Техника нефрэктомий (рис. 158). По обнажении забрюшинного пространства и рассечении ретроренальной фасции выделяют почку из жировой капсулы и мобилизуют почечную ножку. До выведения почки в рану отыскивают мочеточник, который окружен забрюшинной клетчаткой и при отсутствии периуретерита легко из нее выделяется. При отодвигании париетального листка брюшины мочеточник легко с ним уходит. Ориентиром для обнаружения мочеточника является место перекреста его с подвздошными сосудами. Облегчает нахождение мочеточника поднятие нижнего полюса почки, вследствие чего мочеточник натягивается. Мочеточник выделяют возможно ниже, пальпацией проверяют, нет ли в нем конкрементов. При выделении мочеточника надо избегать ранения внутренней семенной вены у мужчин и овариальной — у женщин, а при наличии больших спаек — ранения подвздошных сосудов. Не следует стремиться к выделению мочеточника вплоть до мочевого пузыря. В случаях нефро-литиаза это не оказывает никакого влияния на успех операции и течение послеоперационного периода. Выделив мочеточник в пределах возможного, его перевязывают двумя кетгутовыми лигатурами и пересекают между ними. Культю мочеточника обрабатывают йодной. настойкой. Потягиванием за центральную культю мочеточника освобождают его кверху вместе с лоханкой, что значительно облегчает выделение почки из жировой капсулы и ее сосудистой ножки.
В области верхнего полюса почки и у ее ворот часто имеются спайки, из которых надо выделять почку с осторожностью из-за возможности наличия аномальных добавочных сосудов. Очень трудно, часто невозможно, производить выделение верхнего полюса почки под контролем глаза, особенно когда почка значительно увеличена. Доступ к верхнему полюсу почки в таких случаях облегчается поднадкостничной резекцией XII ребра. При этом надо избегать ранения плевры. Определяется ранение плевры сразу по характерному свистящему звуку, возникающему при насасывании воздуха в плевральную полость. Надо попытаться ушить ранение плевры сразу до удаления почки, а если это не удается, ограничиться тампонадой области ранения с тем, чтобы ушить плевру после удаления почки. По окончании операции аспирируют проникший в плевральную полость воздух. Особую осторожность надо проявлять при выделении из сращений области ворот почки и почечной ножки. Если последняя утолщена, укорочена и инфильтрирована, то при вмешательстве на правой почке имеется опасность ранения нижней полой вены. Обычно это ранение бывает ограниченным и его ушивают, а если это не удается, то накладывают на место ранения зажимы, оставляя их на 3—4 дня. Этот метод успешно применил Н. Ф. Лежнев. Если ранение нижней полой вены произошло ниже впадения почечных вен, то ее можно перевязать без опасных последствий, отток венозной крови в таких случаях совершается по сильно расширяющимся коллатералям (vv. azygos и w. hemiazygos). Перевязка нижней полой вены выше впадения почечных вен влечет за собой смерть от анурии. Ранение нижней полой вены опасно также ввиду возможности воздушной эмболии. Мобилизовав почечную ножку и почку, последнюю выводят в рану. Отделив жировую ткань от почечной ножки, подтягивают почку вместе с мочеточником, чтобы мочеточник не попал в одну лигатуру с ножкой. Если почечная ножка достаточно длинна и не утолщена, на нее накладывают крепкую кетгутовую лигатуру. После этого кнаружи от лигатуры у ворот почки всю ножку сдавливают специальной клеммой С. П. Федорова или другим мощным зажимом.
Участок между зажимом и ранее наложенной кетгутовой лигатурой перевязывают еще одной кетгутовой лигатурой на игле во избежание соскальзывания нитки после отсечения почки.
Почку отсекают у ее ворот над клеммой и удаляют. Шелковых лигатур на почечную ножку накладывать не следует во избежание лигатурных послеоперационных свищей. Постепенно разжимают бранши зажима, остающегося после отсечения почки, и убеждаются в отсутствии кровотечения из ножки в течение 1—2 минут. В редких случаях наблюдается медленное просачивание крови из культи почечной ножки, это связано с тем, что наложенные на ножку лигатуры затянуты слабо. Тогда нужно снова перевязать сосуды почечной ножки.
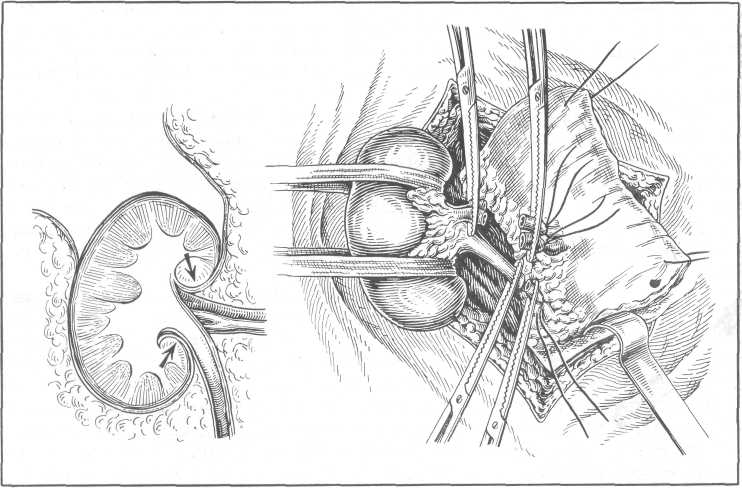
Рис. 159. Субкапсулярная нефрэктомия.
Очень толстую плотную склерозированную ножку осторожно разъединяют в центре и с помощью иглы Дешана перевязывают ее по частям. До раздельного датирования сосудов ножки надо ее хорошо сжать мощной почечной клеммой Федорова. Лигатуры накладывают на борозду, остающуюся на ножке после снятия зажима. Все же наблюдаются случаи, когда почечная ножка бывает настолько коротка и инфильтрирована, что лигировать ее не представляется возможным. Для таких случаев С.П. Федоров рекомендовал не лигировать ножку, а наложить на нее специально предложенный им зажим со съемными ручками. Этот зажим оставляют на ножке после отсечения почки на 4—5 и даже б суток, пока хорошо не организуются тромбы в крупных почечных сосудах. Снятие зажима производят в операционной при полной готовности к операции ушивания сосудов. Если во время операции после удаления почки появилось сильное угрожающее жизни больного кровотечение из сосудов почечной ножки (это бывает при отрыве почки от ножки или надрыве сосудов при сильном натяжении ножки, при соскальзывании лигатур с ножки), не следует пытаться вслепую наложить зажим на культю ножки. Надо сдавить культю ножки, стараясь захватить ее между пальцами. Если это не удается, то, не теряя времени, надо прижать ее большим тампоном и, постепенно его извлекая, найти кровоточащие сосуды почечной ножки и под контролем глаза наложить на них зажимы. Если это также не дает положительных результатов, надо чрезбрюшинно сдавить аорту и потом перевязать ножку. Если и это безуспешно, то прибегают к последнему средству — тугой тампонаде раны со сдавленней тампонами почечной ножки. В процессе нефрэктомии должно быть все подготовлено для переливания крови.
Больной с оставленным на ножке постоянным зажимом укладывается на здоровую сторону. Персонал и больной должны быть хорошо инструктированы, чтобы случайно при изменении положения больного, перекладывании его не была нарушена фиксация зажима в ране.
При большой, малоподвижной, замурованной в спайки почке, когда ее выделение крайне затруднено и связано с опасностью ранения не только брюшины, плевры и нижней полой вены, но и двенадцатиперстной, реже — ободочной кишки, С. П. Федоров предложил в 1906 г. метод с у б-капсулярной нефрэктомии, получившей общее признание (рис. 159).
Фиброзную капсулу рассекают продольно по выпуклому краю почки и отслаивают ее вдоль линии рассечения. Под фиброзную капсулу подводят палец и почку тупо освобождают из-под капсулы на всем протяжении. Иногда к продольному разрезу на капсуле надо добавить поперечные. При малой подвижности почки, что отмечается при инфильтратах в полюсах, вывести почку в рану не удается по следующим причинам:
1) ворота почки после декапсуляции находятся по другую сторону фиброзной капсулы;
2) почку удерживают в глубине спайки почечных ворот с капсулой, мочеточником, инфильтрированной окололоханочной и околомочеточнико-вой клетчаткой. Чтобы сделать почку подвижной, необходимо освободить ее ворота и отделить от мочеточника. Для этого С. П. Федоров предлагает отклонить и оттянуть почку книзу и кнаружи. Помощник в то же время отводит кнутри передний край брюшной части разреза широким почечным крючком (лопаткой), введенным между почкой и отслоенной от нее фиброзной капсулой. Такой прием создает хороший доступ к воротам почки. Если теперь сделать полукруговой разрез только фиброзной капсулы, то через него легко проникнуть в окололоханочное и околомоче-точниковое пространство противоположной стороны капсулы.
Через образованное в фиброзной капсуле почки окно проводят палец и тупым путем освобождают переднюю поверхность лоханки и прилегающую к ней часть мочеточника. После этого почку приподнимают в обратном направлении — кверху и кнутри. Помощник устанавливает почечный крючок на противоположной стороне раны и оттягивает кнаружи нижнезадний край поясничного разреза. Такой прием позволяет освободить заднюю поверхность глиуса почки. Здесь на фиброзной капсуле делают такой же разрез, как и спереди.
Таким образом, почечные ворота со всех сторон окружены разрезом через фиброзную капсулу. Через этот разрез они освобождаются от жировой клетчатки и почка становится более подвижной. После освобождения лоханки и почечной ножки накладывают зажимы на почечные сосуды и мочеточник за пределами почечной капсулы и лигируют их отдельно. Почку отсекают.
Летальность после нефрэктомии, производимой по поводу нефроли-тиаза, колеблется в пределах 4—5,5%. Причинами смерти являются: сердечно-сосудистая недостаточность, печеночно-почечная недостаточность, пневмонии, реже перитонит и кровотечение из почечной ножки.
Нефростомия (nephrostomia) и пиепостомия (pyelostomia)
Эти операции производят с целью временного или постоянного дрен-рования лоханки почки и улучшения функции почки при почечной недостаточности, обусловленной пиелонефритом. Иногда к этим операциям приходится прибегать в случаях тяжелого течения калькулезного пионефроза, особенно закрытого, когда нефрэктомия невозможна.
Нефростомия может потребоваться при отсутствии успеха от консервативного лечения при уролитиазе, осложненном апостематозным нефритом и гнойным пиелонефритом. Дренирование почки путем нефростомии или пиелостомии производят также после удаления камней при значительной инфекции в почке или лоханке ее, особенно когда последняя расширена. Дренажная трубка временно оставляется в почке также после операции, сопровождавшейся значительным почечным кровотечением. Следует предпочитать нефростомический свищ пиелостомическому, так как первый функционирует лучше. При гидро- и пионефрозе, при внут-рипочечной лоханке, когда требуется длительное или постоянное отведение мочи из почки, показана нефростомия.
Техника нефростомии. Почку подводят выпуклым краем вместе с жировой капсулой к операционному полю. По выпуклому краю почки рассекают ее собственную капсулу на расстоянии 1—2 см. Далее с помощью тупоконечного кровоостанавливающего зажима в паренхиме почки образуют канал до лоханки, через который в нее проводят резиновый дренаж. Дренажную трубку фиксируют к почке кисетным кетгутовым швом, проведенным через фиброзную капсулу, и выводят через задний угол раны, где пришивают к коже шелковым швом. Рану послойно ушивают.
Однако при такой методике нефростомии, особенно при резком увеличении почки, при неизмененных чашечках и внутрипочечном типе лоханки дренажная трубка может быть проведена не в лоханку почки, а в пространство между паренхимой почки и стенкой лоханки или чашечки. В таких случаях надежнее воспользоваться разрезом лоханки, через который удалялся камень. Со стороны лоханки через паренхиму почки на ее поверхность в области одной из чашечек проводят зажим с длинными браншами и надсекают над ним фиброзную капсулу. Дренажную трубку захватывают инструментом и проводят в лоханку почки. Последующие этапы операции аналогичны описанным выше.
Техника пиелостомии. При значительно расширенной лоханке на задней ее поверхности делают разрез и его края сшивают с краями поясничной раны. В лоханку вводят резиновую дренажную трубку и фиксируют ее к коже шелковыми швами.
Если расширения лоханки нет или оно незначительно, то края разреза лоханки не сшивают с краями поясничной раны, а дренажную трубку непосредственно вводят в лоханку и фиксируют к ней кисетным кетгутовым швом и дополнительно к коже — шелковыми лигатурами.
После операции дренажную трубку, введенную в почку или лоханку, удлиняют присоединением к ней резиновой трубки, которую опускают в стерильный сосуд, наполненный 50—60 мл 1—2% раствора марганцовокислого калия или борной кислоты.
Послеоперационный период и уход за больными, оперированными по поводу нефролитиаза, имеют некоторые особенности. У больных в течение первых 2—3 суток после нефрэктомии отмечается умеренная олигурия,. которая при нормальной функции оставшейся почки через 3—4 суток заканчивается. Анурия после удаления почки исключительно редкое явление. Она может быть вызвана токсическими влияниями на оставшуюся почку, значительным поражением этой почки до операции, обтурацией ее конкрементом, операционным шоком, большой кровопотерей в процессе операции (явления ишемии, сосудистого спазма в оставшейся почке). Крайне редко анурия может также носить рефлекторный характер. Поэтому после нефрэктомии необходимо следить за состоянием функции оставшейся почки (исследование мочи, остаточного азота и мочевины крови каждые 2—3 дня в течение первых 6—7 дней после операции, при необходимости — проба Зимницкого; постоянное измерение диуреза первые 4—5 суток). При выявлении почечной недостаточности необходимо провести мероприятия, изложенные в разделе „Анурия" при нефро- и уретероли-тиазе. Хорошим средством, стимулирующим диурез, является внутривенное вливание 40% глюкозы ежедневно по 20 мл первые 10—12 суток после операции. В этот раствор следует добавить 2 мл 5% раствора витамина В2 и 2 мл 5% раствора аскорбиновой кислоты. Специального ухода требуют больные после нефро- или пиелостомии. Надо следить за функцией дренажной трубки, количеством и характером мочи, выделяемой по ней (измерять и исследовать отдельно количество мочи, выделяемой по нефро-стомической трубке и из мочевого пузыря). Необходим тщательный уход за нефростомической и присоединенной к ней резиновой трубками. Отводящую резиновую трубку присоединяют к дренажу, введенному в почку, короткой стеклянной трубкой, через которую можно макроскопически определять внешний характер мочи, выделяемой оперированной почкой. Отводящую резиновую трубку меняют каждые 2—3 дня. Дренажная трубка, введенная в почку, как и отводящая резиновая трубка, может обтурироваться сгустками гноя, крови, мочевыми солями. В таких случаях трубки разъединяют и заменяют. Это мероприятие обычно восстанавливает хороший отток мочи из почки. Если же это успеха не дает, обрабатывают концы нефростомической трубки эфиром, спиртом и 5% йодной настойкой, затем просвет ее очищают от солей, гноя и крови стерильным металлическим зондом или мочеточниковым катетером. Лучше не промывать по дренажной трубке почечную лоханку и чашечки во избежание заноса инфекции. При необходимости их отмывают небольшими порциями стерильного физиологического раствора или 0,3% раствора аспирина. Тщательный уход за дренажем, введенным в почку, и присоединенной к нему отводящей резиновой трубкой обеспечивает хороший отток мочи и патологических продуктов из оперированной почки, а это является важным фактором, ускоряющим регенеративные процессы в ране почки, предупреждающим развитие в ней инфекции и рецидива камней.
В течение нескольких суток моча из оперированной почки может просачиваться помимо дренажа в околопочечную и забрюшинную клетчатку, на кожу в области раны. Туалет кожи (1% синтомициновая эмульсия), подвергающейся раздражению мочой, частая смена пропитанных мочой повязок являются необходимыми мероприятиями послеоперационного ухода за подобными больными.
До сих пор нет единого мнения относительно сроков извлечения дренажной трубки из почки при временной нефростомии. В. И. Воробцов и др. предлагают удалять трубку на 8—10—15-й день после операции, А. Я. Пытель, И. П. Погорелко и др. — только через 4—6 и даже 8 недель после удаления камня (при наличии пиелонефрита).
Сроки удаления нефростомической трубки определяются характером оперативного вмешательства, объемом воспалительно-гнойного процесса в почке и проходимостью мочевых путей. Последнее определяется введением по нефростомической трубке в лоханку почки 10 мл стерильного раствора 0,4% индигокармина. При хорошей проходимости мочевых путей индигокармйн тут же появляется в мочевом пузыре, что обнаруживается путем катетеризации его. Можно также воспользоваться антеградной пиелографией через дренажную трубку.
Если нефростому накладывают на длительный срок, то периодически, один раз в месяц, необходимо менять дренажную трубку в почке. Извлечение длительное время не меняемого дренажа из почки и смена его иногда бывают затруднены. В таких случаях может потребоваться рассечение поверхностных рубцов у кожного отверстия мочевого свища.
Больным с нефростомой или пиелостомой надо назначать внутрь окисляющие мочу средства (соляную, фосфорную кислоту, хлористый аммоний, борную кислоту с уротропином, пенициллин и т. п.).
У больных, подвергнутых различным операциям на почке или мочеточнике по поводу камней, в послеоперационном периоде может иметь место рецидив камнеобразования, в том числе и в оставшейся после нефрэктомии единственной почке. В литературе описаны случаи, когда камни в единственной почке образовались в самые короткие сроки после нефрэк-томии, исчисляющиеся днями и неделями. По мнению М. Ф. Мурадова, в таких случаях, по-видимому, имеет место отхождение образовавшихся еще до нефрэктомии не видимых на рентгеновских снимках камней. Повышение диуреза в оставшейся почке способствует отхождению камней в раннем послеоперационном периоде. Поэтому вскоре после операции назначают больным для профилактики рецидивов нефролитиаза соответствующую характеру мочекаменного диатеза диету, витамины, медикаментозное и питьевое лечение.
Особое внимание в послеоперационном периоде надо уделить борьбе с мочевой инфекцией, профилактике пиелонефрита как одной из мер предупреждения рецидивов почечных камней.
Двусторонний нефролитиаз
Двусторонний нефролитиаз встречается в среднем у 14—15% всех больных мочекаменной болезнью. У большинства больных двусторонним нефро-литиазом наблюдаются множественные рецидивные камни (часто коралловидного типа), причем количество инфицированных конкрементов значительно больше, чем при одностороннем нефролитиазе. У 50% при фосфатных камнях моча имеет щелочную реакцию.
Больные двусторонним нефролитиазом многие годы, даже десятилетия, обычно находятся в сравнительно удовлетворительном состоянии. Даже при наличии коралловидных камней и двустороннего инфицированного гидронефроза они сохраняют работоспособность.
У большинства больных азотовыделительная функция длительное время не страдает, если только не развивается острый гнойный пиелонефрит. Колебания удельного веса мочи у 30% больных нормальны.
У некоторых больных при наличии двусторонних коралловидных камней многолетней давности и хронического пиелонефрита почки все же сохраняют способность удовлетворительно выделять индигокармин (при нормальных показателях остаточного азота и мочевины в крови).
Расстройства функции почек не соответствуют глубоким анатомическим изменениям (атрофия, склероз, хроническое воспаление).
Стремление к сохранению почки даже при наличии в ней глубоких анатомических изменений у больных двусторонним нефролитиазом имеет особое значение. Показанием к нефрэктомии могут явиться лишь гематурия, угрожающая жизни больного, и тяжелые гнойные заболевания почки, которые не удается ликвидировать консервативным путем.
В литературе встречаются описания отдельных успешно произведенных двухмоментных операций удаления коралловидных камней из обеих почек путем сочетания пиелотомии и нефротомии, но без анализа отдаленных результатов (Hartmann).
И. П. Погорелко (1963), Hienzsch (1960) значительно расширяют показания к удалению двусторонних коралловидных камней почек.
Подавляющее большинство авторов (А. Я. Абрамян, Н. Ф. Лежнев, И. М. Тальман, С. П. Федоров, Р. М. Фронштейн, А. А. Чайка, И. М. Эпштейн, Boeminghaus, Fey и True, Staehler) считает, что показания к оперативному лечению двусторонних коралловидных камней должны быть значительно ограничены. Такой консерватизм обусловлен частым и быстрым возникновением рецидивов после удаления коралловидных камней, значительной травмой почек, связанной с полным рассечением и потерей большого количества паренхимы и опасностью профузных кровотечений, угрожающих вынужденной нефрэктомией.
Вследствие этого при коралловидных или множественных камнях обеих почек больные должны быть оперированы лишь при анурии, профузной гематурии, пионефрозе с задержкой гноя в почке, тяжелых формах пиелонефрите, сепсисе. В таких случаях органосохраняющая операция сводится к нефростомии, извлечению камней, препятствующих оттоку мочи из почки.
При двустороннем нефролитиазе больные с неразветвленными почечными и лоханочными камнями подлежат оперативному лечению лишь в тех случаях, когда эти камни можно удалить пиелотомией или ограниченной нефротомией, без значительной травмы почечной паренхимы (Н. Ф. Лежнев, Д. Е. Левант, С. П. Федоров, А. А. Чайка).
А.П. Цулукидзе считает, что оперативное лечение двустороннего неф-ролитиаза должно проводиться возможно раньше, чтобы предупредить развитие в почке осложнений, причем операция должна быть щадящей (пиелотомия).
Одни авторы (Н. Ф. Лежнев, Д. Е. Левант, М. И. Мамиконов, И. П. По-горелко, Marion) допускают одномоментное удаление камней из обеих почек, другие (С. П. Федоров, А. П. Цулукидзе) считают подобную тактику неоправданной.
И. П. Погорелко (1963) указывает на то, что новейшие достижения хирургической техники и антибактериальной терапии дают право пересмотреть вопрос в сторону значительного расширения показаний к одномоментному удалению камней из обеих почек и обоих мочеточников, и приводит в пользу этого личный опыт 100 подобных операций с благоприятным исходом. При показаниях к двухмоментной операции одни авторы, в том числе С. П. Федоров, рекомендуют вначале оперировать более пораженную почку, чтобы возможно раньше устранить вредное ее влияние на организм и на менее пораженную почку. Другие предлагают первым этапом оперировать менее пораженную почку, чтобы иметь возможность при острой необходимости удалить более пораженную. Надо указать на необходимость строгой индивидуализации при решении этого вопроса.
При наличии абсолютных показаний к операции на одной и относительных— на второй почке мы в первую очередь оперируем на почке, в отношении которой имеются абсолютные показания к операции.
При наличии камня лоханки и камня в противоположном мочеточнике следует удалять сначала камень мочеточника, если нет надежды на его самопроизвольное отхождение или извлечение его эндовезикальным путем. В случаях двусторонней обтурационной анурии в первую очередь следует оперировать ту почку, отток из которой прекратился в последнюю очередь. Ankenmann и Balfour (1963) рекомендуют при двусторонних коралловидных камнях, протекающих с явлениями нарастающей азотемии и уремии, для уменьшения риска хирургического вмешательства применять экстракорпоральный гемодиализ (искусственную почку).
Лечение больных с камнями мочеточника
Камни мочеточников являются по своему происхождению почечными. Больные уретеролитиазом составляют 28—30% всех больных, страдающих мочекаменной болезнью. М. Д. Джавад-Заде наблюдал подобную локализацию у 43,8% больных. В настоящем разделе мы приводим особенности лечения больных уретеролитиазом.
КОНСЕРВАТИВНОЕ ЛЕЧЕНИЕ
Лечение больных уретеролитиазом начинается с консервативных мероприятий, за исключением лиц, у которых имеются абсолютные показания к хирургическому вмешательству.
У 75—80% больных камни мочеточников удается вывести консервативным путем. У многих из них камни мочеточников отходят спонтанно, без всякого лечения, что объясняется хорошей динамикой и значительной растяжимостью мочеточника. Иногда наблюдается отхождение больших камней.
В. И. Воробцов наблюдал у одного из больных самопроизвольное отхождение 3 больших камней правого мочеточника (длиной 6 см и диаметром 1 см). Отошедшие камни были подвергнуты цистолитотрипсии. Им же наблюдалось спонтанное отхождение 3 больших камней левого мочеточника у больного после аденомэктомии. Все они оказались фосфатами, один камень размером 3 см XI см, другой — 2,3x1,1 см, третий — 1,6x1 см.
Консервативные мероприятия должны быть направлены на то, чтобы усиливать перистальтику мочеточника, ликвидировать спастические сокращения его и тем самым способствовать отхождению камня.
С целью усиления сократительной способности мочеточника применяют водяную нагрузку, прием внутрь глицерина, инъекции 1 % пилокарпина.
Водяную нагрузку (водяной удар) назначают 2—3 раза в сутки в зависимости от состояния сердечно-сосудистой системы, функции почек и возраста больного. Больному предлагают выпить в течение 30—60 минут 1—2 л кипяченой воды или слабого чая. Если состояние здоровья позволяет, то больному после этого рекомендуется много двигаться, выполнять умеренную физическую нагрузку. Подобное лечение противопоказано при сердечно-сосудистой и почечной недостаточности, при наличии единственной почки, нарушениях мозгового кровообращения. С осторожностью оно должно проводиться у пожилых людей.
Одновременно следует назначить глицерин по 1 столовой ложке 2 раза в день в течение не более 4—6 недель, так как в дальнейшем может появиться гемоглобинурия, роватин или цистенал, спазмолитические средства (см. раздел „Консервативное лечение камней почек").
Boeminghaus считает нецелесообразным применение водяной нагрузки при полной обтурации мочеточника, так как экскреторная урография в подобных случаях показывает, что количество мочи, выделяемое блокированной почкой не увеличивается.
Лечение водяной нагрузкой оправдано лишь при достаточной проходимости верхних мочевых путей.
Метод рентгенооблучения по Франку. Ежедневно или один раз в 2 дня больной получает 20—50—80 р при фильтре 0,5 Си и напряжении 200 kV. Соответствующей величины поле внизу живота (в среднем 10 X Х15 см) отгораживают свинцовой резиновой пластинкой толщиной 2 мм.
У мужчин дополнительно защищают яички. Как правило, облучение производят у мужчин, а у женщин лишь после менопаузы или при выраженной неспособности к зачатию. Рентгеновских облучений производят в среднем 5—8 раз.
При отсутствии успеха от упомянутых способов лечения прибегают к различным методам инструментального извлечения камней.
Наиболее простым и сравнительно безопасным приемом для этой цели является катетеризация мочеточника.
Катетеризацию производят несколько раз с перерывами 2—3 дня с постепенным увеличением диаметра катетера. Важно провести мочеточни-ковый катетер выше камня.
Если встречаются трудности в проведении катетера выше камня, то вводят по катетеру 3—5 мл 1—2% раствора новокаина.
Б. Н. Хольцов, Р. М. Фронштейн рекомендовали оставлять катетер в просвете мочеточника на 6—12—24 часа.
Введение катетера способствует не только расширению, но и усилению перистальтики мочеточника. С этой же целью одновременно с катетеризацией применяют медленное введение в просвет мочеточника 4—5 мл подогретого стерильного глицерина. Глицерин создает также более благоприятные условия для перемещения камня.
Расширение мочеточника желательно сочетать с . применением водяной нагрузки. Для расширения мочеточника при наличии небольших камней в тазовом его отделе был предложен ряд специальных инструментов: дилятаторы, бужи, навинчивающиеся на мочеточниковый катетер металлические оливы, мочеточниковые катетеры с раздуваемыми резиновыми баллончиками. Дилятаторы и бужи большинством урологов в настоящее время оставлены. Широкое распространение получили мочеточниковые катетеры с раздуваемыми резиновыми баллончиками (катетер Дурмашкина и его модификации). С. В. Волков и М. А. Марголин используют двухходовой мочеточниковый катетер, состоящий из двух склеенных мочеточниковых катетеров № 4 с двумя резиновыми баллончиками. Расстояние между ними 1,5—3 см. Катетер с нераздутыми баллончиками проводят выше камня. Наполняют жидкостью верхний баллончик и катетер низводят по мочеточнику, пока не станет ощущаться препятствие со стороны камня. После этого наполняют нижний баллончик, находящийся под камнем. Таким образом камень захватывается и сдвигается вниз. Катетер Дурмашкина удобен тем, что его надо только подвести к камню, ибо пройти выше конкремента не всегда возможно. Постепенно извлекая катетер, расширяют баллончиком мочеточник ниже камня, что способствует самопроизвольному отхождению конкремента.
Все приемы насильственного расширения мочеточника связаны с опасностью восходящей инфекции. Форсированная дилятация может привести к тяжелым осложнениям вплоть до смертельного исхода (перитонит).
Особенно опасны в этом отношении металлические расширители. Известны случаи отрыва металлических олив в мочеточнике, что потребовало оперативного вмешательства. Наибольшее распространение получили методы эндовезикального (эндоскопического или трансуретрального) извлечения камней мочеточника специально предложенными инструментами (петли Цейсса, экстрактор камней системы доктора Дормиа, петля Джонсона, Дэвиса и др.).
Петля Цейсса представляет собой- мочеточниковый катетер, к концу которого прикреплена капроновая нить. Свободный конец нити пропущен в просвет катетера через отверстие, сделанное в нем на 2—3 см ниже места ее прикрепления.
Манипулируя свободным концом петли, можно менять ее радиус и захватить камень. Экстрактор Дормиа представляет собой мочеточниковый катетер, в просвете которого на металлическом стержне вмонтирована выдвижная металлическая раздвигающаяся корзинка для захвата камня мочеточника. Саса (1963) применил экстрактор Дормиа у 150 больных. Он не наблюдал серьезных осложнений. Все же наличие металлических частей в экстракторе Дормиа требует большой осторожности при его применении.
Петля Цейсса является наиболее безопасным и эффективным инструментом.
Zeiss, имеющий наибольший опыт извлечения камней мочеточника предложенной им петлей (3000 наблюдений), считает, что этот метод может быть применен при камнях мочеточника любой локализации и даже при камнях почечной лоханки, чашечек. Подавляющее большинство авторов, однако, считает показанным инструментальное удаление только при небольших или среднего размера камнях, расположенных в тазовом отделе (рис. 160) мочеточника. Krebs подчеркивает, что чем выше камень, тем труднее извлекать его инструментальным (трансуретральным) путем.
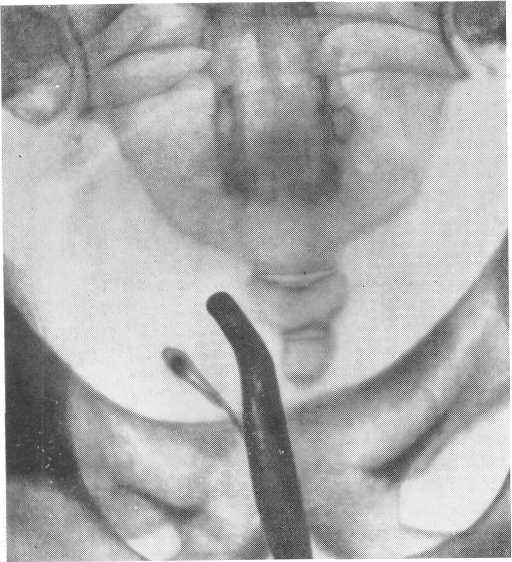
Рис. 160. Извлечение камня из мочеточника петлей Цейсса.
Камень верхнего отдела мочеточника ему удавалось низвести только у 7,5% больных, а при расположении в тазовом отделе — у 67%.
Камни верхнего отдела мочеточника чаще приходится удалять оперативным путем. Наличие единственной почки, острый пиелонефрит являются противопоказаниями к инструментальному извлечению камней мочеточника.
Техника зндовезикального извлечения камней мочеточника петлей
Цейсса следующая.
1. Перед извлечением камня рентгенологически определяют его локализацию.
2. За 30 минут до извлечения камня вводят больному спазмолитические и болеутоляющие средства (0,5—1мл 0,1% раствора атропина с 1 мл 2% раствора пантопона или 1мл 2% раствора промедола, 1 мл 0,2% раствора платифиллина или 1 мл 2% раствора папаверина под кожу).
3. Проводят с помощью катетеризационного цистоскопа петлю Цейсса выше камня, после чего рентгенологически проверяют ее положение.
4. Петлю затягивают и низводят до получения контакта с камнем.
5. Если камень небольшой, то надо попытаться извлечь его сразу осторожным потягиванием за петлю, пока основание петли не покажется в устье мочеточника.
Петля Цейсса может соскользнуть с камня, когда он низведен в около-нузырный отдел мочеточника, и мочеточник в этом месте окажется обту-
рированным камнем. Для предупреждения этого Krebs рекомендует извлекать петлю под контролем глаза.
6. Если основание петли показывается из устья мочеточника, передняя стенка устья выбухает, а камень, захваченный петлей, ущемляется в устье и не поддается извлечению, то извлечение камня надо прекратить.
7. В таких случаях переднюю стенку мочеточника на протяжении б— 8 мм рассекают над ущемленным камнем электрокоагулятором, после чего можно извлечь петлей Цейсса довольно большие камни.
Этот метод Krebs назвал электроцистоскопической уретеролитотомией. Таким путем в один прием он удалил камни нижнего отдела мочеточника у 57% больных.
8. Если камень при умеренно дозированной тяге не поддается извлечению, то делать попытки насильственного его удаления недопустимо. Это связано с опасностью разрыва мочеточника, которая тем больше, чем выше расположен камень.
Многие авторы за последние годы вообще не применяют немедленного извлечения камня мочеточника активной тягой за петлю Цейсса, а оставляют ее в мочеточнике на 3—4 дня, закрепив затянутую нить петли лейкопластом (Funfack, Koher, Pecherstorfer, Zinner).
В таких случаях больному одновременно назначают спазмолитические средства, антибиотики, обильное питье. Через несколько дней благодаря перистальтике мочеточника у многих больных происходит самостоятельное отхождение петли и камня. Нарушения пассажа по мочеточнику в период длительного нахождения в нем петли не наблюдается (моча протекает между нитками петли). В тех случаях, когда камень с петлей самостоятельно в течение 3—5 дней не выходит, его извлекают тягой за петлю под наркозом или привешивают к петле небольшой груз (200 г).
Zinner и Pecherstorfer при длительном оставлении петли в мочеточнике отмечали успех у 76 и 80% больных. В случае отрыва петли предпринимают операцию только после 4—5 дней выжидания самостоятельного отхождения петли и камня. Развитие острого пиелонефрита является в таких случаях показанием к срочному оперативному вмешательству.
У многих больных испытываются большие трудности при попытках провести петлю выше камня, без чего извлечение камня невозможно. Экстрактор камней Дорми имеет то преимущество, что его легче провести выше камня, но он более опасен, им легче перфорировать мочеточник, так как захватывающая его часть сделана из металла (рис. 161).
Описаны случаи, когда не удавалось извлечь петлю при ее ущемлении в мочеточнике вместе с камнем (А. Н. Логашов, Г. А. Хазанов), что вынудило прибегнуть к хирургическому вмешательству (уретеротомия, цитотомия с рассечением интрамуральной части мочеточника).
Таким образом, инструментальное извлечение камней мочеточника является сложным вмешательством, которое даже при умелом его осуществлении может вызвать тяжелые осложнения. Оно должно производиться только в стационарных условиях.
В качестве отдаленных осложнений инструментального низведения камней мочеточника надо указать на стриктуры и облитерации мочеточника (вследствие нарушения целости слизистой оболочки мочеточника при насильственном извлечении камня) и пузырно-мочеточниковый ре-флюкс после рассечения устья мочеточника на значительном протяжении.
Отхождение камня, находящегося в интрамуральной части мочеточника, особенно при буллезном отеке устья или уретероцеле, может быть облегчено рассечением устья эндовезикальной электрокоагуляцией.
Электрокоагуляцию устья производят по передней его стенке над камнем. Камень после этого вмешательства часто отходит самопроизвольно.
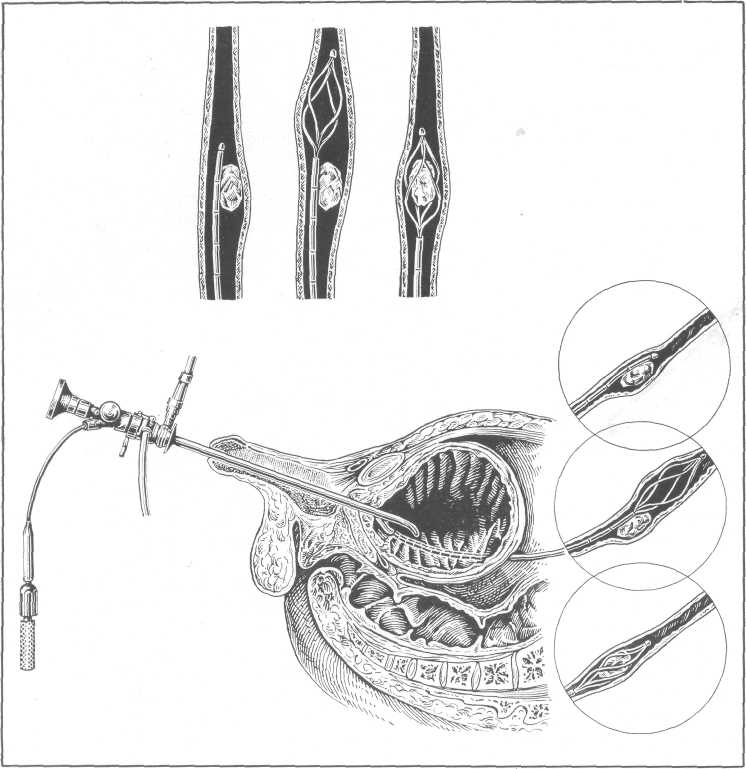
Рис. 161. Извлечение камня из мочеточника петлей Дормия (Porges).
Но не следует торопиться с рассечением устья мочеточника, если камень недостаточно вклинился в его интрамуральную часть. Если камень после электрокоагуляции не выйдет, то термический отек устья, сохраняющийся обычно 5—8 дней, вызовет обтурацию мочеточника. Если камень значительно выступает из устья, то можно попытаться извлечь его, захватив щипцами операционного цистоскопа.
При всех эндоуретеральных вмешательствах для профилактики инфекции назначают антибиотики.
При установлении показаний к хирургическому лечению уретероли-тиаза приходится учитывать многочисленные и разнообразные факторы, как состояние функции почки, лоханки и мочеточника; длительность и степень нарушения пассажа мочи по мочеточнику; размеры, форма и подвижность камня; характер инфекции верхних мочевых органов.
Особого внимания требуют показания к операции при двустороннем заболевании, а также при камнях мочеточника единственной почки.
Вопрос о том, как быстро наступают необратимые патологические процессы в почке после обтурации мочеточника камнем, окончательно не ре-
шен. В случаях острой полной закупорки мочеточника камнем атрофия почки или гидронефроз могут развиться в течение ближайших недель. Однако после ликвидации даже длительной обтурации почка может восстановить функцию. Этого не наблюдается в случаях острого пиелонефрита, когда гибель почки наступает быстрее.
В клиническом наблюдении Н. Л. Эфендиева почка сохранила функцию через 40 дней после освобождения правого мочеточника от шелковой лигатуры, которой он был перевязан во время операции надвлагалищной ампутации матки с удалением придатков справа.
С. П. Федоров (1925), В. И. Воробцов (1955), Г. С, Масленников (1961) наблюдали больных, у которых значительно нарушенная функция почки вследствие нахождения в мочеточнике камня и инфекции мочевых путей восстанавливалась после уретеролитотомии. Но такие благоприятные исходы наблюдаются редко. Длительная выжидательная тактика оправдана у больных с достаточно сохраненной функцией почки, лоханки и мочеточника, когда камень мочеточника не инфицирован и не фиксирован, а форма его и размеры дают основания рассчитывать на самопроизвольное отхождение.
В отношении таких больных необходимо динамическое рентгенологическое наблюдение. Если в течение 2 месяцев все попытки низведения камня мочеточника консервативным путем оказываются безрезультатными, то даже при спокойном безлихорадочном течении заболевания следует камень удалить хирургическим путем. Длительная выжидательная тактика таит в себе опасность закупорки почки камнем, вспышки в ней инфекции и гибели органа от гнойного пиелонефрита.
ОПЕРАТИВНОЕ ЛЕЧЕНИЕ
При первых признаках закупорки почки камнем и острого пиелонефрита (появление лихорадочного состояния, острых болей в почке, отсутствие функции почки, изменение картины крови — гиперлейкоцитоз, сдвиг лейкоцитарной крови влево, токсогенная зернистость нейтрофилов, высокая РОЭ) абсолютно показана неотложная операция. Отказ от хирургического вмешательства может привести к гибели не только почки, но и больного.
Абсолютными показаниями к операции являются также анурия, если в течение 1—2 суток консервативными мерами не удается ее ликвидировать, профузная гематурия, пионефроз и все формы острых воспалительно-гнойных заболеваний почек.
Если инфекция почек и верхних мочевых путей протекает безлихорадочно и отток мочи по мочеточнику сохранен, то показания к операции носят относительный характер.
Не следует откладывать операцию при явном несоответствии размеров камня и диаметра мочеточника, так как случаи спонтанного отхож-дения больших камней наблюдаются редко, а полная обтурация мочеточника подобными камнями — явление обычное.
Учитывая, что консервативное выведение „вколоченных", обычно ши-повидных фиксированных камней крайне затруднено и, как правило, безрезультатно, такие камни, если они не находятся в интрамуральной части мочеточника, надо оперировать возможно раньше, чтобы предупредить развитие необратимых изменений в почке. Предпринимается хирургическое лечение и в тех случаях, когда консервативное выведение камня затягивается, а функция почки непрерывно ухудшается и начинают развиваться атония мочеточника, гидронефроз.
Операция показана при очень часто повторяющихся коликах, изнуряющих силы больного.
При камнях мочеточника единственной почки необходима ранняя операция, так как окклюзия мочеточника единственной почки особенно опасна для больного.
Что касается камней обоих мочеточников, то в случае отсутствия эффекта от консервативного лечения надо прибегать к операции и освободить от камней хотя бы один мочеточник. Раньше оперируют на мочеточнике более сохранной почки, чтобы своевременным вмешательством предупредить развитие в этой почке необратимых патологических процессов. Если состояние больного позволяет, то следует одномоментно удалить камни из обоих мочеточников. Эта тактика может стать особенно необходимой, если оставление камня в более пораженной почке угрожает жизни больного (острый пиелонефрит, пионефроз с лихорадочным состоянием больного). В крайнем случае, при трудностях удаления камня из мочеточника более пораженной почки, следует ограничиться временной нефросто-мией или пиелостомией.
Методы хирургического лечения. Удаление камней мочеточника производят внебрюшинньш путем (рис. 162). С. П. Федоров чрезбрюшинный путь считал ошибочным и опасным. Отдельные авторы являются сторонниками этого доступа при камнях тазового, особенно околопузырного, отдела мочеточника (Michalowski и Modelski, Szieberth). Чрезбрюшинный путь в виде исключения может быть применен в случаях периуре-терита, особенно при локализации камня в нижнем отделе мочеточника, когда выделение мочеточника из спаек трудно технически и связано с опасностью ранения подвздошных сосудов.
Из различных доступов, предложенных для обнажения мочеточника, наиболее удобен внебрюшинный разрез Федорова. Пользуясь им, можно обнажить мочеточник на всем протяжении.
Разрез Федорова начинается сейчас же под XII ребром, проходит косо ближе к краю m. sacrolumbalis и приблизительно на уровне передней ак-силлярной линии переходит параллельно пупартовой связке на переднюю стенку живота, рассекает в поперечном направлении х/з прямой мышцы живота и спускается по ней уже продольно до лобковой кости. Этот разрез в его паховой части дает хороший доступ к тазовому и околопузырному отделу мочеточника, а также к боковой и задней стенке мочевого пузыря. Напоминает разрез Федорова косой боковой разрез Израэля. Для обнаружения мочеточника в средней трети можно также пользоваться разрезом Пирогова, применяемым при перерезке больших подвздошных сосудов.
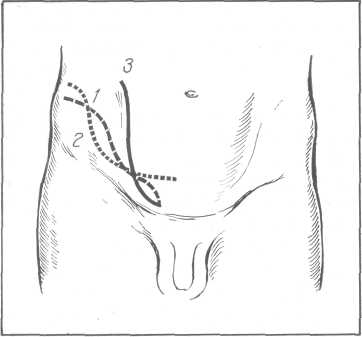
Рис. 162. Разрезы для впебрюшинного обнажения мочеточника. 1 — Израэля; 2 — Федорова; 3 — Цулукидзе.
А. П. Цулукидзе предложил S-образный параректальный разрез, который дает удобный доступ к нижнему отделу мочеточника. Разрез начинается на 2 поперечных пальца ниже точки на границе внутренней и средней трети линии, проведенной между пупком и наружной верхней осью гребешка подвздошной кости. Линию разреза продолжают книзу и дугой поворачивают к лобку, проходя по наружному краю прямой мышцы. Апоневрозы наружной и внутренней косой, а также поперечной мышц рассекают и проникают в предбрюшинную клетчатку. Тупыми крючками оттягивают наружный край разреза вместе с мышцами кнаружи, пристеночный листок брюшины отслаивают внутрь, что дает возможность проникнуть в подвздошную ямку и внебрюшинную часть малого таза. Мочеточник можно проследить до вхождения в мочевой пузырь; опознавательным пунктом является пульсирующая общая подвздошная артерия.
При операциях на мочеточнике более широко используют перемежающиеся межмышечные доступы (в „клетку"), описанные выше для операций на почке.
К. Т. Овнатанян и В. С. Карпенко предложили для обнажения тазового отдела мочеточника дугообразный поперечно идущий внебрюшинный разрез длиной 15—18 см, проводимый выше симфиза выпуклостью книзу.
Удаление камней верхней и средней трети мочеточника с помощью описанных выше доступов сложности не представляет. Наиболее трудно удалить камни нижней трети мочеточника, особенно его околопузырной части, ввиду узости и глубины раны, получаемой при боковых разрезах. В этих случаях лучший доступ получается от параректального разреза по Цулукидзе и от срединного разреза Кея.
Разрез идет по белой линии от пупка до симфиза. Рассекают поперечную фасцию. Тупо проникают в полость малого таза. Боковую стенку мочевого пузыря и спаянную с нею брюшину отодвигают в сторону, противоположную больному мочеточнику. Обнажают большие подвздошные сосуды, запирательную вену и нерв. Брюшину тупо отодвигают кверху. Мочеточник отыскивают лежащим на париетальном листке брюшины в области бифуркации подвздошной артерии. Надо иметь в виду, что при отслаивании брюшины вместе с ней может отойти и мочеточник. Нижняя треть мочеточника у мужчин перекрещивается с семявыносящим протоком, который имеет вид круглого плотного шнура. К околопузырному отделу мочеточника доступ прикрыт венами (впадающими в запирательную вену), которые надо лигировать. Венозное сплетение значительно развито в этом месте у женщин. Маточную артерию, лежащую в одной плоскости с мочеточником, надо обойти.
Для хорошего доступа к мочеточнику очень важно придать больному соответствующее положение, способствующее созданию достаточного простора в глубине раны. Если операцию производят в верхнем отделе мочеточника, то больной лежит так же, как при операции на почке, т. е. на здоровой стороне с подложенным под талию валиком, при выпрямленной ноге больной стороны и согнутой ноге на здоровой стороне. При операциях на тазовом отделе мочеточника больной лежит на спине с приподнятой больной стороной под углом 45°, для чего под ягодицу подкладывают плотный валик. Нога больной стороны выпрямлена, здоровой — согнута в коленном и тазобедренном суставах. Придается умеренное тренделенбур-говское положение. Стол после фиксирования больного слегка наклоняется в здоровую сторону. Таким путем достигается отодвигание кишечника вверх и в сторону, противоположную месту операции, а также широкое расхождение в ходе операции краев раны.
При вскрытии забрюшинного пространства и обнаружении мочеточника в последнем отыскивают камень. Выделять мочеточник на значительном протяжении не следует, чтобы не нарушать его трофики. Если камень расположен низко, то лучше при возможности передвинуть его кверху до уровня безымянной линии, где извлечение его легче. Если камень мочеточника расположен недалеко от лоханки, то рекомендуется продвинуть его в лоханку и удалить путем пиелотомии. До рассечения мочеточника под него подводят выше и ниже камня марлевые или резиновые держалки либо захватывают его специальными щипцами — фиксаторами. Кроме того, чтобы избежать инфицирования раны мочой, заранее подводят под мочеточник марлевую салфетку и мочеточник сжимают выше разреза. Разрез мочеточника делают продольно по передней его стенке над камнем (рис. 163, а, б).
При извлечении камня, особенно если он вколочен, следует избегать применения инструментов, так как ими можно травматизировать и даже разорвать мочеточник и раздробить камень. Надо стремиться вывести камень в разрез мочеточника легким давлением на него сзади пальцем и после этого удалить камень, захватив его пинцетом или зажимом Кохера.
По извлечении камня эластичным зондом проверяют проходимость мочеточника. Металлический гибкий зонд для этой цели надо предпочесть мочеточниковому катетеру, так как зондом лучше ощутить оставшиеся осколки камня или наличие еще не извлеченного конкремента. Если стенка мочеточника на месте рассечения не была значительно склерозирована и инфильтрирована, то разрез мочеточника ушивают тонкими парамукозными узловыми швами. Однако осуществить это в околопузырном отделе мочеточника технически очень трудно. Поэтому здесь чаще всего рану мочеточника оставляют открытой. Но и незашитая рана мочеточника быстро закрывается, если имеется хорошая его проходимость. К области раны подводят марлевый тампон, на который укладывают резиновую дренажную трубку. Оставлять дренажную трубку без защиты ее тампоном в области подвздошных сосудов нельзя, так как описаны случаи пролежней с перфорацией сосудов. Рану послойно ушивают до дренажа и тампона. На 7—8-й день дренаж и тампон извлекают, если нет просачивания мочи в рану.
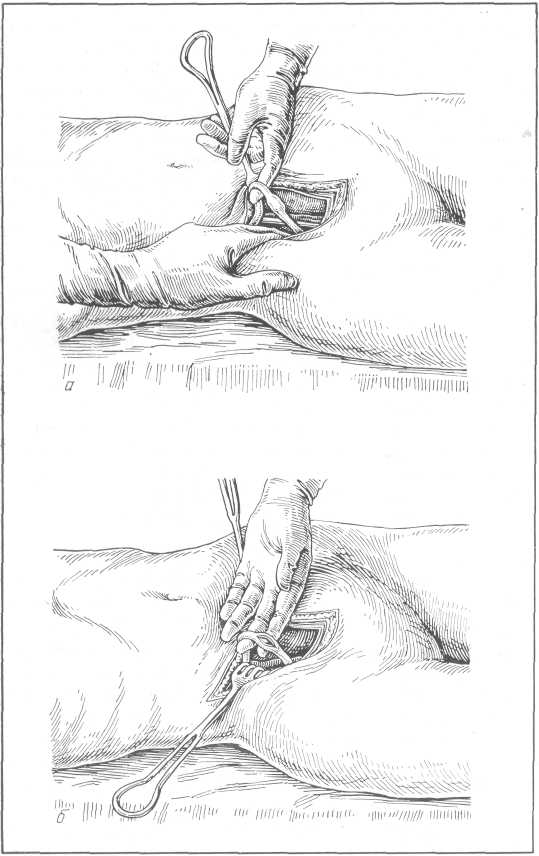
Рис. 163, а, б — этапы уретеролитотомии.
При чрезбрюшинном доступе производят нижнюю срединную лапа-ротомию. Органы брюшной полости отодвигают в здоровую сторону. Париетальную стенку брюшины рассекают соответственно расположению камня мочеточника по наружному краю восходящей, нисходящей или сигмовидной кишки. Из этого разреза отыскивают мочеточник. Наилучший для этого ориентир — место перекреста мочеточника с подвздошными сосудами или место впадения мочеточника в мочевой пузырь. Мочеточник рассекают продольно над камнем и последний извлекают. Накладывают параму-козные узловые тонкие кетгутовые швы на рану мочеточника, образуют контрапертуру в поясничной области, откуда дренируют ретроперитонеальное пространство. Рану мочеточника экстраперитонизируют. Париетальную брюшину над мочеточником зашивают. Брюшную стенку послойно ушивают.
Камни мочеточника, расположенные в интрамуральной части или в уретероцеле, которые не поддаются эндовезикальному извлечению, удаляют щипцами или узким корнцангом, произведя предварительно высокое сечение мочевого пузыря (С. П. Федоров и др.). Так же поступают при удалении камня из дивертикула околопузырного отдела мочеточника.
Если камни околопузырного отдела мочеточника очень велики и их удаление требует рассечения мочеточникового устья на большом протяжении, то имеется опасность развития атонии мочеточника вследствие разрушения его жома или появления стриктуры. Для предупреждения этих осложнений в указанных случаях целесообразно произвести резекцию околопузырного отдела мочеточника вместе с камнем и реимплан-тацию мочеточника в мочевой пузырь.
Из послеоперационных осложнений чаще всего наблюдаются моче-точниковые свищи и стриктуры.
Свищи мочеточника обусловливают все те причины, которые вызывают нарушение оттока мочи ниже свища: рубцовые спайки, инфильтраты, смещение и сдавление ими мочеточника, ограничение его подвижности, периуретерит, стриктура, осколок камня. Поэтому для закрытия свища необходимо выявить его причину и по возможности устранить.
Стриктура мочеточника развивается при наличии изъязвления слизистой оболочки мочеточника, хронического воспалительного процесса в нем и периуретеральных тканях или его травмы в процессе операции. Для предупреждения стриктуры мочеточника надо в послеоперационном периоде вести борьбу с инфекцией мочевых путей, следить за их функцией и при необходимости периодически осуществлять катетеризацию мочеточника.
Flick на 154 уретеролитотомии наблюдал 8 послеоперационных стриктур мочеточника, из них в 2 случаях потребовалась нефрэктомия. У 6 больных успех получен от консервативного лечения. В большинстве случаев для образования послеоперационных стриктур имели значение предоперационные изменения в мочеточнике, мочевая инфекция.
Иногда стриктура мочеточника образуется еще до операции (хроническое воспаление, язва слизистой оболочки мочеточника на месте расположения камня, инкрустация стенки мочеточника солями). А. М. Ша-тин в одном из подобных случаев вынужден был для ликвидации большой протяженности стриктуры мочеточника при операции удаления камня произвести одновременно операцию Боари.
Результаты лечения
После удаления камней из почки, лоханки или мочеточника функция почек быстро улучшается, восстанавливаясь постепенно до нормы, если только не имели места глубокие изменения деструктивного, атрофического и склеротического порядка. Медленное восстановление функции почки наблюдается даже в случаях гидронефроза. При пиелоэктазии лоханка постепенно уменьшается в размерах. Операция в значительной мере способствует ликвидации воспалительного процесса в мочевой системе.
Для выявления возможных рецидивов заболевания большое значение имеет изучение отдаленных результатов хирургического лечения.
Надо отличать истинные рецидивы от ложных. Под последними понимают обнаружение в почке камней или осколков, не замеченных во время операции. По существу ложные рецидивы нельзя вообще причислять к рецидивам. До самого последнего времени частота рецидивов, по литературным данным, сильно колеблется.
Р. М. Фронштейн среднее количество рецидивов после различных операций по поводу нефролитиаза определяет в 15—20%.
По данным И. М. Тальмана, рецидивы в операционной почке были обнаружены у 12,2% больных, А. Я. Абрамяна (1958) после пиелолитото-мии — у 12%, после нефролитотомии — у 16%, после нефрэктомии в противоположной почке — у 7,8%, после уретеролитотомии — у 7% больных (сроки наблюдений за больными от 3 до 10 и 13 лет).
В. П. Смеловский (1958) наблюдал рецидив почечнокаменной болезни после органосохраняющих операций у 19,8% больных, образование камней в оставшейся почке — у 2,5% больных (сроки наблюдения за больными от 2 до 10 лет). У 2/3 этих больных рецидивы возникали при наличии инфицированной мочи и пониженной функции почек.
П. И. Гельфер и X. П. Блатной (1958) после органосохраняющих операций по поводу нефро- и уретеролитиаза истинные рецидивы в оперированной почке отмечали у 5,3% больных, а появление камней в оставшейся после нефрэктомии почке — у 3,7% (сроки наблюдения за больными от 1 года до 12 лет).
М. Н. Ефенджиев (1961) отмечал у 18,8% больных рецидив после пиело-литотомии и у 25% — после нефролитотомии (сроки наблюдений за больными от 3 месяцев до 10 лет).
Ререг (1960) рецидив нефролитиаза наблюдал у 15,65% больных. При этом у 33,08% из них камни образовались в противоположной почке и у 7% рецидивы были двусторонними. Прогноз после нефрзктомии, произведенной по поводу нефролитиаза, автор считает плохим из-за опасности нефролитиаза единственной почки. Как видно из изложенного выше, чаще всего рецидивы наблюдаются после нефролитотомии, сравнительно редко — после пиелолитотомии и еще реже — после нефрэктомии. Suby приводит данные о 2789 операциях, произведенных по поводу камней почек, в том числе 343 (6,4%) нефрэктомии. Истинные рецидивы камней в оставшейся почке возникли только у 3,7% больных. Эти больные были оперированы по поводу анурии, значительной гематурии, инфекции и боли. Удаленные из единственной почки камни в 80% случаев были фосфатами или смешанными (состояли из фосфатов и оксалатов кальция), в 12% — уратами и в 8% — цистиновыми. Большинство атворов подчеркивает значительное уменьшение рецидивов нефролитиаза после резекции пораженного камнями сегмента почки (ликвидация „каменных гнезд" и пораженной инфекцией застойной полости почки). Г. А. Маточкина на основании опыта резекции почки по поводу нефролитиаза у 30 больных за период с 1946 по 1957 г. наблюдала значительное количество рецидивов в оперированных почках с сохранением в них инфекции, несмотря на значительное улучшение динамики опорожнения полостей почки.
Редко имеет место рецидивирование камней мочеточника (6—7%).
М. Б. Пластунов отмечает, что в почке рецидивы после удаления камней мочеточника наблюдаются в Зраза реже, чем после операций по поводу камней почек. М. Д. Джавад-Заде изучил отдаленные результаты консервативного и оперативного лечения у 550 больных уретеролитиазом (до 1 года —142 больных, от 1 года до 3 лет — 180, отЗ до 5 лет — 189 и от 5 до 7 лет — 39 больных). Рецидивы появились у 24 больных (4,3%), из них у 4 (1,6%) после операции уретеролитотомии. У 13 из 24 больных отмечены рецидивные камни почки, а у 11 — мочеточника.
Рецидивы при инфицированной моче наблюдаются чаще, чем при асеп-тичной. Особенно часты рецидивы после операций при фосфатных камнях с щелочной аммониакальной мочой и у больных двусторонним нефролитиа-зом. Хронический пиелонефрит, нарушения динамики верхних мочевых путей являются факторами, особенно способствующими рецидивному нефролитиазу.
Ряд авторов считает, что в 15% случаев рецидивного нефролитиаза причиной его является гиперпаратиреоидизм (см. „Этиология и патогенез").
Профилактика рецидивов нефролитиаза заключается в уменьшении концентрации солей в моче и повышении их растворимости, в усилении выведения их из организма. Назначают обильное питье, соответствующую диету, витамины и указанные ранее медикаменты с учетом рН мочи, химического состава камня, руководствуясь положениями и практическими указаниями, изложенными в разделе „Консервативное лечение". Нельзя забывать о воздействии на центральную нервную систему больного, особенно при фосфатурическом диатезе. Фосфатурия, как правило, протекает с явлениями функциональных расстройств центральной нервной системы. Уролог должен осуществлять лечение и профилактику мочекаменной болезни в тесном контакте с невропатологом, физиотерапевтом, используя весь комплекс средств, благотворно влияющих на нервную систему больного. Полезно также лечение на питьевых курортах для тех больных, у которых после операции удаления камня остаются воспалительные явления в верхних мочевых путях.
Литература
А б и е в М. Б. и И з р а и л е в и ч И. 3. Урология, 1963, 5, 52.
Абрамян А. Я. В кн.: Труды 3-й Всесоюзной конференции урологов (19—24 мая 1958 г. Тбилиси). Под ред. А. Б. Топчан. М., 1960, стр. 74.
АбуллаевА. А. Мочекаменная болезнь у детей. Дисс. Ташкент, 1962.
Апакова С. А. В кн.: Труды 3-й Всесоюзной конференции урологов (19—24 мая 1958 г. Тбилиси). Под ред. А. Б. Топчан. М., 1960, стр. 81.
Б а р с е л ь В. А. Урология, 1961, 4, 17.
БеккерманА. Г. иБерманЛ. М. Урология, 1941, 2, 40.
Б о б р о в а Н. В. В кн.: Тезисы первой конференции урологов Грузинской ССР (посвященной 40-летию установления Советской власти в Грузии). Тбилиси, 1961, стр. 77.
Бондаренко Б. И. В кн.: Современные вопросы урологии. Под ред. М. А. Сресели. Л., 1962, стр. 100.
Борисова В. М. Урология, 1963, 3, 19.
Б р а г и н. К. А. Урология, 1963, 5, 22.
Б р а у н И. (Прага). Урология, 1959, 3, 65.
Бутлиашвили Н. С. Урология, 1960, 3, 40.
Б у т у з о в А. А. Урология, 1959, 5, 62.
Великанов К. А. Урология, 1958, 2, 37.
Войно-ЯсенецкийА. М. Урология, 1964, 1, 11.
В о л к о в С. В. и К о р о л и х и н В. В. Урология, 1962, 5, 38.
ВолковС. В. иМарголинМ. А. Урология, 1960, 4, 49.
Воробцов В. И. Почечнокаменная болезнь. М., 1955.,
ВоробцовВ. И. В кн.: Многотомное руководство по хирургии. Т. IX. Гл. X. Хирургия мочевых и половых органов и забрюшинного пространства. Под ред. А. Я. Пы-теля. М., 1959, стр. 217.
ГаглоевА. В. В кн.: Труды 2-го Закавказского съезда хирургов (9—14 сентября 1935 г., Тбилиси). Т. II. Грузмедгиз, 1937, стр. 247.
Гаспарян А. М. и Овчинников Н. М. Урология, 1929, VI, 4, 164.
Г е б л е р К. Физико-химические проблемы в хирургии. Биомедгиз, 1935.
ГельферП. И.иБлатнойХ. П. В кн.: Труды 3-й Всесоюзной конференции урологов (19—24 мая 1958 г., Тбилиси). Под ред. А. Б. Топчан. М., 1960, стр. 79.
Гзиришвили А. 3. В кн.: Труды 1-й Республиканской конференции урологов Азербайджана (16—19 ноября 1955 г.). Под ред. проф. М. Б. Абиева. Баку, 1953, стр. 117.
Гзиришвили Т. А. В кн.: Труды 1-й республиканской конференции урологов Азербайджана (16—19 ноября 1955 г.). Под ред. М. Б. Абиева. Баку, 1958, стр. 85.
Г о р а ш В. А. Вестн. хир. и погран. обл., 1930, XXII, 64, 185.
Г о р а ш В. А. Сов. хир., 1933, V, в. 1—3, 368.
Г о р к у н Н. Ф. В кн.: Труды Военно-морской медицинской академии Т. 48. Под ред. проф. Н. Ф. Горкун. Л., 1955, стр. 63.
Г о х и а А. Ф. К вопросу о морфологических изменениях, развивающихся в почках и некоторых других органах после односторонней перевязки мочеточника (экспериментально-клиническое исследование). Дисс. Тбилиси, 1956.
Гребенщиков Г. С. Мочекаменная болезнь (этиология, патогенез). Дисс. Л., 1951.
Г р и д н е в А. Б. Нов. хир. арх., 1928, VI, 2, 146.
Г р у н д В. Д. Урология, 1956, 4, 54.
Д а р е н к о в А. Ф. Урология и нефрология, 1965, № 1.
Джавад-Заде М. Д. Камни мочеточников. Медгиз, 1961.
Добротворский В. И. В кн.: С. П. Федоров. Хирургия почек и мочеточников,, вып. V. М.—Л., 1925, стр. 696.
Дробнер В. Л. Хирургия, 1963, 12, 106.
Дудченко М. А. Урология, 1961, 4, 22.
Егоров М. Н. Солевые (мочекаменные) диатезы: фосфатурия, оксалурия (клинико-экспериментальное исследование). Дисс. Л., 1940.
Егоров М. Н.иМанусоваН.Б. Клиническая медицина, 1937, XV, 2, 1413.
ЕгоровМ. Н.иФедоровИ.И. Вестн. хир. и погран. обл., 1932, XXXI, 92—94, 35.
Еланский Н. Н. Урология, 1937, 2, 5.
Е ф е н д ж и е в М. Н. (София). Урология, 1961, 2, 11.
Е о л я н Р. О. Вестн. хир. и погран. обл., 1930, XXI, 62—63, 134.
Золотарева И. И. Урология, 1961, 9, 21.
ИванушкинА. Г. В кн.: Сборник научных трудов Военно-медицинской академии им. С. М. Кирова. Л., 1941, XXVII, 263.
И д е л ь с о н Л. А. Урология, 1958, 2, 64.
Икрамов 3. X. Сборник научных трудов Самаркандского медицинского института.-Самарканд, 1952, VIII, 258.
Икрамов З.Х. Врач, дело, 1953, 6, 559.
Капетивадзе И. И. Урология, 1963, 5, 22.
Карпенко В. С. Урология, 1961, 4, 24.
К е ч е к А. С. Труды I съезда хирургов Закавказья (16—20 октября 1925 г.). Баку,, 1926, стр. 205."
Козловский Ю. Г. Урология, 1961, 4, 59.
К о л о м и й ц е в А. П. и Л е в и н Э. Г. Урология, 1959, 2, 62.
Кравчинский Б. Д. Современные основы физиологии почек. Л., 1958.
К р е б с В. Урология, 1962, 2, 42.
Левант Д. Е. иГурвичИ. А. Урология, 1956, 4, 37.
Л е ж н е в Н. Ф. Врач, газ., 1925, 15—16, 375.
Л е ж н е в Н. Ф. Курорт, дело, 1928, 12, 66.
Л е ж н е в Н. Ф. и"Л е в а н т Д. Е. Нов. хир. арх., 1930, XI, 4, 374.
Л и д с к и й А. Т. В кн.: Труды госпитальной хирургии клиники Свердловского государственного медицинского института, 1948, IV, 428.
Логашев А. Н. Урология, 1963, 1, 59.
ЛогашевА. Н. Урология, 1963, 6, 22.
Лорин-ЭпштейнМ. Ю. Сов. врач, журн., 1938, 2, 105.
Максудов Н. X. Химико-биологическое исследование полыни метельчатой (Artemisia scoparta W. et К.) и применение препарата артемизола в урологической практике. Автореф. дисс. Ташкент, 1963.
МамиконовМ. И. Нов. хир. арх., 1931, 24, кн. 1 (93), 113.
Марточкина Г. А. Труды 3-й Всесоюзной конференции урологов (14—19 мая 1958 г., Тбилиси). Под ред. А. Б. Топчан. М., 1960, стр. 84.
МартынюкА. Г. Состояние и функция оставшейся почки. Киев, 1953.
Масленников Г. С. Урология, 1961, 6, 62.
Минчин Н. 3. Урология, 1958, 2, 28.
Мир-Касимов М. А. Материалы к изучению мочекаменной болезни в Азербайджане. Дисс. Баку, 1928 (реф. Московск. мед. журн., 1929, 5, 92).
Мир-Касимов М. А. В кн.: Труды II Закавказского съезда хирургов (9— 14 ноября 1935 г., Тбилиси). Ч. II. Грузмедгиз, 1937, стр. 185.
Москаленко В. В. Вестн. хир. и погр'ан. обл., 1931, XXII, 65—66, 144.
М у р а д о в М. Ф. В кн.: Труды 1-й Республиканской конференции урологов Азербайджана (16—19 ноября 1955 г.). Под ред. проф. М. Б. Абиева. Баку, 1958, стр. 54.
Мурадов М. Ф. и Шахбазов Р. А. В кн.: Труды 3-й Всесоюзной конференции урологов (19—24 мая 1958 г., Тбилиси). Под ред. А. Б. Топчан. М., 1960, стр. 105.
Никобадзе И. И. В кн.: Труды 3-й Всесоюзной конференции урологов (19—24 мая 1958 г., Тбилиси). Под ред. А. Б. Топчан. М., 1960, стр. 110.
Никобадзе И. И. В кн.: Тезисы первой конференции урологов Грузинской ССР (посвященной 40-летию установления Советской власти в Грузии). Тбилиси, 1961, стр. 104.
Ни Кольская О. Д. и Потемкина 3. Ф. Урология, 1961, 4, 64.
ОвнатанянК. Г. иКовалевМ. М. Урология, 1956, 4, 43.
ПаливодаН. И. Урология, 1963, 4, 53.
Перешивкин Н. С. Врач, газета, 1924, 24, 517.
Пластунов М. Б. Урология, 1959, 4, 3.
П л а с т у н о в М. Б. Труды 3-й Всесоюзной конференции урологов (14—19 мая 1958 г., Тбилиси). Под ред. А. Б. Топчан. М., 1960, стр. 106.
ПогорелкоИ.П. Мочекаменная болезнь (хирургическое вмешательство при камнях почек и мочеточников). Ташкент, 1960.
Погорелко И. П. Хирургия, 1963, 11, 116.
Померанцев А. А. и Топчан А. Б. Урология, 1934, XI, 2, 35.
П р а т В., Бенешова Д., Дейдар Р. и ГаталаМ. (Прага). Урология, 1963, 5, 11.
ПресайвенП. 3. Врач, дело, 1948, 9, 765.
П ы т е л ь А. Я. Урология, 1955, 1, 5.
П ы т е л ь А. Я. В кн.: Труды 1-й Республиканской конференции урологов Азербайджана (16—19 ноября 1955 г.). Под ред. М. Б. Абиева. Баку, 1958, стр. 103.
П ы т е л ь А. Я. Лоханочно-почечные рефлюксы и их клиническое значение. М., 1959.
ПытельА. Я. и ГолигорскийС. Д. Пиелонефрит. М., 1961.
ПытельА. Я. и ГолигорскийС. Д. Клин, мед., 1962, 11, 7.
ПытельА. Я. и Джавад-ЗадеМ. Д. Клин, хир., 1964, 1, 16.
ПытельА. Я. иЛопаткинН.А. Урология, 1962, 3, 23.
ПытельА. Я., Погорелко И. П. Основы практической урологии. Ташкент, 1964.
П ы т е л ь Ю. А. Урология, 1960, 6, 9.
Разенков И. П. Роль желудочно-кишечного тракта в межуточном обмене. Изд. АМН СССР. М., 1949.
С в е н т и ц к и й Г. А. Патогенез оксалурии у раненых и диетическая профилактика оксалатного нефролитиаза. Дисс, 1946.
С е р о в В. В. Урология, 1959, 3, 6.
СмеловскийВ. П. Мочекаменная болезнь. Куйбышев, 1965.
СмеловскийВ.П. Труды 3-й Всесоюзной конференции урологов (19—24 мая 1958 г., Тбилиси). Под ред. А. Б. Топчан. М., 1960, стр. 101.
Соболев И. И. и Воробцов В. И. Неотложная хирургическая урология. М., 1954, стр. 5—30 и 87—109.
Спасокукоцкий С. И. В кн.: Труды академика С. И. Спасокукоцкого. Т. II. М., 1948, стр. 201.
Стогов В. А. В кн.: Труды Государственного института усовершенствования врачей (юбилейный сборник, посвященный В. М. Мыш). Т. VI. М., 1936, стр. 28.
ТагировК. X. Мочекаменная болезнь у детей в Узбекистане. Ташкент, 1962.
Тальман И. М. Хирургия почек и мочеточников по материалу клиники проф. С. П. Федорова. Под ред. заслуженного деятеля науки С. П. Федорова. Л., 1934, стр. 5.
ТалышинскийК. Б. В кн.: Труды II Закавказского съезда хирургов (9—14 ноября 1935 г., Тбилиси). Т. II. Грузмедгиз, 1937, стр. 215.
ТарановичЛ. Е. Мед. журн. Белорусок. ССР, 1940, 3—4, 3.
ТеплицкийГ. Б. Урология, 1958, 2, 32.
Топ чан А. Б. и ХазановИ. О. Тер. арх., 1951, 28, 4, 62.
ТопчибашевМ. А. и ЗейналоваВ.А. В кн.: Труды 3-й Всероссийской конференции урологов (19—24 мая 1958 г., Тбилиси). Под ред. А. Б. Топчан. М., 1960, стр. 71.
УчугинаА. Ф. Урология, 1959, 4, 18.
Федорове. П. Хирургия почек и мочеточников. М.—Л., 1925, стр. 369.
ФинкельштейнС. И. Урология, 1959, 1, 56.
ФронштейнР. М. Избранные труды. Гл. V и VI. Под ред. Б. Д. Петрова. М., 1958, стр. 185—198 и 222—226.
Ф р у м к и н А. П. Нов. хир. арх., 193", 40, 1—2, 128.
ФрумкинА. П. В кн.: Опыт советской медицины в Великой Отечественной войне 1941—1945 гг. Т. XV. М., 1953, стр. 63.
ФрумкинА. П. Урология, 1957, 5, 17.
ХазановГ. А. Урология, 1963, 1, 58.
Хольцов Б. Н. Частная урология. В. V. Отдел VIII. Камни мочеполовых органов. Л., 1928, стр. 681.
X о м е н к о В. Ф. Урология, 1959, 3, 13.
Хоменко В. Ф. Урология, 1960, 4, 45.
Цулукидзе А. П. В кн.: Труды II Закавказского съезда хирургов (9—14 ноября 1935 г., Тбилиси). Т. II. Грузмедгиз, 1937, стр. 197.
Цулукидзе А. П. Хирургические заболевания мочевых и половых органов. М., 1955, стр. 260.
Цулукидзе А. П. В кн.: Труды 1-й Республиканской конференции урологов Азербайджана (16—19 ноября 1955 г.). Под ред. М. Б. Абиева. Баку, 1958, стр. 44.
Цулукидзе А. П. Очерки оперативной урологии. Изд. 2-е. Тбилиси, 1959, стр. 142.
Цулукидзе А. П. В кн.: Труды 3-й Всесоюзной конференции урологов (19—24 мая 1958 г., Тбилиси). Под ред. А. Б. Топчан. М., 1960, стр. 61.
Ч а й к а А. А. Нов. хир. арх., 1929, XVIII, 1—3, 42—46, 69—71.
Шабанов А. М. иНепомнящихЛ. М. Урология, 1962, 4, 49.
Шапиро И. Н. В кн.: Труды 1-й Республиканской конференции урологов Азербайджана (16—19 ноября 1955 г.). Под ред. М. Б. Абиева. Баку, 1958, стр. 23.
Шатин А. М. Урология, 1960, 5, 63.
ШебановаВ. А. Урология, 1962, 3, 20.
Ш е м е т о в В. Д. Урология, 1963, 2, 6.
Шмуклер Б. А. Фосфатурия (мочекаменный диатез). Л., 1941.
Шмуклер Б. А. В кн.: Труды 3-й Всесоюзной конференции урологов (19—24 мая 1958 г., Тбилиси). Под ред. А. Б. Топчан. М., 1960, стр. 108.
Шольская И. Б. Урология, 1959, 1, 39.
Эпштейн И. М. В кн.: Труды 1-й Республиканской конференции урологов Азербайджана (16—19 ноября 1955 г.). Под ред. М. Б. Абиева. Баку, 1958, стр. 124.
Эрямкин Г. И. Урология, 1955, 1, 75.
Эфендиев Н. Л. Урология, 1959, 4, 67.
Яковлев Н. А. Урология, 1958, 2, 35.
ЯмпольскийВ. Л. и Куренной Н. В. Урология, 1963, 3, 50.
Ярославцев С. А. Урология, 1957, 4, 3.
Ясинский Б. В. Урология, 1959, 4, 15.
AbeshouseG., Abeshouse В. a. D о г о с h ow L., J. Urol., 1961, 86, 1, 69.
Aboulker P., Thomas J., Tanr e t P. et S t e g A., J. d'Urol., 1962, 68, 3, 224.
AlkenC. E. u. Hermann G., Urol. internal,., 1957, 4, 6, 335.
A s о d a S., Acta Urol. (Japan.), 1959, 5, 9, 940.
A u v i g r e J., J. d'Urol., 1954, 60, 12, 884.
A u v г а у P., Acta Urol. Belgica, 1962, 30, 4, 592.
A n k e n m a n S. J. a. Ball our J. D., J. Urol., 1963, 89, 2, 145.
В а с k e г R. а. С о n e 11 у J. P., J. A. M. A., 1956, 100, 13, 1006.
BasagicE. u. Gasparovic, Ztschr. Urol., 1962, 55, 1, 7.
Battke H. u. Weiner W., Zbl. Chir., 1961, 1, 18.
BergmannM. u. Dictner W., Ztschr. Urol., 1962, 55, 5, 259.
BibusB., Ztschr. Urol., 1963, 56, 1, 1.
BodaschM., RossentalO. a. Murphy J., J. Urol., 1957, 78, 3, 216.
Boeminghaus H., Urologie. Operative Therapie. Klinik. Indikationen. 3 Auflage.
Bd 1. Munchen, 1960.
Borm Dietrich., Dtsch. med. Wschr., 1960, 85, 1880. BoshamerK., Ztschr. Urol., 1961, 54, 8, 483. BoshamerK., BiischerH. K., Cottet J., GagaA., HenningO., Handbuch
der Urologie. Bd X. Die Steinerkrankungen. Berlin, 1961.
В о у с e W. H., G a r v e у F. K. a. G a v e n G. E., J. A. M. A., 1958, 106, 13, 1577. В r a d s h a w H. H., В о у с е W. Н., М о о г е С. L. а. Н о 11 е m a n I. L., Surg. Gyn.
Obst., 1962, 115, 2, 171.
В г i n к m a n n W., Ztschr. Urol., 1955, 48, 6, 337. BrosigW.u. К о 11 w i t z A. A., Urologie, 1962, 4, 223. BrozinskiM., Dtsch. med. Wschr., 1961, 6, 255. BuchbergerH. G., Chirurg., 1960, 11, 515. BuntsR. C.,J. Urol., 1958, 79, 4, 733. Butt A. J., Treatment of urinary lithiasis. Springfield, 1960. ChwallaR., Ztschr. Urol., 1963, 56, 8/9, 421. Claereboudt E. et Vanwelkenhuyzen P., Acta Urol. Belgica, 1962, 30, 4,
596.
С о a t s E. C, J. Urol., 1956, 75, 5, 265. ComarA. E. а. С a r n e H. O., J. Urol., 1958, 79, 6, 911. DessJ.E., J. Urol., 1955, 73, 3, 445. Dulce H. J., Urologe, 1962, 4, 233. D u r a n d L., J. d'Urol., 1955, 61, 810.
E b b i n g h a u s. K. D. u. P r i e b e r S., Dtsch. med. Wschr., 1960, 24, 1045. E 11 i о t J. S. a. T о d d H. E., J. Urol., 1961, 86, 5, 484. FeyB.,LegrainM. et SifalakisZ.,J. d'Urol., 1958, 64,10—11, 613; Ibid. Pr. med.,
1957, 65, 17, 371.
F 1 i с к Н., Ztschr. Urol., 1958, 51, 11, 661. F I о t h H., Ztschr. Urol., 1962, 55, 11, S. 621. F о s t v e d t G. A. a. BarnesR. W., J. Urol., 1963, 89, 3, 329. Funf ack., Ztschr. Urol., 1959, 52, 4, 265. Frank H., Fortschr. Rontgenstr., 1961, 94, 1, 72. G а с a A. u. К 1 i t e 1 H., Ztschr. Urol., 1960, 53, 7, 353. G a s s e r G., Ztschr. Urol., 1960, 53, 4, 203.
Ge ge sy J., Ztschr. Urol., 1960, 53, 7, 399; Ibid., 1961, 54, 2, 103. Goormatigh N. et Boddaert J., Rapports et communic. IV Congres med. intern.
la lithiase urinaire d'Evian. Paris, 1955, p. 28. Gotzen G., Ztschr. Urol., 1962, 55, 10, 601. G r a h a m J. В., J. A. M. A., 1962, 181, 993. Gregoir W., Acta Urol. Belgica, 1962, 30, 4, 591. H a a s e H., Urol. Internat,. 1958, 7, 1—3, 96. H a j 6s E., Ztschr. Urol., 1958, 51, 4, 193; Ibid, 1960, 53, 1, 43. HartmannE., Ztschr. Urol., 1958. 51, 1, 63. H a r r i s о n A. K., Brit. J. Urol., 1960, 32, 4, 383. Hasselbacher K., Zbl. Chir., 1959, 84, 1, 20. H e i n t z K., Dtsch. med. Wschr., 1956, 16, 625. HennickeW., Ztschr. Urol., 1956, 49, 12, 727. H e p w о r t h R, G., Canad. J. Surg., 1963, 6, 3, 276. H e r m a n n G., Urol. Internat., 1958, 7, 1—3, 56. H i e n z s ch E., Ztschr., Urol., 1960, 53. 11, 621. HoflmannH. A., Am. J. Surg., 1960, 79, 4, 598. К a m i n a g a J., Japan. J. Urol., 1959, 50, 3, 191. KeutelH.J., Wien. med. Wschr., 1962, 1, 32. К i n g J. S. а. В о у с е W. H., Some aspects metabol. dis. man and animals, 1963, 104, 2,
571.
К б h e r F., Ztschr. Urol., 1962, 55, 5, 255. К oil wi t z A. A., Chirurg., 1960, 4, 182. Krebs W., Ztschr. Urol., 1959, 52, 4, 264. Kreie K., Ztschr. Urol., 1960, 53, 11, 605. L a n d e с к e r H. M., Urologe, 1962, 4, 219. Larsen J.u.PhilipJ., Urol. Internat., 1962, 13, 1, 53. Linke К. Н., Ztschr. Urol., 1962, 55, 7, 402. Ljunggren E., Ztschr. Urol.. 1961, 54, 11, 643. Lurz H., Ztschr. Urol., 1960, 53, 11, 613. Magasi P., Ztschr. Urol., 1962, 55, 1, 3. MatouschekE., Ztschr. Urol., 1963, 56, 1, 25. M а у о г G., Urol. Internat., 1962, 13, 5—6, 28. M i с h a I о v s к i E. u. M о d e 1 s к i V., Chirurg., 1961, 554.
М о n t H. L. u. N о w а к P., Ztschr. Urol., 1964, 57, 1, 3.
Mul wan e у W. P. a. H e n nig P. G., J. Urol., 1962, 88, 2, 145.
M u 1 w a n e у W. P. a. L о f 1 e r I., Ztschr. Urol., 1963, 56, 8/9, 445.
M u r p h у G. P. a. F i s с h b e i n R. H., J. Urol., 1961, 85, 6, 879.
M u s i a n i U., Urologia (Treviso), 1959, 3, 330.
N e v e u J., J. d'Urol. et Nephrol., 1963, 69, 12, 725.
Pecherssforfer M., Ztschr. Urol., 1963, 56, 3, 172.
P e p e r R., Ztschr. Urol., 1960, 53, 11, 593.
Petri W., Ztschr. Urol., 1960, 50, 10, 581.
PopoviciC. u. TeodorescuA. u. Matescu L., Ztschr. Urol., 1961, 54, 1, 37.
P о r t w i с h F., Uber das Milch-Alkali Syndrom. Ztschr. Urol., 1963, 56, 2, 61.
Prat V., Klinicky obraz polycystickych ledvin u dospelych. Praha, 1963.
Prince Ch., S a r d i n о P. a. V о 1 a n V., J. Urol., 1956, 75, 2, 209.
P r i e n E. L. a. W a 1 к e r B. S., J. A. M. A., 1956, 5, 335.
P u ig ve rt A., J. d'Urol., 1955, 61, 1, p. 63.
Q о i s t G., M u h s e n U. J. a. A 1 w a i d h M., Brit. J. Surg., 1963, 50, 223, 502.
Randall A., Ann. Surg., 1937, 105, 6, 1009.
Renyi-Vamos F., Das innere Lymphgefassystem der Organe. Budapest, 1960.
R i e s S. a. M a 1 a m e t M., J. Urol., 1962, 87, 5, 657.
Rosenstein P., Ztschr. Urol., 1961, 54, 1, 9.
Russell M., J. Urol., 1962, 88, 2, 141.
Schade H., Ztschr. klin. Med., 1922, 93, 1.
S с h e m i n s к у F., Ztschr. Urol., 1960, 53, 4, 202.
S chm e lz W., Ztschr. Urol., 1961, 54, 4, 231.
S с h о 1 z D. А. а. К 1 a t i n g F., Am. J. Med., 1956, 21, 75.
S i g e 1 A., Langenbeck's Arch. klin. Chir., 1958, Bd 289, Verhandlungen, S. 629.
Sorentino F., Ztschr. Urol., 1959, 52, 5, 281.
StaemmlerM., Ztschr. Urol., 1959, 52, 1, 3.
Steffens-KrebsD., Ztschr. Urol., 1961, 54, 12, 725; Ibid., 1958, 51, 11, 676.
S t о 11 H. G., Ztschr. Urol., 1959, 52, 10, 610.
S u b у H. J., J. Urol., 1952, 68, 1, 96: Ibid., 1959, 81, 3, 369.
Sucker J., Urologe, 1962, 4, 205; Ibid., 1963, 4, 229.
S z i b e r t h K., Ztschr. Urol., 1957, 50, 1, 38.
Глава четырнадцатая
Гидронефроз
и гидроуретеронефроз
Гидронефроз — стойкое и прогрессивно нарастающее расширение лоханки и чашечек, возникающее вследствие застоя мочи и нарушения иннервации и кровообращения почечной паренхимы.
Гидронефроз и гидроуретер бывают обусловлены препятствием, возникшим в результате органического или функционального поражения стенки мочевых путей (нарушение иннервации).
Термин „гидронефроз" был введен в 1841 г. для обозначения расширения лоханки,, которая содержала большое количество асептической мочи.
Многие исследователи пытались дать более правильное название этому весьма распространенному заболеванию: обратно застойная почка (Лихтен-берг, 1924), пиелоэктазия (С. П. Федоров, 1925) и др. В последние годы весьма широкое распространение получает термин „гидронефротическая трансформация". Однако и это название не вскрывает патогенетической сущности болезни, как и все предыдущие.
Краткий исторический очерк. Учение о гидронефрозе развивалось вначале очень медленно, и все знания об этом заболевании основывались лишь на секционных данных и весьма медленно внедрялись в практику. Скудные сведения о патологической анатомии и патогенезе этого заболевания, несовершенная иагностика, базировавшаяся вначале лишь на клинической симптоматологии, не давали возможности урологам успешно развивать учение о гидронефрозе, которое лишь в более поздние сроки, когда были внедрены в практику современные методы диагностики, значительно продвинулось вперед.
Начальный период развития учения о гидронефрозе характеризуется чисто описательными сведениями, полученными при вскрытии трупов. Приводится описание больших истонченных почек, наполненных бесцветной жидкостью, представлявших, по этим сведениям, одно- или многокамерные образования. В более поздние годы — начало XVIII века — уже начали появляться описания причин образования „застоя мочи в почках" или „водянки почки", как иногда называли это заболевание в литературе того времени. Этот период можно было бы назвать введением в учение о гидронефрозе. Истинным же рождением учения о гидронефрозе следует считать 40-е годы XVIII столетия, когда возникло определение болезни „гидронефроз" и началось экспериментальное и клиническое изучение этого заболевания.
За весьма короткий период было опубликовано много работ, основной целью которых было выявление роли нарушения проходимости мочеточника в возникновении гидронефроза. Опытами было доказано, что даже частичная непроходимость мочеточника после наложения на него лигатуры ведет к расширению вышележащих отделов мочевого тракта и к развитию гидронефроза. Большое внимание в экспериментах уделялось гистологическим изменениям в почках при развитии гидронефроза (С. А. Протопопов, 1896; В. К. Линдеман, 1896; И. О. Алексне, 1928; К. В. Караффа-Корбут, 1908, и др.).
С.А. Протопопов (1896) обнаружил в стенках нижнего и верхнего отделов мочеточника крупные нервные образования, являющиеся источником самопроизвольных движений мочеточника. В. К. Линдеман (1896), нарушая проходимость мочеточника, установил, что следствием этого может быть первичная атрофия почки или первичный гидронефроз со вторичной атрофией почечной паренхимы. Он первый указал на роль расстройства венозного и артериального кровообращения в почке как основной фактор развития атрофии почечной паренхимы при гидронефрозе. До настоящего времени не потеряли своего значения работы И. О. Алексне (1907), который, как и С. А. Протопопов, в стенке мочеточника обнаружил нервные образования, являющиеся источником его автономных движений. И. О. Алексне придавал большое значение в развитии гидронефроза нервной системе мочеточника, изменения которой могут привести к его дискинезии и последующему развитию гидронефроза. Исследования последних лет (Ю. А. Пытель, 1960) подтверждают возможность развития гидронефроза при дискинезии мочеточника, что особенно выражено бывает при нарушении проходимости в лоханочно-мочеточниковом сегменте. К. В. Караффа-Корбут (1908) своими опытами на животных доказал роль полного или частичного нарушения проходимости мочеточника в развитии гидронефроза. Его концепция о незначительной роли чрезмерной подвижности почки в развитии гидронефроза опровергает многочисленные исследования о роли нефроптоза в развитии гидронефроза и подтверждается клиническими наблюдениями.
Ограниченные технические возможности экспериментаторов той эпохи легли в основу механистического понимания патогенеза гидронефроза, но не остановили дальнейших поисков в вопросах этиологии гидронефроза, его патогенеза и методов лечения. Второй период был непродолжительным вследствие успешного развития других отраслей медицинской науки, физики и химии.
Внедрение в практику ретроградной пиелографии в значительной степени разрешило проблему прижизненной диагностики гидронефроза, а в некоторых случаях позволило установить и его причину. Однако, если этот метод давал в руки врачей данные о морфологическом состоянии чашечек, лоханки почки и мочеточника, то с применением экскреторной урографии стала возможной разработка многих вопросов гидронефроза.
По мере разработки и внедрения новых методов диагностики (анте-градная пиелография, почечная ангиография, изотопная ренография и др.) стала более точной как морфологическая, так и функциональная диагностика гидронефроза и более доступной расшифровка патогенеза отдельных его клинических форм. Большую роль в изучении патогенеза гидронефроза сыграли исследования А. Я. Пытеля (1950, 1959), посвященные лоханочно-почечным рефлюксам при этом заболевании.
Такие рефлюксы, как пиелоинтерстициальный, пиелотубулярный, субкапсулярный, ускоряют развитие склеротического процесса в почечной паренхиме и ее атрофии. Вопросам патогенеза гидронефроза посвящены многочисленные работы Fuchs (1931), А. А. Васильева (1930), Berlyne (1961), Harteroff (1948), Herdmann и Jaco (1950) и многие другие.
Появлением экскреторной урографии (1929) и других функциональных методов диагностики было определено начало третьего этапа в развитии учения о гидронефрозе — патофизиологического.
Использование функционально-морфологических методов диагностики позволило убедительно доказать, что гидронефротическая почка — орган функционирующий, способный в зависимости от стадии болезни сравнительно быстро восстановить свою функцию и обеспечить здоровье человеку, если она является даже единственной.
Изучению резервных возможностей почки при ее гидронефротической трансформации посвящено большое количество экспериментальных и клинических наблюдений.
Hinman (1945) убедительно доказал способность почки восстанавливать свою функцию после устранения причины гидронефроза. Им же было отмечено, что более быстрое восстановление функции наблюдается при более раннем устранении причины гидронефротической трансформации единственной почки. Наблюдения Hinman и исследования других авторов в этом вопросе явились обоснованием широкой пропаганды органосохраня-ющих оперативных методов лечения. Возможно поэтому история развития учения о гидронефрозе — это более всего история развития оперативного лечения гидронефроза, история развития реконструктивных операций на различных отделах мочеточника. Этому вопросу принадлежит одна из крупных глав оперативной урологии.
Проблема гидронефроза неоднократно обсуждалась на съездах и конференциях российских хирургов. Особенно большое значение в клиническом изучении гидронефроза сыграли работы С. П. Федорова и его учеников. С. П. Федоров уже в 1900 г. на I съезде российских хирургов выступил с докладом об оперативном лечении гидронефроза, а в 1923 г. он и его ученики в монографии „Хирургия почек и мочеточников" раскрыли суть многих вопросов этой актуальной до сегодняшнего дня проблемы. Вопросы диагностики гидронефроза, его лечения являлись предметом обсуждения многочисленных последующих съездов. В этой области работали С. И. Спасокукоцкий, который в 1908 г. произвел первую в России пластическую операцию на мочеточнике при гидронефрозе.
В.М. Мыш в своих лекциях обращал особое внимание на роль выявления клинического проявления гидронефротической трансформации при определении диагноза гидронефроза и особенно лечебной тактики. Он указывал на недопустимость слепого доверия данным ретроградной пиелографии.
Несмотря на то, что практическое применение консервативных операций при гидронефрозе, или, как их теперь принято называть, органосо-храняющих, началось с конца прошлого столетия, вопрос этот не потерял своей актуальности до настоящего времени. Еще далеко не все авторы признают необходимость широкого использования пластических операций с целью сохранения органа. Подобное положение явилось результатом того, что в первые годы внедрения в практику реконструктивных операций их применяли в далеко зашедших случаях гидронефротической трансформации, когда функция почки была полностью потеряна, и авторы имели большой процент неудачных операций.
Оперативному лечению гидронефроза посвящены работы последних лет Я. Кучера „Хирургия гидронефроза и уретерогидронефроза" (1963) и С. Д. Голигорского и А. М. Кацыфа (1966) „Хирургия лоханочно-моче-точникового сегмента".
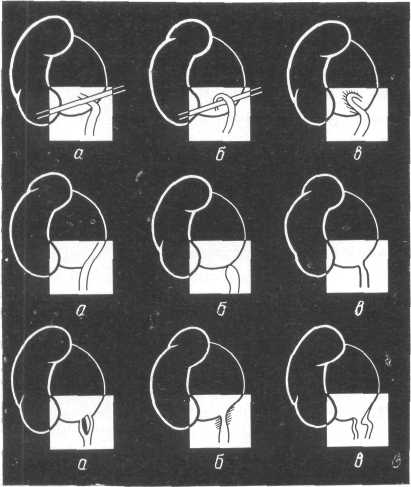
Рис. 164. Схема нарушения причин проходимости в лоханочно-мочеточпиковом сегменте.
Весьма большой проблемой современного изучения гидронефроза является вопрос о его комбинации с пиелонефритом. Актуальность этого пока еще не разрешенного вопроса несомненна: результаты органосохраня-ющих операций находятся в полной зависимости от степени и активности воспалительного процесса в почке и весьма нередко блестяще произведенная операция, обеспечивающая достаточно полный отток мочи из почечной лоханки, заканчивается нефрэктомией в связи с активизацией латентно протекавшего пиелонефрита. Именно поэтому имеет существенное значение разрешение вопросов предоперационной подготовки и длительности послеоперационной антибактериальной и противовоспалительной терапии. Не могут считаться разрешенными и вопросы замены мочеточника петлей кишки, а также проблема создания мочеточника из синтетических материалов.
Статистические данные заболеваемости. Большое количество причин гидронефроза определяет его сравнительно большую частоту. По данным большинства авторов, гидронефроз в 1,5 раза чаще наблюдается у женщин, чем у мужчин (А. Я. Абрамян), и преимущественно в возрасте до 45—50 лет. Наибольшая частота, по данным клиники II МГМИ, падает на возраст от 25 до 35 лет. Двусторонний гидронефроз, по данным нашей и других клиник, явление весьма редкое. Из 76 оперированных в нашей клинике за 1965—1966 гг. по поводу гидронефроза лишь у 6 имелся двусторонний процесс. А. Я. Абрамян наблюдал двусторонний гидронефроз в 9% среди всех больных гидронефрозом.
Этиология и патогенез. Как и при многих других заболеваниях, этиология и патогенез гидронефроза тесно переплетаются между собой, и в известной степени патогенез отдельных форм гидронефроза зависит от их этиологических факторов. Существует весьма большое количество причин гидронефроза и уретерогидронефроза. Причина, вызывающая гидронефроз, далеко не всегда может быть поводом к возникновению уретерогидронефроза (добавочный сосуд и пр.).
Этиологическими факторами гидронефроза могут быть различные изменения в лоханочно-мочеточниковом сегменте — как следствие экс-трауретеральных причин, так и возникающих в толще самой стенки этого сегмента (рис. 164). Изменение лоханочно-мочеточникового сегмента вызывает нарушение динамики лоханки почки. Однако не следует думать, что механическая причина расстройства пассажа мочи всегда находит себе подтверждение анатомическими нарушениями в лоханочно-мочеточниковом сегменте. В некоторых случаях при макроскопическом анализе состояния лоханочно-мочеточникового сегмента не удается найти его сужения. Тогда остается считать причиной гидронефротической трансформации функциональные нарушения динамики лоханочно-мочеточникового сегмента.
Добавочные сосуды почки, по данным Я. Кучера, А. Я. Абрамяна, А. П. Фрумкина и др., являются наиболее частой причиной развития гидронефроза. Артерия и вена являются мощным, постоянно меняющимся по своей интенсивности раздражителем лоханочно-мочеточникового сегмента. Эти раздражения и в известной степени давление на стенку мочеточника вызывают усиленное сокращение этого отдела при значительно нарушенном в нем питании. Весьма нередко удается видеть странгуля-ционную борозду от давления артерии на мочеточник, а при резекции этого отдела и гистологическом исследовании — атрофию всех его слоев и замещение их соединительной тканью. Таким образом, аберрантные сосуды нижнего полюса почки часто вызывают вначале пер-систирующее нарушение пассажа мочи вследствие дискинеза в лоханоч-но-мочеточниковом сегменте, а в последующем приводят к рубцовому его сужению.
Значительно реже сдавление лоханочно-мочеточникового сегмента наблюдается при неправильно проходящей по передней поверхности лоханки передненижней ветви почечной артерии. В клинике мы наблюдали 2 больных с такой причиной гидронефроза, а у 2 больных сдавление лоханочно-мочеточникового сегмента наступило вследствие варикозного расширения мочеточниковой вены.
Второе по частоте место среди причин гидронефрозов занимают различной формы перегибы мочеточников. Однако следует подчеркнуть, что для развития гидронефроза имеют значение лишь фиксированные перегибы мочеточника соединительнотканными тяжами. Чаще всего перегибы мочеточников развиваются попутно с воспалительными процессами в окружающих тканях. Грубые перегибы мочеточников представляют серьезное механическое и функциональное препятствие для полного оттока мочи из лоханки.
Из пороков развития мочеточника и лоханки, влекущих за собой развитие гидронефроза, следует указать прежде всего на клапан между лоханкой и мочеточником. Клапан образуется из дубликатуры слизистой оболочки мочеточника и часто бывает весьма отчетливо выражен. Однако следует указать, что и различимые лишь под микроскопом клапаны могут явиться серьезным препятствием для оттока мочи из лоханки. Серьезным] препятствием для оттока мочи из лоханки может быть высокое от-хождение мочеточника от лоханки и образуемая при этом шпора. Следует согласиться с мнением Я. Кучера (1963), считающим этот вид препятствия самостоятельным. Подобное соотношение между лоханкой и мочеточником возникает в результате неравномерного увеличения лоханки за счет нижнего сегмента. Устье мочеточника при этом подымается вверх и образуется шпора, которая является дополнительным механическим фактором, нарушающим отток мочи из почечной лоханки, особенно в поздних фазах развития болезни.
Типичным результатом порока развития мочеточника и развивающегося в результате этого гидронефроза является сегментарная нейро-мускулярная аплазия в пельвиоуретеральной области. В результате подобной аномалии в одном участке образуется выпячивание, которое является не только механическим препятствием, но и функциональным. При подобном заболевании между движениями лоханки и мочеточником нет координации и отсутствует активное изгнание мочи лоханкой в мочеточник. Пассаж мочи осуществляется лишь под действием гидростатического давления.
Нет надобности говорить о том, что любое препятствие в мочеточнике или вне его просвета, но его сдавливающее (камень, экстра- или интра-уретеральная опухоль и пр.) может привести к образованию гидронефроза. Однако независимо от первопричины гидронефроза при тщательном анализе всех сторон развития болезни всегда удается отметить большую или меньшую комбинацию механических препятствий для оттока мочи через лоханочно-мочеточниковый сегмент с одной стороны между собой и в то же время с функциональными расстройствами динамики.
Долгие годы существовало мнение о том, что нефроптоз является наиболее частой причиной гидронефротической трансформации. Однако анализ литературных данных и наблюдений клиники подтверждает мнение К. В. Караффа-Корбута (1908), Я. Кучера (1963) и Couvelaire (1956) о том, что гидронефроз при нефроптозе если и возникает, что бывает крайне редко, то только как основное заболевание, а не следствие патологической подвижности почки.
А.Я. Абрамян (1956) объясняет сравнительно редкое развитие гидронефроза при нефроптозе мощными перистальтическими движениями мочеточника. Анализ уретерограмм, произведенных в вертикальном и горизонтальном положении больного в клинике II МГМИ, убеждает в другом факте: мочеточник, если он не имеет спаек, с перемещением почки вниз при вертикальном положении больного значительно сокращается по своей длинной оси. Поэтому в течение многих лет отсутствуют перегибы мочеточника. Последние возникают при нарушении тонуса мочеточника в связи с нервно-мышечными расстройствами вследствие воспалительного процесса в его стенке или в окружающей клетчатке. Только при этих условиях могут образоваться улиткообразные фиксированные перегибы, способные вызвать развитие гидронефроза.
Аномалия почки (удвоенная или подковообразная почка, дистопирован-ная почка или гипопластическая почка и другие виды), по мнению некоторых клиницистов и экспериментаторов, является самостоятельной и частой причиной развития гидронефроза. Анализ опубликованных случаев аномалий почек позволяет отвергнуть это мнение и согласиться с А. Я. Абрамяном, Я. Кучером и др. в том, что частота гидронефротической трансформации аномалий почки не превышает частоту гидронефроза правильно развитой почки. Однако нет сомнений в том, что неправильное положение почки, удвоение мочеточника и лоханки, большее количество сосудов и другие патоанатомические варианты развития создают более благоприятные условия для стаза мочи в лоханке почки; гемодинамические сдвиги в аномальной почке бесспорно возникают раньше и бывают значительнее выражены, чем в нормальной почке. Изменяется и динамика Лоханки и мочеточника вследствие тех или иных патоанатомических условий. Все эти анатомические отклонения являются благоприятным фоном для развития воспалительного процесса как в самой почке и мочевых путях, так и в паранефральной клетчатке. Следствием воспалительного процесса являются образование стриктур, перегибов мочеточника, нарушение трофики его стенки и нервно-мышечные изменения с последующим нарушением его активно всасывающей деятельности и застоем мочи в лоханке. Финалом этих изменений является гидронефротическая трансформация.
Таким образом, совершенно очевидно, что анализ этиопатогенеза гидронефроза невозможен без учета причин, вызывающих изменения внутри-лоханочного давления вследствие нарушения пассажа мочи, т.е. факторов, конечным итогом влияния которых является гидронефротическая трансформация.
Изучение патогенеза гидронефроза в эксперименте и клинике вызвало интерес к последовательности развития болезненного процесса в почке, первопричине атрофии почечной паренхимы, функциональным особенностям гидронефротической почки и другим вопросам, имеющим теоретическое и практическое значение. Все эксперименты по изучению патогенеза гидронефротической трансформации почки основывались на создании искусственного застоя мочи в почечной лоханке путем кратковременной или длительной перевязки мочеточника.
Вопрос о том, как долго почка секретирует мочу после перевязки мочеточника, вызывает большие споры. Hinman (1945) и другие авторы полагают, что при гадронефрозе процесс секреции и реабсорбции все время сохраняется.
Некоторое отставание резорбции от секреции мочи обусловливает накопление содержимого почечной лоханки.
Persky, Storaasli, Austen (1955) показали, что в ток крови из закупоренной почечной лоханки реабсорбировались изотопы натрия, йода и коллоидного золота.
Idbohrn (1956), изучая при помощи экскреторной урографии функцию гидронефротической почки после уретеростомии, показал, что по прекращении мочевого стаза спустя неделю у всех, а спустя 2—3—4 недели у половины животных почечная экскреция контрастного вещества была хорошей. При стазе мочи, продолжавшемся более 5 недель, по дренажной трубке выделялось только несколько капель мочи, а по истечении 6 недель функция почки у кроликов прекращалась и экскреции контрастного раствора не было.
А. Я. Пытель (1959) считает, что при гидронефрозе мочевая секреция вначале не изменяется, а затем несколько сокращается; происходит это из-за повышения внутрипочечного давления, вследствие чего понижается и замедляется фильтрация мочи в мальпигиевых клубочках. Часть сецер-нированной мочи вновь реабсорбируется из почечной лоханки и даже из мочеточника, что подтверждается исследованиями Maluf и Helpert (1956).
В начальных стадиях гидронефротической трансформации при стазе мочи в лоханке наступает гипертрофия мускулатуры лоханки и чашечек. К постепенной гипертрофии спиральной мускулатуры чашечек приводит резко повышенное давление мочи на сосочек и форникальную зону по сравнению с секреторным давлением в мочевых канальцах; это создает трудности нормальному выделению мочи из сосочков в почечную лоханку, компенсируемые уменьшенной секрецией мочи. Однако это относительное равновесие в функции почки продолжается недолго. Рабочая гипертрофия мышечных элементов малых чашечек и лоханки сменяется их истончением и разволокнением (Hinman, 1945; КШ, 1957; А. П. Фрумкин, 1962), что нарушает отток мочи из них и приводит к дилятации почечной лоханки и чашечек с последующей атрофией сосочков и почечной паренхимы. КШ (1957) указывает, что расширение почечной лоханки после обструкции является моментом, предшествующим поражений) почки. Однако с этим выводом вряд ли можно согласиться, ибо одним из важных моментов в возникновении гидронефроза является задержка выведения мочи из функционально деятельных участков почки, что наблюдается даже при кратковременных повышениях внутрилоханочного давления, когда еще нет расширения лоханки. Высокое давление в почечной лоханке вызывается, по мнению А. Я. Пытеля (1950), не только поступающей в нее из канальцев мочой, но и сокращением мускулатуры чашечек, особенно форникального и чашечного сфинктеров, значительной гипертрофией которых в начальных стадиях гидронефроза объясняются боли. Сокращения этих гипертрофированных сфинктеров способствуют нарушению целости форниксов, что облегчает поступление мочи из лоханки в тубулярную систему. А. Я. Пытель (1950) придает большое значение мышечной системе чашечек и лоханки в оттоке мочи и отечной межтканевой жидкости по лимфатическим и венозным сосудам. Повышение внутриканальцевого давления, а вместе с ним и венозного способствует проталкиванию большого количества жидкости в ток крови (Gottschale, Mylle, 1959).
Экспериментальные исследования Fuchs (1931), А. А. Васильева (1930), Hinman (1936) и А. Я. Пытеля (1959) показали, что уже спустя 24 часа после обструкции мочеточника начинается медленная атрофия почечных пирамид вследствие сдавления их трансфорникальным отеком; сосочки постепенно уплощаются. Через 6—10 дней атрофия пирамид достигает большой степени; сосочки постепенно делаются вогнутыми. К концу второй недели исчезают форниксы, стенки чашечки и лоханки в области форникса становятся более пологими, округлыми. При всем этом бертиниевы колонны остаются неизмененными. Укорачиваются или медленно исчезают петли Генле. Увеличивающееся давление жидкости в почечной лоханке приводит к постепенной облитерации пирамид, а также сдавлению бертиниевых колонн. Повреждение мальпигиевых клубочков в это время небольшое. Некоторые клубочки функционируют с высоким фильтрационным давлением, другие — со слабым. Поэтому гломерулярный фильтрат, продуцированный одной частью паренхимы, где клубочковая фильтрация еще обеспечивается высоким кровяным давлением, достигает лоханки, а оттуда поступает в собирательные канальцы той части паренхимы, где клубочки еще функционируют, но при сниженном кровяном давлении. Большая разница в кровяном давлении двух таких групп клубочков содействует обратной фильтрации мочи в клубочки низкого давления.
В связи с исчезновением форниксов происходит расширение просвета собирательных канальцев, облегчающее поступление мочи из лоханки в тубулярную систему. Ток мочи все время не прекращается, а пиеловеноз-ный рефлюкс и лимфатическая реабсорбция замещаются гломерулярной обратной фильтрацией. Циркулирующая теперь в почке моча идентична клубочковому фильтрату вследствие обширной атрофии тубулярного аппарата (А. Я. Пытель, 1959). Опытами Hinman (1945), Sigel (1962), Kucera (1963) показано, что присоединяющееся к этим изменениям перемежающееся повышение внутрибрюшинного давления постепенно приводит к расстройству циркуляции в мальпигиевых клубочках и постепенному их разрушению (чаще к 6—8-й неделе от начала мочеточниковой обструкции). В дальнейшем при полной обструкции мочеточника и в меньшей мере при его частичной обструкции происходят множественные форникальные разрывы, в результате чего обеспечивается свободный ток мочи в почечные интерстициальные пространства, в кровеносную и лимфатическую систему. Внутрилоханочное давление при обструкции мочеточника, равное в среднем 70 мм рт. ст., достигая коркового слоя и бертиниевых колонн, значительно снижается и уже не может служить причиной нарушения ни гло-мерулярного кровотока, ни кровотока через постгломерулярные капилляры. Несмотря на это, повышенное внутрипаренхиматозное давление нарушает кровоток в сосудистых колоннах мозгового вещества почки, таким образом создаются условия для атрофии пирамид. Атрофия почечной паренхимы вследствие длительного трансфорникального отека особенно заметна в пирамидах, тогда как в корковом слое и бертиниевых колоннах она менее выражена. Нарушение кровообращения в кортикальных и медуллярных капиллярах приводит к общему нарушению капиллярного кровообращения в паренхиме, кислородному голоданию и нарушению тканевого обмена, способствуя тотальной атрофии коркового вещества почки.
Sigel (1962) полагает, что гидронефротическая трансформация развивается в две фазы: в первой атрофируется мозговое вещество, во второй — корковое. В дальнейшем наступают изменения кровеносной системы почки, чашечек и постепенно развивается картина локального гидронефроза. При атрофии коркового слоя почки и облитерации сосудов выявляется ее пирамидальное строение, аналогичное тому, какое имеет место в период эмбрионального развития почки. Kucera (1963) утверждает, что повышенное давление в лоханке, сдавливая канальцы, повышает внутрипочечное давление. Повышенное внутрипочечное давление вызывает все большее расширение системы чашечек, которые сдавливают кровеносные сосуды почки и ее главные сосудистые стволы. Кровеносные капилляры облитерируются, большие сосуды истончаются, в итоге кровообращение почки страдает в целом. В результате повышения внутрилоханочного давления происходит сдавливание сосудов почечной ножки напряженной, расширенной лоханкой гидронефротической почки.
Сосудистый аппарат почки в условиях гидронефротической трансформации претерпевает значительные изменения. Так, Altschul и Fedor (1953) показали, что кортикальные сосуды при гидронефротической перестройке становятся более извитыми, тогда как интерлобарные выпрямляются. При этом наблюдаются нарушение эластической мембраны внутрипочечных сосудов, а также пролиферация эндотелия. Гиперэластоз артерий может способствовать усилению их тонуса, и это позволяет высказать предположение, что каждая гидронефротическая почка может являться потенциальным источником нефрогенной гипертонии. Однако Anderson (1963) полагает, что гидронефроз сам по себе не может явиться причиной гипертонии и поэтому такую почку безопасно сохранить. По его мнению, ишемия служит агентом, разрушающим почку, поэтому при операциях на почках каждый сосуд, питающий почку, должен быть сохранен. Рассечение добавочных сосудов может повлечь развитие гипертонии.
Idbohrn (1956) с помощью ангиографии изучал калибр почечных артерий при гидронефротической трансформации у животных. Он обнаружил, что уменьшение калибра почечной артерии наполовину приводило к уменьшению кровотока через нее более чем на 50% нормы. В течение первых 2 недель после лигирования мочеточника уменьшение калибра почечной артерии повышало скорость деструкции паренхимы. На 3-й неделе стаза мочи гистологические изменения стали развиваться быстрее, нежели можно было предположить по последующей быстроте уменьшения калибра почечной артерии. При гистологическом исследовании были установлены утолщение интимы почечной артерии (6ej тромбообразования) и изменения в эластической мембране сосудов. В процессе гидронефротических изменений наиболее стойкими оказались сосуды клубочков. Околоканальцевые сосуды были вовлечены в интерстициальный процесс (отек—фиброз—гиали-ноз), вследствие чего почечные канальцы постепенно лишались кровоснабжения и атрофировались. Таким образом, прогрессирующее уменьшение калибра артерий приводит к прогрессирующим гистологическим изменениям в почечной паренхиме.
Артериографические исследования показывают, что при гидронефрозе сосудистые изменения сопровождаются уменьшением объема функционирующих участков паренхимы. Так, Chiaudano в 1958 г., а Н. А. Лопаткин в 1960 г. установили, что в начальных стадиях гидронефротической трансформации поражается только мозговой слой; при этом уменьшается количество мелких сосудов. Отдельные сосуды приобретают дугообразную форму, более крупные стволы становятся ригидными, количество их уменьшается, они истончаются, располагаются вокруг образовавшихся в почке полостей.
Большая роль в патогенезе гидронефроза, в частности в развитии компенсаторных механизмов, обеспечивающих сохранение почки как экскреторного органа, принадлежит ее лимфатической системе. Babies и Renyi-Vamos (1957), Magasi и Matyus (1954) нашли увеличение количества гиста-мина в гидронефротических почках, чем объясняют повышение проницаемости капилляров, в результате чего в интерстициальную ткань почки проникает большое количество белка из крови. Вследствие этого развивается отек и наступает компенсаторное расширение лимфатических сосудов, участвующих в резорбции мочи.1Еще Kaierling и Soostmeyer в 1939 г. своими экспериментами показали исключительное значение в патогенезе гидронефротической трансформации нарушенного лимфатического дренажа.
При стазе мочи происходит увеличение просвета лимфатических сосудов почки вследствие переполнения их большим количеством жидкости, проникшей из почечной лоханки в интерстициальную ткань в результате форникальной реабсорбции и рефлюкса. Эта отечная жидкость отводится лимфатической системой и всасывается тубулярным аппаратом почки. Winkel (1964) с помощью радиоактивных изотопов изучал экспериментальный гидронефроз на белых крысах и установил, что чем длительнее была обструкция мочеточника, тем больше йодгиппурана накапливалось в почке. Вводимое животным коллоидное золото всасывалось интерстициальной тканью и отводилось лимфатическими путями, тогда как здоровыми почками, как известно, этот препарат не выводится, вследствие чего каналь-цевая реабсорбция радиоактивного золота исключалась. В результате токсического действия мочи наступает гибель эпителия канальцев и интерстициальной ткани, что приводит к склеротическим изменениям. До той поры, пока еще лимфатическая система функционирует удовлетворительно, гибель почечной ткани предотвратима. Там же, где лимфатические сосуды почки при гидронефрозе не обеспечивают надлежащего оттока межтканевой жидкости, быстро прогрессирует почечная атрофия.
Исследования Ю. А. Пытеля (1960) показали, что при далеко зашедших стадиях гидронефроза, вызванного обтурационным фактором, в нервах лоханки, чашечек и мочеточника возникают дегенеративные изменения, аналогичные тем, какие наблюдаются при асептическом нефролитиазе. Эти изменения объясняются высоким внутрилоханочным давлением и как следствие этого развитием гипоксемии, которая приводит к дегенеративным изменениям в нервных элементах, что в свою очередь способствует еще большему снижению тонуса и прогрессированию гидронефроза. Нарушение нервных связей почечной лоханки и чашечек с сосудами и паренхимой почки наряду с затрудненным оттоком мочи способствует прогрессирующему развитию в ней атрофических процессов и снижению функции.
Schuck, Andysek и Andryskow (1962) изучили распределение Na24 в почке при экспериментальном гидронефрозе и установили, что через 24 часа после начала возникновения гидронефроза уже наступало нарушение его распределения. Они объясняют это: 1) уменьшением фильтрации в почечных клубочках одновременно более низкой индукцией Na24 в медулярном слое почки; 2) нарушением активного транспорта Na24 из петель Генле в интерстициальную ткань и 3) деформацией сосочков и в связи с этим деформацией морфологической основы системы противотока.
Продукция мочи и поступление ее в почечную лоханку, а также некоторая реабсорбция гломерулярного фильтрата происходят даже при далеко зашедшей гидронефротической трансформации. В поздней стадии гидронефротической трансформации после исчезновения форниксов реабсорбция гломерулярного фильтрата происходит путем тубуловенозного рефлюкса. Все это показывает, что лоханочно-почечные рефлюксы играют важную роль в патогенезе гидронефротической трансформации органа.
Эти компенсаторные механизмы приводят к снижению максимального мочевого давления и тем способствуют сохранению почечной секреции (А. Я. Пытель, 1949).
Только благодаря лоханочно-почечным рефлюксам почка как экскреторный орган сохраняет свою функцию. Однако в процессе гидронефротической атрофии не только уменьшается секреция, но и меняется состав мочи. В начальных стадиях в моче уменьшается содержание солей, мочевины и других азотистых веществ. Содержимое гидронефротической почки становится все менее концентрированным, в нем обнаруживают белок, элементы крови, обломки эпителиальных клеток, следы мочевины и мочевой кислоты.
Большой интерес представляет определение причин существующих различий в сроках развития стадий гидронефроза. Достоверно установлено, что полная окклюзия просвета лоханочно-мочеточникового сегмента приводит к быстрому развитию гидронефроза. Однако ликвидация препятствия в ранние сроки болезни способствует восстановлению полной функционально-морфологической ценности почки. Иначе обстоит дело в случаях гидронефроза, осложненного пиелонефритом. Последний, поражая все структурные элементы почечной ткани и стенки лоханки, приводит к рубцеванию ткани почки, к замещению ею мышечных элементов лоханки. Подобные морфологические изменения в почке значительно ускоряют процесс гидронефротической трансформации и делают его необратимым. В этих случаях ликвидация причины гидронефроза лишь останавливает дальнейшее развитие гидронефротической трансформации и создает благоприятные условия для борьбы с пиелонефритом.
В тех случаях, когда препятствие для оттока мочи располагается в нижних отделах мочеточника, развивается комбинированное заболевание —уретерогидронефроз. Это препятствие может быть механическим и носить функциональный характер. В последнем случае уретерогидронефроз возникает в связи с расстройством динамики мочеточника и рецидивирующими везико-уретеральными рефлюксами.
При расположении механического препятствия в пузырном или пред-пузырном отделах мочеточника вышележащие его отделы постепенно расширяются.
Этот процесс развивается весьма медленно и всегда сопровождается изменением динамики мочеточника — уменьшается амплитуда сокращений и их частота. С течением времени мочеточник превращается в атоническую трубку, которая после устранения препятствия очень медленно восстанавливает свои функциональные свойства. Если препятствие не устранено, заболевание распространяется на вышележащие отделы мочевых путей и постепенно развивается уретерогидронефроз.
Без механического препятствия в мочеточнике уретерогидронефроз развивается из „везико-уретерального рефлюкса", а позже — из „везико-ренального рефлюкса" (Я. Кучера, 1963). Возникновение рефлюкса связано с повышенным внутрипузырным давлением. Подобное патологическое состояние может наблюдаться при хронической задержке мочи в мочевом пузыре, при так называемой атонии мочевого пузыря или при рубцово сморщенном мочевом пузыре.
Несколько изолированно от этих механизмов развития уретерогидро-нефроза стоит возникновение гидронефроза в связи с мегауретером. Не рассматривая причин возникновения мегауретера, так как этот вопрос относится к области аномалий развития, здесь следует лишь указать, что гидронефроз в связи с мегауретером имеет ранее описанный патогенез развития, но сам патологический процесс развивается очень медленно.
Таким образом, в процессе гидронефротической трансформации почка претерпевает функциональные и в первую очередь морфологические изменения.
Патологическая анатомия гидронефроза в значительной степени зависит от стадии болезни. В начальных стадиях почка, претерпевающая гидро-нефротическую трансформацию, внешне мало отличается от здорового органа как в случаях внутрипочечного расположения лоханки, так и при внепочечной ее локализации. Основные изменения в ранних стадиях болезни бывают выражены со стороны лоханки и чашечек. Под действием повышенного внутрилоханочного давления увеличивается емкость чашечек и в значительной степени изменяется их конфигурация — они становятся круглыми, шейка их укорачивается и увеличивается в поперечном размере. Подобная картина чаще наблюдается при внутрипочечном расположении лоханки и носит название гидрокаликоза. Одновременно с увеличением размеров бокалов идет увеличение емкости лоханки и при этом более быстрое в случаях внепочечного ее расположения. Таким образом, к гидро-каликозу присоединяется пиелозктазия, что в сумме уже может быть названо гидронефрозом. При гидронефротической трансформации почка продолжает продуцировать мочу, преимущественное количество которой всасывается обратно, но с течением времени абсорбция мочи начинает отставать и количество ее в лоханке медленно увеличивается. В ответ на это гипертрофированная стенка лоханки начинает постепенно истончаться в связи с прогрессивной атрофией гладких мышечных волокон и заменой их соединительной тканью; атрофируются нервные окончания, облитери-руются сосуды лоханки, как кровеносные, так и лимфатические. Таким образом, чем длительнее существует препятствие для оттока мочи и повышенное внутрилоханочное давление, тем более лоханкой бывает потерян ее нервно-мышечный тонус. В конечных стадиях гидронефроза лоханка представляет собой тонкостенный дряблый мешок, стенка которого в основном состоит из грубоволокнистой соединительной ткани. В тех случаях, когда препятствие располагается ниже лоханочно-мочеточникового сегмента, скапливающаяся в мочеточнике под повышенным давлением моча над препятствием вызывает аналогичные изменения в его стенке. С течением времени гипертрофия стенки мочеточника сменяется атрофией его мышечных волокон, собственных нервных элементов; облитерируются ка-вернозноподобные образования, в значительной степени страдает лимфо-и кровообращение мочеточника. Все эти изменения приводят к потере тонуса и мочеточник превращается в полую соединительнотканную трубку с перехватами в области границ цистоидов, перегибами, в многочисленных спайках с окружающими тканями. Иногда мочеточник достигает диаметра 2—4 см. В таком мочеточнике нет движений и маловероятно их восстановление после ликвидации препятствия. Большие изменения верхних мочевых путей уже в самых начальных стадиях способствуют повышению внутрилоханочного давления. Прогрессивно растягивающаяся лоханка оттесняет почечную паренхиму к периферии. Таким образом, паренхима оказывается зажатой между фиброзной капсулой и лоханкой. Прогрессивно повышающееся гидростатическое давление на почечную папиллу ведет к ее уплощению. Сдавливаются форникальные вены и артериолы и в значительной степени нарушается крово- и лимфообращение в почечной ткани, прежде всего в корковом слое почки. По мнению В. К. Линдемана, А. Я. Абрамяна, Я. Кучера, Doss (1947) и др., нарушение крово- и лимфообращения в почечной ткани имеет первостепенное значение в развитии атрофии почки.
Повышение давления в лоханке и чашечках сравнительно быстро распространяется и на канальцевую систему почки и приводит к повышению внутрипочечного давления. Канальцы расширяются, а выстилающий их уротелий постепенно теряет свою функцию. Вследствие указанного при гидронефротической трансформации почки прежде всего страдает тубуляр-ная функция. Таким образом, два фактора приводят к нарушению кровообращения — внутрилоханочное и внутричашечное повышенное давление и высокое внутрипочечное давление. При этом, по мнению Линдемана, наибольшее значение имеет нарушение артериального кровообращения, которое не компенсируется коллатералями, как это происходит в венозной системе почки. Данные хронометрированной серийной артериографии почки подтверждают это положение и позволяют обнаружить значительное замедление кровотока в артериальной сети почки (Н. А. Лопаткин, 1961). Вследствие такого количественного (анатомического) и качественного (динамического) нарушения кровообращения понижается снабжение почки кислородом, уменьшается клубочковая фильтрация. Не менее грубый склеротический процесс происходит и в межуточной ткани почки. Склероз в межуточной ткани развивается вследствие постоянно действующего при гидронефротической трансформации компенсаторного механизма — пиелоренальных рефлюксов. Защищая почку от резкого повышения внутрилоханочного давления, пиелоренальные рефлюксы приводят к пропитыванию межуточной ткани мочой. Вследствие этого под действием высвобождающегося гистамина увеличивается проницаемость капилляров (Я. Кучера, 1963) и из крови межуточная ткань пропитывается белками плазмы; макроскопически почка выглядит несколько гиперемированной и отечной. Отток отечной жидкости по лимфатической системе и всасывание ее тубулярным аппаратом почки в должной мере не осуществляются, что еще более угнетает функцию канальцев. Вследствие этого межуточная ткань почки превращается в рубцовую соединительную, которая постепенно замещает почечную паренхиму.
Артериография удаленных почек и прижизненная серийная ангиография позволили обнаружить сужение магистральной почечной артерии и облитерацию, а также и запустевание ее ветвей. При этом чем глубже выражен процесс атрофии, т. е. чем более поздняя стадия гидронефроза, тем меньше артерий, тем уже их просвет, тем дальше отстоят ветви одна от другой. При конечной стадии гидронефроза почка бывает резко увеличена в размерах, бугриста; корковый слой ее очень тонкий. Гидронефроз содержит большое количество мочи низкого удельного веса в связи с малой концентрацией в ней солей мочевины и других азотистых соединений. На разрезе почка представляет собой многокамерную полость; камеры сообщаются между собой через лоханку. В перемычках, разделяющих одну камеру от другой, обычно проходят дугообразные артерии.
Классификация гидронефроза. Многие клиницисты предлагали свою классификацию, однако ни одна из них не удовлетворяет полностью требованиям клиники. Некоторые из классификаций построены с учетом этиологических особенностей, тогда как в основу других положен патогенетический признак. Прав Я. Кучера, считающий вопрос классификации гидронефроза очень трудным и пока еще не разрешенным. В гидронефрозе механического генеза всегда имеются в той или иной степени признаки расстройства уродинамики и наоборот. В развитии врожденных гидронефрозов принимает участие фактор как динамический, так и механический. Не отрицая критических замечаний Я. Кучера по поводу трудностей классифицировать гидронефроз по клинико-этиопатогенетическим признакам, нельзя и полностью отказаться от классификации этого заболевания. Наиболее приемлемым с практической точки зрения и не лишенным обоснования будет подразделение гидронефроза на две группы.
1. Первичный, или врожденный, гидронефроз, развивающийся вследствие какой-либо аномалии верхних мочевых путей или паренхимы почки. Сюда же следует отнести и динамические гидронефрозы.
2. Вторичный, или приобретенный, гидронефроз как осложнение какого-либо заболевания (мочекаменная болезнь, опухоли почки, лоханки, мочеточника, травматические повреждения мочевых путей).
Не потеряла своего клинического значения классификация, предложенная С. П. Федоровым (1906). Однако она является скорее определением стадии болезни, глубины патологического процесса, нежели объединяющей все формы гидронефроза с точки зрения этиологии, патогенеза и клиники.
В основу этой классификации были положены клинические и патоморфо-логические признаки заболевания. Стадия I — начальная, она определяется С. П. Федоровым как пиелозктазия. Стадия II — поздняя, объединяет гидронефроз и пионефроз и подразделяется на три большие группы:
1) гидронефроз (открытый, закрытый и интермиттирующий): а) асептич-ный, б) инфицированный, в) гематонефроз;
2) пионефроз (открытый, закрытый, интермиттирующий): а) калькулез-ный, туберкулезный и т. д.;
3) эта группа объединяет травматические истинные и ложные гидронефрозы.
Пионефроз в настоящее время выделен в самостоятельную нозологическую единицу, а травматические гидронефрозы относятся к группе: вторичных.
Исходя из современного состояния учения о гидронефрозе и в научно-практических интересах течение заболевания следует разделять на 3 стадии: I — начальную, II — раннюю и III — терминальную.
Каждой из этих стадий свойственны своя патоморфологическая картина болезни, только ей присущие функциональные сдвиги в деятельности почки и клинические проявления.

Течение и симптомы. Клинические картины гидронефроза и уретеро-гидронефроза практически ничем не отличаются и дифференцировать одно заболевание от другого по отдельным симптомам без инструментально-рентгенологического обследования невозможно.
Проявление гидронефроза весьма разнообразно, но, к сожалению, ни один из симптомов не является для него специфическим. Тщательный анализ анамнеза, развития заболевания, оценка каждого симптома в отдельности и их сопоставление дают возможность лишь предположительно высказать мнение о диагнозе, а уточнить его можно только с помощью функционально-морфологических рентгеновских методов диагностики. Однако следует указать, что сопоставлением клинического проявления болезни и данных рентгенологического и лабораторного методов исследования всегда почти можно определить стадию заболевания, его осложнения и тем самым избежать ошибок при выборе метода лечения.
Между отдельными стадиями болезни нет четких границ, не всегда можно определить III стадию и дифференцировать ее от II стадии, так как отдельные признаки болезни сходны для всех или каких-либо двух стадий болезни. Для гидронефроза наиболее типичными клиническими признаками являются боль, пальпируемая опухоль в поясничной области, гематурия, большие или меньшие изменения со стороны мочи, изменения в общем состоянии больного и сопутствующие симптомы со стороны органов брюшной полости.
Боль является наиболее частым признаком гидронефроза. По данным Я. Кучера, она имеет место у 80% больных гидронефрозом и часто может быть единственным признаком заболевания. Характер боли весьма разнообразен — от тупых ноющих, едва заметных для больного, до жестоких приступов почечных колик, полностью лишающих больных работоспособности. Столь большое разнообразие в характере боли при гидронефрозе зависит от полиэтиологичности заболевания и его стадии.
Наиболее часто боль носит тупой характер, нередко она усиливается к вечеру и полностью исчезает ночью, уменьшается в покое и лишает больного возможности выполнять малейшую физическую работу днем. Боль всегда локализуется в области почки и нередко, особенно при уретеро-гидронефрозе, иррадиирует в пах, в бедро. Иногда больные отмечают тяжесть в поясничной области, переходящую в зависимости от нарушения питьевого режима или физической работы в тупую боль. Причиной тупых болей в почке при ее трансформации в гидронефроз являются постоянное медленное повышение внутрилоханочного и внутрипочечного давления, смещение почки под действием тяжести и натяжение сосудов почечной ножки, а также ишемия почечной ткани от повышенного внутрилоханочного давления, увеличивающаяся в вертикальном положении больного в связи с изменением положения и уменьшением просвета почечных сосудов. Тупые боли чаще наблюдаются при врожденных медленно развивающихся гидронефрозах.
У половины больных гидронефрозом могут наблюдаться различные по интенсивности и продолжительности приступы острых болей в области почки (почечные колики). Эти приступы могут возникать на фоне существования постоянных тупых болей или являться единственным признаком гидронефроза и вызываться литиазом или возникать без него в связи с другими видами препятствий оттоку мочи из верхних мочевых путей.
Анализ катамнеза больных гидронефрозом позволяет согласиться с мнением большинства клиницистов, что характер боли в известной степени позволяет определить стадию гидронефроза, высказать предположение в отношении этиологического фактора и даже прогноза. Так, например, развитие гидронефроза на почве мочекаменной болезни чаще всего сопровождается приступами почечной колики. Они продолжаются на протяжении всей первой стадии болезни, когда функция почки в основном сохранена. Чем глубже функционально-морфологические изменения в почке, претерпевающей трансформацию в гидронефрозе, тем реже становятся приступы почечной колики. Боли из периодически острых меняют свой характер на постоянные тупые и иногда переходят в ощущение, которое больным трактуется как тяжесть в поясничной области. Такая последовательность развития болевого синдрома наиболее типична для вторичных гидронефрозов, особенно „калькулезных". Для первичных или врожденных гидронефрозов патогномоничными являются тупые боли или ощущение тяжести в поясничной области, что объясняется медленной трансформацией почки в гидронефроз, постепенным увеличением лоханки, атрофией паренхимы и нарушением функции почки.
Нередким признаком гидронефроза является прощупываемая опухолевидная масса в поясничной области. Анализ наблюдений клиники показывает, что пальпаторное определение увеличенной почки при ее трансформации оказалось возможным у 15% больных гидронефрозом. Я. Кучера удавалось определить пальпацией почку лишь у 10% больных гидронефрозом. Не являясь специфическим для гидронефроза симптомом, пальпируемость почки в сочетании с другими признаками помогает уточнить диагноз.
Почка иногда может достигать колоссальных размеров, вмещая в себя до 5 л и даже более мочи. Увеличение почки приводит к ее опущению и относительной мобильности. При пальпации она сравнительно легко смещается в забрюшинном пространстве, заполняя иногда всю соответствующую половину брюшной полости или даже полости таза. Прощупываемый гидронефроз обычно имеет гладкую поверхность, туго-эластическую консистенцию, он малоболезненный, баллотирующий. Флюктуацию определить удается далеко не во всех случаях и только у лиц со скудно развитым подкожножировым слоем.
Некоторые авторы описывают как частый признак гидронефроза периодическое его увеличение и уменьшение. Это интермиттирующий гидронефроз, возникающий чаще всего на почве почечнокаменной болезни при так называемом „вентильном камне" — „клапанном гидронефрозе". Периодическое уменьшение размеров гидронефроза связано с частичным опорожнением лоханки. Этот симптом является патогномоничным для гидронефроза, но наблюдается крайне редко. Так, за 10 лет в нашей клинике на 100 с лишним больных только двое имели интермиттирующее течение гидронефроза.
Более частым признаком гидронефроза является гематурия. По мнению А. Я. Абрамяна, Я. Кучера и др., гематурия стоит на втором месте после болевого симптома. Проводя анализ течения болезни у больных нашей клиники, мы отметили, что лишь у 8% больных имела место гематурия, в то время как, по данным Я. Кучера, она встречается у 20% больных. При этом весьма интересно заметить, что у 6% наблюдавшихся нами боль ных гидронефрозом с гематурией причиной заболевания являлись доба вочные сосуды; все эти люди были связаны с физическим трудом (рабочие, спортсмены) и гематурия у них возникала в связи с физическим перенапряжением. Весьма часто вслед за усилением болей, а иногда и возникновением почечной колики появляется гематурия. Она редко бывает со сгустками и продолжительной.
Причиной гематурии является травма вен форникальных зон вследствие острого нарушения гемодинамики в сосудах почки. Гематурия может повторяться и в этих случаях увеличивается возможность появления гема-тогидронефроза, создаются условия для возникновения литиаза в гидронефрозе. Бесспорным является тот факт, что гематурия — это симптом I и II стадии гидронефроза, когда еще в почке имеется много функционирующей паренхимы и мало нарушена ее ангиоархитектоника.
Общие признаки. Проявление гидронефроза изменениями в общем состоянии этих больных наблюдается весьма часто. Однако эти признаки настолько многообразны и многочисленны, что нет возможности все их перечислить, да в этом и нет необходимости, так как ни один из них не является специфическим для гидронефроза. Характер общих признаков, их количество в значительной степени зависят от стадии заболевания и осложняющих его моментов — литиаза, пиелонефрита, одно- и двусторон-ности поражения и т. д.
Нередко гидронефроз развивается латентно и не сопровождается ни местными, ни общими симптомами. В этих случаях больные узнают о своем заболевании при случайном осмотре врача или определяют сами у себя наличие опухоли. Весьма нередко впервые оно проявляется признаками присоединяющегося осложнения.
Однако, если провести анализ тщательно собранных историй заболеваний, то без сомнения можно отметить в истории жизни этих больных общие признаки заболевания, которые появились за много лет до его диагностирования. Нередко это боли в животе, заканчивающиеся аппендэктомией или пробной лапаротомией. В других случаях отмечаются интермиттирующее повышение артериального давления, головные боли, повышенная утомляемость, бессонница и т. п. Нередко больные отмечают медленную потерю веса, ухудшение аппетита. К оценке этих симптомов следует относиться очень осторожно, ибо они могут быть признаками различных заболеваний, а не только гидронефроза. Интенсивность общих симптомов бывает зачастую весьма невелика и больные не придают им никакого значения и к врачу не обращаются. Однако в случаях двустороннего гидронефроза уже во II стадии заболевания достаточно отчетливыми становятся признаки хронической почечной недостаточности: жажда, полиурия, головные боли и прогрессирующая потеря работоспособности и общего жизненного тонуса.
Дискутабельным является вопрос о характере изменений мочи при гидронефрозе. Неосложненный односторонний гидронефроз не вызывает изменений в клеточном и химическом составе мочи или в связи с отсутствием поступления мочи из больной почки, или вследствие смешивания мочи из больной почки с мочой из здоровой почки. Во всех случаях патологических примесей в моче при наличии гидронефротической трансформации следует думать об осложненном гидронефрозе.
Осложнения гидронефроза встречаются весьма часто и подчас первое проявление гидронефроза бывает связано с присоединившимся осложнением. Наиболее частым осложнением является присоединение инфекции, которая ведет к переходу асептического гидронефроза в инфицированный гидронефроз.
Пиелонефрит. Клинические исследования показывают, что сравнительно часто при гидронефротической трансформации параллельно развивается и пиелонефрит. Согласно данным Jackson, Grieble (1957), в 58% случаев односторонний гидронефроз осложняется пиелонефритом. По наблюдениям А. М. Кацыфа (1962), в 27 из 32 удаленных по поводу гидронефроза почках при гистологическом исследовании был обнаружен пиелонефрит.
Для развития пиелонефрита в гидронефрозе имеются все благоприятные условия: стаз мочи и нарушение гемодинамики (В. С. Рябинский). Развитие гидронефроза в значительной степени зависит от соотношения секреции и резорбции мочи, т. е. механизма, благодаря которому предупреждается первичная атрофия почки и создаются условия для гидронефротической трансформации. Последняя вызывает в почке такие морфологические изменения, которые благоприятствуют локализации микробов. Попав гематогенным путем в почку возбудители инфекционного процесса находят в гидронефрозе благоприятную среду для своего размножения и развития.
Развитие воспалительного процесса в почке определяется: 1) видом инфекции и тропизмом микробов; 2) общим состоянием организма; 3) врожденными факторами и приобретенными нарушениями в анатомической структуре почки и мочевых путей и, наконец, 4) функцией почек как экскреторного органа (А. Я. Пытель и С. Д. Голигорский, 1961; А. М. Кацыф, 1962; Jackson и Grieble, 1957, и др.). Одними из проявлений пиелонефрита при гидронефрозе служат стойкая пиурия, периодические повышения температуры вплоть до тяжелой интоксикации, особенно в начальной стадии гидронефроза, когда наблюдаются рефлюксы (А. Я. Пытель), которыми и объясняется такая резкая интоксикация.
Вряд ли можно в настоящее время проводить грань между пиелонефритом, осложняющим гидронефроз, и инфицированным гидронефрозом. Это единый процесс, ибо нельзя представить себе наличие инфекции в почечной ткани и неинфицированную мочу в лоханке той же почки и, наоборот, отсутствие пиелонефрита при инфицированной моче в почке, где непрерывно возникают рефлюксы и процесс секреции чередуется с процессом резорбции.
Нередким осложнением гидронефроза, чаще инфицированного, является литиаз. Образование конкрементов только в случаях открытого гидронефроза несколько видоизменяет клиническую картину болезни, выдвигая на первый план приступы болей и атаки пиелонефрита, особенно в ранней и начальной стадиях болезни.
В литературе встречаются описания спонтанного или травматического разрыва гидронефроза. С нашей точки зрения, к осложнениям гидронефроза можно отнести только спонтанный разрыв гидронефроза, диагностика которого не трудна, если было известно о существовании гидро-нефротической почки. В случаях „острого" начала болезни, когда не было известно о гидронефрозе, диагноз разрыва гидронефроза представляет большие трудности, тем более что больной обычно находится в коллаптоидном состоянии, в связи с чем осуществление рентгенологических методов диагностики оказывается невозможным. Таким больным часто производят операции с предположительными диагнозами на острое заболевание органов брюшной полости.
Диагноз. Чем раньше установлен диагноз гидронефроза, тем раньше будет начато лечение и тем лучше окажутся его результаты.
В начальных стадиях гидронефроз редко бывает осложненным инфекцией и воспалительным процессом. Отсутствие этих двух отрицательных компонентов в значительной степени изменяет характер оперативного вмешательства, облегчает его и сокращает период послеоперационного лечения. Вторым важным моментом, обязывающим к предельно ранней диагностике гидронефроза, является то, что в начальных и ранних стадиях еще нет необратимых изменений в динамике мочевыводящих путей и своевременно устраненное препятствие для оттока мочи приводит к быстрому восстановлению полного пассажа мочи. И, наконец, самое главное — ранняя диагностика гидронефроза позволяет сохранить функционирующий орган, от нормальной деятельности которого зависит жизнь человека.
Диагностика гидронефроза далеко не всегда оказывается легкой, и весьма часто до настоящего времени встречаются диагностические ошибки. Причиной их является неумелое использование многочисленных методов диагностики, при этом достаточно тонких и точных, а также отсутствие навыка и знаний при интерпретации получаемых данных.
Другой причиной диагностических ошибок является латентное течение гидронефроза, отсутствие достаточно четких признаков, особенно в первых двух стадиях болезни. Однако тщательно собранный анамнез и правильная оценка даже небольших клинических признаков заболевания являются основным условием своевременной диагностики гидронефроза. Изучение анализов мочи остается обязательной частью исследования больного с заболеванием, подозрительным на гидронефроз. Результаты исследования мочи у больного неинфицированным гидронефрозом оказываются обычно малоубедительными. Иногда удается обнаружить небольшую протеинурию, единичные лейкоциты и эритроциты, реже четко выраженную гематурию и отдельные фрагменты цилиндров.
Осмотром больного в положении лежа и стоя только у истощенных и астеников и при сравнительно больших гидронефрозах удается заметить изменение конфигурации передней брюшной стенки, а еще реже — поясничной области. В поздних стадиях гидронефроза удается пальпировать увеличенную почку.
Исследование только рентгенологическими методами следует начинать с простого обзорного снимка. По этим рентгенограммам можно определить увеличение почки и другие косвенные признаки патологического процесса — отсутствие контуров m. psoas, сколиоз и т. п.
Наиболее важным методом диагностики гидронефроза является экскреторная урография (рис. 165). Являясь функционально-морфологическим методом, она отображает как выделительную способность больной почки, так и состояние ее отводящего аппарата. Весьма ценным положительным качеством этого метода является возможность получения полной информации о состоянии второй почки.
Рентгенограммы при экскреторной урографии должны производиться до тех пор, пока не будет получено ясного представления о функционально-морфологическом состоянии почек с интервалом 15—30 минут. Последний снимок должен быть сделан через 2 часа после введения контрастного вещества. Этот метод с использованием специального вертикального кимографа дает возможность получить представление и о состоянии динамики верхних мочевых путей. В наше время вопросы выбора операции и прогноза не могут решаться без урокимографии или урокинематографии.
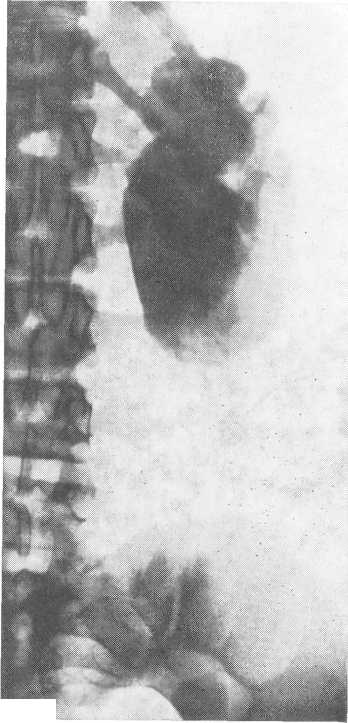
Рис. 165. Гидронефроз единственной почки. Урограмма
Большое значение для диагностики гидронефроза имеет хромоцисто-скопия. При осмотре мочевого пузыря следует обращать особое внимание на состояние шейки мочевого пузыря, форму и функцию устьев мочеточников. Обычно на стороне гидронефроза сокращения устья реже и более вялые, чем на здоровой стороне. Выделение индигокармина из устья больной почкой происходит медленно в виде ленты и весьма слабой "окраски, редкими порциями, а в конце процесса гидронефротической трансформации выделение индигокармина может вообще отсутствовать.
Уретеропиелографию целесообразно производить одномоментно с хро-моцистоскопией. Если катетер удастся провести в лоханку, то по нему можно отметить выделение мочи каплями или струей в зависимости от наполнения лоханки накануне операции. При производстве пиелографии необходима крайняя осторожность и тщательность выполнения. Не следует вводить рентгеноконтрастного вещества больше, чем оттекло мочи из гидронефроза по мочеточниковому катетеру: артифициальный рефлюкс приводит к пиелонефриту и вынуженной нефрэктомии даже при ранней стадии гидронефроза. Однако во многих случаях бывает необходимо произвести уретеропиелографию и не только при уретерогидронефрозе, но и в случаях только гидронефроза для определения его причины, уровня препятствия и т. д. При этом исследовании надо избегать перенаполнения лоханки и мочеточника и стремиться предотвращать пиелоренальные рефлюксы, а само исследование производить накануне операции. В случае атаки пиелонефрита операцию отменять не следует.
Уретеропиелография позволяет определять характер, протяженность и место расположения препятствия и косвенно судить о степени расширения чашечек почки и ее лоханки. На основании рентгенограмм в некоторых случаях удается составить впечатление о толщине оставшейся паренхимы, а производством серии рентгенограмм после пиелографии с интервалом 4 секунды (Я. Кучера) определить резервные возможности динамики чашечек и лоханки по быстроте их опорожнения (рис. 166).
Антеградная пиелография (рис. 167) в диагностике гидронефроза в первую очередь является морфологическим методом диагностики, т. е. позволяющим определить степень увеличения лоханки и уровень препятствия. Однако правильное использование метода позволяет выявить и функциональную способность оставшейся паренхимы, ее резорбтивную активность. При сохранившейся резорбтивной активности уже через 20 минут после введения контрастного вещества в гидронефротически расширенную лоханку удается получить экскреторную урограмму с контралатеральной стороны.
Применение антеградной пиелографии показано в тех случаях, когда экскреторная урография не позволяет определить степень функционально-морфологических расстройств в почке и уровень окклюзии мочеточника, а ретроградная пиелография невыполнима в связи с непреодолимым препятствием в мочеточнике.
Значительно реже для диагностики гидронефроза применяют аортографию (Н. А. Лопаткин, 1961). Однако в случае необходимости определить стадию болезни, выявить аберрантные полярные артерии и установить их роль в кровоснабжении почки этот метод является наиболее точным из всех существующих, единственным, позволяющим выявить остаточную функцию почки. При гидронефрозе основная почечная артерия удлинена, истончена и тем более, чем глубже изменения в паренхиме почки. Ветви почечной артерии удлинены и истончены, расстояние между ними резко увеличено (рис. 168). Изменения в ангиоархитектонике почки в значительной степени зависят от стадии патологического процесса и они, по мнению большинства исследователей, определяют функцию почки. Другими словами, функция гидронефроза такова, каково его кровообращение.
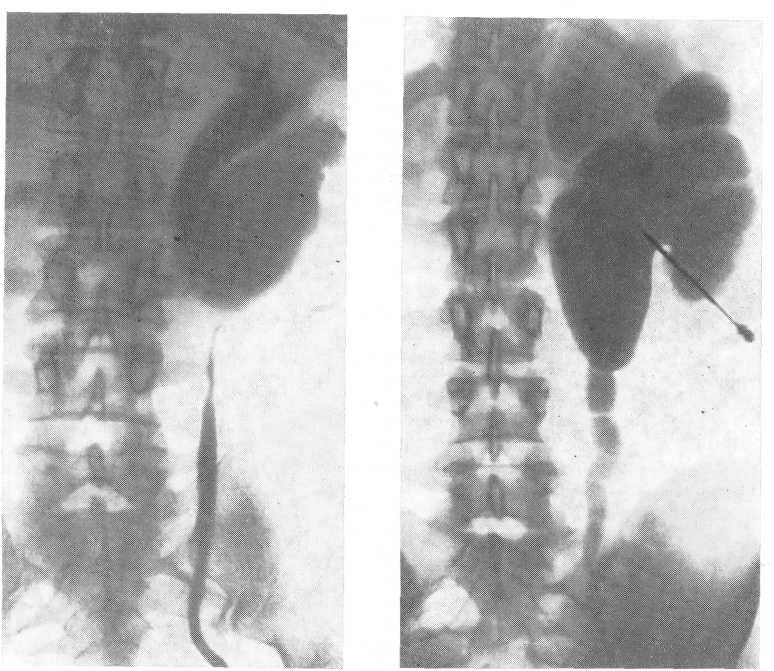
Рис. 166. Гидронефроз на почве добавочного сосудистого пучка. Уретеро-пиелограмма.
Рис. 167. Гидронефроз в связи с окклюзией мочеточника камнем. Антеградная пиелограмма.
В последнее время находит широкое применение изотопная ренография. Последняя позволяет определить сосудистую, секреторную и экскреторную функции почки. Соответственно ренограмма состоит из трех частей: начальной, характеризующейся быстрым подъемом и отражающей накопление изотопа в сосудистом русле почки, средней, отличающейся более медленным подъемом и показывающей секреторную деятельность тубулярного аппарата, и конечной части — это спад кривой, обусловленный экскреторной функцией почки. В зависимости от стадии гидронефроза изменяется та или иная часть ренограммы. Так, если в III, заключительной, стадии гидронефротической трансформации резко изменены все три компонента ренограммы, то в I стадии сосудистая ее часть будет мало отличаться от нормальной по своему внешнему виду, но значительные изменения окажутся в двух других компонентах (рис. 169). Изотопная ренография с точки зрения ее роли для диагностики гидронефроза на данном этапе имеет ориентировочное значение: так, аналогичные изменения могут быть и при пиелонефрите и при других заболеваниях почек. Дифференциально-диагностическое значение изотопной ренографии весьма относительное. При определении гидронефротической трансформации весьма большое значение имеет правильная оценка данных анамнеза и дополнительных методов исследования. Только сопоставлением всех данных можно определить правильно стадию болезни и избрать наилучший метод лечения.
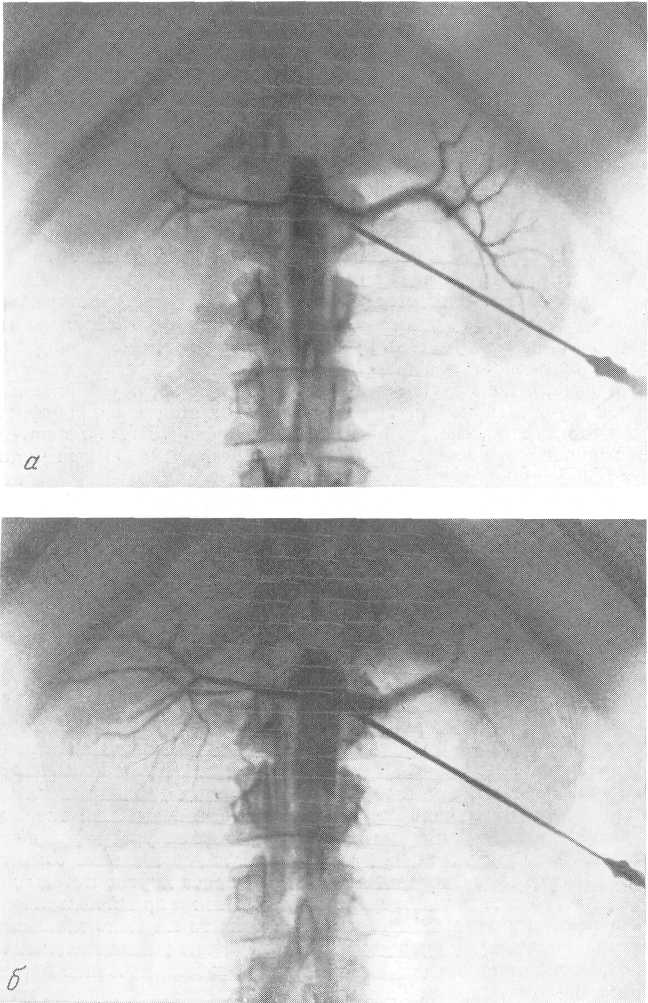
Рис. 168. Почечная артериограмма. а — начальная фаза; б — конечная фаза; в — паренхиматозная фаза.
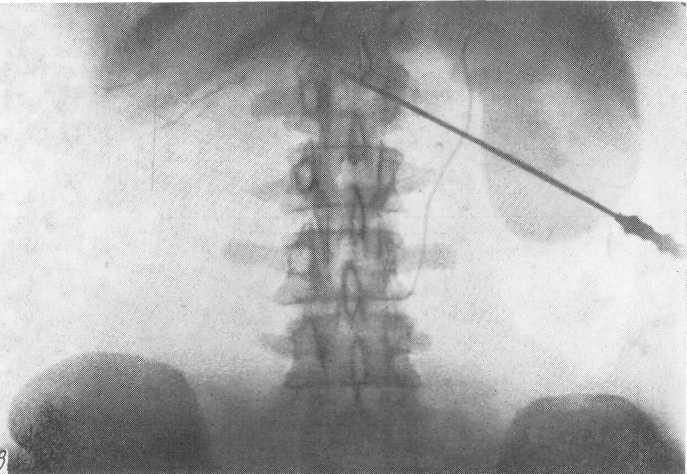
Оценивая данные анамнеза, следует иметь в виду, что трансформация почки в гидронефроз — процесс медленный, продолжающийся иногда годами и даже десятилетиями. Продолжающиеся приступы почечных колик в пораженном органе, атаки пиелонефрита всегда указывают на то, что орган живет, что его можно спасти правильно выполненной операцией и последующим лечением. Весьма часто экскреторная урография дает указание на полную гибель почки, а анамнез заставляет в этом сомневаться и применять для окончательного решения вопроса другие методы диагностики и, в частности, почечную ангиографию. В то же время нельзя переоценивать и роль анамнеза. Отсутствие каких бы то ни было признаков заболевания, типичное для врожденных или медленно развивающихся гидронефрозов, не является свидетельством полной гибели почечной паренхимы и форникального аппарата. Только сопоставлением всех данных клинико-рентгенологического обследования больного могут быть решены вопросы диагноза.
Дифференциальный диагноз гидронефроза в большинстве случаев не представляет особых затруднений. Однако иногда возникает необходимость дифференцировать гидронефроз от заболеваний соседних органов. Необходимость в дифференциальном диагнозе чаще всего вызывается общностью симптомов, из которых пальпируемость почки и гематурия являются наиболее частыми. Эти признаки могут наблюдаться при различных заболеваниях почки; чаще всего приходится дифференцировать гидронефроз от опухоли почки и от нефроптоза.
Отличительной особенностью неосложненного нефроптоза является хорошая функция почки и резкая смещаемость органа в зависимости от положения тела. Рентгенологические методы исследования позволяют безошибочно установить диагноз, особенно при выполнении обследования в положении лежа и стоя: смещение почки в зависимости от положения тела более чем на один позвонок указывает на нефроптоз, а резкое увеличение лоханки и чашечек всегда говорит в пользу гидронефроза. При пальпируемой в поясничной области или в подреберье опухоли перед врачом всегда встает необходимость определить принадлежность новообразования. Оно может относиться к желчному пузырю, эхинококку печени, оказаться увеличенной селезенкой, опухолью кишечника или поджелудочной железы, кистой брыжейки или яичника. Пальпацией бывает очень трудно определить принадлежность опухоли к тому или иному органу и дифференцировать гидронефроз от опухоли органов брюшной полости. Однако следует помнить, что во многих случаях определить состояние почки, выявить ее заболевание бывает гораздо легче, чем заболевание, скажем, желчного пузыря в связи с большой доступностью диагностическим приемам. Из этого не следует делать вывод об исключительном применении урологических методов диагностики в дифференциации заболеваний органов брюшной полости и почки: методы диагностики заболеваний органов брюшной полости также могут оказать существенную помощь в уточнении диагноза. Однако недостаточно установить принадлежность опухоли к почке. Весьма часто бывает необходимо исключить целый ряд почечных заболеваний и в первую очередь новообразования, поликистоз, нефроптоз, солитарную кисту.
Данные пальпации лишь иногда позволяют с определенной достоверностью высказаться в пользу гидронефротической трансформации почки. Такая почка обычно имеет округлые очертания, гладкую поверхность, эластическую консистенцию и иногда флюктуирует. Более четко удается дифференцировать новообразование почки. В подобных случаях она плотна на ощупь, бугриста и часто малоподвижна. Не редким и ценным дифференциально-диагностическим признаком является сопутствующее расширение вен семенного канатика. Типичные данные пиелограммы — дефекты наполнения в лоханке и чашечках, деформации их — признаки опухоли, позволяющие полностью исключить гидронефроз.
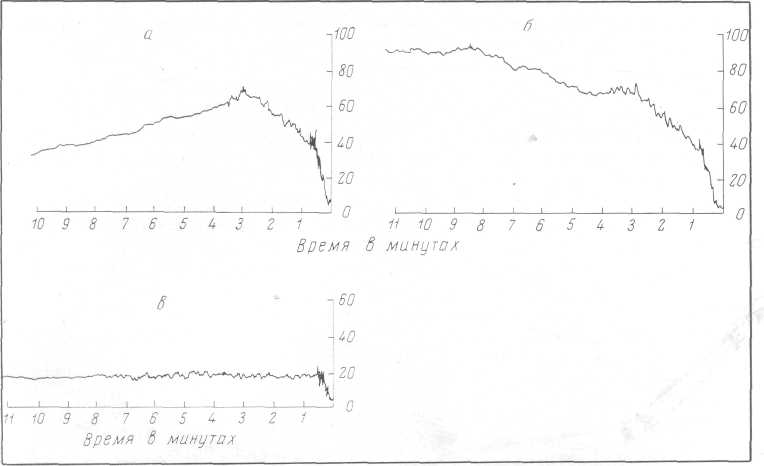
Рис. 169. Изотопная ренограмма.
а - в норме; б — при окклюзии мочеточника; в - при полном отсутствии функции почки.
Весьма большие затруднения встречает врач при диагностике новообразований почечной лоханки, которые вызывают расширение лоханки, а иногда и полную трансформацию почки в гидронефроз. В подобных случаях указание в анамнезе на гематурию как на первый признак заболевания обязывает врача применить модификации пиелографии с менее концентрированным рентгеноконтрастным веществом, на фоне которого может быть виден дефект наполнения, зависящий от опухоли лоханки.
Диагноз поликистоза почек и дифференцирование этого заболевания с гидронефрозом не представляют особого труда. Поликистоз — всегда двустороннее заболевание, сопровождающееся симптомами почечной недостаточности и пиелонефрита. Почти всегда прощупываются обе почки, большие бугристые. Длинные шейки чашечек, внутрипочечно расположенная и тоже вытянутая лоханка, изогнутый в прилоханочном отделе мочеточник являются достоверными отличительными признаками поликистоза от гидронефроза.
Дифференциальный диагноз гидронефроза в полисимптомных случаях должен основываться на полном урологическом клинико-рентгенологиче-ском обследовании.
Прогноз при гидронефротической трансформации полностью зависит от стадии болезненного процесса, состояния контралатеральной почки и осложнений (пиелонефрита и др.). В значительной степени прогноз зависит и от этиологического фактора гидронефротической трансформации.
Прогноз лечения следует определять с точки зрения жизни больного, возможности сохранить почку и ее функциональной способности.
При одностороннем гидронефрозе и здоровой контралатеральной почке даже конечная стадия трансформации, вынуждающая к нефрэктомии, не сокращает жизнь больного, не лишает его работоспособности, а молодых женщин и радости материнства. Тем более благоприятным будет прогноз при начальных стадиях гидронефроза и своевременно предпринятой и правильно выполненной реконструктивной операции. Лишь в случаях гидронефроза, осложненного пиелонефритом, требуется длительная противовоспалительная терапия. Оперативное лечение и противовоспалительная терапия создают благоприятные условия для мобилизации богатых резервных возможностей почки. Даже при двустороннем процессе разумными оперативными вмешательствами и правильной последовательностью лечебных мероприятий удается сохранить жизнь больным и в значительной степени вернуть им работоспособность.
Прогноз зависит и от этиологического фактора гидронефроза. Так, например, при гидронефрозе на почве аберрантного сосуда простым анте-вазальным пиело-пиелоанастомозом удается ликвидировать стаз мочи в почечной лоханке и создать благоприятные условия для восстановления нормальной функции почки.
Во всех случаях неосложненного гидронефроза своевременной реконструктивной операцией удается добиться полного выздоровления и восстановления трудоспособности. При осложненном гидронефрозе, особенно двустороннем, практически можно добиться значительного улучшения в состоянии здоровья больного и даже восстановления трудоспособности. Однако абсолютной ликвидации патологического процесса даже длительной противовоспалительной терапией в комбинации с тонизирующей динамику лоханки и мочеточника получить практически невозможно. И все же такое неполное выздоровление не исключает восстановления трудоспособности пациента.
Лечение гидронефроза и уретерогидронефроза может быть консервативным и оперативным. Каждый из этих видов терапии имеет свои показания, которые зависят от стадии болезни, этиологического фактора, вызвавшего гидронефротическую трансформацию, и осложнений. От правильного определения показаний к тому или иному виду терапии в значительной степени зависит успех лечения. Исходя из этих положений и основного принципа медицины — „раннее начало лечения — залог успеха", во всех случаях подозрения на гидронефроз показаны госпитализация и тщательное обследование вплоть до окончательного установления диагноза и определения лечебной тактики. Консервативное лечение допустимо весьма ограниченному числу больных, страдающих небольшими и неосложненными гидронефрозами, которые не нарушают работоспособности этих людей, не вызывают сколько-нибудь значительных расстройств функции почки и в субъективном состоянии больного. Такие гидронефрозы принято называть компенсированными. Однако эти больные подлежат систематическому клинико-рентгенологическому контролю и лишь при стойком неизмененном функционально-морфологическом состоянии почки им доступны профилактическая противовоспалительная терапия и применение диетически-гигиенических мер. Следует согласиться с точкой зрения Я. Кучера, предупреждающего о необходимости тщательного контроля за этими больными: компенсаторные механизмы почки не оставляют ее ткань безразличной к предъявляемым повышенным к ней требованиям и почечная паренхима повреждается даже тогда, когда на протяжении нескольких лет нет видимого увеличения объема чашечек и лоханки. К консервативной терапии следует отнести и некоторые виды хирургических инструментальных манипуляций, как, например, катетеризацию мочеточника или лоханки. Эта лечебная манипуляция бывает необходима как средство оказания срочной помощи в случаях обострения латентно протекавшего пиелонефрита и внезапного полного нарушения пассажа мочи из лоханки почки. Такое дренирование почки с параллельно проводимой противовоспалительной терапией является лишь паллиативным средством. Таким образом, консервативное лечение гидронефроза может быть охарактеризовано как симптоматическое, а оперативное радикальное — причинным, т. е. устраняющим причину нарушения пассажа мочи из лоханки. В то же время радикальное оперативное лечение может быть органосохраняющим и органоуносящим. К паллиативным способам оперативного лечения следует относить операции по временному созданию противоестественного пути для отведения мочи (пиелонефростомия или уретеростомия).
Нефростомия для лечения гидронефроза как самостоятельная операция не применяется. Однако она весьма часто используется в случаях необходимости срочного отведения мочи при осложнении гидронефроза острым пиелонефритом, как разгрузочная операция и первый этап последующих пластик в месте препятствия для оттока мочи. Пиелостомию применять при гидронефрозах не рекомендуется.
Нефрэктомия — операция вынужденная и может применяться только в случаях далеко зашедшего гидронефроза, когда почечная ткань безвозвратно погибла, или в случаях инфицированного гидронефроза при хорошей функции контралатеральной почки у пожилых больных (старше 60 лет).
Установлено, что почка, претерпевая даже значительную гидронеф-ротическую трансформацию, сохраняет большие резервные возможности и при создании благоприятных условий ее функция восстанавливается в значительной степени и настолько, что может обеспечить жизнь больному на многие годы в случае потери функции другой почки. Именно это послужило поводом к широкому распространению органосохраняющих, пластических операций.
Критериями для выбора способа оперативного лечения являются возраст больного и его общее состояние, функционально морфологическое состояние пораженной почки, активность инфекции и воспалительного процесса в ней и, наконец, состояние другой почки.
Возраст больного и его общее состояние в значительной степени определяют исход пластической операции. Кроме этого, следует учитывать более слабые регенеративные возможности у пожилых лиц и замедленное восстановление функции почки и, что особенно важно, тонуса лоханки и мочеточника. Эти больные в пожилом возрасте часто оказываются весьма ослабленными болезнью, состояние их ухудшается операционной травмой и блестяще выполненная операция с хорошим анатомическим эффектом в функциональном отношении оказывается безрезультатной. Исходя из этих соображений, Я. Кучера рекомендует пластические операции до 50 лет. В более пожилом возрасте и особенно у лиц истощенных или страдающих какими-либо другими сопутствующими тяжелыми заболеваниями более правильно произвести нефрэктомию или даже нефростомию.
Большое значение для прогноза имеет стадия гидронефротической трансформации. Чем раньше произведена операция, тем лучше отдаленные и непосредственные результаты реконструктивных операций на лоханке или мочеточнике. При этом степень расширения лоханки, если она не внут-рипочечная, имеет весьма относительное значение, когда решается вопрос в пользу органосохраняющей операции. Самым главным в решении этого вопроса является сохранность достаточного количества функционирующей паренхимы и активных сократительных движений в лоханке и мочеточнике. Отток мочи из лоханки под повышенным давлением даже через анатомически полноценный лоханочно-мочеточниковый сегмент по сути дела ничего не меняет по сравнению с положением до операции и оставляет почку под угрозой окончательной гибели. Однако отсутствие у лоханки и мочеточника перистальтических движений в дооперационном периоде не является указанием на безвозвратную их гибель. Иногда длительное дренирование почки и соответствующая терапия восстанавливают динамику мочевыводящих путей и прогноз становится весьма благоприятным.
Серьезным противопоказанием в доантибиотическую эру для пластических операций являлась инфекция. В современных условиях большого разнообразия различных антибиотиков широкого спектра действия, препаратов нитрофуранового и сульфаниламидного ряда это возражение не считается принципиальным и требует лишь хорошей предоперационной подготовки и борьбы с инфекцией в послеоперационном периоде.
Если при наличии здоровой контралатеральной почки реконструктивная операция считается относительно показанной, то при гидронефрозе солитарной почки она неизбежна и должна производиться незамедлительно.
Гидронефротическая трансформация сопровождается значительными изменениями в топографии почки и мочеточника. В ответ на прогрессивное увеличение почки, нарушение в ней кровообращения паранефральная клетчатка претерпевает значительные изменения. Количество ее уменьшается, и даже у полных лиц она иногда тонким, но уплотненным листком покрывает гидронефроз. При выделении почки из паранефральной клетчатки отмечается умеренное кровотечение в связи с повреждением мелких сосудов, врастающих из паранефральной клетчатки в капсулу и ткань почки.
Лоханка при внепочечном ее расположении бывает обычно резко увеличена, напряжена, при надавливании не опорожняется. Верхняя ее половина передней стенки обычно покрыта редкой сетью распластанных почечных сосудов — ветвей артерии и вены. Нижняя ветвь почечной артерии и вены обычно проходит по границе между лоханкой и почечной тканью и входит в последнюю где-то у нижней трети нижней половины гидронефроза.
В случае гидронефроза, осложненного воспалительным процессом, паранефральная клетчатка отслаивается во время операции с трудом, стенка лоханки бывает резко утолщена, она покрыта отечной клетчаткой ворот почки и густой сетью легко кровоточащих собственных артериальных и венозных сосудов.
Обычно на нижнем полюсе почки бывает распластан и улиткообразно изогнут резко суженный прилоханочный отдел мочеточника. Эта его часть всегда покрыта спайками, фиксирующими мочеточник к стенке лоханки.
При наличии добавочных нижнеполярных сосудов последние обычно изменяют несколько положение почки — нижний полюс оказывается как бы подтянутым к средней линии. Добавочный сосудистый пучок всегда бывает покрыт клетчаткой и становится видимым только по снятии ее. Она почти всегда рубцово изменена и отделяется от сосудов в области их перекреста с мочеточником с некоторым трудом. Под сосудами на мочеточнике обычно отчетливо видно сужение его — странгуляцйонная борозда и отсутствие перистальтических движений.
Гидронефротическая трансформация сопровождается некоторым птозом органа вследствие его тяжести и возникающими в связи с этим перегибами мочеточника. При сохранившемся тонусе мочеточника последнее не сказывается на уродинамике, но по мере прогрессирования процесса ликвидация птоза и вторичных перегибов, особенно при парауретеральном спаечном процессе, становится обязательной. Все эти моменты патологической топографии гидронефроза важно иметь в виду и при выполнении любой операции органосохраняющего типа, руководствоваться принципом максимального щажения тканей. Операция должна выполняться in situ. Паранефральную клетчатку и клетчатку sinus renalis следует максимально сохранять, ибо они содержат дополнительные кровеносные и лимфатические сосуды.
Подготовка больного к операции имеет весьма существенное значение особенно в тех случаях, когда предстоит вмешательство при осложненном пиелонефритом или почечной недостаточностью одно-, а тем более двустороннем гидронефрозе или трансформации в гидронефроз солитарной почки.
Помимо общеукрепляющих мероприятий, направленных на улучшение функции легких и сердечно-сосудистой системы, следует особое внимание обращать на улучшение функции печени и на борьбу с воспалительным процессом, с пиелонефритом; применением соответствующих возбудителю антибиотиков или химиопрепаратов воспалительный процесс должен быть сведен до минимума. Это обеспечит благоприятное течение послеоперационного периода, предупредит возможные серьезные осложнения. Признаки почечной недостаточности являются серьезным препятствием к производству радикальной реконструктивной • операции. У подобных больных необходимо использовать все средства по ликвидации малейших проявлений этого тяжелого осложнения. Желудочно-кишечный лаваш, соответствующая диета, ванны у многих больных позволяют снять проявления азотемии. В тех случаях, когда консервативные мероприятия не эффективны, может быть показанным перитонеальный диализ или гемодиализ. Однако в подобных случаях эти меры являются первым этапом в подготовке больных к двухмоментной операции.
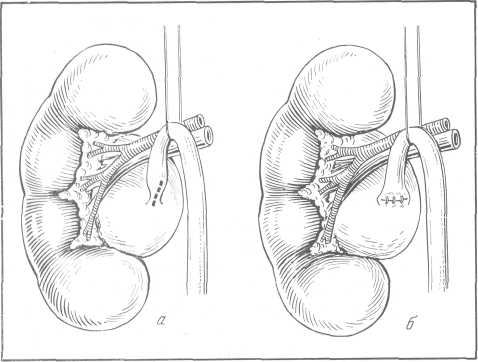
Рис. 170. Пластика лоханочно-мочеточникового сегмента по Fenger.
а — разрез стриктуры прилоха-ночной части мочеточника; б — наложение швов в поперечном направлении раны мочеточника.
При таком стечении обстоятельств нефростомия становится средством подготовки больного к реконструктивной операции.
Обезболивание должно быть полным и давать хирургу возможность произвести в спокойной обстановке любую реконструктивную операцию in situ. Этим требованиям отвечает интубационный газовый наркоз с применением миорелаксантов.
Выбор способа оперативного лечения гидронефроза — не менее ответственная задача, чем определение показаний к операции. Успех операции зависит не только от правильного определения показаний к ней и избрания наиболее целесообразного способа реконструкции мочевых путей, но и от опыта хирурга. К настоящему времени предложено большое количество способов реконструкции лоханочно-мочеточникового сегмента. Я. Кучера разделяет их на 7 основных групп.
1. Уретеролизис — наиболее простая и наименее эффективная операция, ибо устранением внешнего препятствия далеко не всегда ликвидируются последствия его давления на стенку мочеточника. В связи с такой длительной компрессией, тяжом или добавочным сосудом в толще стенки мочеточника могут возникнуть тяжелые склеротические процессы, вызывающие сужение просвета мочеточника. В подобных случаях весьма целесообразно сочетать уретеролизис с резекцией суженного участка, особенно тогда, когда по рассечении спайки или тяжа на стенке мочеточника отчетливо видна „странгуляционная борозда".
2. Реконструкция пельвиоуретерального сегмента предложена много десятков лет назад (Fenger, 1894) и за эти годы подвергалась различным усовершенствованиям и модификациям. Наиболее простым способом является продольное рассечение задней стенки мочеточника в области стриктуры (рис. 170) и последующее сшивание слоев его стенки в поперечном направлении. Однако даже использование атравматических швов не исключает последующей деформации пельвиоуретеральной области в виде ее выпячивания. Такое же выпячивание остается и после пластики по Gibson (1939, 1945), который предложил делать два продольных разреза через стриктуру. По нашему мнению, этим только усугубляется возможность более быстрого и грубого рецидива стриктуры в пельвиоуретеральной области. Как первый способ, так и второй могут применяться только в случаях гидронефроза с низким отхождени ем мочеточника. При высоком отхождении мочеточника Fenger (1894) предложил рассекать стриктуру в углу лоханочно-мочеточникового сегмента от каудальной стенки лоханки через стриктуру до здоровой ткани мочеточника. Поперечными швами на разрез стриктура значительно расширяется, но при этом не исключается деформация лоханочно-мочеточникового сегмента. Как операция по Fenger, так и ее модификации малоэффективны и в настоящее время практического применения почти не имеют.
Широкое распространение долгие годы имел способ по Schwyzer (рис. 171), который иногда в модификации Foley применяется и в наши годы. Метод заключается в создании из лоскута лоханки воронкообразного расширения на месте стриктуры в лоханочно-мочеточниковом сегменте.
При пластике по Schwyzer производят мобилизацию верхней трети мочеточника и задней поверхности расширенной лоханки. Лоханку и мочеточник рассекают по задней поверхности эпсилонообразным разрезом и треугольный лоскут из стенки лоханки своей вершиной подшивают к нижнему углу разреза мочеточника. Боковые края разрезов вновь образуемой воронки сшивают узловым или непрерывным без прошивания слизистой оболочки атравматической иглой швом. Модификация Foley (рис. 172) заключается лишь в том, что эпсилонообразный разрез производят по медиальному краю лоханки и мочеточника, т. е. в лоханочно-мочеточниковом углу. Наиболее длинная ветвь разреза — вертикальная. Этим разрезом рассекают на всем протяжении стриктуру. Однако надо следить за тем, чтобы все три разреза были одинаковыми. Эта операция особенно показана в случаях высокого отхождения мочеточника, а при низком отхож-дении мочеточника она дает резкую деформацию лоханочно-мочеточникового сегмента. Частым осложнением пластики по Foley бывает некроз верхушки лоскута. Следствием этого возможны мочевые затеки и грубые вторичные рубцовые сужения мочеточника. Учитывая это, в последние годы стал применяться полулунный разрез на лоханке выпуклостью к стриктуре мочеточника и от его центра вертикальный разрез по лоханочно-мочеточниковому сегменту.
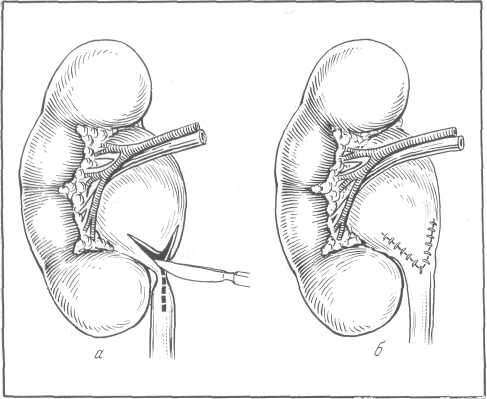
Рис. 171. Пластика лоханочно-мочеточникового сегмента по Schwyzer.
а — линия разреза; б — наложение швов.
К этой же группе операций относится пельвиоуретеральная миотомия по Allemann и полное продольное рассечение стеноза с интубацией мочеточника по Marion-Davis.
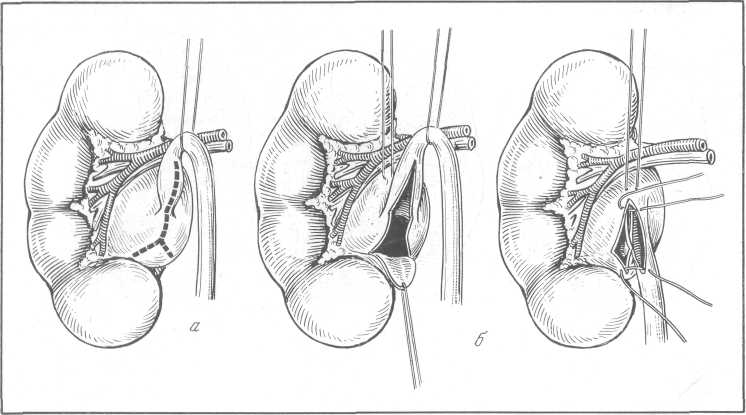
Рис. 172. Пластика лоханочно-мочеточникового сегмента по Foley.
а — линия разреза; б — пластика лоханочно-мочеточникового сегмента треугольным лоскутом из лоханки.
Однако, как покавывает опыт многочисленных авторов, ни та, ни другая операция не является анатомически обоснованной и не дает хорошие функциональные результаты.
3. Ортопедическая реконструкция лоханки и мочеточника (resectio orthopedique pyelorenalis) no Albarran показана только в случаях резкого расширения лоханки и высокого отхождения мочеточника. Эта операция в том виде, как она была предложена, патогенетически не обоснована: резекция нижней половины лоханки и нижнего полюса почки вместе с чашечкой без реконструкции лоханочно-мочеточникового сегмента не может обеспечить достаточно свободного, активного оттока мочи и полного восстановления функции почки. Аналогичным недостатком страдает и пластика лоханки по Hryntschak, заключающаяся в резекции верхнего — медиального — сегмента лоханки. Более обоснованная операция Пристлея. Она заключается в резекции большей части нижнего сегмента лоханки с рассечением мочеточника вплоть до его здоровой части и сшивании краев рассеченного мочеточника с краями оставшейся части нижней половины лоханки. Остальные способы, как и метод Юнга, имеют лишь историческое значение.
4. Изолированная пластика лоханочно-мочеточникового сегмента, как и резекция лоханки, не всегда может обеспечить ликвидацию патологического процесса. В связи с этим был разработан ряд операций, объединяющих резекцию лоханки с пластикой лоханочно-мочеточникового сегмента. К этим операциям относится способ Deuticke и Gibson. Эти операции сложны, малоэффективны и в настоящее время не применяются. Широкое признание получила операция Gulp-de Weerd-Scardino-Prince. Для ее успешного выполнения необходима тщательная мобилизация передней и задней поверхности лоханки и мочеточника. Разрез на задней поверхности мочеточника от здоровых тканей продолжается через стриктуру на заднюю стенку лоханки и дальше по ее медиальному краю до верхнего угла расширенной лоханки. Продолжением этого разреза выкраивается длинный лоскут из задней стенки лоханки шириной 0,8—1 см с основанием у нижнего ее края. Лоскут откидывают книзу, в соответствии с его длиной адаптируется разрез мочеточника. Эта операция может применяться как при высоком, так и при низком отхождении мочеточника (рис. 173).
5. Весьма распространена операция анастомоза бок в бок между мочеточником и лоханкой по Albarran в модификации Lichtenberg. В отличие от Albarran он не отсекает мочеточник от лоханки. Lichtenberg рекомендует после тщательного выделения мочеточника и разделения спаек между ним и лоханкой при высоком отхождении его от лоханки вскрыть мочеточник по медиальному, а лоханку — по латеральному краю и наложить между ними анастомоз бок в бок. Мы в своей практике избегаем рассекать спайки между лоханкой и мочеточником по задней их поверхности, так как они фактически являются уже готовым рубцом (рис. 174).
6. Фактически все причины, затрудняющие отток мочи из гидронефроза, заключаются в нарушении проходимости лоханочно-мочеточникового сегмента. Конечный результат, т. е. функциональная и морфологическая неполноценность этого отдела верхних мочевых путей, всегда является следствием воспалительных изменений или врожденных пороков развития. Поэтому при гистологическом изучении этого участка нервно-мышечные элементы оказываются резко измененными или даже вообще отсутствуют, будучи замещенными рубцовой тканью. В связи с этим многие исследователи (Kiister, Lubash, Neuwirth, Kucera и др.) предлагают иссекать этот участок и накладывать новый анастомоз в условиях сравнительно мало измененных тканей мочеточника и лоханки. Я. Кучера правильно считает, что оставление этого участка не только не оправдано, но и небезопасно, так как может явиться источником рецидива стеноза нового анастомоза.
Старый, стенозированный лоханочно-мочеточниковый сегмент не является „возбудителем" нового стеноза, но мы все же полагаем наиболее правильным методом оперативного лечения гидронефрозов резекцию пельвио-уретеральной области, а в случае большой лоханки — в комбинации с резекцией большей части лоханки.
Kuster предложил отсекать мочеточник в пределах здоровых тканей, а мочеточник вшивать в самый низкий отдел лоханки. При этом он рекомендует культю мочеточника на протяжении 1 см рассечь для расширения его и удобства наложения анастомоза. Резекцию лоханки при этом способе не производят.
Оригинален, но технически труден в исполнении метод Любаша. По этому способу мочеточник отсекают в пределах здоровых тканей, часть резко расширенной лоханки резецируют, а мочеточник вшивают в нижнюю ее стенку изнутри, проведя его через новое отверстие (рис. 175). Операцию заканчивают ушиванием лоханки и несколькими фиксирующими наружными швами между лоханкой и мочеточником.
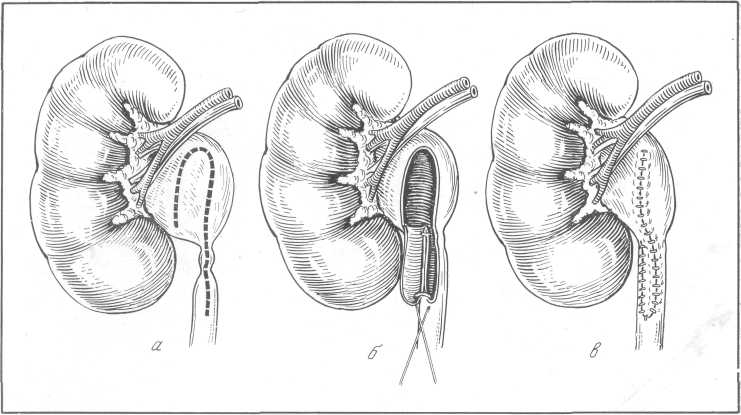
Рис. 173. Пластика лоханочно-мочеточникового сегмента по Culp-de Weerd-
Scardino-Prince.
а — пунктиром обозначена линия разреза; б, в — этапы пластики.
Большие трудности представляет реконструкция лоханочно-мочеточникового сегмента при внутрипочечно расположенной лоханке.
В подобных случаях может быть использован способ Нейвирта — уре-терокаликостомия. Отсеченный в пределах здоровых тканей мочеточник вшивают в нижнюю чашечку. Перед фиксацией культю его рассекают на два лепестка и последние фиксируют к чашечке внутренними швами. Мочеточник следует фиксировать также наружными швами к капсуле почки (рис. 176). Отрицательными моментами способа являются трудность фиксации мочеточника внутри чашечки и возможное вследствие этого отхождение лопастей культи, которые могут образовать подобие клапана.
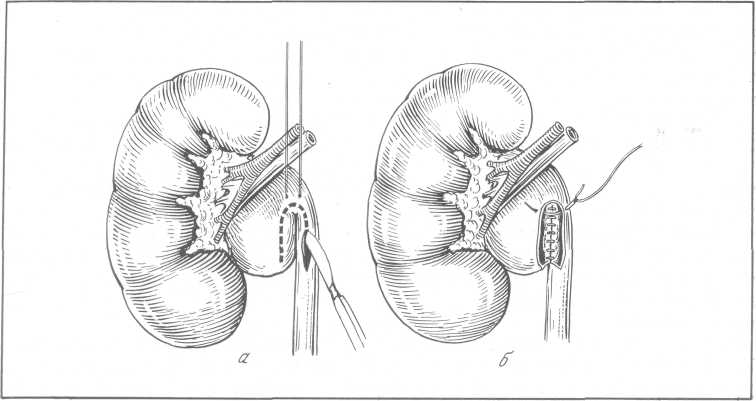
Рис. 174. Пластика лоханочно-мочеточникового сегмента по Albarran—Lichtenberg.
а — направление разреза лоханки и мочеточника; б — наложение анастомоза.
Такое осложнение мы наблюдали у 2 больных. Описаны случаи рубцевания нижнего полюса почки и стеноз вследствие этого мочеточника.
7. Частой причиной гидронефротической трансформации бывает добавочный сосудистый пучок к нижнему полюсу почки. В некоторых случаях причиной гидронефроза может оказаться одна добавочная вена или одна добавочная артерия. Было бы неправильным считать эти полярные сосуды всегда самостоятельными, берущими начало от аорты или какого-либо другого крупного артериального ствола. Причиной гидронефроза может оказаться и рано отошедшая от стволовой части почечной артерии нижняя ее ветвь.
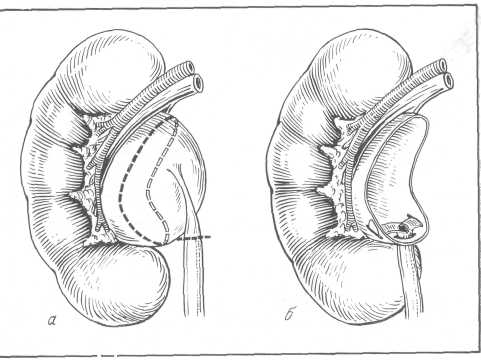
Рис. 175. Пластика лоханочно-мочеточникового сегмента по Lubasch.
а — линия резекции лоханки и мочеточника; б — имплантация мочеточника в лоханку.
В настоящее время достоверно установлено, что одно лишь давление добавочной артерии на лоханочно-мочеточниковый сегмент не ведет к нарушению пассажа мочи, но развивающиеся под действием пульсирующей артерии изменения в стенке лоханочно-мочеточникового сегмента являются причиной гидронефроза. Исследованиями последних лет доказана безусловная роль ишемии почки или ее участка в возникновении вазо-ренальной гипертонии. Исходя из этих двух положений, не следует резецировать добавочный сосуд. Эта операция создает условия для возникновения вазоренальной гипертонии и в то же время не ликвидирует изменений в лоханочно-мочеточниковом сегменте.
Недопустимы и такие операции, как изменение оси почки, мобилизация добавочной артерии и последующая ее фиксация на более высоком уровне к стенке лоханки.
Наиболее физиологичным следует считать иссечение суженного участка лоханочно-мочеточникового сегмента и антевазальный пиелоуретероана-стомоз. В детской практике добавочный сосуд как причина гидронефроза встречается редко, но если и бывает, то изменения в лоханочно-мочеточни-ковом сегменте обычно настолько малы, что ими можно пренебречь и произвести антевазальный пиело-пиелоанастомоз (рис. 177).
Из описанных операций по реконструкции лоханочно-мочеточникового сегмента как наиболее эффективные и физиологические могут быть рекомендованы способы Фолея, Кульпде-Вирда, Альбарана—Лихтенберга. При аберрантной нижнеполярной артерии рекомендуют антевазальный пиелоуретероанастомоз или пиелопиелоанастомоз.
Большие трудности представляет реконструкция лоханочно-мочеточникового сегмента при сужении верхней трети мочеточника на большом протяжении. Я. Кучера на Чехословацком конгрессе урологов в 1966 г. предложил метод замещения суженной части мочеточника лоскутом из нижней половины лоханки. Для этого производят широкую мобилизацию лоханки и рассечение ее в поперечном направлении косо и вверх (рис. 178). Нижний сегмент лоханки оттягивают книзу и с его просветом бок в бок сшивают мочеточник. Остальную часть раскрытой лоханки зашивают наглухо. Метод применим только при больших экстраренальных лоханках.
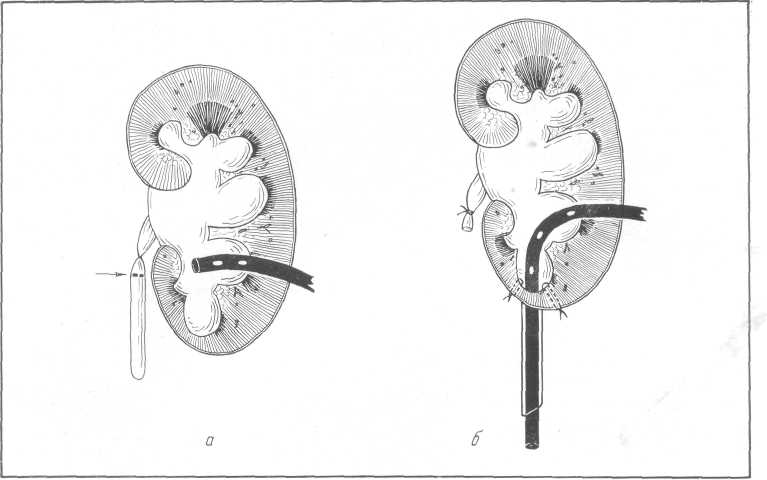
Рис. 176. Уретерокаликоанастомов по Neuwirth (С. Д. Голигорский и А. М. Кацыф)
а, б — этапы операции.
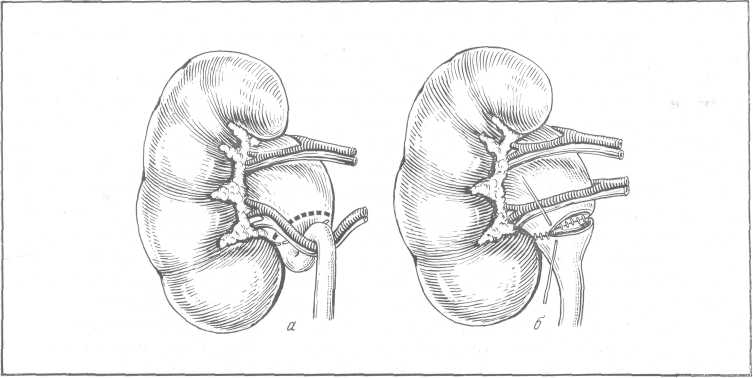
Рис. 177. Антевазальный пиело-пиелоанастомоз.
а, б — этапы операции.
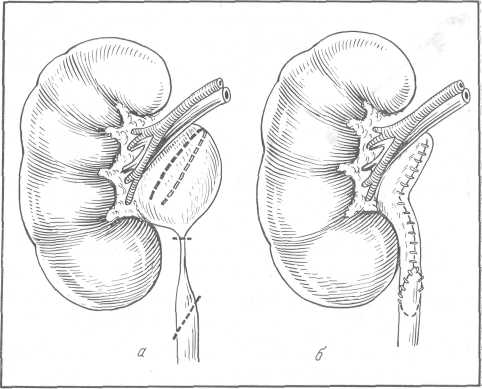
Рис. 178. Замещение верхней трети мочеточника сегментом лоханки (по Кучера).
а — пунктиром обозначена линия рассечения лоханки и резецируемый участок мочеточника; б — заключительный этап операции.
Эффективность операции по любому методу зависит не только от правильного выбора способа реконструкции лоханочно-мочеточникового сегмента, но и от отдельных ее этапов. Их нельзя назвать второстепенными, ибо иногда от них зависит исход операции. Весьма важно правильно определить роль трех моментов — дренирования почки, длительности катетеризации мочеточника и дренирования послеоперационной раны.
На основании анализа литературы и собственных наблюдений мы пришли к выводу, что дренирование почки — нефростомию — следует считать обязательным завершающим этапом реконструкции лоханочно-мочеточникового сегмента. Нефростомия абсолютно показана в тех случаях, когда гидронефроз осложнен пиелонефритом. Как бы идеально не был выполнен анастомоз между лоханкой и мочеточником, в послеоперационном периоде неизбежны отек области анастомоза и нарушение перистальтики лоханки и мочеточника. Эти два фактора — механический и динамический — приводят к стазу мочи в почке. Нарушенный пассаж мочи и операционная травма могут активизировать воспалительный процесс и привести к апостематозному нефриту, инфаркту почки, просачиванию мочи через анастомоз в паранефральную клетчатку и паранефриту. Любое из этих осложнений не только ухудшает результаты операции, но и может вынудить к нефрэктомии, т. е. свести на нет даже идеально выполненную органосохраняющую операцию.
Дренировать почку следует на 2—3 недели путем прямой пиелонефро-стомии. Катетеризация мочеточника через лоханку и нефростому (шинирование) себя не оправдывает. Инородное тело в области вновь созданного анастомоза лишь усиливает реактивный воспалительный процесс в рубце и замедляет процесс восстановления проходимости анастомозов. Ввиду этого дренирование мочеточника в настоящее время большинство авторов не рекомендует. В то же время дренирование паранефральной клетчатки на 2—5 суток резиново-марлевым или целлофаново-марлевым тампоном мы считаем обязательным, видя в этом профилактику паранефральной гематомы или мочевого затека.
Лечение уретерогидронефроза может быть только оперативным, а характер последнего в значительной степени определяется его этиологическим фактором. Операция может быть относительно простой и заключаться в удалении камня и весьма сложной, как, например, замещение мочеточника кишкой. В то же время она может не иметь прямого отношения к мочеточнику, когда гидронефроз вызван атонией пузыря на почве аденомы простаты, и заключаться всего лишь в удалении аденомы простаты или обычном дренировании мочевого пузыря. Нарушения динамики мочеточника, особенно когда они носят врожденный характер, не устраняются оперативным путем.
Большинство предложенных операций применяется при механических препятствиях — стенозах или стриктурах предпузырного отдела мочеточников. Способ операции избирается в зависимости от уровня препятствия.
В случаях локализации препятствия в интрамуральном или юкставе-зикальном отделе мочеточника чаще всего производят реимплантацию мочеточника в стенку мочевого пузыря (рис. 179).
В последние годы весьма частым осложнением рентгенорадиотерапии органов малого таза является облитерация нижнего отдела мочеточников.
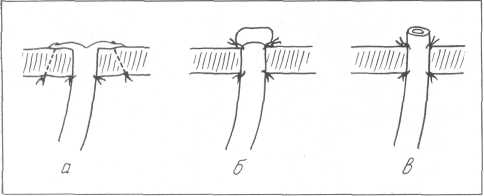
Рис. 179. Реимплантация мочеточника в мочевой пузырь.
а — по Bazy; б — по Ricard; в — по Lichtenauer-Payne (по Кучера).
Для лечения подобных осложнений предложено пересекать мочеточник над стенозом, продольным разрезом от шейки по передней и задней поверхности рассекать мочевой пузырь. После этого в верхушки образовавшегося рогообразного мочевого пузыря вшивают мочеточники и пузырь зашивают в поперечном направлении. Эта операция требует обязательного дренирования мочеточников и мочевого пузыря. Недостатком способа является возможность его применения только при облитерации мочеточников на сравнительно коротком протяжении (рис. 180). При одностороннем поражении мочеточника на протяжении всего тазового его отдела может быть использован метод Дешела (рис. 181). Однако оба эти способа вытеснены методом Боари, который является, по нашему мнению, лучшим. Он может быть использован как при поражении одного мочеточника, так и при облитерации обоих мочеточников. Метод заключается в выкраивании лоскута из переднебоковой стенки мочевого пузыря и формировании из него трубки, в которую и вшивают конец мочеточника.
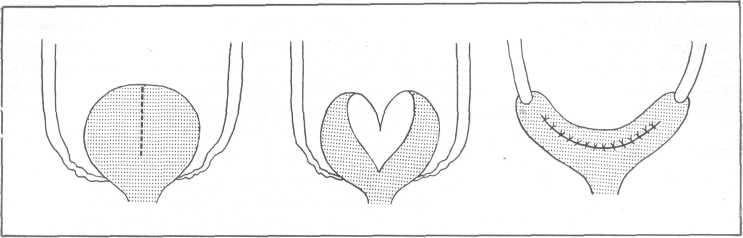
Рис. 180. Замещение нижнего отдела мочеточника по Bedrna.
При поражении двух мочеточников выкраивают по лоскуту с каждой стороны мочевого пузыря и в них вшивают мочеточник. Эта операция также требует дренирования мочеточников и мочевого пузыря (рис. 182).
При необходимости двустороннего замещения мочеточников операцию выполняют в два этапа; лишь в отдельных случаях оказывается возможной одномоментная операция. Трудность одномоментного замещения мочеточников двумя лоскутами состоит в том, что при дефекте в пределах 5 см имеет место опасность большого натяжения анастомоза.
При этом трубки оказываются не только короткими, но и относительно узкими. Эти обстоятельства грозят нарушением кровообращения в них и некрозом лоскута. Опасность некроза лоскута особенно велика у больных, подвергшихся рентгенорадиотерапии области таза.
Для одномоментного замещения нижних отделов мочеточников можно производить пересадку одномоментно двух мочеточников в единый лоскут {Н. А. Лопаткин, 1966). При этом лоскут выкраивают шириной 6—8 см, начиная от шейки мочевого пузыря по передней его стенке с переходом на купол, по всему куполу до границы перехода его в заднюю стенку. Экстра-перитонизацию мочевого пузыря не производят. Мочеточники фиксируют к лоскуту таким образом, чтобы концы их открывались в просвет трубки на расстоянии 1—1,5 см от края лоскута. Мочеточники между собой целесообразно сшить, не накладывая между ними анастомозов.
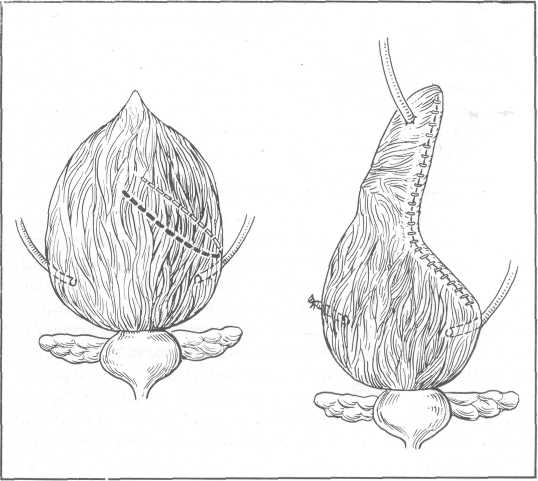
Рис. 181. Замещение нижнего отдела мочеточника по Demel.
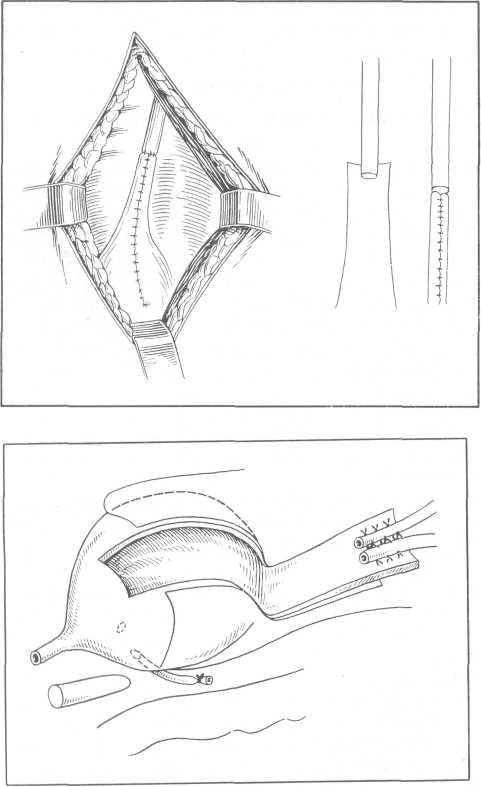
Рис. 182. Пластика мочеточника по Boari.
Рис. 183. Одномоментная пересадка мочеточников в единый центральный лоскут мочевого пузыря.
Трубка формируется двурядными узловыми кетгутовыми швами. Заднюю стенку трубки, покрытую брюшиной, фиксируют к париетальной брюшине таза. Внебрю-шинную часть стенки мочевого пузыря вместе с мочеточниками покрывают париетальной брюшиной задней стенки таза. Таким образом, всю операцию выполняют чрезбрюшинно, но в конечном итоге пузырь и лоскут оказываются перетонизированы (рис. 183).
В сравнительно редких случаях возникает необходимость замещать нижнюю половину мочеточника или весь мочеточник отрезком тонкой кишки. К этому чаще всего вынуждают повторные неудачные реконструктивные операции на том или ином участке мочеточника с последующим образованием стриктур на большом его протяжении или полная функциональная несостоятельность мочеточника. Основным недостатком этих операций считаются нарушения химизма крови. Однако, как показывают отдаленные наблюдения, эти нарушения, выражающиеся в ацидозе, бывают временными и никогда не угрожают жизни больного.
Для ликвидации анатомической или функциональной недостаточности мочеточника с целью лечения гидронефроза или уретерогидронефроза могут применяться операции двух видов: 1) пельвеоилеоцистопластика — замещение всего мочеточника с включением изолированной петли тонкого кишечника между лоханкой и мочевым пузырем; 2) уретероилеоцистоплас-тика — замещение нижнего отдела мочеточника с использованием изолированной петли тонкого кишечника.
Больные, требующие подобных расширенных вмешательств, бывают обычно истощены, находясь в состоянии печеночно-почечной недостаточности. Вследствие этого необходима соответствующая предоперационная подготовка. Подобные операции выполнимы под наркозом с применением миорелак сантов.
Доступ ко всем органам, на которых предстоит вмешательство, должен быть комбинированным — забрюшинно-брюшнополостным.
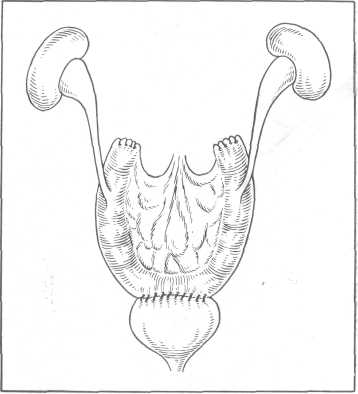
Рис. 184. Замещение нижней половины мочеточников отрезком петли тонкой кишки (по Кучера).
Замещение нижнего отрезка мочеточника выключенным отрезком тонкой кишки производят с учетом стороны поражения, природы заболевания и общего состояния больного. Существует три основных метода замещения кишечной петлей нижнего отдела обоих мочеточников и два мало отличающихся один от другого — для замещения нижнего отрезка одного мочеточника (рис. 184). Основными принципами техники этих операций являются включение петли изоперистальтически и при внутрибрюшинном расположении выключенной петли тонкой кишки забрюшинное расположение участков анастомоза кишки с мочеточником и мочевым пузырем. Наибольшие трудности хирург встречает при замещении нижнего отдела правого мочеточника. Короткая брыжейка кишки и в то же время необходимость включать кишку изоперисталь-тически, что требует иногда ее поворота вокруг оси брыжейки, могут создать условие для возникновения некроза петли. Другой не менее важной деталью этой операции является соразмерность кишки дефекту мочеточника. Чрезмерно длинная петля плохо опорожняется от мочи и слизи, что обусловливает приступы болей и способствует ацидозу.
Вместе с тем отверстие анастомоза должно соответствовать диаметру просвета кишки во избежание застоя мочи в кишечном трансплантате.
Замещение всего мочеточника производят длинной петлей тонкой кишки, но она не должна превышать 30 см и иметь больших перегибов. При выполнении замещения всего мочеточника нет необходимости удалять его остатки по двум соображениям: 1) он не мешает функции кишки, его заменяющей, и 2) неизбежная большая травма приведет к повреждению иннервации лоханки, что еще более ухудшит и без того плохую ее динамику.
При замещении всего мочеточника особенно важно расположить кишку изоперистальтически. В противном случае не исключена возможность скопления слизи в кишке и даже ее забрасывания в лоханку. Это правило легко выполнить при замещении левого мочеточника и не всегда удается при замещении правого мочеточника. В подобных случаях применяют различные варианты поворота отрезка кишки вокруг продольной оси брыжейки (рис. 185).
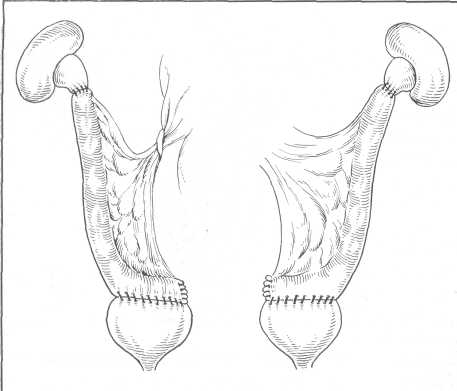
Рис. 185. Замещение всего мочеточника отрезком петли тонкой кишки. Схема операции.
Весьма большие трудности встречает лечение мегауретера. Это результат врожденной неполноценности нервно-мышечных элементов того или иного отдела мочеточника, и оперативное лечение уретерогидронефроза этой этиологии носит весьма паллиативный характер. Наиболее широкое распространение получили операции Бишофа и Иннес Вильяме. При сохраненной полноценности устья мочеточника и поражении только его терминального отдела операция должна заключаться в пересечении мегауретера над препятствием в расширенном и гипертрофированном его отделе и последующей его реимплантации в верхушку мочевого пузыря. Способ реимплантации должен предотвращать пузырно-почечный рефлюкс. Этому требованию лучше всего соответствует способ реимплантации, предложенный Bischoff (рис. 186, а, б, в). В тех случаях, когда мочеточник полностью потерял свои анатомо-функциональные свойства, наиболее целесообразна его замена петлей тонкого кишечника.
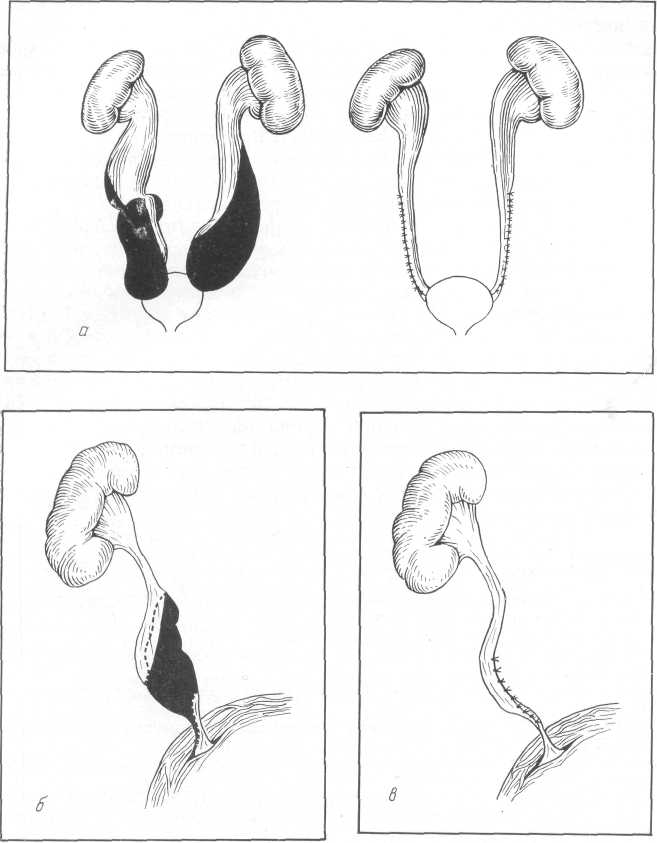
Рис. 186. Операция Бис;оффа при мегауретере (а, б, в).
Особенностью ухода в послеоперационном периоде является обеспечение бесперебойной работы дренажей. С этой целью весьма уместны осторожные их промывания раствором антибиотиков или 0,3% раствором аспирина. Из диеты больного после операции должны быть исключены солеобразующие продукты и ощелачивающие реакцию мочи вещества.
Целесообразно рекомендовать обильное питье, в том числе нещелочных минеральных вод. Если анастомоз между лоханкой и мочеточником накладывался с натяжением, предпочтительно удерживать больного на постельном режиме до 12—14-го дня. При благоприятных обстоятельствах операции можно разрешить больному вставать как только позволят ему силы — на 3—4-е сутки.
Заключительным этапом лечения больного является проверка проходимости нового анастомоза с помощью антеградной пиелографии. Этот метод контроля результатов операции должен применяться с определенной осторожностью. Перед исследованием надо за сутки сменить дренажную трубку и лишь при отсутствии температурной реакции можно произвести исследование. Не надо добиваться проходимости мочеточника путем переполнения лоханки. Необходимо помнить, что послеоперационный отек анастомоза иногда исчезает весьма поздно — к 24—28-му дню, а тонус лоханки восстанавливается в еще более поздние сроки. Лучше повторить исследование, чем вызвать неосторожными манипуляциями атаку пиелонефрита, которая может закончиться нефрэктомией. Убедившись в хорошей проходимости лоханочно-мочеточникового соустья, следует провести 3—5-дневную „тренировку" путем постепенного увеличения срока пережатия дренажа. Лишь при отсутствии ощущения распираний и температурной реакции можно удалить дренаж из почки. Экскреторная урография, подтверждающая восстановление функции почки, является разрешающим выписку больного фактором. В случае осложненного пиелонефритом гидронефроза в дальнейшем должны быть продолжены противовоспалительная терапия с систематическим контролем за составом мочи и периодический контроль за проходимостью новогг соустья путем экскреторной урогра-фии. В целях более полного и быстрого восстановления тонуса лоханки, уменьшения ее объема, предупреждения грубого рубцового процесса в лоханочно-мочеточниковом сегмегге весьма целесообразно применять соответствующую „рассасывающую'' терапию —алоэ, стекловидное тело — пирогенал, гидротерапию, лечебную гимнастику и т. п.
Правильно выполненная но с1основанным показаниям соответствующая виду этиологического фактора гидронефроза пластическая операция не дает летальных исходов, но, к сожалению, не лишена осложнений.
Из наиболее частых осложнений в ближайшие после операции дни следует указать на обострение пиелонефрита. При хорошем оттоке мочи по дренажу у большинства больных удается ликвидировать его. Однако в некоторых случаях при устойчивой к антибиотикам флоре воспалительный процесс продолжает прогрессировать и может в конечном счете привести к нефрэктомии.
Воспалительный процесс в окружающих анастомоз тканях способствует развитию рецидива стриктуры. Поэтому эти операции должны выполняться с большой осторожностью и соблюдением всех правил производства пластических операций — бережное обращение с тканями, ограниченная мобилизация почки, тщательное соблюдение асептики и антисептики. Соответствующая подготовка в предоперационном периоде уменьшает возможные осложнения и является залогом успеха реконструктивного вмешательства на лоханочно-мочеточниковом сегменте.
Несмотря на, казалось бы, хорошо разработанные показания к операции, а также успешное лечение возможных осложнений, результаты оперативного восстановления проходимости лоханочно-мочеточникового сегмента пока еще остаются весьма скромными и могут быть оценены лишь как удовлетворительные. По данным урологической клиники II МОЛМИ, из 109 больных, оперированных по поводу гидронефротической трансформации за 12 лет (1953—1965), меньше чем у половины из них (46%) были получены хорошие отдаленные анатомо-функциональные результаты. У 40% больных результаты были лишь удовлетворительными и у 14% — неудовлетворительными. Основной причиной столь скромных результатов лечения гидронефротической трансформации является пиелонефрит, ускоряющий течение нефросклеротического процесса вплоть до развития почечной недостаточности и нарушения структуры и динамики лоханки и мочеточника.
Литература
Абрамян А. Я. Гидронефрозы. Этиология, клиника, лечение. Медгиз, 1956.
А л к с н е И. О. Урология, 1928, V, 1.
В а с и л ь е в A. A. Z. urol. Chir. 1930, 30, 273.
Голигорский С. Д., К а ц ы ф А. М. Хирургия лоханочно-мочеточникового сегмента. Кишинев, 1966.
Караффа-КорбутК. В. В кн.: Труды VII съезда Российских хирургов. Москва, 1907.
Караффа-Корбут К. В. Значение мочеточников в этиологии почечных заболеваний. Дисс. СПБ, 1908.
К а ц ы ф А. М. К патологии и хирургии лоханочно-мочеточникового сегмента. Дисс. Кишинев, 1962.
К у ч е р а Я. Хирургия гидронефроза и уретерогидронефроза. Прага, 1963.
ЛиндеманВ.К.О влиянии перевязки мочеточников на строение и функцию почки. Дисс. Киев, 1896.
ЛопаткинН. А. Транслюмбальная аортография. Медгиз, 1961.
ЛопаткинН. А. В кн.: Труды Чехословацкого конгресса урологов. Братислава,. 1966.
Л о п а т к и н Н. А. Урология и нефрология, 1966, № 4.
Лопаткин Н. А. В кн.: Труды Кишиневского медицинского института. Кишинев,. 1966.
М ышВ.М. Нов. хир. арх., 1928, 16, 2.
М ы ш В. М. Клинические лекции по урологии. Биомедгиз. М., 1936.
Протопопов С. А. Материалы по анатомии и физиологии мочеточников. Дисс. Казань, 1896.
П ы т е л ь А. Я. Хирургия, 1950, 7, 8.
П ы т е л ь А. Я. Хирургия, 1954, 1, 116.
Пнтель А.Я. Лоханочно-почечные рефлюксы и их клиническое значение. М., 1959..
П ы т е л ь Ю. А. Интрамуральный нервный аппарат верхних мочевых путей человека. Дисс. М., 1960.
П ы т е л ь Ю. А. В кн.: Вопросы нормальной и патологической морфологии периферической нервной системы. Волгоград, 1962, стр. 211.
Спасокукоцкий С. И. В кн.: Труды VIII съезда Российских хирургов. М., 1908..
Федоров СП. Хирургия почек и мочеточников. Л., 1925.
Ф р у м к и н А. П. Урология, 1957, № 3.
ФрумкинА. П. В кн.: Актуальные вопросы урологии. М., 1962, стр. 7.
А к к i 1 i с М., Ztschr. Urol., 1965, 3, 25—34.
Albarran J., Medicine operatoire des voies urinaires. Masson, Paris, 1909.
Allemann R., Ztschr. Urol., 1935, 29, 414.
A 11 s с h u 1 R., FedorS., Am. Heart J., 1953, 46, 291.
Anderson C, Hydronephrosis. London, 1963.
Babies A.,Renyi-Vamos F., Das LymphgefaGsystem der Niere und seine Bedeu-
tung in der Nierenpathologie und Ghirurgie. Budapest, 1957. В e d r n a J., Rozhl. Chir., 1947, 26, 157. В e d г n a J., S t e f a n H., Lek. Zplavy VLA, 1957, 2, 3. Berlyne G., Quat. J. Med., 1961, 30, 120, 339. Chiaudano M., Minerva chir., 1958, 13, 1074. С о u v e J a i r e R., L e с a J., J. Urol. med. chir., 1956, 62, 253. Gulp O.S., De Wee rdJ. H., Proc. staff meet. Mayo clinic, 1951, 26, 483. CulpO.S.,De Weerd J. H., J. Urol., 1954, 71, 523. DemelR, Zbl. Chir., 1924, 51, 2008. Deuticke P., Urol. Cut. Rev., 1949, 53, 74. D о s s A. K., J. Urol., 1947, 57, 521. FengerC.J.A.M. A., 1894, 22, 335. F о 1 e у F., J. Urol., 1937, 38, 6, 643. F u с h s F., Ztschr. urol. Chir., 1931, 33, 1. G i b s о n Т. В., Surg. Gynec. Obstet,. 1945, 80, 485. G i b s о n T. E. J. Urol., 1956, 75, 1. G i b s о n Т. В., J. Urol., 1956, 76, 708.
Go t ts chal к G., My 11 e M., Am. J. Physiol., 1959, 196, 927. H e r d m a n J., J а с о N., Brit. J. Urol., 1950, 22, 1, 55. HinmanF.J, Urol., 1919, 3, 147.
HinmanF., Principles and practice of urology. Philadelphia, 1936, p. 232, 487. HiiimanF, Surgery, 1945, 17, 6, 816. H i n m a n F., J. Urol., 1957, 78, 4, 376. Hryntschak Th., Ztschr. Urol., 1936, 30, 598. I d b о h r n H., Acta radiol., Suppl., 136, 1956.
Jackson G., GriebleH. Arch, intern, med., 1957, 100, 5, 692. К a i s e r 1 i n g H., Soostmeyer Th. Wien, klin. Wschr., 1939, 1113. Kiil F., The function of the ureter and renal pelvis. Philadelphia—London, 1957. К ti s t e r B. G. E., Arch. klin. Surg., 1892, 44, 850. L i с h t e n b e r g A., J. A. M. A., 1929, 93, 1706. LichtenbergA., Radiology, 1929, 15, 664. Li ch t e nberg A., J. A. M. A., 1929, 93, 1706. L u b a s h S. J. Urol., 1935, 34, 222.
Maluf N., Helper t В., Surg. Gynec. Obstet., 1956, 102, 1, 27. Marion G., Traite d'urologie. Masson, Paris, 1935. M a r i о n G. J. d'Urol., 1939, 48, 5.
Michalowski E., Urologia operacyjna. Warszawa, 1954. MichaZowskiB. u. Modelski W., Ztschr. Urol., 1958, 51, 10, 549. M о d e 1 s к i W., Pol. przegl. chirurg., 1960, 32, 11, 1125. Mohacsi L., Ztschr. Urol., 1965, 149. N e u w i r t K., Urol. Cut. Rev., 1948, 52, 351. N i с о 1 a i С h., J. Urol. (Baltimore), 1964, 92, 5, 347.
PerskyL, Storaasli J., AustenG., J. Urol. (Baltimore), 1955, 73, 740. Renyi-Vamos F., Magasi P., Matyus E., Acta med. Acad. Sci. hung., 1954,
6, 1.
SachdevaJ. a. MaryaS., Indian J. Surg., 1965, 27, 1, 18. Scardino P., Prince Ch., Vertical flap ureteropelvioplasty.: Preliminary report.
South M. J., 1953, 46, 325, Git. Year'Book Urol., 1953—1954.
Schiick O., Andrysek O., Andryskova, J. Urol. int. (Basel), 1962, 14, 111. SchwyzerA.,A new pyelo-ureteral-plastic for hydronephrosis. Surg. Clin. North Amer.,
1923 3
S i g e 1 A., Ztschr. Urol., 1962, 55, 7, 361. Singh Sh., Indian J. Surg., 1964, 26, 11, 870.
Stefan H., Hydronefroza у detskem veku. Rozh. v. chirurg., 1964, 43, 9, 633. VoelckerF. u. LichtenbergA. von (1906), Munch, med. Wschr., 1906, 53, 105. W i n к e 1 K., Nierendiagnostik mit Radioisotopen. Stuttgart, 1964, S. 45. YoungH.H, Surg. Gynec. Obstet., 1932, 54, 26.
Глава пятнадцатая
Опухоли почек
и верхних мочевых путей
За последнюю четверть века опухоли почек встречаются чаще, чем это отмечалось раньше, что следует объяснить значительным улучшением диагностики, притом в более ранних стадиях заболевания. Так, по данным клиники, руководимой С. П. Федоровым (1934), новообразования почек составляли 10,3% по отношению к другим хирургическим заболеваниям почек. По материалам урологической клиники II МОЛМИ, за период с 1953 по 1966 г. этот процент достиг 19,4.
Среди всех больных с опухолью почек доброкачественные новообразования встречаются у 6%, злокачественные — у 94%. Почечные раки составляют 1,9—2,4% (В. А. Самсонов, 1964) всех раковых новообразований вообще. По отношению ко всем заболеваниям мочеполовой системы новообразования почек составляют 6%. Двусторонние злокачественные новообразования почек встречаются исключительно редко (1,1%).
Эпителиальные опухоли почечной лоханки и мочеточника являются более редкими видами новообразований, нежели опухоли почечной паренхимы. По отношению ко всем опухолям почек и верхних мочевых путей, по данным Д. С. Мураткина (1961), они составляют 16%. Fierro и Scarsi собрали к 1964 г. из литературы описание 623 случаев опухолей лоханки и 549 случаев опухолей мочеточника.
В то время как у взрослых опухоли почек составляют 4% всех новообразований вообще, у детей этот процент достигает 25 (С. Д. Терновский, 1931; Allen, 1962) и даже 32,7 (Ю. А. Шелудько, 1965).
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
В возникновении и развитии опухолей ряд клиницистов придает известное значение травме, хроническим воспалительным процессам в почке и мочевых путях, влиянию химических веществ на почечную ткань, раздражению мочевых путей камнями, порокам развития и др. Однако вряд ли эти факторы имеют решающее значение в этиологии и патогенезе бласто-матозного процесса. Во всяком случае убедительных доказательств в пользу существования причинной связи между указанными этиологическими моментами и опухолью почки у человека не имеется.
По аналогии с развитием папиллярных опухолей мочевого пузыря, в возникновении которых доказана роль дериватов анилина (бетанафтил-амин, бензидин и другие ароматические амины), возможно, что и в появлении папиллярных новообразований почечной лоханки эти факторы также играют известную этиологическую роль. Еще в 1934 г. М. Л. Мухаринский экспериментально показал, что в результате введения в почечную лоханку
животных каменноугольной смолы возникала в большем проценте случаев опухоль лоханки. Возможно, что некоторые папиллярные опухоли лоханки и мочевых путей имеют инфекционно-вирусное происхождение. Ряд клиницистов отмечал частую связь опухолей почечной лоханки, особенно непапиллярного рака, с камнями и инфекцией в лоханке (Kretschmer, 1917, и др.).
За последние годы рядом экспериментаторов получены данные, указывающие на большое значение эндокринных факторов в происхождении опухолей почек. Так, Kirkman и Bacon (1950) показали, что у самцов хомяков подкожное введение таблеток диэтилстильбэстрола способствует возникновению в корковом веществе почек двусторонних аденом и аденокарцином. У самцов, у которых, помимо диэтилстильбэстрола, вводили подкожно и холестерол, а также у самок такие опухоли не возникали.
Особый интерес представляют случаи возникновения опухоли после многолетнего нахождения в почке торотраста (Th232).
Hubmann и Нoer (1964) наблюдали 4 больных (возраст от 55 до 62 лет) раком почечной лоханки, развившимся в связи с длительным нахождением рентгеноконтрастного вещества — торотраста — в почечной ткани. Торо-траст проник в паренхиму почки путем пиелоренального рефлюкса в момент ретроградной пиелографии, имевшей место 18—30 лет назад. У больных наблюдался плоскоклеточный рак лоханки и обнаруживались остатки торотраста в sinus renalis и в перисосочковой форникальной клетчатке.
Эти же авторы собрали из литературы описания 15 подобных случаев за период с 1949 по 1963 г. (Alken с соавт., 1960). Возраст больных колебался от 44 до 75 лет. У 8 имел место плоскоклеточный рак лоханки у 2 — солидный рак почки, у 1 — медуллярный рак, у 1 — аденокарцинома, у 1 — гипернефроидный рак и у 2 — саркома почки. Латентный период (срок от момента пиелографии торотрастом до появления первых симптомов болезни) составлял у этих больных от 15 до 30 лет.
Chamot (1965) наблюдал 4 больных, у которых развился рак почки спустя 15—20 лет после пиелографии с применением тория. У каждого из этих больных были обнаружены отложения тория в ткани опухоли удаленной почки. Об аналогичных наблюдениях сообщил Biicheler (1966).
В возникновении гипернефроидного рака и смешанной опухоли Вильмса в прежние годы придавали большое значение порокам эмбрионального развития почки.
В 1883 г. видный немецкий патолог Grawitz выдвинул гипотезу, согласно которой большинство опухолей почки, имеющих строение, схожее с клетками коркового слоя надпочечника, развиваются якобы из занесенных в почку еще в эмбриональном периоде островков ткани надпочечника. Вследствие этого предложено было называть эти опухоли гипернефромами. Эта надпочечниковая теория возникновения опухолей почки, несмотря на существовавшие критические возражения видных патологоанатомов, прочно вошла в медицинскую науку и сохранялась до недавнего времени. Однако тщательные гистологические исследования многих морфологов последних лет с убедительностью показали несостоятельность теории Гравица и установили почечный генез этих опухолей (А. И. Абрикосов, 1930; И. В. Давыдовский, 1961; А. И. Струков, 1961; А. И. Маянц, 1949; Allen, 1962, и др.). Работы Е. В. Евстюхиной (1955), О. М. Ординой (1959), Allen (1962), Meli-cow (1944) и др. убедительно свидетельствуют о том, что источником роста гипернефроидного рака является, за небольшим исключением, эпителий почечных канальцев и что эти опухоли в своем развитии проходят фазу аденомы.
Исходя из современных воззрений на гистогенез этих гипернефроидных опухолей, нужно признать несостоятельным старый термин „гипернефрома". Более правильно называть эти опухоли гипернефроидным раком, что было предложено А. И. Абрикосовым еще в 1929 г.
Что же касается патогенеза смешанных опухолей почки (опухоль Вильмса), то наиболее гармонирующим с гистологической и эмбриологической точки зрения является установление тесной их взаимосвязи с почечной бластомой, т.е. признание неопластических изменений в почечной закладке. Смешанные опухоли Вильмса — мезенхимального происхождения и не имеют ничего общего с органоидной тератомой. По мнению Wilms (1899), смешанные опухоли происходят из недифференцированной мезодер-мальной ткани, клетки которой проникают в паренхиму первичной почки, а затем во вторичную почку, где и возникает опухоль.
Есть основание полагать, что карциногенные субстанции, выделямые почками или уротелием лоханки, могут вызвать опухолевый рост на любом месте протяжения мочевого тракта. Наряду с этим папиллярные опухоли, располагающиеся в нижних мочевых путях, могут имплантироваться вверх по уротелию из мочевого пузыря.
ПАТОЛОГИЧЕСКАЯ АНАТОМИЯ
Поскольку опухоли почечной паренхимы и опухоли лоханки во многом отличаются как по своей структуре, так и путям распространения и требуют различных оперативных методов лечения, вполне оправдано их выделение в отдельные группы.
В практических целях наиболее целесообразно выделять следующие группы и виды новообразований почек.
I. Опухоли почечной паренхимы
ДОБРОКАЧЕСТВЕННЫЕ ОПУХОЛИ ПОЧКИ
Аденома. Аденомы встречаются в 4% исследованных почек на аутопсии. Они обычно малых размеров: редко достигают большой величины. Наблюдаются твердые и кистозные аденомы. Они желтоватого цвета, в виде сферических узлов, располагаются в корковом слое почки. К 1950 г. в литературе было описано 56 случаев большой величины кортикальных аденом. Такие большие аденомы могут вызвать гематурию, боль и привести к гидронефрозу. У мужчин аденомы наблюдаются в 3 раза чаще, чем у женщин. Кортикальные аденомы происходят из канальцевого эпителия (дистальной части канальцев). В кистовидных аденомах часто имеются очаги сосочковой пролиферации.

Морфологические исследования Е. В. Евтюхиной (1959), О. М. Ординой (1959), Allen (1962) и др. показали, что кортикальные, канальцевые аденомы независимо от их разновидности следует рассматривать как новообразования в предраковом состоянии.
Липомы. Липомы наблюдаются в почечной паренхиме, в почечной капсуле и в паренефральной клетчатке. Липомы почечной паренхимы обычно имеют диаметр 3—5 мм, располагаются в субкапсулярной зоне коркового слоя. Редко они достигают больших размеров. Липомы, возникающие из жировой ткани почечного синуса, т.е. вблизи ворот почки, могут инвагини-ровать лоханку и тем самым симулировать опухоль, исходящую из лоханки. Липомы часто сочетаются с гемангиомами.
Большие параренальные липомы дают симптомы в зависимости от степени сдавления ими прилегающих тканей, сосудов, мочеточника, соседних органов. Эти опухоли достигают часто очень больших размеров, смещают почку в противоположную сторону и рецидивируют. Уместно отметить, что при кахексии больного параренальные липомы не уменьшаются в размерах.
Фибромы и лейомиомы. Это обычно маленькие опухоли, серо-белого цвета, величиной от 3 до 5 мм в диаметре. Фибромы располагаются преимущественно в мозговом веществе и редко в корковом и капсуле почки, а лейомиомы, наоборот, — преимущественно субкапсулярно. Клиническое значение эти опухоли имеют лишь тогда, когда они достигают больших размеров. Большие лейомиомы часто приобретают черты, напоминающие по гистологическому строению лейомиосаркому: иногда они могут метастази-ровать.
Ангиномы и гемангиомы. К 1963 г. было описано в литературе 144 случая ангиомы почки больших размеров (Hagen, 1963). Ангиома почки встречается более часто, чем принято считать. Гемангиомы — сравнительно редкие доброкачественные опухоли, обычно единичные. Они располагаются в мозговом веществе или почечной лоханке, редко — в корковом веществе. Диаметр их от 1—2 мм до нескольких сантиметров: они губчатого строения, темно-красного цвета. Микроскопически гемангиомы состоят из тонкостенных синусов, напоминающих лимфатические сосуды или канальцы. Даже маленькие гемангиомы могут давать профузную гематурию.
Лимфангиомы. Лимфангиомы по своему строению близки к ангиомам. Опухоли эти, обычно множественные, имеют кавернозное строение. Размеры их от конопляного зерна до лесного ореха. Из вещества опухоли при разрезе вытекает лимфа. Располагаются лимфангиомы чаще всего в мозговом веществе и вблизи почечного синуса, в непосредственной близости к лоханке.
Прочие доброкачественные опухоли почки — остеомы, хиндромы, мик-сомы, дермоиды, шваннома и др. — встречаются очень редко, вследствие чего они большого практического значения не имеют (Р. А. Шахбазов, 1957; Galde-гоп с соавт., 1965). Наоборот, злокачественные опухоли встречаются часто и значение морфологии их весьма важно для диагностики и выбора соответствующих видов лечения.
Рис. 187. Гипернефроидный рак почки (макрофото)
ЗЛОКАЧЕСТВЕННЫЕ ОПУХОЛИ ПОЧКИ
Гипернефроидный рак. Эта опухоль в литературе обозначается различными терминами— „гипернефрома", „аденокарцинома", „опухоль со светлыми клетками", и т. п., однако наиболее правильным термином является „гипернефроидный рак".
Гипернефроидный рак составляет 9/ю всех злокачественных опухолей почки и около 3,5% всех висцеральных, раков. Гипернефроидный рак может занимать часть почечной паренхимы, полюс ее или центральную часть, иметь размеры от 3 см в диаметре до огромного образования. Известны случаи гипернефроидного рака весом 3300 г (Bell, 1946).
Маленькие гипернефроидные опухоли возникают исключительно в корковом веществе почки и диагностика их возможна только при помощи ангиографии. Диаметр 3 см избран как пограничный между доброкачественной канальцевой аденомой и гипернефроидным раком. По Bell (1946), лишь одна опухоль из 45 аденом размером менее 3 см является злокачественной. Важно, что гипернефроидные опухоли менее 5—6 см в диаметре редко дают метастазы.
Гипернефроидный рак почки — образование сферической, куполообразной формы, умеренно мягкой консистенции (рис. 187, 188, 189). На разрезе опухоль имеет необычайно пестрый рисунок желтовато-коричневого, местами красного цвета. Опухоли больших размеров содержат некротические и геморрагические очаги и серые участки — полосы новообразованной фиброзной ткани: местами имеются кисты с плотными, гладкими, беловатыми стенками; эти кисты содержат геморрагическую, прозрачную или шоколадного цвета жидкость. Опухоли длительное время, особенно если они небольших размеров, оказываются инкапсулированными. Нарушение целости капсулы в результате прорастания ее опухолью имеет место в 35—40% случаев. Большие опухоли обычно прорастают в соседние участки почечной паренхимы, в лоханку и в паранефральную клетчатку. Прорастание опухоли почки в лоханку встречается более чем в 50% случаев.
Гипернефроидные опухоли обнаруживают особую склонность к врастанию в почечную вену и нижнюю полую вену. Известны случаи, когда при таком врастании опухоли в почечную вену и в нижнюю полую вену отсутствовали метастазы и оперативное удаление почки, пораженной опухолью, с удалением из нижней полой вены опухолевого „языка" приводило к выздоровлению больного.
Рис. 188. Гипернефроидный рак почки (макрофото).
В результате прорастания и сдавления больших сосудов почки опухолью возникает нарушение венозного оттока, вследствие чего наблюдается большое расширение вен околопочечной клетчатки. Такие расширенные вены становятся тонкостенными и могут достичь 1 см в диаметре.
Гистологически клетки опухоли несколько напоминают по виду каналь-цевый эпителий. Некоторые виды опухоли состоят из больших светлых полигональных или цилиндрических клеток с маленькими однообразными ядрами и цитоплазмой, содержащей жир и витамин А, гликоген и гидропи-ческие вакуоли. Другие виды гипернефроидного рака содержат светлые клетки, перемешанные с гранулярными и веретенообразными клетками. Такие виды опухоли иногда принимаются за саркому или вариант смешанной опухоли Вильмса.
Рис. 189. Гипернефроидный рак почки (макрофото)
Гранулярные клетки, по мнению некоторых морфологов (Mehcow, 1944), происходят из висцерального или париетального клубочкового эпителия либо из гранулярных клеток аденомы. Однако мнение о происхождении этих опухолей из капсулы Шумлянского—Боумена мало кем поддерживается. Отдельные клетки опухоли имеют включения гиалиновых капель, гемосидерина гранул; они напоминают эпителий почечных канальцев.
Различают два основных вида опухолевых клеток: 1) чаще клетки содержат светлую вакуолизированную ячеистую протоплазму и гипохромное ядро, располагающееся в центре клетки или слегка эксцентрично. Эти клетки весьма напоминают клетки надпочечников; 2) клетки много реже содержат темно окрашивающуюся зернистую протоплазму с овальным или округлым ядром. Из этих клеток состоят различные опухолевые структуры: папиллярные, трубчатые, солидные (В. А. Самсонов, 1964). В зависимости от преобладающего вида клеток в опухоли многие морфологи различают светлоклеточный, или гипернефроидный, рак и темноклеточную, зернисто-клеточную аденокарциному. Поскольку оба вида клеток могут находиться в одной и той же опухоли, указанное разграничение новообразований является условным: гипернефроидная опухоль почки в 40% случаев имеет смешанное строение. Установлено, что все виды железистого рака и близко стоящие к нему злокачественные эпителиальные новообразования почек исходят из эпителия почечной паренхимы (В. А. Самсонов, 1964).
Следовательно, имеется большая вариабильность клеток гипернефро-идной опухоли. Нередко опухоли содержат альвеолярные, сосочковые, кистозные и канальцевые включения, а также широкие тонкостенные синусы. В таких синусах часто обнаруживаются инвазированные бластоматозные клетки.
Гипернефроидная опухоль может содержать очаги некроза, кальцифика-ции, старые и свежие кровоизлияния.
Экстраренальная гипернефрома. В забрюшинном пространстве по соседству с почкой иногда развивается гипернефроидная опухоль типа мезо-нефромы, исходящая из эмбриональных остатков. Опухоль располагается обычно впереди почки, распространяясь медленно. Почка сдавливается опухолью, но прорастания ее капсулы не наблюдается (при дифференциальном диагнозе следует иметь в виду параганглиому). Такие опухоли рецидивируют. Метастазы бывают в легких и в печени. Опухоль имеет капсулу; в веществе опухоли некрозы и кровоизлияния. Гистологическое исследование выявляет картину гипернефроидного рака. Лечение — удаление опухоли. Рентгенотерапия после операции не эффективна. Smith, Webb и Price (1965), описавшие 5 таких наблюдений, указывают на большое сходство гистологического строения гипернефроидного рака, ретроперитонеальной мезонефромы, овариальных и цервикальных мезонефром.
Гипернефроидный рак почки у детей в противоположность взрослым наблюдается очень редко. М. Н. Егоров (1930) среди 15 000 вскрытий детей в возрасте до 14 лет смог найти лишь 2 случая гипернефроидного рака почки. По С. Д. Терновскому (1931), гипернефроидный рак почки у детей — явление весьма редкое; он наблюдал это у 2 детей.
Негипернефроидный рак. К этой группе новообразований относят: а) аденокарциному, б) альвеолярный рак и в) скирр.
Ряд морфологов не выделяет аденокарциному как отдельный вид новообразований почек, а считает ее разновидностью гипернефроидного рака. При аденокарциноме опухоль содержит трубчатые образования, выстланные однослойным эпителием. При альвеолярном раке опухоль имеет ячеистое строение, ячейки заполнены мелкими, беспорядочно расположенными опухолевыми клетками. Капсула опухоли выражена слабо. Альвеолярные раки очень редко дают метастазы в костную систему и в то же время отличаются большой злокачественностью.
Почка, пораженная скиррозным раком, имеет весьма плотную консистенцию. Опухоль серого цвета, пронизанная белыми тяжами. Для этого вида рака характерно обильное развитие стромы, состоящей из волокнистой соединительной ткани.
Саркома. Истинные саркомы почечной паренхимы очень редки. Их не следует смешивать с опухолью Вильмса, которую иногда называют аде-носаркомой. Большинство описанных фибросарком в действительности является лейомиосаркомами и липосаркомами, фибромикросаркомами и миксосаркомами. Опухоли, принимаемые за круглоклеточные карциномы, в действительности оказываются лимфомами, эмбриональными миосарко-мами или анапластическими карциномами. В 1932 г. Judd и Donald описали 20 случаев гистологически доказанных сарком почки среди 570 почечных злокачественных опухолей (3,5%). Саркомы могут быть круглоклеточные, веретенообразные и смешанные. Смешанные саркомы крайне злокачественны.
Саркомы почек взрослых редко метастазируют, хотя они могут достигать больших размеров.
Смешанная опухоль (опухоль Вильмса). Смешанная опухоль почки — заболевание детей. Опухоль располагается как в центре, так и на полюсах ее, занимает преимущественно корковое вещество. Первичное двустороннее поражение почек встречается редко. Опухоль имеет круглую форму и окружена псевдокапсулой. Размеры опухоли могут достигать значительной величины и большого веса. На разрезе опухоль имеет пестрый вид, напоминает тератому с неравномерными твердыми и желатиноподобными кистоз-ными и геморрагическими участками.
Гистологические разновидности смешанных опухолей почки весьма велики. Типичным строением этих опухолей является гломеруло-тубулярная структура с незрелыми гиперхромными веретенообразными клетками стромы. Эти новообразования являются в большей или меньшей степени аналогами структуры субкапсулярной части почки человеческого эмбриона. Такое смешанное строение являлось поводом для наименования этих новообразований аденосаркомой (синоним опухоли Вильмса).
Помимо рассеянных в опухоли очагов пролиферации гломерулотубуляр-ных структур, имеются и другие элементы: 1) очаги, напоминающие лейо-миосаркому, 2) очаги поперечнополосатых мышц, 3) канальцевые кисты, 4) фиброматозные очаги, 5) хондроматозные и остеоидные очаги, 6) участки дегенерации, включая очаги плотного фиброза, некроза и жирового замещения. При опухоли Вильмса метастазы могут отличаться от основного новообразования. Как и в других сложных опухолях наиболее анапласти-ческие элементы опухоли, вероятно, метастазируют первыми. Основная опухоль может не содержать участков ткани, имеющихся в метастатических ее узлах. Хотя смешанная опухоль Вильмса — новообразование преимущественно детского возраста, она иногда встречается и у взрослых. В 1958 г. в литературе описано около 150 случаев смешанной опухоли почки у взрослых.
Для детей раннего возраста характерны смешанные опухоли; у детей более старшего возраста иногда встречается гипернефроидный рак. Среди 54 детей, наблюдавшихся К. А. Москачевой (1953) по поводу опухолей почек, гипернефроидный рак встретился у одного мальчика 14 лет. Hourse и Yurdin (1959) описали 3 наблюдения гипернефроидного рака почки у детей. К 1960 г. в литературе было описано 54 случая гипернефроидного рака почки у детей и новорожденных.
Рост почечной опухоли. Рост почечной опухоли широко варьирует. Известно наблюдение Johnson (1946), когда злокачественная опухоль почки в течение 5 лет увеличилась только на 3 см в диаметре, оставаясь округлой и хорошо ограниченной. Лишь спустя 5 лет опухоль проросла окружающие ткани и метастазировала в легкие. Наряду с этим часто наблюдаются больные с весьма быстрым ростом новообразования. Гипернефроидный раковый узел может в течение длительного времени быть инкапсулирован и весьма медленно увеличиваться в размерах.
Множественные опухоли в почке. Иногда рак поражает обе почки. Bailey и Goungblood (1950) описали такой случай и собрали из литературы 11 подобных наблюдений. Эти авторы справедливо указывают, что далеко не всегда возможно установить, является ли каждая опухоль в почке первичной или вторичной, т.е. метастатической. Malament (1965) описал случай 14-летнего наблюдения за больным двусторонним гипернефроидным раком почки. Сравнительно редко встречаются в одной и той же почке множественные опухоли. Однако большинство описанных в литературе таких наблюдений представляет собой не диссеминированные опухоли, а единую опухоль, имеющую в разных ее сегментах неоднородное строение. Исключительно редко приходится наблюдать в почке комбинацию злокачественной и доброкачественной опухолей с опухолью почечной лоханки (Pennisi, Russi, 1957) и, наоборот, нередко встречается сосуществование в почке опухоли и кисты.
Рак в единственной почке встречается редко. Stackpole (1965) собрал из литературы 22 таких случая. Ранее у больных была удалена одна почка по разным причинам, в том числе по поводу новообразования. Гипернефроидный рак наблюдался у 12 больных, рак лоханки — у 9 и саркома почки — у одного больного (случай Burghele, 1956).
Опухолевые метастазы в почке. Почка является органом, в котором сравнительно часто возникают метастазы. Опухоли, способные давать распространенные метастазы, часто сопровождаются метастазированием и в почки. Среди таких опухолей следует назвать бронхогенные раки, злокачественные меланомы и различные лимфомы. Они могут иногда поражать не только почечную паренхиму, но и почечную лоханку. Далее приходится наблюдать опухолевые метастазы в почку при раке молочной грудной железы, раке глотки, гортани, контралатеральной почки, надпочечника, щитовидной железы, желудка, поджелудочной железы, печени, пищевода, толстого кишечника и др.
Опухоли надпочечника (33%), легких (18%), щитовидной железы (15%) и противоположной почки (12%) являются главными источниками метастазов в почку (Allen, 1962).
Метастазирование опухолей в почку осуществляется: 1) прямым внедрением опухоли в почку с соседнего органа, а также с соседнего пораженного бластомой лимфатического узла; 2) лимфогенным и венозным путем; 3) гематогенно, по аорто-артериальной системе.
Поражение почки метастазом по лимфатическим сосудам особенно часто наблюдается при эпидермоидном раке почечной лоханки.
Ретроградная инвазия почечных вен и их внутрипочечных разветвлений наблюдается при раке яичника и других органов, новообразования которых распространяются в первую очередь по системе нижней- полой вены. Довольно часто встречаются эмболические артериальные метастазы опухоли в почку. Они могут быть настолько большими, что закупоривают крупные ветви и вызывают инфаркт почки.
Метастатические очаги в почке макроскопически выявляются сферическими лентовидными или ромбоидальными узлами различной величины. Иногда метастатические узлы принимают пирамидальную или коническую форму.
Несмотря на значительно частое появление в почке метастазов, функция ее из-за этого редко нарушается.
Известны случаи, когда обширные метастазы опухоли в области ворот почки, окружающие основные ее сосуды и сдавливающие мочеточник, приводят к артериальной гипертонии и развитию гидронефроза.
