
Лабораторная работа № 13
ОПЫТНОЕ ОПРЕДЕЛЕНИЕ ПОКАЗАТЕЛЯ АДИАБАТЫ
ВОЗДУХА
Цель работы – изучение основных соотношений между термодинамическими параметрами и величинами, процессов происходящих в идеальном газе; экспериментальное определение показателя адиабаты для воз-
духа методом Клемана и Дезорма. |
|
О |
1. Метод измерения и расчетные соотношения |
|
|
Адиабатным называют процесс, происходящий в термодинамической |
||
системеФбез теплообмена с окружающей средой. Первое начало термоди- |
||
намики в д фференциальной форме для адиабатного процесса имеет вид: |
||
и |
0 dU δA . |
(1) |
|
||
Здесь dU — бесконечно малое изменение внутренней энергии системы, |
|||
Я |
|
|
|
A — бесконечно малая работа, совершаемая термодинамической систе- |
|||
мой в ходе данного процесса. |
|
|
|
С |
|
|
|
Известно, что для одного моля идеального газа |
|
|
|
dU CV dT , |
|
(2) |
|
НδA pdV , |
|
(3) |
|
где CV — молярная теплоемкость газа при постоянном объеме ; р — дав- |
|||
ление; dT и dV — бесконечно Ималые изменения температуры и объема |
|||
соответственно. Подставляя (2) и (3) в (1), получаем |
|
|
|
У |
|
(4) |
|
CV dT pdV |
0. |
|
|
Запишем уравнение состояния для одного моля идеального газа: |
|
||
pV RT . |
М |
|
|
Дифференцируя это уравнение, получаем |
|
||
|
Э |
|
|
pdV Vdp RdT . |
(5) |
||
Выразив из (5) dT и подставив в (4), получим дифференциальноеИуравнение, связывающее объем и давление идеального газа в адиабатном процессе:
CV R pdV CVVdp 0. |
(6) |
Учитывая, что CV R Cp — молярная теплоемкость идеального газа
при постоянном давлении, и, вводя обозначение γ |
Сp |
, получим: |
||||
C |
||||||
|
|
|
|
|
||
|
dV |
dp |
|
V |
|
|
γ |
0. |
|
(7) |
|||
V |
|
|||||
|
p |
|
|
|
||
Для идеального газа молярные теплоемкости CV и C p |
не зависят от тем- |
||||||||||
пературы: |
i 2 |
|
|
|
|
i |
|
|
|
||
|
|
|
|
|
|
|
|
||||
C p |
|
|
R |
; CV |
|
|
R , |
|
|
(8) |
|
2 |
|
|
2 |
|
|
||||||
где i — число степеней свободы молекулы идеального газа. Считая воз- |
|||||||||||
дух при атмосферном давлении идеальным газом, получаем, что показа- |
|||||||||||
тель — постоянная для данного газа величина. В этом случае интегри- |
|||||||||||
О |
|
|
|
|
рование уравнения |
(7) |
дает |
||||
|
|
|
|
выражение: |
|
|
|
||||
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
pV γ const. |
|
(9) |
|
|
|
|
|
|
Уравнение |
(9) |
называют |
||||
и |
|
|
|
|
уравнением |
адиабаты (урав- |
|||||
Ф |
|
|
|
|
нением Пуассона), |
а показа- |
|||||
Я |
|
|
|
|
тель степени — показателем |
||||||
|
|
|
|
адиабаты. |
|
|
|
||||
|
|
|
|
|
|
|
|
||||
С |
|
|
|
|
Проведя экспериментально |
||||||
|
|
и |
|
анализируя процесс адиа- |
|||||||
|
|
батного расширения воздуха, |
|||||||||
|
|
|
|
|
|||||||
Н |
можно определить |
значение |
|||||||||
показателя |
адиабаты |
при |
|||||||||
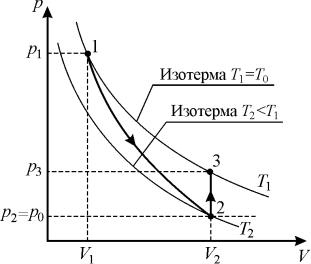
Рис. 1 Адиабатное расширение 1–2 |
|
|
комнатной |
температуре (ме- |
|||||||
и изохорный нагрев воздуха 2–3 |
|
||||||||||
|
тод Клемана и Дезорма). |
|
|||||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
Имеем баллон достаточно |
||||
большой емкости, который наполнен воздухом при атмосферном давле- |
|||||||||||
нии. С помощью компрессора вИбаллоне создается избыточное давление, |
|||||||||||
которое может быть измерено манометром. Баллон снабжен клапаном |
|||||||||||
большого проходного сечения. |
|
|
|
У |
|
|
|
||||
|
|
|
|
|
|
М |
|
|
|||
Мысленно выделим в центральной части сосуда небольшой объем V1, |
|||||||||||
занимаемый некоторой массой воздуха. В дальнейшем будем рассматри- |
|||||||||||
вать процессы, происходящие с этой массой воздуха. |
Пусть начальная |
||||||||||
|
|
|
|
|
|
|
|
Э |
|
||
температура воздуха равна комнатной температуре Т1, а начальное давле- |
|||||||||||
ние р1 несколько выше атмосферного. |
|
|
|
Давление р1 |
можно выразить через атмосферное и избыточное давле- |
||
ние: |
|
, |
И |
|
p1 p0 p |
(10) |
|
где p0 — атмосферное давление; p — избыточное давление воздуха, ко-
торое можно определить по показаниям манометра.
Если быстро открыть клапан, соединяющий сосуд с атмосферой, то в результате адиабатного расширения давление воздуха в сосуде упадет до р2 = р0, а объем рассматриваемой массы воздуха увеличится до V2. Температура воздуха при его адиабатном расширении снижается до Т2 < Т1, так как уменьшается его внутренняя энергия. Пусть клапан закрывается точно в момент окончания адиабатного расширения. В этот момент состоя-
ние воздуха характеризуется параметрами p2,T2,V2 (рис. 1). При адиабат-
ном переходе воздуха из состояния 1 в состояние 2, из выражения (9) получаем
|
|
|
|
|
pV γ |
p V γ . |
|
|
|
|
|
|
|
|
(11) |
|||||||||||||
|
|
|
|
|
1 |
1 |
|
|
|
|
|
2 |
2 |
|
|
|
|
|
|
|
|
|
|
|||||
После закрытия клапана происходит |
|
теплообмен воздуха с окружаю- |
||||||||||||||||||||||||||
щей средой через стенки баллона при постоянном объеме. Температура |
||||||||||||||||||||||||||||
воздуха приближается к температуре окружающей среды T1. При этом |
||||||||||||||||||||||||||||
давление воздуха в сосуде возрастает до |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
p3 p0 p . |
|
|
|
|
|
|
|
|
(12) |
||||||||||||||
ОПараметры состояния рассматриваемого количества воздуха после |
||||||||||||||||||||||||||||
Ф |
|
|
|
|
|
|
|
p3,T3,V3 |
, причем V2 V3. |
|
||||||||||||||||||
окончания изохорного процесса: |
|
|
||||||||||||||||||||||||||
Поскольку температуры воздуха в состояниях 1 и 3 одинаковы, то для |
||||||||||||||||||||||||||||
выделенной массы воздуха можно записать: |
|
|
|
|
|
|
||||||||||||||||||||||
|
Я |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
и p1V1 p3V3 p3V2 . |
|
|
|
|
|
(13) |
|||||||||||||||||||||
Решая систему уравнений (11) и (13), получаем |
|
|
|
|||||||||||||||||||||||||
|
Сp γ p |
|
|
|
|
|
|
|
|
|
|
p2 |
|
|
||||||||||||||
|
|
|
|
|
|
|
ln |
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
p |
|
||||||||||||||||||
|
|
3 |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
||||
|
|
|
|
|
|
|
|
|
, γ = |
|
|
|
|
|
|
|
. |
|
||||||||||
|
p |
|
p |
|
|
|
|
p |
|
|||||||||||||||||||
|
|
Н |
|
|
|
|
|
|
|
3 |
|
|
|
|||||||||||||||
|
1 |
|
|
|
|
1 |
|
|
|
|
|
|
|
ln |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
p |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|||
С учетом (10) и (12) находим |
|
И |
|
|
|
|||||||||||||||||||||||
Тогда |
|
|
|
|
p3 p1 (p p ). |
(14) |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
p |
|
|
|
p |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
ln |
|
|
1 |
|
|
|
|
У |
|
||||||||||||||
|
|
|
|
|
|
p |
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
М |
|
|||||||
|
γ = |
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
. |
(15) |
||||||||
|
|
|
|
|
|
|
|
|
|
p |
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
ln |
|
p1 |
|
(p |
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
p1 |
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Поскольку избыточные давления |
|
|
|
|
и |
|
|
|
|
|
|
|
||||||||||||||||
|
|
p |
|
|
p |
|
p весьма малы по сравне- |
|||||||||||||||||||||
нию с |
p1, то можно использовать разложение функцииЭln(1 x) в ряд при |
|||||||||||||||||||||||||||
x = 1, |
ограничившись первым членом разложения: ln(1 x) x . |
Тогда |
||||||||||||||||||||||||||
из (15) получим |
|
|
|
|
|
|
|
γ |
|
|
p |
|
|
|
|
|
|
|
|
И |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
. |
|
|
|
|
|
(16) |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
p p |
|
|
|
|
|
|
|
|
|
||||
Избыточные давления p и p измеряются экспериментально. В уста-
новках последней модификации измерения давления производится двумя различными приборами. Пьезоэлектронный манометр с цифровой индикацией непосредственно на экране дисплея высвечивает значение избыточного давления. Водяной U-образный манометр позволяет определить значение избыточного давления по разности уровней воды в коленах ма-
нометра. При этом p ρgH , а p ρgh, где H и h разности уровней воды
в коленах манометра в состояниях 1 и 3 воздуха; — плотность воды; g
— ускорение свободного падения. Расчет коэффициента адиабаты по данным этого манометра производится по формуле
γ |
H |
|
(17) |
|
H h |
||||
|
|
|||
2. Описание схемы установки |
|
|||
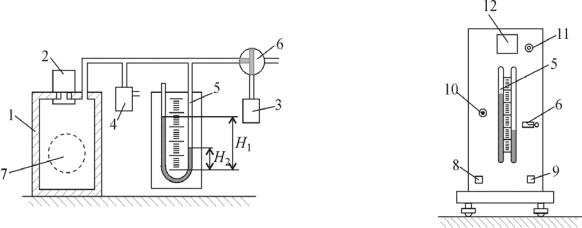
Схема установки представлена на рис. 2,3. Основными элементами |
||||
Оустановки (рис. 2) являются баллон 1, изготовленный из стекла, с быстро- |
||||
Ф |
|
|
|
|
действующим электромагнитным клапаном 2; микрокомпрессор 3, пред- |
||||
назначенный для создания избыточного давления воздуха в баллоне; |
пье- |
|||
и |
|
|
|
|
зоэлектронный манометр 4; водяной U — образный манометр 5 с милли- |
||||
метровой шкалой, который позволяет измерять давление газа в баллоне |
||||
Я |
|
|
|
|
относительно атмосферного (избыточное давление) по положению уровней в трубках H1 и H2; трехходовой кран 6 служит для подключения баллона к микрокомпрессору, соединения системы с атмосферой либо пере-
крытию системы. Как уже сказано выше, все процессы происходят с не- |
|
которой массой газаС7, мысленно выделенной внутри объема баллона и |
|
Н |
|
находящегося вдали от стенок и клапана. |
|
И |
|
У |
|
М |
|
|
И |
Рис. 2. Схема установки |
Э |
Рис. 3. Лицевая панель лабораторного модуля
Установка размещена в стандартном модуле (рис. 3). Баллон с газом и электромагнитным клапаном, а также микрокомпрессор расположены внутри модуля. На лицевую панель выведены:
–тумблер 8 «СЕТЬ» подключения модуля к электрической сети;
–тумблер 9 «КОМПРЕССОР» включения микрокомпрессора;
–кнопка 10 открытия и закрытия клапана;
–трубки U — образного манометра 5;
–тумблер 11 включения пьезоэлектронного измерителя давления;
–дисплей 12 измерителя давления;
– ручка трехходового крана 6, которая может устанавливаться в положениях «КОМПРЕССОР» (бал-
|
лон подключен к компрессору), |
||||
|
«ЗАКРЫТ» (линия, связываю- |
||||
|
щая баллон с компрессором пе- |
||||
|
рекрыта), |
«АТМОСФЕРА» |
|||
|
(баллон соединен с атмосфе- |
||||
О |
рой). |
|
|
|
|
В исходном |
состоянии |
||||
давление |
воздуха |
в баллоне |
|||
|
|||||
Ф |
равно атмосферному давлению, |
||||
а температура равна температу- |
|||||
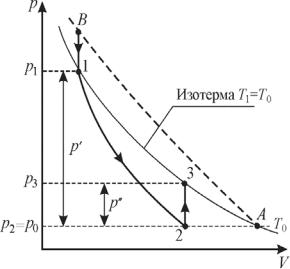
ре окружающей среды (точка А |
|||||
на рис. 4). |
|
|
на |
||
Рис. 4. Процессы, происходящие с |
Согласно указаниям |
||||
выделенной массой газа в ходе |
установке установив кран 6 в |
||||
и |
|||||
эксперимента |
положение |
«КОМПРЕССОР», |
|||
Я |
включают |
микрокомпрессор |
и |
||
С |
|
|
|
|
|
повышают давление в системе, при этом выделенный объем воздуха 7 в баллоне сжимается и его температура становится выше температуры
окружающей среды. Условно этот процесс можно представить на зависимости р(V) в виде пунктирнойНкривой А–В (рис. 4). После закрытия крана
6 происходит процесс изохорного охлаждения воздуха до температуры
шается, что фиксируется по уменьшениюИизбыточного давления в системе. Этот процесс занимает несколько минут. О его окончании судят по
окружающей среды Т0 (процесс В–С). При этом давление воздуха умень-
стабилизации показаний манометров. Таким образом система приведена к |
|
начальному состоянию с давлением р1Увыше атмосферного и температу- |
|
|
М |
рой Т1, равной температуре окружающей среды Т0 (комнатная температу- |
|
ра) (точка 1 на графике р(V)). По показаниям приборов записывают избы- |
|
|
и разницу уровней в коленах U-образного манометра |
точное давление p |
|
|
Э |
H = H1 – H2. Нажмем и быстро отпустим кнопку 10. После нажатия кноп-
ки 10 клапан открывается и происходит процесс адиабатного расширения воздуха. При этом температура газа уменьшается, и давлениеИтакже уменьшается до атмосферного (процесс 1—2). Поскольку электромагнитный клапан срабатывает очень быстро, и время открытия достаточно мало, то клапан закрывается точно в момент окончания адиабатного процесса (состояние 2). После закрытия клапана начинается процесс изохорного нагрева воздуха до комнатной температуры T0, при этом давление начнет возрастать (процесс 2—3). Об окончании этого процесса судят по стабилизации показаний манометров. Записывают показания манометров p и
h = h1 – h2.
3. Порядок выполнения работы
1. Заполните табл. 1 спецификации измерительных приборов. Запишите данные установки и условия проведения опытов.
2. В соответствие с указаниями на установке подключите модуль к электрической сети, нажав тумблер 8 «СЕТЬ».
3. Включите пьезоэлектронный измеритель избыточного давления, нажав кнопку 11. При этом на экране дисплея высветятся цифры.
4. Убедитесь, что уровни жидкости в коленах U-образного манометра 5 совпадают и находятся посредине манометрических трубок.
5. Рукоятку трехходового крана 6 установите в положение «КОМ- |
|||
ПРЕССОР». Тумблером 9 включите компрессор. Нагнетание воздуха |
|||
Ф |
|
|
|
производите до тех пор, пока разность уровней в коленах манометра не |
|||
достигнет 200-250 мм, а показания измерителя — (2000—2500) Па. |
|||
и |
|
|
|
6. Установ те кран 6 в положение «ЗАКРЫТО» и выждите 2—4 ми- |
|||
нуты, пока температура воздуха в баллоне не станет равной температуре |
|||
Я |
|
|
|
окружающей среды Т0. При этом показания манометров стабилизируют- |
|||
ся. Запишите в табл. 2 показания измерителя давления |
|
||
p и высоту уров- |
|||
С |
|
|
|
ней воды в коленах U-образного манометра Н1 и Н2. |
|
|
|
7. Нажмите и быстро отпустите кнопку 10. Произошел процесс адиа- |
|||
батного расширения воздуха до атмосферного давления p0 (при этом |
|||
Н |
|
|
|
температура воздуха в баллоне упала) и начался процесс изохорного |
|||
нагрева, при этом давление в системе стало возрастать. |
|
||
И |
|
|
|
8. После выравнивания температур давление стабилизируется. Запи- |
|||
шите в табл. 2 значение избыточного давления |
|
и разность уровней в |
|
p |
|||
трубках водяного манометра h1 и h2.
9.Установите кран 6 в положение «АТМОСФЕРА», при этом давление в системе станет равным атмосферному.
10.Пункты 5—9 повторите пять раз. Результаты опытов занесите в табл. 2. УМ
|
|
|
|
|
Таблица 1 |
|
|
|
|
|
Э |
|
|
Спецификация измерительных приборов |
|
|||||
|
ния |
ния |
заний |
|
Инструменталь |
|
Название прибора |
Пределы |
Цена |
Дискрет- |
|
|
- |
и его тип |
измере- |
деле- |
ность пока- |
ная погрешность |
||
|
|
|
|
|
|
|
Водяной U- |
, мм |
1 мм |
- |
|
1 мм |
|
образный мано- |
|
|
|
|
|
|
метр |
|
|
|
|
|
|
Пьезоэлектрон- |
, Па |
- |
1 Па |
|
5 Па |
|
ный манометр |
|
|
|
|
|
|
|
|
|
|
Данные установки, условия опытов |
|
|
|
|
|
|
||||||||||||||
|
Температура окружающей среды |
|
|
t0 = |
|
|
|
|
|
|
|
|
|
|
||||||||||
|
Давление окружающей среды |
|
|
|
р0 = |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
Результаты измерений |
|
|
|
|
|
|
|
|
Таблица 2 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
№ |
p , |
|
p , |
|
Н1, |
|
Н2, |
|
Н = Н1 – Н2 |
|
|
|
h1, |
|
|
h2, |
h = h1 – h2 |
||||||
О |
|
|
|
|
|
|
мм |
|
мм |
|
|
|
|
|
|
мм |
|
|
мм |
|
мм |
|||
|
опыта |
Па |
|
Па |
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ф |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
и |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
4. Обработка результатов измерений |
|
|
|
|
|
|
||||||||||||||
|
|
Я |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
1. По формулам (16) и (17) рассчитайте значения γ . Проведите расчет |
|||||||||||||||||||||||
|
|
|
|
С |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
среднего |
значения |
γ |
|
, полученного |
по данным |
|
каждого |
из |
приборов. |
||||||||||||||
|
Сравните результаты. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
2. Рассчитайте абсолютные погрешности измерения |
|
при использова- |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
Н |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
нии показаний манометров 5 и 12 по формулам |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
H 2 |
|
2 H |
|
2 |
|
|
p 2 |
|
|
2 p |
|
2 |
||||||||
|
γ = γ |
|
|
|
, γp = γp |
|
|
|
|
|
|
|
|
. |
||||||||||
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
H |
|
H h |
|
|
У |
|
p p |
|
|
|
|||||||||||
|
|
|
|
|
|
|
p |
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
И |
|
|
|
|
|
|
||||||||
3.Запишите окончательный результат в стандартной форме.
4.Рассчитайте теоретическое значение , считая воздух идеальным двухатомным газом. Сравните теоретическое и экспериментальное значе-М
ния .
5.Контрольные вопросы
1.Какой процесс называется адиабатным. Запишите первое начало термодинамики для адиабатного процесса.
2.Изобразите графически на диаграмме (р,V) процессы адиабатного
иизотермического расширения газов. Почему при адиабатном расширении температура газа убывает?
3.Напишите уравнение Пуассона для адиабатного процесса. От чего зависит теоретическое значение показателя адиабаты для идеального газа?
4.Как в лабораторной работе определяется экспериментальное значение показателя адиабаты? Какие величины измеряются непосредствен-Э
но?
5. |
Расскажите порядок выполнения работы. Изобразите графически |
|
на диаграмме (р,V) термодинамические процессы, происходящие с неко- |
||
торой массой воздуха в сосуде. |
||
6. |
Почему процесс, происходящий с воздухом в сосуде после откры- |
|
тия клапана можно считать адиабатным? |
||
7. |
Изобразите графически на диаграмме (р,V) процессы, происходя- |
|
щие после открытия клапана. К какому термодинамическому состоянию |
||
придет воздух, если удерживать клапан в открытом состоянии достаточно |
||
долго? Изобразите в (р,V) диаграмме соответствующий процесс. |
||
8. |
Представьте вывод уравнения адиабаты. |
|
О |
Рекомендуемая литература |
|
Ф |
|
|
1.Савельев И.В. Курс общей физики: Учебное пособие. В 3-х тт. Т.1. Механика. Молекулярная физика. 5-е изд., стер. — СПб.: Изд-во «Лань». 2006 г. С. 268 — 286, 302 — 310.
2.Д.А. Иванов, И.В. Иванова, А.Н. Седов, А.В. Славов. Механика. Молекулярная физика и термодинамика: Конспект лекций/ Под ред. А.В.Я
Кириченко. — М.:СИздательство МЭИ. 2003. С.118 — 121, 122 — 134.
Н И У М Э И
