
- •Физико-химические основы технологии электронных средств
- •2. Технологии связанные с травлением
- •2.1. Травление материалов в жидких средах
- •2.2. Химическое полирующее травление поверхности
- •2.3. Электро-химическое полирующее травление поверхности
- •2.4. Ионно-плазменное травление
- •2.4.1. Ионно – плазменное травление.
- •2.4.2. Газовое травление полупроводниковых подложек. Пример
- •2.4.3. Плазмохимическое травление полупроводниковых пластин
- •2.4.4. Оборудование, технологические приемы и контроль качества плазмохимического травления
Высшее профессиональное образование
Физико-химические основы технологии электронных средств
Допущено
Учебно-методическим объединением вузов
по университетскому политехническому образованию
в качестве учебного пособия
для специальности 000000000 «Проектирование и технология электронных средств»
Оглавление
Стр.
Введение…………………………………………………………………………………….
Раздел 1……………………………………………………………………………………..
Раздел 2……………………………………………………………………………………..
Раздел 3……………………………………………………………………………………..
Раздел 4……………………………………………………………………………………..
Раздел 5……………………………………………………………………………………..
Раздел 6……………………………………………………………………………………..
Раздел 7……………………………………………………………………………………..
Заключение………………………………………………………………………………….
Приложение 1……………………………………………………………………………….
Приложение 2……………………………………………………………………………….
Приложение 3……………………………………………………………………………….
Приложение 4……………………………………………………………………………….
Приложение 5………………………………………………………………………………..
Принятые сокращения
ЭА – электронная аппаратура
ЭВС – электронно-вычислительные средства
ЭВМ – электронно-вычислительные машины
РЭА – радиоэлектронная аппаратура
2. Технологии связанные с травлением
2.1. Травление материалов в жидких средах
Химическое травление подразделяют на изотропное, анизотропное и селективное.
И з о т р о п н о е т р а в л е н и е —растворение материала, например, полупроводникового, с одинаковой скоростью по всем кристаллографическим направлениям — позволяет равномерно стравливать тонкие слои и получать ровную поверхность. Такое травление называют такжеполирующимилихимическим полированием.
А н и з о т р о п н о е т р а в л е н и е— растворение материала, например, полупроводникового с неодинаковой скоростью по различным кристаллографическим направлениям — позволяет вытравливать глубокие канавки и щели.
С е л е к т и в н о е т р а в л е н и е— растворение материала, например, полупроводникового с повышенной скоростью травления в местах выхода на поверхность структурных дефектов. Благодаря такому травлению они становятся различимыми невооруженным глазом или под микроскопом, поэтому можно определить их вид и плотность.
Процесс травления состоит из пяти этапов:
1) диффузии реагентов к поверхности полупроводникового материала;
2) адсорбции их поверхностью;
3) химического или электрохимического взаимодействия реагента с поверхностью;
4) десорбции продуктов реакции
5) диффузии их от поверхности.
Скорость травления определяется скоростью самого медленного этапа.
Травители, в которых самыми медленными этапами являются диффузионные, называются полирующими.Эти травители нечувствительны к неоднородностям поверхностей, сглаживают шероховатости и выравнивают микрорельеф. Скорость травления существенно зависит от вязкости и перемешивания травителя и незначительно от температуры.
Травители, в которых самыми медленными являются поверхностные реакции, называются избирательными.Скорость травления в них зависит от температуры, структуры и кристаллографической ориентации поверхности и не зависит от вязкости и перемешивания травителя. Избирательные травители с неодинаковой скоростью травления в различных кристаллографических направлениях называютанизотропными, а с большой скоростью в области структурных дефектов —селективными.

Рис. 2.1. Разновидности травления
Химическое травление полупроводниковых пластин основано на процессах окисления их поверхности и растворения образовавшихся оксидов. Поэтому травильные смеси обычно состоят из окислителя, комплексообразователя(для образования растворимых соединений с оксидом),растворителя, ускорителя илизамедлителя реакций окисления и растворения оксида и специальных добавок(например, обеспечивающих избирательное действие травителя). В большинстве случаев составы травителей подбираютсяопытнымпутем.
В процессе изготовления пластин полирующим травлением удаляют нарушенныйслой полупроводникапосле грубой обработки (резки, шлифовки, скругления края), а такжеочищают их от загрязнений(глубокое травление) в водном 20-30%-ном растворе КОН или NaOH при 95-125оС. Травление кремния в щелочном травителе состоит из реакций
его окисления до диоксида, гидратации и взаимодействия его со щелочью с образованием растворимых силикатов:
Si + 2H2O SiO2 + 2H2
SiO2 + xH2O SiO2 x2H2O
SiO2 xH2O + 2KOH K2SiO2 + (x+1)H2O
В этом травителе вода является окислителем, а растворителем оксида (комплексообразователем) — щелочь. Скорость растворения кремния зависит от концентрации щелочи и максимальна при концентрации 1-1,5 моль/л и температуре 100С. Повышение скорости травления обусловлено увеличением степени гидратации окисла, что увеличивает его растворимость в кремнии, а снижение — уменьшением растворимости силикатов, осаждающихся на поверхности пластины. Поэтому очень важно травление выполнять в избытке щелочи, иначе на поверхности возможно образование нерастворимых кремниевых кислот, а следовательно, и полное прекращение процесса.
Недостатками щелочных травителей являются возможность загрязнения поверхности кремния ионами щелочных металлов, которые трудно удаляются, и растворимость в них маскирующей пленки SiO2. Рельеф поверхности после обработки в таком травителе зависит в основном от рельефа предшествующей механической обработки.
В ряде случаев полирующее травление, используемое для уменьшения остаточныхнарушений на рабочей поверхностиокончательно обработанных пластин, выполняют в смеси кислот HF, HNO3, CH3COOH, при этом окислителем является азотная кислота:
Si + 4HNO3 SiO2 + 4NO2+ 2H2O
Фтористоводородная кислота служит комплексообразователем, который переводит диоксид кремния в тетрафторид кремния:
SiO2 + 4HFSiF4+ 2H2O
Уксусная кислота является разбавителем и ингибитором (замедлителем реакции).

Рис. 2.2. Химико-динамическая полировка изделий
При травлении поверхность пластины 1, помещенной во вращающийся стакан 2 специальной установки, омывается ламинарным потоком травителя 3, что обеспечивает хороший доступ его к поверхности и отвод от нее продуктов химических реакций. Этот вид обработки называют химико-динамической полировкой (ХДП).
Для химико-динамической полировки арсенида галлия применяют растворы на основе H2SO4H2O2H2O2 с высоким содержанием серной кислоты, систему Вт2— метиловый спирт (метанол), а также смеси азотной, фосфорной и серной кислот.
Недостатком кислотного травления является необходимость утилизации кислот. Особенно затруднен слив фтористоводородной кислоты, которую нейтрализуют специальными методами из-за повышенной активности фтора.
Анизотропным травлениемполучают микрорельеф (углубления различных конфигураций, мезаобласти) на поверхности полупроводниковых пластин,
дифракционные решетки, разделительные канавки для диэлектрической изоляции и др.


Рис. 1.23. Анизотропное травление полупроводников
Обычно это травление является локальным, т.е. выполняется через окна и дорожки в маскирующих пленках SiO2,Si3N4, поэтому его скорость, форма углубления и боковое подтравливание зависят от кристаллографического направления их сторон. Например, при травлении дорожек, ориентированных в направлении <110> на кремнии с ориентацией (100), можно получить V-образные, а в направлении <100> - прямоугольные дорожки.
Анизотропное травление кремния производят в водном растворе КОН с концентрацией 300-350 г/л. При добавлении в щелочной травитель Н-пропилового или изопропилового спирта температура травления снижается до 70-80 °С. Для арсенида галлия используют кислые или щелочные растворы перекиси водорода и безводные растворы брома в диметилформамиде или метиловом спирте.
Селективное травлениеприменяют для выявления на поверхности пластин дислокаций, дефектов упаковки, точечных дефектов, линий скольжения, а также микроцарапин и микровыколов. Для повышения избирательности действия в состав травителя вводят поверхностно-активные вещества, которые увеличивают разность между скоростями травления дефектного и бездефектных участков.
В качестве травителя для пластин кремния ориентации (111) используют смесь из 250 г хромового ангидрида СгО3, 500 мл воды и 500 мл фтористоводородной кислотыHF, а ориентации (100) - бихроматный травитель, состоящий из 22 г К2Сr207, 500 мл Н2О и 1000 мл HF. Для селективного травления пластин арсенида галлия ориентации (111) применяют травитель, состоящий из 2 ч. Н2О, 1 ч. Сr03и 1 ч. HF с небольшой добавкой азотнокислого серебра АgNО3, а ориентации (100) - расплав КОН при 300-350 °С. Для четкого выявления дефектов на протравленной поверхности время травления должно быть 1-2 мин.
ХИМИЧЕСКИЕ ЖИДКИЕ СМЕСИ ДЛЯ ТРАВЛЕНИЯ
(применяемые в микроэлектронном производстве)
Обработку пластин травлением в жидких смесях применяют для удаления загрязнений, оставшихся после отмывки в растворителях (пленки оксидов и механически нарушенного слоя, возникающего при резке, шлифовке и полировке), доведения толщины исходных пластин до заданных размеров, выявления границы p-n-переходов и структурных дефектов, получения заданного рельефа на поверхности (лунок, мезаструктур, рисунка) , а также при различных структурных исследованиях.
Структура нарушенного слоя после резки:
I– зона рельефа,
II– зона трещин и дислокационных скоплений,
III– упруго-деформированная зона.
Рис. 2.4. Три зоны стравливания поверхности полупроводников
Iзона состоит из поликристаллических структурных элементов, толщина ее составляет 0,3-0,5 размера микронеровностей.
Непосредственно под рельефом находится зона II– зона трещин и дислокационных скоплений, которые являются главными дефектами резки. Это наиболее глубокая зона нарушений. Этот слой в 3-6 раз толще, чем первый, и имеет мозаичную структуру. Плотность и размер трещин уменьшается с глубиной. Между трещинами действуют упругие напряжения.
В зоне IIIнаходятся области с остаточными упругими напряжениями.
В зависимости от обрабатываемого материала для травления используют кислоты, щелочи и соли, которые должны содержать минимальное количество посторонних примесей и механических включений. Травильные смеси приготовляют из материалов трех основных марок: ХЧ (химически чистый), ЧДА (чистый для анализа) и Ч (чистый).
Кислоты— это химические соединения, молекулы которых состоят из кислотного остатка и связанных с ним атомов водорода, способных замещаться атомами металлов с образованием солей. Кислоты бывают кислородные (Н2 SO4, Н2 CO3,HNO3и др). и бескислородные (HCl,H2S,HFи др.). Число атомов водорода в молекуле кислоты определяет ее основность. Так, кислотыHCl,HF,HNO3- одноосновные, Н2 SO4, Н2 CO3- двухосновные, а Н3 PO4- трехосновная. Многие кислоты хорошо растворимы в воде. По степени диссоциации в водных растворах различают сильные (Н2 SO4,HCl,HNO3), средние (Н3 PO4, HF) и слабые (СН3СООН) кислоты. Для обнаружения кислот используют индикаторы - красители, обладающие способностью в присутствии кислоты изменять свою окраску. Например, водные растворы лакмуса (или лакмусовая бумага) и метилоранжа в присутствии свободных кислот окрашиваются соответственно в красный и розовый цвета.
Необходимо помнить, что все кислоты при попадании на кожу вызывают сильные ожоги, поэтому работать с ними необходимо в резиновых перчатках, халате и фартуке.
Щелочи- это растворимые в воде основания. Хорошо растворимыми в воде основаниями являются широко применяемые в полупроводниковом производстве КОН и NaOH. Щелочи, как и кислоты, являются ядовитыми веществами и сильно разъедают кожу, вызывая ожоги. Растворимые в воде щелочи изменяют окраску индикаторов: лакмуса - в синий цвет, а фенолфталеина - в малиновый.
Соли- это химические соединения, молекулы которые состоят из атомов кислотного остатка и связанных с ними атомов металла. Обычно соли являются продуктами замещения атомов водорода атомами металла в кислотах.
Травители для германияприготовляют в зависимости от требований химической обработки: зеркальности или матовости поверхности пластин, селективности, выявления дефектов и др. Для травления германия используют пергидролевые, щелочные и кислотные травители.
Пергидролевые травителипредставляют собой смеси пероксида водорода Н2О2с водой различных концентраций (обычно от 5 до 30 % Н2О2). Травление проводят при температуре кипения. После обработки в таком травителе пластины германия имеют матовую поверхность.
Щелочные травителив основном используются для увеличения скорости травления и состоят из смеси пероксида водорода и щелочи (КОН, NaOH).
Кислотные травители,наиболее широко применяемые для травления германия, состоят из определенного количества азотной, плавиковой (фтористоводородной) и уксусной кислот, а также различных добавок. Так, для обработки поверхности пластин германия, имеющих кристаллографическую ориентацию (100), применяют травильную смесь из 10 мл азотной, 5 мл плавиковой и 10 мл уксусной кислот. Для получения полированной (зеркальной) поверхности используют смесь, состоящую из 25 мл азотной, 15 мл плавиковой, 15 мл уксусной кислот и 0,3 мл раствора брома. Для выявленияp-n-перехода или дислокаций используют смесь из азотной и плавиковой кислот, взятых в соотношении 3:1. При обработке пластин, имеющих ориентацию (111), применяют травитель, состоящий из 50 мл азотной, 10 мл плавиковой кислот, 5 мл воды и 200 мгAgN03. Зеркальную поверхность германия получают также, используя травильную смесь, содержащую азотную и плавиковую кислоты, смешанные с 10%-ным раствором Сu(NО3)2.
Травители для кремния бывают щелочными и кислотными. Разновидностью их являются анизотропные травители.
Щелочные травители(смеси водных растворов КОН иNaOH, имеющие концентрацию от 1 до 30 %) используют для получения шероховатой (матовой) поверхности и анизотропного (избирательного) травления.
Кислотные травители (смесь азотной и плавиковой кислот) обладают полирующим действием и создают зеркальную поверхность. Максимальную скорость травления получают при соотношениях НNО3: HF = 2:9. Для замедления скорости травления кремния в такую травильную смесь вводят уксусную кислоту. Для выявления дислокаций используют смесь азотной, плавиковой и уксусной кислот в соотношении 2:9:4.
Анизотропный травитель, состоящий из 250 г гидроокиси калия, 800 мл воды, 25 мл пропанола, 25 мл бутанола и 0,5 г кремния, обладает высокой, низкой и промежуточной скоростями травления соответственно в направлениях кристаллографических плоскостей (100), (111) и (110). Добавка кремния в этот травитель позволяет контролировать процесс. Финишную обработку пластин кремния непосредственно перед процессом окисления или эпитаксиального наращивания проводят, используя следующие смеси: Н2О2: Н2SО4: Н2О = 1:1:3; Н2О2:NН3:NН4ОH: Н2О = 1:1:2; Н2О2 :NН4ОH: Н2О = 1:1:3.
Травители для материалов типа АШВVпредставляют собой смеси кислот. Так, для травления арсенида галлия используют смесь азотной, соляной кислот и воды, взятых в соотношении 1: 2:2, а антимонида галлия - смесь азотной и плавиковой кислот, взятых в соотношении 9:5. Обработку арсенида индия проводят в смеси азотной, плавиковой и уксусной кислот, взятых в соотношении 10:3:3.
Травители для материалов типа АIIВVIпредставляют собой смеси различных химических веществ. Так, для обработкиCdSиспользуют смесь из 1 мл серной кислоты, 100 мл воды и 0-08 г оксида хрома СгО3, а для обработкиZnSможно применять кипящий раствор концентрированной азотной кислоты.
Травители для защитных SiO2 и Si3N4 и тонких металлических пленок имеют различные составы. Так, пленкиSiO2хорошо травятся в плавиковой кислоте, однако ее не применяют из-за малого содержания ионов фтора, а используют буферные травители, состоящие изHF,NH4Fи Н2О, взятых в соотношении 2:9:2. ПленкиSi3N4хорошо травятся в кипящей фосфорной кислоте, концентрированной плавиковой кислоте и буферном травителе.
Пленки медитравят в смеси серной, азотной кислот и хлорного железа. Кислоты берут в соотношении от 2 :1 до 1 : 2. При этом следует учитывать, что азотная кислота ускоряет процесс травления, а серная - замедляет.
Пленки алюминияможно травить в 10-20 %-ных щелочных растворах КОН и NaOH с добавкамиNaCl,NaNO3,Na3PO4,Na2CO3. Для кислотного травления пленок алюминия используют составы на основе серной, ортофосфорной и плавиковой кислот, например травитель, содержащий 65 г СrО3, 350 г Н2S04и 1000 г воды. Для травления алюминиевых пленок используют также смеси на основе хлорного железа:FеС13: НCl= 10:1.
Пленки серебрахорошо травятся в концентрированных азотной и серной кислотах. В качестве сильного травителя применяют смеси азотной и серной кислот, взятых в соотношении 1:1. Более мягкие травители для серебра - 10-30%-ные растворы соляной кислоты, а также следующая смесь: СrО3 : Н2S04 : Н20 = 2 : 1 : 100.
Пленки золотатравят в царской водке - смеси азотной и соляной кислот, взятых в соотношении 1 : 3.
Пленки хроматравят в смеси Н2S04: Н20 = 1 :1, а молибдена - в смеси Н2S04: НN03: Н20 = 1 : 2 : 300.
Пленки вольфрамапри комнатной температуре в соляной, азотной, серной и плавиковой кислотах не травятся. Интенсивное их травление происходит в смеси азотной и плавиковой кислот, взятых в соотношении 1:1.
Пленки никелятравят в 50 %-ной азотной кислоте, а также в следующей смеси НN03: Н2S04:NaCl= 2 : 2 : 1.
Пленки танталаустойчивы к действию азотной кислоты, хромовой смеси, фосфорной и соляной кислот. Однако плавиковая кислота и ее соли энергично реагируют с танталом.
Пленки ниобиялучше всего растворяются в смеси азотной и плавиковой кислот.
Пленки свинцарастворяются в концентрированной соляной кислоте практически с постоянной скоростью. Азотная кислота реагирует со свинцом более энергично в виде разбавленных растворов.
ХИМИЧЕСКИЕ ЖИДКИЕ СМЕСИ ДЛЯ ТРАВЛЕНИЯ
(применяемые в производстве печатных плат)
Особенности жидкостного травления печатных плат
Травление печатных плат — это процесс удаления с поверхности меди окислов, что необходимо для качественного проведения последующих операций, например, покрытия. При этом происходит также выявление структуры основного металла.
Для повторения. Химическое травление металлов является окислительно-восстановительным процессом. Существует электрохимический ряд активности металлов:
K, Na, Ca, Mg, Al, Mn, Zn, Fe, Cr, Ni, Sn, Pb, H, Cu, Hg, Ag, Pt, Au
Положение металла в этом ряду характеризует его окислительно-восстановительные свойства. Чем левее расположен металл в ряду активности, тем он: а) химически более активен — легче окисляется (отдает электроны); б) обладает большими восстановительными свойствами. Каждый металл этого ряда “вытесняет” все металлы, расположенные правее его, из растворов их солей.
Любой металл, расположенный левее водорода в ряду активности, может растворяться в кислотах, т.е. восстанавливать водород:
Fe o + H 2 2+SO 42- Fe 2+ (SO 4) 22- + H 2 o
Металлы, образующие амфотерный окисел, могут растворяться в щелочах (например, это алюминий). Те вещества, которые не могут восстанавливать водород из кислот, требуют для растворения предварительного окисления. Следовательно, вопрос о растворении материалов сводится к вопросу об окислителях для них, так как травление большинства окислов не представляет трудности.
В качестве окислителей могут быть использованы кислород, галогены, ионы металлов Ме n+ , ионы водорода Н+, сложные анионы (CrO4)2-; (NO3)- и др., перекись водорода H2O2.
Травление окислов представляет собой обычные реакции обмена, важную роль в которых играют температура и присутствие катализаторов.
При повышении температуры уменьшается энергия активации химических процессов и становятся возможными взаимодействия, которые при рассмотрении с позиции активности металлов не должны произойти. Продукты реакции могут быть газообразными, жидкими и твердыми нерастворимыми. В последнем случае для протекания процесса травления необходимо вводить добавки, растворяющие основной продукт реакции. Удаление газообразных, жидких и твердых продуктов осуществляется простым перемешиванием раствора. Скорость процесса травления рассчитывают по формуле:
_ Е
kT
= К Се , где
— К - константа скорости;
— С - концентрация молекул травителя;
— Е - энергия активации процесса травления;
— k- постоянная Больцмана;
— Т - абсолютная температура, К.
В этом случае скорость травления определяется в основном, энергией активации Е. Поверхность меди и других металлов имеет нарушения и неоднородности структуры, как и полупроводники, поэтому процесс травления пойдет по типу селективного. В печатных платах это может привести к растравливанию меди, что недопустимо. Поэтому процесс переводят в полирующее травления, для чего искусственно затрудняют отвод продуктов реакции и подход ионов травителя. Тогда скорость травления становится:
_ Е
kT
диф.= К(С - С1) е,
где — С1- концентрация молекул травителя у поверхности детали.
Скорость травления в этом случае ограничивается скоростью диффузии молекул травителя через разделительный слой, и избирательного растравливания материала не происходит. Так обеспечивается процесс химического полирования меди и других металлов.
Травильные растворы на основе хлорного железа
Растворы хлорного железа находят широкое применение в качестве травильных растворов для меди, медных сплавов, ковара и стали, в печатных схемах, фотогравировке и полировке металлов.
Если печатные платы имеют защитное покрытие сплавом олово-свинец, то хлорное железо применять нельзя, так как оно разрушает покрытие.
Травильный раствор на основе хлорного железа представляет собой водный раствор хлорного железа с концентрацией 400 500 г/л. Температура травления Т = 40С. В травильном растворе в результате реакции гидролиза образуется свободная соляная кислота:
FeCl 3 + 3 H 2O = Fe (OH) 3 + 3 HCl.
Для предотвращения образования нерастворимых осадков Fe(OH)3 в травильный раствор обычно добавляют до 5% соляной кислоты. Добавляют также вещества, способствующие смачиванию и исключающие вспенивание травителя.
Химия процесса травления.На поверхности меди, соприкасающейся с трехвалентным железом, ионFe3+окисляет медь до хлористой меди с образованием зеленого хлористого железа:
FeCl3 +CuFeCl2+CuCl
В массе раствора хлористая медь (CuCl) далее окисляется до хлорной меди (CuCl2):
FeCl3 +CuClFeCl2 +CuCl 2
Поскольку в травильном растворе образуется хлорная медь, динамическое равновесие реакции нарушается:
CuCl2+Cu2CuCl
По мере использования, травильный раствор истощается и скорость травления резко уменьшается. Практика показала, что когда раствор содержит 60 г/л или более растворенной меди, травление настолько замедляется, что травильный раствор необходими заменить (см. рис. 2.5).
Теоретическое истощение, %
20 10 20 30 40 50 60 70
Относительное








время травления,
мин 


10













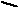

0
4 8 12 16 20
Количество растворенной меди в ед. объема, г/л
Рис. 2.5. Зависимость скорости травления меди от количества меди,
перешедшей в травитель
Скорость травления изменяется не только с изменением концентрации FeCl3 , но и температуры, химических добавок и интенсивности перемешивания.На рис. 2.6 приведены кривые, отражающие зависимость скорости травления от концентрации раствора при различных температурах:
4

Относительное
время

травления, мин

3 25С
35С



2 
70С 55С
1



10 20 30 40
Содержание FeCl 3 в исходном растворе,%
Рис. 2.6. Зависимость времени травления меди от температуры и концентрации травителя
Оптимальная концентрация для минимального времени травления изменяется от 30% FeCl3 при комнатной температуре до 35%FeCl3при 70С. Как и следовало ожидать, увеличение температуры вызывает увеличение скорости травления. Максимальной температурой можно считать ту, при которой травление не приводит к разрушению резиста и (или) к разложению травителя.
Травильные растворы на основе персульфата аммония ((NH 4) 2 S 2 O 8 .
Травильные растворы на основе персульфата аммония применяют для травления меди при использовании фоторезистов и металлических резистов, в том числе и олово-никель, олово-свинец.
Достоинством персульфата аммония является то, что он не разрушает защитные покрытия, выполненные из металлорезистов. Однако он имеет ряд недостатков:
— персульфат аммония имеет более низкую устойчивость к разложению, чем хлоридные травители;
— персульфат аммония дает большее подтравливание (боковой подтрав равен примерно толщине проводника).
Для плат, покрытых оловянно-свинцовым припоем, состав травителя может быть таким: персульфат аммония (240 г/л и 96% серная кислота - 16 мл). Применение этого раствора приводит к образованию на поверхности припоя нерастворимого защитного слоя сульфата свинца. Контроль качества раствора обычно состоит в анализе содержания растворенной меди.
Травильные растворы на основе хлорной меди CuCl 2
Для травления меди применяются растворы хлорной меди (CuCl2 ) с концентрацией 135405 г/л. В состав травильного раствора входят такжеHCl,NaCl,H2O2,Cu. В раствор часто добавляют свободную медь до 30 г/л, чтобы реакция травления не была каталитической. Травление обычно проводят при температуре 2638С. Скорость травления примерно в два раза меньше, чем в хлорном железе. По мере выпадения осадкаCuCl, ванна из темно-коричневой становится зеленой, поэтому корректировку можно производить по цвету раствора. Достоинством метода является малый растрав проводников: боковой подтрав составляет 0,5 толщины покрытия.
Общая схема химической реакции имеет вид:
Cu+CuCl2Cu2 Cl2(хлористая медь)
Корректировка раствора осуществляется добавлением H2 O2иNaClилиHClчерез каждые 1020 г стравленной меди. Ее цель — предотвращение образования нерастворимой солиCuCl :
2CuCl+H2 O2 + 2HCl2CuCl2 + 2H2 O2.
Травильные растворы на основе (CuCl2) не следует применять для плат, покрытых сплавом олово-свинец. Этот сплав не разрушается в хлорной меди, но могут иметь место точечные разрушения защитного покрытия. Для предотвращения этого явления излишки кислоты нейтрализуют, вводяNaOH.
Травильные растворы на основе хромовосерной кислоты (CrO3)
Травильные растворы на основе смеси хромовой и серной кислот являются предпочтительными для плат, покрытых сплавом олово-свинец. Хотя эти растворы являются сильными окислителями, на слой припоя они не оказывают влияния из-за образования нерастворимой пленки сульфата свинца. Этот травитель имеет несколько недостатков: скорость травления значительно ниже, чем при применении других травителей; ванна истощается при накоплении примерно 35 г/л растворенной меди.
Реакцию травления меди в смеси хромовой и серной кислот можно записать в следующем виде:
3Cu + 2CrO3 +6H2 SO4 Cr2 (SO4)3 + 3CuSO4 + 6H2O
В продажу хромовая кислота поступает в кристаллическом виде и стоит дороже, чем хлорное железо, хлорная медь и персульфат аммония.
Практика показала, что перемешивание повышает скорость травления в данном травителе, но для этого лучше использовать наложение вибрации. При перемешивании с помощью нагнетания воздушного потока скорость значительно меньше, а кроме того, образуется токсичный туман и брызги. Пары травителя предельно агрессивны и приводят к выходу из строя оборудования, вызывая коррозию. Также разрушаются резиновые детали, шланги, перчатки. Для предотвращения этого в травитель вводят противотуманные добавки или засыпают на поверхность пластмассовую крошку. Не следует применять этот травитель, если диэлектрик имеет фенольную основу (гетинакс), так как он может быть частично разрушен.
