
Лекции / 1
.pdf
Элементы химической термодинамики и биоэнергетики.

Задачи химической термодинамики:
1 Установление энергетических эффектов химических и физико-химических процессов.
2. Установление критериев самопроизвольного протекания физических
ифизико-химических процессов.
3.Установление критериев равновесного состояния термодинамических систем.

Терминология химической термодинамики:
Термодинамическая система –
Изолированные системы - Закрытые системы - Открытые системы -

Гомогенные и гетерогенные системы.
Гетерогенные системы
–
Пример:
- Zn (тв.) + HCl (ж) → ZnCl2 + H2↑
Фаза –

ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ СОСТОЯНИЯ СИСТЕМЫ (ТПСС)
1. Основные – Т, р, V, m, ρ, η и т.д.
2. Функции состояния : |
В СИ : Дж. |
|
внутренняя энергия |
||
Вне СИ – |
||
(U), |
||
калория. |
||
U = Eкин. + Eпотенц. |
1 кал – 4,18 |
|
∆U = U2 кон. – U1 нач. |
Дж. |
|
|
- энтальпия,- энтропия,- свободная энергия Гиббса
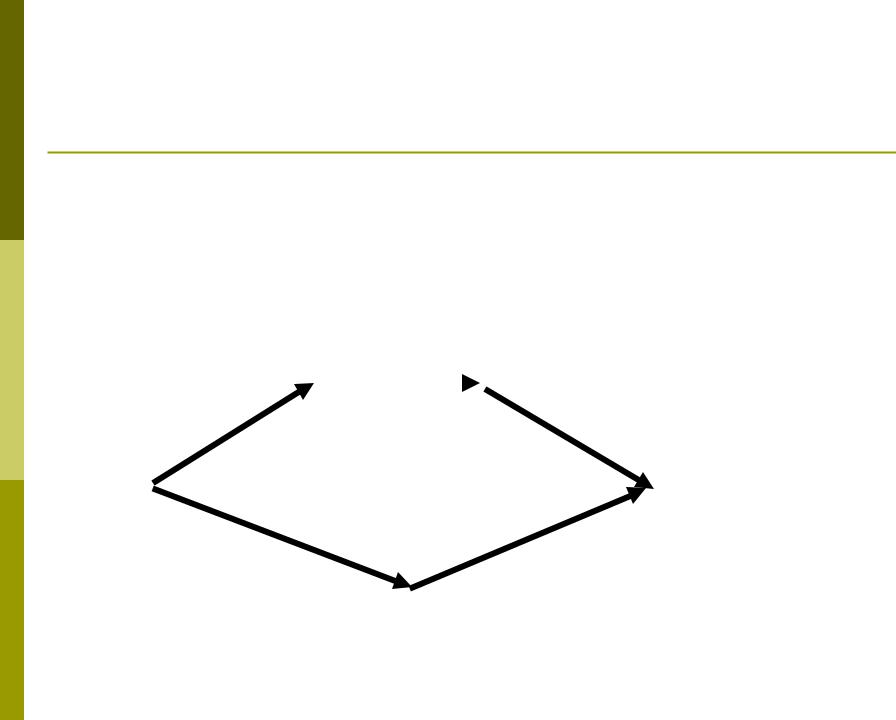
∆P = P2 – P1∆V = V2 – V1
∆Т = Т2 – Т1
P1 |
|
|
|
A |
|
|
B |
|
|
|
P2 |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
||||
V1 |
|
|
|
|
|
|
|
|
|
|
V2 |
|
|
|
|
|
|
|
|
|
|||
|
I* |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|||
T |
|
|
|
|
|
|
|
II** |
|
T2 |
|
|
|
|
|
|
|
|
|
||||
1 |
|
|
|
|
|
C |
|
|
|
||
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
||
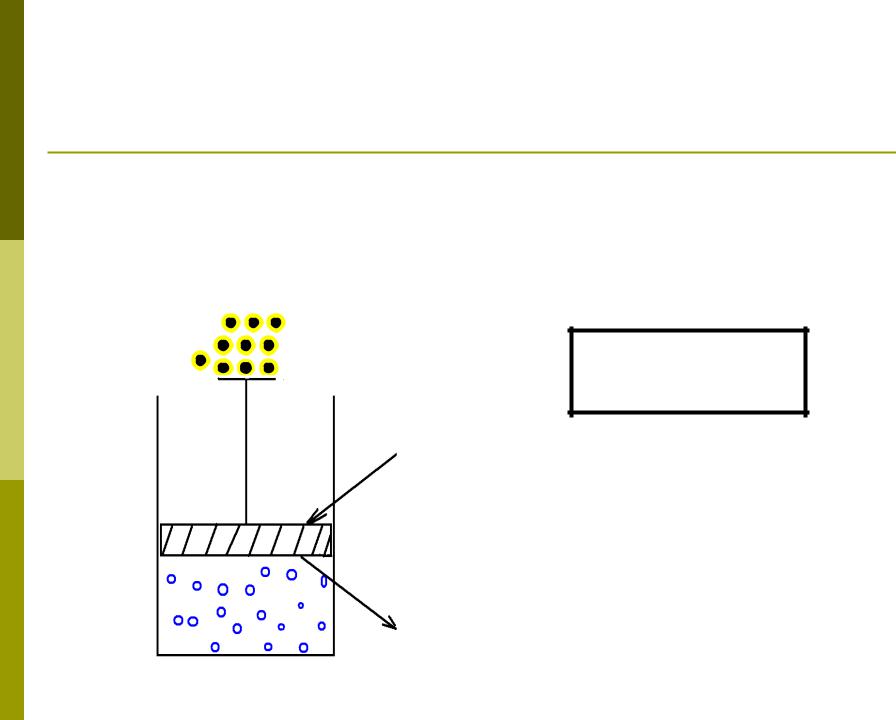
Термодинамические процессы.
1.термодинамически обратимые процессы
2.термодинамически необратимые процессы.
100 г |
Pe |
= Pi |
|
Pe (externus)- наружный
Pi (internus)- внутренний
Ае = Ре · ∆V
Аi = Рi · ∆V
Т.к. Ре = Рi , то Ае = Аi
Аi = Ае. К.п.д.=100%
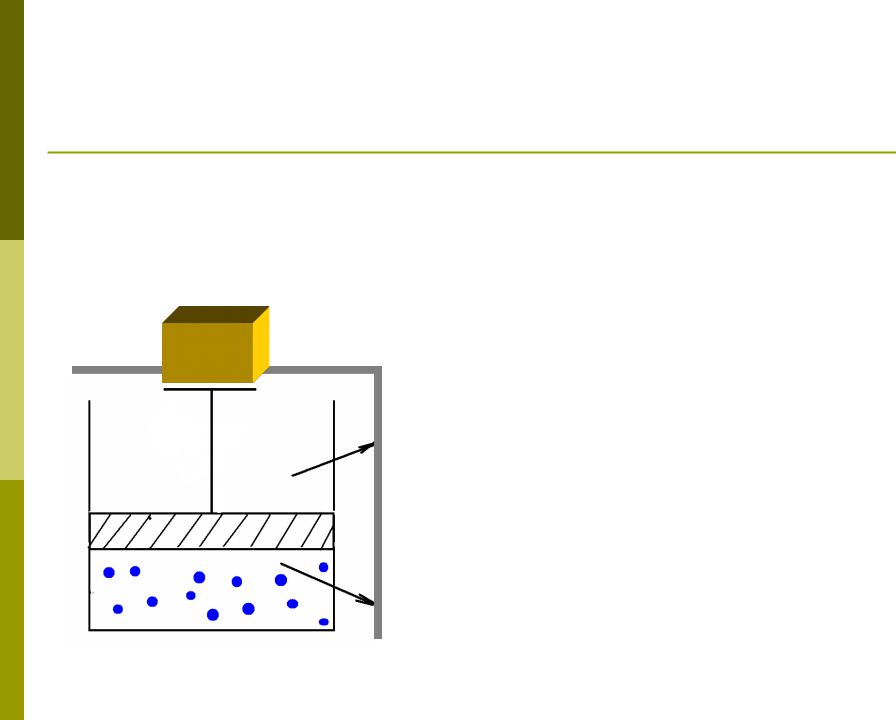
Термодинамически необратимые |
|||||||
процессы |
|
= Pi |
|
|
|
|
|
1. Равновесие Pe |
|
|
|
|
|
||
2. Ре > Рi |
=> Ae >Ai |
|
|
|
|
|
|
|
|
|
|
|
Ae - Ai = Q |
||
100 |
|
|
|
|
|
|
|
г |
|
Pe |
Аобр.процесса > Анеобр.процесса |
||||
|
|
||||||
|
|
|
|
Аобр. - Анеобр.= Q |
|||
|
|
|
|
|
|||
|
|
Pi |
|
|
|
|
|
|
|
|
|
К.п.д. необр. < 100 % |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Белки |
+ О2 |
→ СО2 |
+ Н2О + азотистые |
||
Жиры |
|||||
Углевод |
продукты |
|
|
||
ы |
|
|
+ энергия |
||
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
75% рассеивание |
|
25% на совершение |
||||
|
|
в окр.среду в |
|||
|
работы (А) |
|
|
||
|
|
|
виде теплоты (Q) |
||
|
|
|
|
|
|
