
2149
.pdfБольшое каноническое распределение
Для изучения макросистем с переменной энергией и числом частиц, но постоянными температурой и внешними параметрами применяется общий вид канонического распределения.
Рассмотрим комплекс, состоящий из исследуемой системы и термостата. Эта общая система считается термодинамически замкнутой, ее энергия Е и число частиц N сохраняются.
Система в целом и обе ее подсистемы равновесны, но исследуемая система и термостат взаимодействуют, обмениваясь энергией и частицами. Внешние параметры всех тел постоянные, подсистемы квазинезависимы.
Пусть исследуемая система имеет энергию и число частиц n. Тогда энергия термостата равна
и он |
содержит |
частиц. |
Термостат велик |
; |
и его тем- |
пература и химический потенциал |
, несмотря на |
|
взаимодействие с исследуемой системой, не изменяют своих значений.
Найдем вероятность того, что исследуемая система имеет энергию и число частиц n. Приме-
няя микроканоническое |
распределение |
ко |
всему |
||
комплексу, получаем ( и |
– число микрососто- |
||||
яний системы и термостата): |
|
|
|
||
( ) |
( |
) |
( |
). |
|
41
Действительно, число частиц в системе изменяется, значит, число ее микросостояний изменяется, следовательно, вероятность ( ) должна от этого зависеть. Несмотря на постоянство температуры, вероятность определяется не только числом состояний термостата, но (благодаря T = const) и общим числом состояний, которое определено для , так как изменение энергии с числом частиц (химический потенциал) здесь учтено.
Сумма
∑ ∑ ( ) ( )
дает полное число микросостояний комплекса. Тогда
( ) |
( |
) |
( |
|
) |
. |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
∑ ∑ |
( |
) |
|
|
( |
) |
||||||||||||
Число микросостояний термостата выразим |
|||||||||||||||||||
через его энтропию |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
( |
|
|
|
|
) |
|
|
|
|
( |
|
) |
|||||||
( |
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
). |
|||
Разложим функцию |
( |
|
|
|
|
|
|
) в двойной |
|||||||||||
ряд по степеням переменной |
и |
с точностью до |
|||||||||||||||||
линейных членов: |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
( |
|
|
|
|
) |
|
|
( |
) |
|
|
. |
|||||||
Ранее мы получили формулы |
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
( |
|
|
|
|
|
) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
( |
) |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
42
|
( |
) |
( |
) |
|
|
|
|
|
|
|
|||||
( ) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
∑ ∑ |
( |
) |
|
( ) |
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
( |
) |
|
|
|
|
|
|
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|||||||||||
|
|
∑ ∑ |
( |
|
) |
|
|
|
|
|
|
|
|
|
|
|
Это так называемое большое каноническое распределение.
|
|
|
|
|
( |
) |
|
|
; |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
∑ |
∑ |
( ) |
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
; |
|
|
|
|
|
|||||||||
|
( |
|
) |
|
( |
|
|
|
); |
|||||||||||
|
|
|
( |
|
) |
( |
|
|
) |
|
|
; |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
∑ |
∑ |
( |
) |
|
( |
) |
||||||||||||
|
( |
|
) |
|
|
|
|
( |
); |
|||||||||||
|
|
|
|
|
|
|||||||||||||||
( |
) |
|
( |
|
|
) |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
( |
|
) |
|
|
|
( |
) |
|
|
|
|
|
|
|
. |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
∑ ∑ |
|
|
( |
|
) |
|
|
|
|
|
|
|
|
|||
Большое каноническое распределение является обобщением обычного канонического распределения на системы с переменным числом частиц. С термодинамической точки зрения, как мы это видели в первой части нашего курса, находящаяся в тепловом и диффузионном равновесии
43
с термостатом исследуемая система имеет постоянную температуру T и химический потенциал µ (условия равновесия). Эти же параметры определяют систему и в статистическом смысле. От них зависит большое каноническое распределение, а значит, средние значения физических величин.
Запишем большое каноническое распределение в виде
|
|
|
1 |
|
n |
|
W , n |
|
, n |
e kT |
|
|
|
||||
|
|
|
, |
||
|
|
|
|
|
|
где |
, n exp( |
n ) – |
большая стати- |
||
|
n |
|
kT |
|
|
стическая сумма. |
|
|
|
|
|
|
Видим, что дифференцирование Φ по μ дает |
||||
|
|
|
|
|
n |
|
kT n , n e kT |
||||
|
|
n |
, |
||
|
|
|
|
|
|
тогда среднее число частиц в исследуемой системе ( n N уже не N комплекса)
|
1 |
|
|
n |
|
1 |
|
|
|
|
|
N n n W ,n |
n ,n e kT |
kT |
kT |
ln |
|||||||
|
|
|
|||||||||
n |
n |
|
|
|
|
. |
|||||
|
|
|
|
|
|
|
|
|
|
||
Совмещая с ранее доказанным, для внутрен- |
|||||||||||
ней энергии U получаем |
|
|
|
|
|
|
|
|
|||
|
U kT 2 |
|
ln n |
|
|
|
|||||
|
T |
|
|
|
|||||||
|
|
|
|
. |
|
|
|
||||
44

Канонические распределения – основной инструмент статистической физики. Теперь мы можем приступать к анализу конкретных физических систем.
Максвелл–Больцмановский одноатомный газ. Классический идеальный одноатомный газ. Вычисление статистической суммы
Начнем с простейшего случая классического идеального газа, когда все вычисления удается провести в полном объеме. Воспользуемся полуклассической формулой
|
1 |
|
|
exp( |
(q, p))dqdp |
|
N !(2 |
) |
3N |
|
|||
|
|
|
kT |
. |
||
|
|
|
|
|
|
|
В качестве обобщенных координат выбира- |
||||||
ем обычные декартовы |
всех N частиц системы |
|||||
(x, y, z)i ;i 1...N . Энергия газа |
|
|
||||
(q, p) 1 2m
N
( p, p, p, )
x y z i i 1
есть сумма кинетических энергий всех частиц. Тогда
|
1 |
|
|
|
1 |
N |
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
exp( |
|
( p, |
p, |
p, |
) |
) (d |
d |
d |
dp |
dp |
dp |
) |
||
|
)3N |
|
||||||||||||||||
|
N !(2 |
|
2mkT i 1 |
x |
y |
z |
i |
j 1 |
x |
y |
z |
x |
y |
z |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
. |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Определим пределы интегрирования. Изменение координат ограничено размерами сосуда V, в котором находится рассматриваемый газ. По им-
45

пульсам же предел (поскольку подынтегральная функция быстро убывает с ростом импульса) можно принять ±∞.
|
1 |
|
N |
|
|
|
|
|
( px2 p2y pz2 ) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
(dxdydz) |
|
|
e |
|
2mkT (dp |
dp |
dp |
) |
i |
|
|
|
|
|
|
||||||||||||
|
N !(2 |
)3N |
j 1 |
i |
|
|
|
|
|
x |
y |
z |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
V |
|
|
|
|
|
|
|
|
|
|
|
|
= (экспонента суммы преобразуется в произведение экспонент) =
|
|
V |
N |
|
|
|
( px2 p2y pz2 ) |
|
|
|
|
|
|
|
|
V |
N |
|
|
|
|
|
|
( p2 ) |
|
|
|
|
|||||
|
|
|
|
( e |
2mkT |
|
dp |
dp |
dp |
)N |
|
|
|
|
|
( |
|
|
e |
2mkT dp)3N |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
N !(2 )3N |
|
|
|
|
|
|
x |
|
y |
z |
|
N !(2 |
)3N |
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3N |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
V |
N |
(2 mkT ) |
2 |
|
|
V |
N |
|
mkT |
|
3N |
|
||||||||||
|
( e ax |
2 |
dx |
|
) |
|
|
|
|
|
|
|
|
( |
) 2 |
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
3N |
|
|
|
|
|
|
|
|
2 |
|||||||||||||
|
|
|
|
|
|
|
|
a N ! |
|
|
|
|
|
|
N ! 2 |
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
(4 2 2 ) 2 |
|
|
|
|
|
. |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Основные термодинамические функции и уравнение состояния идеального газа
В случае больших N для факториала справедлива приближенная формула Стирлинга
|
|
|
|
( |
N |
)N ( |
N |
)N (N 103 ) |
|
|
|
|
|
|
|||||
NN! |
! |
|
2 N |
|
|||||
|
|
|
|||||||
|
|
|
|
|
e |
|
e |
. |
|
|
|
|
|
|
|
||||
Тогда
|
Ve |
|
mkT |
|
3N |
|
Z ( |
)N ( |
) 2 |
|
|||
|
|
|
||||
|
N |
|
2 2 |
, |
||
Ve mkT 3 ln Z N ln(( N ) ( 2 2 )2 )
46

|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ve |
|
|
|
mkT |
|
3 |
|
|
||||||||||||||||||||||
U kT |
2 |
|
|
|
|
|
ln Z kT 2 N |
|
ln( |
|
|
|
)2 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
T |
|
|
|
|
|
|
|
|
2 |
2 |
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
Ve |
( mkT ) |
|
|
|
|
|
3 T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
2 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
kNT |
2 |
|
N |
|
|
|
|
|
2 |
2 |
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
3 |
kNT |
|
3 |
|
NkT |
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
Ve |
|
|
|
|
mkT |
|
|
|
3 |
|
3 |
|
|
|
|
|
2 |
2 |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
( |
)2 |
|
T 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
2 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
. |
|
|||||||||||||||||
Калорическое уравнение состояния идеаль- |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ного газа |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ve |
|
|
|
mkT |
) |
3 |
) |
|
||||||||||||||||||||||||||||||||||||||||||||||
|
|
F kT ln Z kNT ln(( |
) ( |
2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
2 |
2 . |
|||||||||||||||||||
Согласно свойствам свободной энергии |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
F |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ve |
|
|
|
|
mkT |
|
3 |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
P ( |
) |
|
|
|
|
|
kNT |
|
|
|
ln( |
( |
|
|
)2 ) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
V |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
T ,N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V N |
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
e |
|
|
mkT |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
( |
|
|
|
|
|
)2 |
|
|
|
|
|
|
|
|
kNT |
|
|
|
R T |
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
kNT |
|
|
N |
2 |
2 |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
e |
|
|
|
|
|
mkT |
|
|
|
|
3 |
|
|
|
|
|
V |
|
|
|
|
|
|
|
|
|
|
V |
|
|
, |
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V |
|
( |
|
|
|
|
)2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N 2 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
где |
N |
; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
N A |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
R kNA , N A |
– число Авогадро. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
Мы получили уравнение Менделеева- |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клапейрона |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
U |
|
|
|
3 |
|
Ve |
|
|
mkT |
) |
3 |
) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
S |
k ln z |
|
|
Nk kN ln( |
|
( |
2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
2 |
|
2 . |
|||||||||||||||||||||
При T → 0 ln(…) → ln(0) S → – |
|
|
. Это про- |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
тиворечит |
|
|
|
|
третьему |
|
|
|
|
|
|
|
началу |
|
|
|
|
|
термодинамики. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
47
Первое указание на неприменимость классической статистической физики в области низких температур. В целом видим, что в термодинамике и статистической физике под идеальным газом понимают одну и ту же систему, описываемую уравнением Менделеева–Клапейрона.
Распределение Максвелла–Больцмана
Энергия идеального газа складывается из кинетических энергий отдельных частиц. Механическое движение одной молекулы никак не связано с состояниями других молекул. Пределы изменения ее координат и импульсов ограничены только размерами сосуда и энергией газовой системы. Следовательно, каждую молекулу можно рассматривать как квазинезависимую подсистему, а все остальные образуют термостат.
Принимаем к такой подсистеме каноническое распределение Гиббса. Энергия молекулы есть
|
|
E |
p2 |
|
U (x, y, z) (внешнее поле) |
|||||||||
|
|
|
|
|
||||||||||
|
|
|
|
2m |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dW dW (x, y, z, px , py , pz ) |
||||||||||
|
|
1 |
|
|
|
|
|
p2 |
|
|
|
U (x, y, z) |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
dW |
|
exp( |
|
|
|
|
|
|
|
) dxdydzdpx dpy dpz |
||||
|
|
|
|
|
|
|
||||||||
|
|
I |
|
|
|
2mkT |
kT |
|
||||||
|
I exp( |
|
|
p |
2 |
|
|
U (x, y, z) |
|
|
||||
|
|
|
|
) dxdydzdpx dpy dpz |
||||||||||
|
|
|
|
|||||||||||
2mkT |
|
|||||||||||||
|
|
|
|
|
|
|
|
kT |
|
|||||
48

Эти соотношения называются распределением Максвелла–Больцмана. Данное распределение может быть представлено в виде произведения
двух распределений вероятности: |
|
|
|
|
|
|
|||||||||||||||||
1) |
распределение Максвелла по импуль- |
||||||||||||||||||||||
сам |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dW ( p |
|
p |
|
p |
) |
|
1 |
exp( |
|
|
p2 |
) dp |
dp |
|
dp |
|
|||||||
x |
y |
|
|
|
|
|
|
|
y |
z |
|||||||||||||
|
|
|
z |
|
|
|
A |
|
2mkT |
|
x |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
2 |
|
|
|
|
|
|
|||
|
|
A exp( |
px |
py |
pz |
)dpx dpy dpz |
; |
||||||||||||||||
|
|
|
2mkT |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
2) |
распределение Больцмана по коорди- |
||||||||||||||||||||||
натам |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dW (x, y, z) |
1 |
|
exp( |
U (x, y, z) |
)dxdydz |
|
|||||||||||||||||
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
B |
|
|
kT |
|
|
|
|
|
|
|||||||
B exp( |
U (x, y, z) |
)dxdydz. |
|
||
V |
kT |
|
|
|
|
С физической точки зрения, возможность разделения связана с представлением классической энергии как суммы кинетической (зависит только от импульса) и потенциальной (только от координат). А при хаотическом движении молекул их положение в пространстве никак не связано с величиной и направлением импульсов.
49
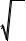
Распределение Максвелла
Распределение Максвелла универсально, то есть его вид не зависит ни от сорта частиц, ни от действующих полей. Параметрами распределения являются только температура и масса частиц. Распределение Максвелла выполняется и для не-
идеального классического газа в силу |
|
P2 |
. |
|
|
|
|
|||||||||||||||||||||
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2m |
|
|
|
|
|
|
||
|
|
С |
|
|
помощью |
|
известного |
интеграла |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
e x |
dx |
|
|
легко |
|
получаем |
|
|
A (2 mkT )2 . |
|||||||||||||||||||
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Элемент объема импульсного пространства |
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 P2 |
|
|
P2 |
|
|||||
|
|
|
|
|
|
|
|
4 P2dP dW (P) |
|
|
|
|
||||||||||||||||
|
dp |
x |
dp |
dp |
z |
|
|
|
|
|
|
|
e 2mkT |
|||||||||||||||
|
|
|
|
3 |
|
|||||||||||||||||||||||
|
|
|
y |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(2 mkT )2 |
. |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
1 |
|
|
3 |
|
P2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Или |
f (P) 4 ( |
|
|
|
)2 e 2mkT |
P2 |
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
2 mkT |
|
|
. |
|
|
|
|
|
|
|
|
|
|||||||
Вывод распределения Максвелла на основе законов статистической физики согласуется с мо- лекулярно-кинетической теорией.
|
Распределение Больцмана |
||||
Если |
внешнее |
поле |
отсутствует |
||
(U (x, y, z) 0) , то B = V и |
|
|
|
|
|
|
dW (x, y, z) |
1 |
dxdydz |
|
|
|
|
|
|||
|
|
V |
. |
||
50
