
806
.pdf
Рис. 13. Делительные воронки: а – коническая; б – цилиндрическая; в – положение воронки при уравнивании давления; 1 – пробка;
2 – экстрагент; 3 – водный раствор; 4 – кран
После встряхивания воронку закрепляют в штативе и дают жидкостям отстояться. Пробку открывают после расслоения жидкостей. Нижний слой сливают в колбу или стакан через кран воронки, верхний слой выливают через горло воронки в другую колбу. Экстракцию повторяют со свежей порцией растворителя.
Раствор после экстракции необходимо высушить от остатков воды. Для сушки используются те же осушители, что и при работе с жидкими веществами.
Выделять вещества методом экстракции можно и из твердой смеси. Простейшим случаем подобной экстракции является взбалтывание вещества с подходящим растворителем в колбе при комнатной температуре. Вещество вымывается растворителем, который по мере насыщения заменяют свежими порциями. Этот метод применяется чаще всего при работе с соединениями, не стойкими при повышенной температуре. Если вещество устойчиво при относительно высоких температурах, экстракцию ведут при температуре кипения растворителя. Конечно, такой процесс идет гораздо быстрее, чем экстракция при обычной температуре. Эту операцию проводят путем кипячения твердого
31
вещества с растворителем в круглодонной колбе, снабженной обратным холодильником. После насыщения растворитель сливают и заменяют новыми порциями до тех пор, пока не будет закончено извлечение вещества.
|
Если вещество плохо раство- |
|||
|
римо в органических растворите- |
|||
|
лях, то для его полного извлече- |
|||
|
ния свежие порции растворителя |
|||
|
приходится добавлять многократ- |
|||
|
но. В итоге расходуется неоправ- |
|||
|
данно большой объем растворите- |
|||
|
ля, а процесс экстракции занимает |
|||
|
весьма длительное время. В таких |
|||
|
случаях |
полезным оказывается |
||
|
использование аппаратов для не- |
|||
|
прерывной |
экстракции. |
Наиболее |
|
|
распространенным из них являет- |
|||
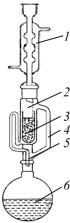
Рис. 14. Прибор Сокслета: |
ся прибор Сокслета (рис. 14). Ос- |
|||
1 – холодильник; 2 – экс- |
новной частью прибора Сокслета |
|||
трактор; 3 – гильза с вещест- |
является экстрактор, соединенный |
|||
вом; 4 – пароотводная труб- |
снизу |
с |
круглодонной |
колбой, |
ка; 5 – сифонная трубка; |
в которой нагревают до кипения |
|||
6 – колба с растворителем |
растворитель, а сверху – с обрат- |
|||
|
||||
ным холодильником.
Экстрактор имеет две трубки: широкую пароотводную и узкую сифонную для слива раствора. Подлежащее очистке вещество в гильзе из фильтровальной бумаги помещают на дно экстрактора. Пары растворителя по пароотводной трубке поднимаются в холодильник и в виде горячего конденсата стекают на дно экстрактора, экстрагируя вещество в гильзе. Раствор, заполнив экстрактор до высоты сифонной трубки, стекает по ней обратно в колбу. Такая экстракция происходит непрерывно в автоматическом режиме и требует сравнительно небольшого количества растворителя.
32
4.3. Перекристаллизация
Перекристаллизация является одним из основных методов выделения и очистки твердых веществ. Метод основан на резком различии в растворимости очищаемого вещества в данном растворителе при разных температурах, а также на различии в растворимости основного вещества и примесей при одинаковой температуре. Смесь веществ растворяют при нагревании в подходящем растворителе. При охлаждении раствора одно из веществ выпадает в осадок, а другое (или другие) остается в растворе. Удобнее подбирать такой растворитель, чтобы в осадок выпадало основное вещество, а примеси оставались в растворе. Неочищенное вещество растворяют при нагревании в определенном растворителе, при последующем охлаждении раствора выпадают кристаллы более чистого вещества.
Перекристаллизация во многом зависит от правильного выбора растворителя. Растворитель должен быть химически индифферентным к очищаемому веществу. Следует помнить, что вещество хорошо растворяется в тех растворителях, которые имеют сходное с ним химическое строение. Полярные соединения обычно кристаллизуются из воды, метилового или этилового спиртов, уксусно-этилового эфира, ацетона, уксусной и других карбоновых кислот. Неполярные соединения лучше растворимы в бензоле, хлороформе, петролейном эфире, четыреххлористом углероде. Из ряда растворителей выбирают тот, в котором вещество ограниченно растворяется при комнатной и хорошо при повышенной температуре. При этом примеси должны растворяться лучше, чем выделяемое вещество, при любой температуре. Тогда они остаются в растворе. Если растворитель совсем не растворяет примеси, их можно удалить, профильтровав горячий раствор.
При промывании и высушивании осадка растворитель должен легко удаляться из вещества. Температура кипения растворителя должна быть ниже температуры плавления вещества не менее чем на 10–15 °С, иначе– вещество может выпадать в виде масла.
33
Поскольку не всегда удается подобрать растворитель, удовлетворяющий этим требованиям, то иногда для перекристаллизации используют смеси растворителей. Состав смеси должен быть подобран так, чтобы в одном из растворителей вещество растворялось хорошо, а в другом плохо. Смешивать можно только взаиморастворимые растворители. При этом чаще используют смеси во- да-спирт, вода-ацетон, спирт-эфир, хлороформ-петролейныйэфир.
Для перекристаллизации растворитель берут в определенном минимальном количестве, достаточном для полного растворения вещества при нагревании.
Подобрать растворитель и его количество можно по данным растворимости соединений, которые приводятся в справочниках и специальной литературе. При отсутствии таких сведений соответствующий растворитель подбирают опытным путем. Для этого небольшие количества вещества (по 0,1–0,2 г) помещают в пробирки, добавляют порциями по 0,5–1 мл различные растворители и нагревают до полного растворения вещества. По скорости кристаллизации, количеству осадка, выпавшего при охлаждении из раствора, величине кристаллов судят о пригодности растворителя. Выбрав подходящий растворитель, присту-
пают к перекристаллизации всей массы вещества. |
|
|
|
В зависимости от свойств рас- |
|
|
творителя и растворимости вещест- |
|
|
ва перекристаллизацию проводят в |
|
|
круглодонной колбе |
подходящего |
|
объема, снабженной обратным хо- |
|
|
лодильником (рис. 15). В колбу по- |
|
|
мещают взвешенное |
количество |
|
очищаемого вещества и раствори- |
|
|
тель. Первоначально берут такое |
|
|
количество растворителя, которым |
|
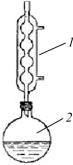
Рис. 15. Прибор для пере- |
можно только покрыть вещество. |
|
кристаллизации: 1 – обрат- |
Содержимое колбы нагревают |
|
ный холодильник; 2 – колба до кипения. Если при этом вещест- с раствором во не растворилось, прекращают
34
нагревание и добавляют в колбу небольшую порцию растворителя через верхний тубус холодильника
Так поступают несколько раз до полного растворения вещества при температуре кипения раствора. При использовании смеси растворителей вещество растворяют при нагревании в небольшом количестве хорошо растворяющего растворителя и к горячему раствору по каплям добавляют растворитель, плохо растворяющий данное вещество. После появления устойчивого помутнения раствор нагревают до исчезновения мути и дают остыть до появления кристаллов.
При растворении органических соединений часто образуются окрашенные растворы. Кристаллизация в таких случаях затрудняется, а получаемые кристаллы содержат адсорбированные окрашенные примеси. Дляобесцвечивания раствор кипятят или
просто взбалтывают в течение 10–15 мин с веществом, адсорбирующим окрашенные соединения.
Полярные растворы обесцвечивают активированным углем, который вносят в количестве 1/20–1/50 от массы растворенного вещества в охлажденный до комнатной температуры раствор. Адсорбция в большинстве случаев мало зависит от температуры, поэтому лучшего обесцвечивания можно достигнуть, не нагревая раствор с углем, а медленно пропуская его при обычной температуре через угольный фильтр. Растворы окрашенных веществ в неполярных растворителях, например, в гексане, хлороформе, четыреххлористом углероде, бензоле, обесцвечивают, пропуская их через слой оксида алюминия.
Адсорбирующие средства следует прибавлять к раствору лишь после полного растворения вещества. Если же имеется нерастворимый остаток, то его отфильтровывают до прибавления адсорбента. Для этого пользуются стеклянной конической воронкой с вложенным в нее складчатым бумажным фильтром. Фильтр смачивают растворителем и пропускают через него горячий раствор. Если вещество на фильтре кристаллизуется, то раствор отфильтровывают на воронке горячего фильтрования, чтобы избежать потерь вещества за счет его кристаллизации на
35
фильтре или в трубке воронки. В крайнем случае перед фильтрованием воронку можно просто нагреть на плитке или в сушильном шкафу.
Фильтрат собирают в коническую колбу и дают ему охладиться до начала кристаллизации. Для более полного выделения кристаллов охлаждение можно вести в бане с ледяной водой. При медленном охлаждении, как правило, образуются крупные кристаллы, а при быстром – мелкие. В первом случае в кристаллы может быть включен растворитель, а следовательно, и примеси; во втором случае благодаря большой суммарной поверхности мелких кристаллов имеется опасность адсорбции на них загрязнений из раствора, поэтому всегда следует стремиться получить кристаллы средней величины.
Некоторые органические вещества склонны образовывать перенасыщенные растворы. Ускорить начало их кристаллизации можно внесением в раствор «затравки» – кристаллика чистого выделяемого вещества или трением стеклянной палочки о стенку сосуда. Если в этом случае кристаллы не выпадают, колбу с раствором помещают на некоторое время в холодильник. Выпадение кристаллов в подобных случаях часто заканчивается через несколько часов или даже дней.
Кристаллический осадок отделяют от маточного раствора фильтрованием. Для более полного отделения кристаллов вещества от жидкости и ускорения фильтрования этот процесс проводят под уменьшенным давлением. Применяемый в этом случае фильтр состоит из фарфоровой воронки с сетчатым дном (воронка Бюхнера) и толстостенной конической колбы для работы под вакуумом (колба Бунзена).
На сетчатое дно воронки накладывают фильтр, размер которого должен точно совпадать с площадью дна воронки. Объем воронки зависит от количества твердого вещества: кристаллы должны полностью покрывать поверхность фильтра, но не слишком толстым слоем, чтобы не затруднялось фильтрование. Воронку с помощью пробки вставляют в горло колбы Бунзена, которую затем присоединяют вакуумным шлангом к водоструйному или вакуум-насосу (рис. 16).
36
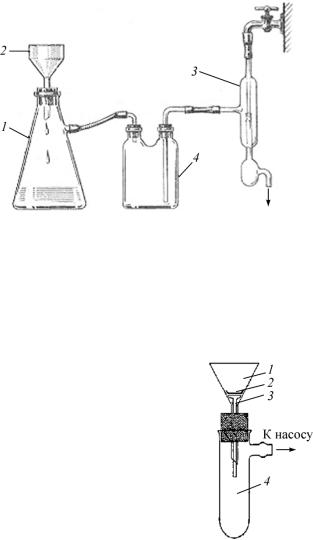
Рис. 16. Прибор для фильтрования: 1 – колба Бунзена; 2 – воронка Бюхнера; 3 – водоструйный насос; 4 – склянка Вульфа
Между колбой и насосом устанавливают толстостенную двугорлую склянку (склянку Вульфа). В случае уменьшения напора воды эта склянка предотвращает засасывание воды в колбу
Бунзена. |
|
|
Для фильтрования малых ко- |
|
|
личеств осадка применяют пробир- |
|
|
ку для отсасывания и воронку с |
|
|
«гвоздиком» (рис. 17). На стеклян- |
|
|
ную шляпку «гвоздика» наклады- |
|
|
вают кружок фильтровальной бу- |
|
|
маги, который должен на 1–2 мм |
|
|
заходить на стенки воронки. |
|
|
Перед началом фильтрования |
|
|
бумажный фильтр предварительно |
|
|
смачивают на воронке растворите- |
|
|
лем, затем включают вакуум- |
Рис. 17. Прибор для фильт- |
|
насос. Разрежение в колбе Бунзена |
рования |
микроколичеств |
создают постепенно, при этом |
осадка: 1 – воронка; 2 – бу- |
|
фильтр плотно присасывается к |
мажный фильтр; 3 – гвоз- |
|
дну воронки. |
дик; 4 – пробирка с отводом |
|
|
|
|
37
Отфильтровываемую жидкость сливают в воронку по стеклянной палочке, концом которой прикасаются к фильтру, кристаллы переносят на фильтр той же палочкой. Осадок на фильтре отжимают плоской частью стеклянной пробки до тех пор, пока не перестанет капать маточный раствор. Необходимо следить, чтобы на поверхности осадканеобразовывались трещины(почему?).
Для удаления остатка маточного раствора кристаллы дважды промывают на фильтре небольшими порциями холодного растворителя, из которого проводилась перекристаллизация. Можно использовать и какой-либо другой растворитель, в котором осадок малорастворим. Отфильтрованные кристаллы хорошо смачивают соответствующим растворителем, прекращая на это время отсасывание, затем вновь подсоединяют вакуум-насос и полностью удаляют растворитель. Если фильтр сильно пропитался загрязнениями, то лучше заменить его новым. После промывания осадок вновь отжимают на фильтре чистой стеклянной пробкой, переносят на лист фильтровальной бумаги иликартона, сушати взвешивают.
Выбор метода сушки зависит от физических и химических свойств вещества.
Остатки легколетучих растворителей могут быть удалены из негигроскопичных веществ путем высушивания на воздухе при комнатной температуре. Вещества, не окисляющиеся на воздухе и устойчивые к действию температуры, можно сушить в сушильном шкафу. Температура сушильного шкафа должна быть на 40–50 °С ниже температуры плавления вещества. Вещество помещают в сушильный шкаф на часовом стекле, в фарфоровой чашке или на блюде. Для ускорения высушивания широко применяют эксикаторы или вакуум-эксикаторы, которые заполняют веществами, поглощающими пары растворителя. Наполнитель по своим свойствам должен соответствовать природе растворителя и высушиваемого вещества. Для поглощения паров воды и спирта применяют серную кислоту, хлорид кальция, едкий натр, фосфорный ангидрид. Едким кали связывают пары веществ, обладающих кислым характером. Высушенное вещество взвешивают и определяют его температуру плавления.
38
5.ИДЕНТИФИКАЦИЯ ТВЕРДЫХ ВЕЩЕСТВ
5.1.Определение температуры плавления
Чистые вещества характеризуются постоянными физическими константами. Наиболее важной характеристикой кристаллических веществ является температура плавления, которая
вбольшинстве случаев настолько характерна для данного соединения, что даже незначительные примеси сильно ее понижают. Поэтому по температуре плавления можно судить о чистоте вещества.
Температурой плавления вещества считают интервал температур с момента появления первой капли жидкости до полного расплавления вещества. Для чистых веществ интервал плавления не превышает 1 °С. Смеси веществ обычно плавятся при более низкой температуре, чем индивидуальные вещества, и плавление происходит в довольно широком интервале температур. Если полученное после кристаллизации вещество плавится
винтервале, превышающем 2 °С, перекристаллизацию повторяют. Температуру плавления определяют после каждой очередной перекристаллизации.
Определяют температуру плавления в стеклянном капилляре с внутренним диаметром 1 мм и высотой 40–50 мм, запаянном с одного конца. Открытым концом капилляра набирают несколько кристалликов растертого в фарфоровой ступке вещества и перемещают их на дно капилляра. Для этого капилляр с веществом несколько раз бросают запаянным концом вниз через длинную стеклянную трубку, поставленную вертикально на твердую поверхность. Таким образом плотно набивают вещество столбиком высотой около 0,5–1 см.
Капилляр с помощью резинового колечка закрепляют на термометре так, чтобы столбик вещества находился на уровне ртутного шарика термометра. Нагревание ведут со скоростью 5–10 град в минуту, а вблизи температуры плавления – 1–2 град
39
в минуту. Отмечают температурный интервал с момента появления первой капли жидкости до полного расплавления столбика вещества. Для чистых веществ он обычно составляет 1,0–0,5 °С.
5.2. Проба смешенного плавления
Температура плавления позволяет судить о чистоте твердого вещества, но ничего не говорит о его структуре. Действительно, из миллионов органических веществ всегда найдется несколько десятков или даже сотен разных соединений, имеющих одинаковые или очень близкие температуры плавления. Поэтому определение температуры плавления вещества неизвестной структуры является обязательной, но совершенно недостаточной для его идентификации процедурой. Окончательно установить структуру вещества можно лишь на основании данных элементного
ифункционального анализа, ультрафиолетовой и инфракрасной спектроскопии и других исследований. Очевидно, что такое всестороннее исследование является трудоемким, дорогостоящим
итребует высокой квалификации химика.
Вместе с тем в повседневной работе химиков нередко возникают ситуации, когда о составе и строении неизвестного вещества можно сделать предположение на основании косвенных данных.
Пример 1. На складе химреактивов рядом стоят две одинаковые банки с белым кристаллическим веществом. На одной банке есть этикетка с формулой, названием, квалификацией чистоты
имолекулярной массой содержимого. На другой банке этикетка отсутствует или сильно повреждена. По цвету, запаху, форме
иразмерам кристаллов можно предположить, что в обеих банках одно и то же вещество, но полной уверенности в этом нет.
Пример 2. В результате синтеза должен получиться целевой продукт А. Однако в ходе синтеза по разным причинам были допущены отступления от методики, в результате чего мог быть выделен побочный продукт В или непрореагировавшее исходное вещество С. Температуры плавления веществ А, В и С по справочным данным одинаковы или близки.
40
