
Современные методы синтеза гетероциклических соединений (110
..pdfМИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РФ ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ «ВОРОНЕЖСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
СОВРЕМЕННЫЕ МЕТОДЫ СИНТЕЗА ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
Учебно-методическое пособие для вузов
Издательско-полиграфический центр Воронежского государственного университета
2012
1
Утверждено научно-методическим советом химического факультета ВГУ 16 февраля 2012 г., протокол № 2
Составители: д-р хим. наук, проф. Х.С. Шихалиев, д-р хим. наук, проф. М.Ю. Крысин, д-р хим. наук, доц. Н.В. Столповская, д-р хим. наук, асс. А.В. Зорина
Рецензент канд. хим. наук, доцент А.С. Шестаков
Учебно-методическое пособие подготовлено на кафедре органической химии химического факультета Воронежского государственного университета.
Рекомендуется для студентов 3-го, 4-го курса дневного отделения химического факультета.
Для специальности 020101 – Химия
2
Современный ритм жизни ставит перед правительствами и общественными организациями разных стран необходимость уделять все больше внимания вопросам энергетики и природных ресурсов, призывает каждого человека к более ответственному использованию ресурсов в целом. Промышленность, а в особенности химические производства, нацелены на сокращение затрат потребления различных природных ресурсов и уменьшения негативного воздействия на окружающую среду. Если раньше главными параметрами при выборе пути технологического процесса были экономические затраты, то в настоящее время предпочтение отдается более экологичным схемам проведения реакций, сокращающим необходимость дополнительной переработки и утилизации отходов производства. Реакционная способность растворителей и вопросы разделения полученных продуктов – важные проблемы современной химии, нашедшие свое отображение в двенадцати принципах зеленой химии, описанных Анастасом и Уорнером. В работе было показано, что для осуществления экологически безопасного и экономически выгодного производства необходимо выполнение следующих условий: интенсификация протекания процессов, изучение альтернативных путей проведения реакций, использование микрореакторов, суперкритических жидкостей, возобновимого сырья, энергонезависимых растворителей, катализа, проведение реакций без растворителей. Было установлено, что 60–80 % затрат на проведение той или иной реакции тратится на разделение полученных продуктов вследствие неселективности использованного процесса. Наиболее остро проблема разделения продуктов органического синтеза касается фармацевтического производства. В связи с этим еще более актуальным становится вопрос разработки новых методов синтеза гетероциклических соединений, которые позволят сократить затраты, связанные с очисткой продуктов реакции и решить ряд экологических проблем на предприятиях химической и фармацевтической промышленности. Кроме того, зачастую выбор новых методов проведения органических реакций решает вопросы регио-, диастерео- и энантиоселективности, помогает расширить возможности использования катализа. В настоящий момент среди новых методов в синтезе гетероциклических соединений можно выделить следующие:
•проведение реакций в отсутствии растворителя,
•проведение реакций в воде,
•проведение реакций в среде полиэтиленгликоля (ПЭГ),
•проведение реакций в сверхкритическом СО2,
•использование в качестве растворителей ионных и перфторированных жидкостей,
•использование микроволновой активации химических превращений.
3
Реакции, протекающие без использования растворителя
Большая часть отходов производства и очистки продуктов органического синтеза представляет собой растворители, в среде которых осуществлялось взаимодействие. Использование растворителей в органическом синтезе облегчает процесс теплообмена между реакционной массой и окружающей средой, решает проблемы массопереноса и облегчает равномерное распределение субстратов в реакционном объеме. Все это привело к тому, что долгое время считалось обязательным использование растворителей для проведения синтетических реакций. В настоящее время известно, что из-за особенностей кристаллических решеток проведение реакций без растворения способствует более селективному протеканию процесса. Хотя попрежнему часто используются различные растворители для осуществления изучаемых взаимодействий. Проведение реакций в отсутствии растворителя позволяет избежать ранее указанных затрат. Кроме того, данная методология имеет ряд преимуществ таких как:
•уменьшение рисков, связанных с работой с органическими растворителями;
•отсутствие необходимости утилизации или очистки для повторного использования растворителей;
•в случае проведения реакции на неорганической подложке сокращаются расходы на ее восстановление;
•увеличение чистоты получаемых продуктов;
•уменьшение времени протекания реакции;
•отсутствие необходимости защиты реакционно-способных функциональных групп;
•сокращение затрат производства.
Большое число реакций, протекающих без растворителя, активируют при помощи микроволнового излучения.
Можно привести множество примеров реакций, протекающих без растворителя.
Азиридины – известный класс трехчленных гетероциклов. Их уникальная структура обладает огромным потенциалом в качестве промежуточного звена в органическом синтезе, кроме того, многие из них являются биологически активными. Получить азиридины можно из илиденнитроалканов и [4-нитробензосульфонил] оксикарбамата простым трением друг об друга данных реагентов (схема 1). В качестве неорганической базы используется оксид кальция.
4
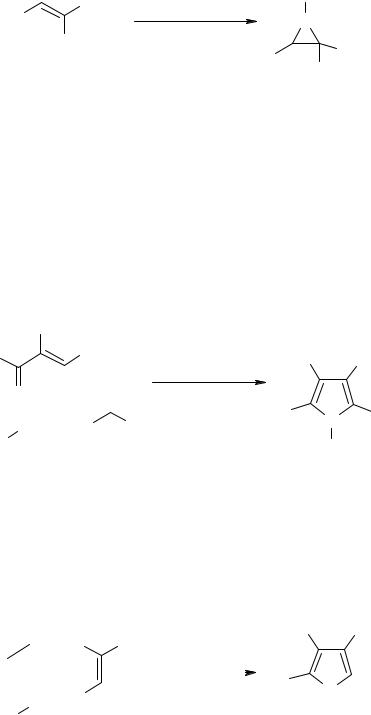
Схема 1
|
NO2 NsONHCOOEt |
COOEt |
|
R1 |
N |
||
CaO |
|||
R2 |
NO2 |
||
R1 |
|||
|
|||
|
|
R2 |
Без растворителя можно проводить синтез пирролов по реакции Паля– Кнорра. Зачастую реакцию проводят с использованием микроволновой активации, это позволяет в значительной мере снизить время протекания процесса. Варьируются условия синтеза пирролов в зависимости от исходных субстратов. Так, например, взаимодействие α,β-непредельных карбонильных соединений с аминами и нитроалканами (схема 2) протекает на подложке из нитроаклкана на силикагеле, в таких же условиях реагируют N,N- дизаме-щенные тиобарбитуровые кислоты, образуя пирроло[2,3- d]пиримидины.
Схема 2
R2 |
|
|
|
|
|
|
R3 |
R1 |
MWI |
R2 |
|
R1 |
|
O + |
|
|
|
|
||
|
SiO2 |
R3 |
|
R5 |
||
|
|
N |
||||
NH2 |
R5 |
NO2 |
||||
|
|
|||||
|
|
|
||||
R4 |
|
|
|
R4 |
|
|
|
|
|
|
|
Другой вариант синтеза пирролов основан на трехкомпонентной реакции карбонильной компоненты, амина и α-замещенногонитроалкена на оксиде алюминия. Интересно, что обязательно использовать замещенный нитроалкен (схема 3), иначе реакция идет в нескольких направлениях.
Схема 3
|
|
|
R1 |
|
|
|
R3 |
|
R1 |
|||
|
|
|
|
|
|
R4 |
NO2 |
|
|
|||
|
|
|
|
|
|
MWI |
|
|
||||
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
+ |
|
|
|
|
R4 |
|
|
|
O |
R3 |
|
|
|
N |
|||||||
|
|
|
|
|
|
|
|
Al2O3 |
|
|
||
|
|
|
|
|
|
|
|
|
|
|||
R2 |
|
NH2 |
|
|
R2 |
|||||||
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|||||
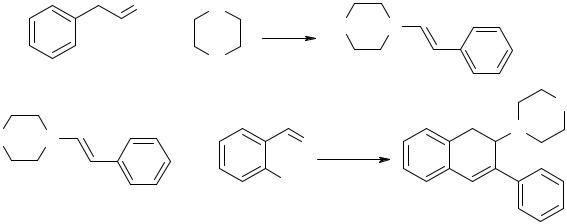
Также без растворителя протекает алкилирование алкенами ароматических соединений – реакция Фриделя–Крафтца. Например, пиррол алкилируется в α-положение (схема 4) с хорошими выходами при комнатной температуре в присутствии органического катализатора N,N’-ди(3,5- дитрифтор-метилфенил)-(тио)мочевины.
5
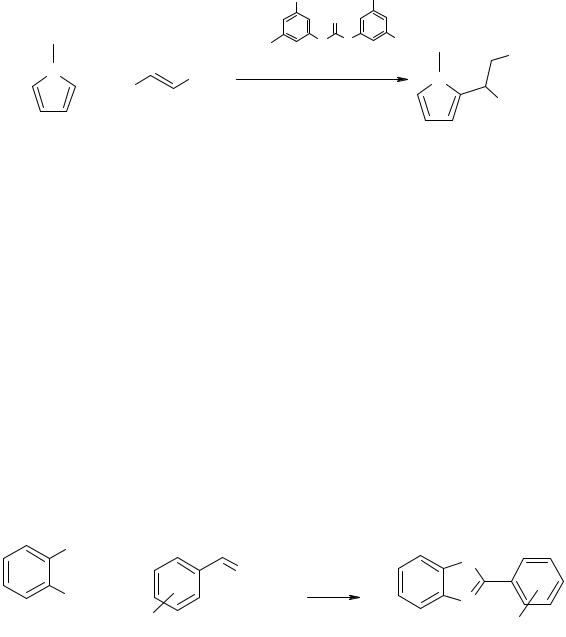
Схема 4
CF3 CF3
|
|
cat: |
|
X |
|
|
|
|
|
|
|
|
|
|
|
|
|
CF |
3 |
N |
N |
CF3 |
NO2 |
|
|
|
H |
H |
|
||
|
|
|
|
|
|||
N |
|
NO2 |
|
X=O,S |
|
|
|
+ |
|
|
|
|
N |
||
|
R |
|
r.t. |
|
|
R |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
Вода как растворитель
Использование воды в качестве растворителя – не только дань экономическим, экологическим и химическим предпосылкам оптимизировать процессы проведения химических реакций, но и стремление людей быть еще ближе к природе, где вода выступает в роли основного растворителя. Исходя из этого, можно говорить о том, что вода – самый экономически выгодный и доступный растворитель. Кроме указанных преимуществ, предпочтительность использования воды в качестве растворителя проявляется еще и ее непосредственным участием во многих реакциях, протекающих в водной среде.
Как бы это ни казалось противоречивым, вода не относится к самым экологически безопасным растворителям. Растворимость соединений в воде обычно выше, чем, например, в СО2. В результате увеличивается риск загрязнения окружающей среды в случае выброса такой загрязненной воды в атмосферу. Тем не менее, множество химических превращений протекает в воде, например, синтез арилбензтиазолов (схема 5).
Схема 5
SH |
|
|
S |
|
+ |
O |
kat |
||
|
||||
NH2 |
|
water |
N |
|
R |
|
R |
||
|
|
|
Предложен новый one-pot метод синтеза 4-гидроксипирролов в результате трехкомпонентной реакции β-дикарбонильных соединений с арилглиоксалями и ацетатом аммония при комнатной температуре в воде (схема 6). При этом в течение 30–45 минут образуются чистые продукты с превосходными выходами.
6

Схема 6
O |
O |
|
O |
NH4OAc |
|
H |
O |
+ O |
|
Ar |
N |
|
|||
|
|
|
|
|
R1 |
||
R |
|
|
|
|
|
||
|
R1 |
Ar |
вода, r.t. |
HO |
|
R |
|
|
|
|
|
||||
|
|
|
|
|
|
Установлено, что использование воды в качестве растворителя позволяет проводить реакцию Дильса–Альдера в несколько раз быстрее, чем в случае органических растворителей. При этом применение воды позволяет увеличить селективность протекания данной реакции. Положительный гидрофобный эффект на протекание органических реакций объясняется возможностью образования клатратов между водой и несмешивающимися с ней неполярными растворами участвующих в реакции соединений.
Низкая растворимость кислорода в воде предопределяет проведение реакций, чувствительных к нежелательному воздействию О2, в водной среде. И не менее важно, что в отличие от органических растворителей отсутствует необходимость дополнительных трудностей, связанных с выделением продуктов реакции, которые, как правило, оказываются водонерастворимыми.
Уникальные физические и химические свойства воды позволяют проводить в ней широкий спектр органических реакций:
•реакции рециклизации;
•гетеролитические реакции;
•радикальные реакции;
•реакции карбенов;
•металлоорганические реакции;
•реакции окисления и восстановления.
Некоторые реакции, протекающие в воде, активируют при помощи микроволнового излучения (схема 7).
Схема 7
Вода используется как растворитель для реагентов, которые в ней растворяются. Для нерастворимых в воде веществ предложена возможность проведения реакции на границе раздела фаз – реакции «на воде». Установлено, что такие процессы протекают гораздо быстрее по сравнению с аналогичными взаимодействиями с использованием органических растворителей (схема 8). На границе раздела фаз вода – органическое нерастворимое в воде соединение в каждых 4 граничных молекулах воды есть свободная ОН-
7
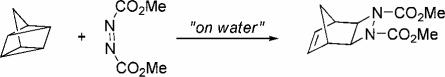
группа, которая за счет образования водородной связи с органическим соединением оказывает каталитическое влияние на протекание процесса, что и объясняет увеличение скорости реакции.
Схема 8
Небольшой размер и высокая полярность молекулы воды в сочетании с трехмерной сеткой водородных связей дают воде уникальные свойства: высокая плотность энергии связи (около 550 кал/см3), высокое поверхностное натяжение (72 dyn/см) и высокая теплоемкость.
Использование ПЭГ в качестве растворителя
Полиэтиленгликоли (ПЭГ) HO-(CH2CH2O)n-H обладают характеристиками, которые обуславливают их широкое применение как экологически безвредных химических веществ. Вследствие практически полного отсутствия токсичности, данные полимеры входят в состав лекарственных форм, разрешенных к употреблению внутрь, косметических средств. По этой же причине составы на основе ПЭГ также используются в биотехнологии и медицинских исследованиях. Еще одним достоинством ПЭГ является легкая биоразлагаемость этих полимеров. ПЭГ доступны в широком диапазоне молекулярных масс от 200 до десятков тысяч. При комнатной температуре полимеры представляют собой вязкие малолетучие жидкости до М < 600, с большей молекулярной массой – воскоподобные твердые вещества. Жидкие ПЭГ неограниченно смешиваются с водой, высокая растворимость сохраняется и для твердых. Это дает возможность использовать ПЭГ с различной молекулярной массой, как в чистом виде, так и в композициях с водой или другими водорастворимыми растворителями. С другой стороны, несомненным преимуществом ПЭГ является их очень низкая цена и коммерческая доступность в больших количествах, что имеет существенное значение при проведении крупномасштабных синтезов. Следует также отметить, что при промышленном производстве полиэтиленгликолей какие-либо вредные и токсичные отходы отсутствуют.
В органической химии ПЭГ применяются в течение последних 20 лет. До недавнего времени ПЭГ в основном использовались как реакционная среда, обладающая катион-сольватирующей способностью, т.е. в качестве альтернативы краун-эфирам и другим катализаторам межфазного переноса, причем это было также обусловлено благоприятными экологическими свойствами полимеров (нетоксичность, биоразлагаемость). С развитием ме-
8
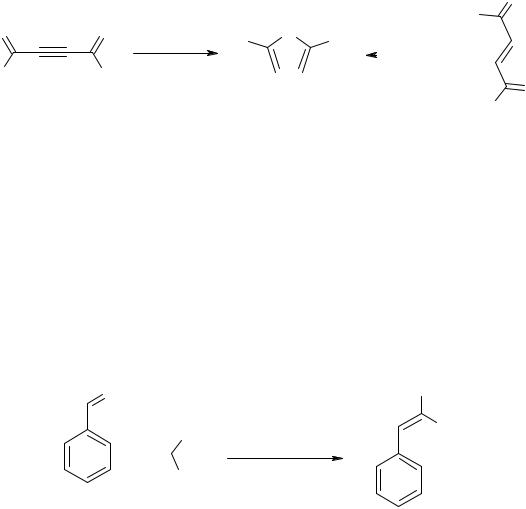
тодологии комбинаторной химии полиэтиленгликоли стали применяться как жидкофазные растворимые подложки для связывания как реагентов, так и катализаторов. По данным характеристикам ПЭГ, если не превосходили, то, по крайней мере, не уступали твердофазным носителям, обладая при этом существенно более низкой стоимостью.
Однако наиболее перспективным и к настоящему времени практически не изученным является применение полиэтиленгликолей в качестве реакционной среды в синтезе гетероциклических соединений.
Впервые был изучен ПЭГ-200 как растворитель для органических реакций. Этот полимер оказался подходящим в реакциях гидрирования с палладиевым катализатором и для реакций Паля–Кнорра (схема 9).
|
|
|
|
|
|
|
|
Схема 9 |
|
|
HCONH4 |
R |
|
HCONH |
|
O |
|
|
|
или |
4 |
Ar |
||||
O |
|
|
|
|
или |
|||
O HCONH3R Ar |
N |
Ar HCONH3R |
|
|
||||
Ar |
Ar |
ПЭГ-200 |
|
|
|
ПЭГ-200 |
|
O |
|
|
|
||||||
MW |
|
|
|
MW |
|
|||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
Ar |
Различные арилзамещенные пирролы были получены с высокими выходами в течение 1–5 минут из ендионов или индионов с формиатом аммония или алкиламмония.
Известны единичные примеры использования ПЭГ в реакциях Биджинелли, Паля–Кнорра и некоторых других (схема 10), причем выбор полимеров ограничен только ПЭГ-400, реже ПЭГ-600. По сравнению с обычными (токсичными и легковоспламеняющимися) органическими растворителями в этих случаях, как правило, не требуются катализаторы, а выходы целевых продуктов – хорошие.
Схема 10
O |
CN |
CN PEG 400/H2O |
CN |
+ |
|
CN |
|
Большие, во многом новые и необычные возможности открывает комбинированное использование в гетероциклическом синтезе микроволнового облучения, полиэтиленгликолей, а также их водных растворов, высокой температуры и давления. Комплексное исследование и разработка различ-
9
ных методов проведения синтеза гетероциклических соединений при активации в MW-реакторе существенно расширяет возможности методологии экологически чистой химии по снижению антропогенной нагрузки на окружающую среду. Использование микроволнового излучения часто позволяет превратить многостадийные реакции в one-pot процессы и исключить применение растворителей (схема 11).
O |
|
|
O |
|
|
Схема 11 |
|
|
mv |
O |
N |
||
|
+ |
|
|
|||
|
|
|
|
|||
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
O |
O N |
|
+ |
|
|
O mv |
N |
|
|
|
|
|||
|
|
|
OH NH4OAc |
|||
|
|
|
|
|||
Использование ионных жидкостей, как растворителей
Ионные жидкости – это жидкие при нормальных температуре и давлении соли неорганических и органических кислот с объемными органическими основаниями. Как правило, они состоят из органических катионов (имидазолия, пиридиния, тетраалкиламмония, гуанидиния, тетраалкилфосфонаты) (схема 12) и неорганических анионов (галогениды, сульфаты, сульфанаты, фосфаты, тетрафторбораты, гексафторфосфаты и др.) и имеют относительно низкую температуру плавления (обычно ни-
же 100 °С).
Обычно они нелетучи, негорючи, стабильны, обладают хорошими растворяющими свойствами и способны к регенерации.
Подбором подходящей комбинации катиона и аниона можно в широких пределах регулировать свойства ионных растворителей: полярность, растворяющую способность, нуклеофильные и электрофильные свойства, и тем самым влиять на направление, глубину и селективность реакций.
10
