
Беседы с нашим абитуриентом о химии Учебное пособие
..pdf
Химические измерения и средства, необходимые для их проведения, упоминались в самых ранних источниках. Первый аналитический прибор – весы – известен с глубокой древности. Вавилоняне считали весы настолько важным инструментом, что их использование контролировали жрецы.
Во времена алхимии выполнен огромный объем экспериментальных работ, что обеспечило накопление обширной информации о свойствах соединений. Для анализа веществ стали использовать растворы.
В период алхимии появились новые способы обнаружения веществ, основанные на переводе их в раствор. В этот период было открыто большинство химических реакций, использованных впоследствии при разработке классической схемы качественного анализа.
Роберт Бойль (17 в.) ввел термин “химический анализ”. Антона Лавуазье (18 в.) считают “отцом аналитической химии” благодаря тщательным количественным экспериментам, которые он провел (с использованием аналитических весов) для доказательства закона сохранения массы.
Большой вклад в развитие аналитической химии внесли члены Петербургской академии наук, активно занимавшиеся химическим анализом: М.В. Ломоносов, Т.Е. Ловиц, В.М. Севергин, Г.И. Гесс и др.
Наука аналитическая химия состоит из качественного анализа и количественного анализа.
Задача первого – идентификация элементов, ионов, вещества или соединений, присутствующих в образце.
Задача количественного анализа – определение того, сколько данного компонента или нескольких компонентов (концентрация, масса, массовая доля) содержится в образце.
Для сравнения качественного и количественного анализа рассмотрим, например, последовательность аналитических процедур допинг-контроля во время Олимпийских игр.
Список запрещенных препаратов включает более 500 физиологически активных веществ различных классов: стимуляторов, стероидов, диуретиков, наркотиков, анальгетиков и др. средств.
Необходимо быстро протестировать большое количество спортсменов, поэтому нерационально подвергать каждую пробу детальной процедуре количественного анализа.
На стадии скрининга (предварительного качественного анализа) пробы мочи в течение короткого времени тестируют на наличие в них целых классов соединений. Пробы, вызвавшие подозрение, заново подвергают качественному анализу, идентифицируя отдельные компоненты. И, наконец, на заключительном этапе, чтобы подтвердить, что концентра-
Отец спрашивает сына: — Что сегодня было на уроках? — На химии изучали взрывчатые вещества. — А что завтра будете делать в школе? — В какой школе, папа?
11

ция запрещенных веществ превышает норму, используют методы количественного анализа.
Усилия химиков-аналитиков направлены на удовлетворение нужд многих наук и областей.
Вмедицине аналитическая химия составляет основу клинических лабораторных тестов, помогающих врачам диагностировать заболевания и добиваться успехов в их лечении.
Аналитическая диагностика генов предрасположенности позволяет "заглянуть в будущее" человека и обеспечить своевременную защиту организма от нежелательных эффектов, которые могут возникнуть под действием неблагоприятных эндогенных и экзогенных факторов (лекарства, продукты питания, среда обитания, инфекции и т.д.).
Обращает на себя внимание возрастающий интерес к изучению состава выдыхаемого воздуха.
Полагают, что диагностика, опирающаяся на газовый анализ выдыхаемого воздуха, может обладать большой достоверностью и универсальностью и позволит проводить комплексные исследования организма.
Интерес к анализу волос проявляет судебно-медицинская экспертиза, химико-токсикологический анализ наркотических и психотропных веществ, психиатрия, клиническая терапия. Важной особенностью волос является их способность поглощать токсичные вещества из организма человека и сохранять их практически неизменными в течение длительного времени (например, известны факты обнаружения морфина в волосах египетской мумии спустя несколько тысяч лет).
Возможность получения информации о содержании “нелегальных” препаратов в волосах автомобилистов, спортсменов, сотрудников особо опасных областей производства объясняет интерес к этой проблеме в социальной сфере.
Впромышленности аналитическая химия предоставляет средства для испытаний сырья и гарантии качества готовой продукции. Многие продукты, используемые в быту, в т.ч. продукты питания, гигиены, лекарства, топливо и др. вещества, перед тем как поступить в продажу, анализируют с помощью методик, разработанных и проведенных химикамианалитиками.
Степень загрязнения окружающей среды часто оценивают при помощи тестов на предполагаемые загрязнители, используя средства и методы аналитической химии.
Открытие новых элементов – это аналитическая задача. Так было до последнего времени, когда новые элементы стали “делать” физики-ядерщики, да и то без химикованалитиков обойтись они не могут. Развитие атомной энер-
Гламурная школьница не сделала физику, так как в салоне делала химию
Жизнь химика Александра Порфирьевича Бородина связана не только с химией, но и с музыкой
12
гетики, исследование лунного грунта, установление подлинности произведений искусств – лишь некоторые примеры практического применения химического анализа. Трудно назвать область, где бы не использовались результаты аналитической химии!
К настоящему времени достигнут громадный прогресс в |
|
развитии химического анализа, который включает сложные |
|
приборы, управляемые компьютерами, проводятся весьма |
|
трудные анализы и измерения при очень низких концентра- |
|
циях веществ (10-12 –10-15 г). |
|
Современные высокочувствительные аналитические при- |
|
боры могут обнаружить при анализе три молекулы какого- |
|
либо соединения среди трех миллиардов молекул исследуе- |
|
мого материала. |
|
На сегодняшний день мировой рынок аналитических при- |
|
боров составляет более 1 триллиона долларов. Число еже- |
|
годных химических анализов – 10 млрд. |
|
Задачи |
Из-за реакции |
Пример 1. |
окисления на |
а) Как приготовить 400 мл 25%-ного раствора магнезии |
стенах ущелий и |
(MgSO4) с плотностью ρ =1,2 г/мл из более концентрирован- |
карьеров появ- |
ного 5 М раствора? |
ляются цветные |
б) Раствор MgSO4, приготовленный в предыдущем зада- |
рисунки. |
нии, был проверен фармацевтом. Обнаружено, что точная |
|
концентрация раствора равна 2,5 моль/л. Каков курс лечения |
|
данным препаратом (сколько дней), если пациенту назначи- |
|
ли инъекции по 5 мл один раз в день и суммарная (кумуля- |
|
тивная) доза должна составить 125 ммоль? |
|
Решение: |
|
а) Найдем массу раствора, который мы собираемся приго- |
|
товить: |
|
m = V·ρ = 400 ·1,2 = 480 г |
|
В соответствии с определением массовой доли этот рас- |
|
твор должен содержать |
|
25 г (MgSO4) в 100 г (раствора), |
|
х г (MgSO4) в 480 г (раствора), |
|
таким образом, находим х = 25·480/100=120 г. |
|
Однако, по условию задачи у нас нет кристаллического |
|
MgSO4, который мы могли бы взвесить для приготовления |
|
раствора: нужно разбавить более концентрированный рас- |
|
твор, который содержит 5 моль (MgSO4) в 1 л, |
|
т.е. m (MgSO4)= n· M = 5 моль · 120 г/моль = 600 г. |
|
Следовательно, найдем объем 5 моль/л раствора, который |
|
содержит 120 г MgSO4: |
|
13
600г (MgSO4) – в 1000 мл
120г (MgSO4) – в х мл, тогда х = 200 мл.
Таким образом, мы отбираем 200 мл 5 моль/л раствора MgSO4, помещаем в колбу на 400 мл, добавляем необходимое количество дистиллированной воды до метки (фактически раствор должен быть разбавлен в 2 раза).
Существуют и другие способы решения этой задачи. Предложите свои варианты.
б) Если раствор магнезии используется в качестве лекарственного препарата, то с разовой дозой 5 мл пациент получает следующее число моль MgSO4 :
2,5 моль (MgSO4) – в 1000 мл (раствора) х моль (MgSO4) – в 5 мл (раствора), тогда х = 0,025 моль = 2,5 ммоль
моль (в день) · число дней = моль (суммарная доза) 2,5 · число дней = 125, => число дней = 10.
Курс лечения 10 дней.
Ответ: а) 200 мл 5 моль/л раствора разбавить до 400 мл; б) 10дней.
Пример 2.
Вычислите рН, рОН, [ОН-] спинномозговой жидкости, ес-
ли [H+]=3,9·10-8моль/л.
Решение:
Согласно определению pH = -lg[H+] = -lg(3,9·10-8)= -lg3,9 -lg10-8=8-lg3,9=7,4
Показатель рОН легко найти, пользуясь соотношением рН+рОН=14.
Тогда получаем, рОН=14-рН=14-7,4=6,6.
Концентрацию гидроксильных ионов найдем, пользуясь
определением рОН:
рОН=-lg[ОН-]=6,6; lg[ОН-]=-6,6; [ОН-] =10-6,6 = 2,5·10-7
моль/л, или вспомним, что ионное произведение воды
Кw=[H+]·[ОН-]=1·10-14, тогда
[ОН-]=1·10-14/[H+]= 1·10-14/3,9·10-8 = 0,25·10-6= 2,5·10-7. Ответ: 7,4; 6,6; 2,5·10-7 моль/л.
1. Найдите число моль и массу вещества в каждом из растворов:
а) 0,1л сыворотки крови с концентрацией холестерола (C27H46O), равной 5,04·10-3 моль/л (нормальный средний показатель человеческой крови);
Один из синтезируемых растениями фитогормонов, газ этилен, способствует созреванию плодов, причём он образуется, даже если плод уже сорван с ветки. Поэтому фрукты перед длительной транспортировкой собирают недозрелыми, и в дороге они поспевают сами. А для контролируемого процесса фрукты помещают в камеры, куда принудительно подаётся этилен. Уже спелые плоды выделяют ещё больше газа, что можно использовать для ускорения созревания неспелых в домашних условиях, просто положив их в один пакет.
14

б) 325 мл питьевой воды с концентрацией сульфата железа (FeSO4) 1,8·10-6 моль/л (минимальное количество, которое можно различить на вкус).
Ответ: а) 5,04·10-4 моль; 0,195 г; б) 5,8·10-7 моль; 8,9·10-5г.
2.Найдите молярную концентрацию следующих растворов: а) 1,9·10-4 г NaCN на 100 мл крови (минимальная леталь-
ная доза цианида);
б) 27 г глюкозы (C6H12O6) в 500 мл раствора для внутривенных инъекций.
Ответ: а) 3,9·10-5 моль/л; б) 0,3 моль/л.
3. Концентрация ионов калия (К+) в сыворотке крови составляет в среднем 16 мг на 100 г. Найдите молярную концентрацию и массовую долю, если плотность сыворотки
1,025 г/мл.
Ответ: 4.2 ммоль; 0,016%.
4.Сульфат натрия (Nаtrium sulfuricum, глауберова соль) обладает слабительным действием. Какую массу кристалло-
гидрата Na2SO4∙10H2О надо добавить к 100 мл 0,06 моль/л раствора сульфата натрия (ρ ≈1,07 г/мл), чтобы получить 15%-ный раствор?
Ответ: 52,2 г.
5.Пероксид водорода (Hydrogenii peroxidum) относится к фармацевтическим препаратам, однако его концентрация с
течением времени уменьшается, так как Н2О2 активно окисляет примеси органических веществ, находящихся в воде, и разлагается под действием солнечного света. Поэтому его обычно хранят в склянках из темного стекла. Периодически концентрацию пероксида водорода необходимо контролиро-
вать. Концентрацию пероксида водорода определяют в сернокислой среде на основе реакции:
5H2O2 2KMnO4 3H2SO4 2MnSO4 K2SO4 5O2 8H2O
Расставьте коэффициенты методом электронного баланса в уравнении окислительно-восстановительной реакции.
Рассчитайте объем (мл) 0,1000 моль/л KMnO4, который пойдет на взаимодействие с 50,00 мл 0,2000 моль/л Н2О2.
Ответ: 40,00 мл.
6. Пациент принял таблетку, содержащую 10 мг лекарственного вещества. Предполагается, что за сутки с мочой (~1,5 л) выделится около 80% принятого лекарственного вещества.
Последние слова учителя химии: «Дети! Этот опыт совершенно безопасен!»
С помощью углекислого газа можно получить большое количество других веществ
15

Определить, достаточно ли возможностей выбранной аналитической методики (предел определения равен 5 мкг вещества), чтобы определить данное вещество в пробе объемом 10 мл, взятой из собранной за сутки мочи пациента.
Ответ: 53 мкг > 5 мкг; c помощью данной методики можно определить лекарственное вещество.
7.Определение жесткости воды – один из самых распространенных химических анализов, проводимых в лаборатории методами аналитической химии. Анализируемая жесткая вода содержит гидрокарбонат кальция (массовая доля 0,015%) и гидрокарбонат магния (массовая доля 0,005%). Какую массу гидроксида кальция надо добавить к воде объ-
емом 10 л для устранения жесткости? (ρ(Н2О) ≈1 г/мл). Ответ: 1,19 г.
8.В лаборатории в ходе предварительных испытаний было установлено, что анализируемый раствор содержит нитрат двухвалентного металла. Далее 200 г раствора разделили на две равные части. К одной добавили избыток раствора сульфида аммония, причем выпало 4,78 г осадка. К другой части добавили избыток раствора сульфата калия, при этом образовалось 6,06 г осадка. Найдите массовую долю соли (какого металла?) в исходном растворе.
Ответ: Pb(NO3)2; 6,62%.
9.Два юных химика исследовали взаимодействие раствора
сульфида калия K2S c раствором дихромата калия K2Cr2O7. Один из них получил осадок, нерастворимый в разбавленной серной кислоте, но растворяющийся при нагревании в концентрированной азотной кислоте. Второй – осадок, частично растворимый в разбавленной серной кислоте. Как можно объяснить результаты, если известно, что все наблюдения правильны?
Подсказка: достаточно правильно составить окислитель- но-восстановительное уравнение реакции, чтобы все стало ясно.
10.В исследуемом растворе могут содержаться ионы: K+, NH+, Pb2+, Ag+, Ca2+, Ba2+. Составьте план качественного анализа раствора и напишите соответствующие химические реакции.
Для меня задача по физике/химии выглядит примерно, так: летели два верблюда, один рыжий, другой налево. Сколько весит килограмм асфальта, если ёжику 24 года?
Ложки, содержащие галлий, могут расплавиться в горячей воде
Небольшое количество метанола может привести к слепоте
16

Раздел 3. ОРГАНИЧЕСКАЯ ХИМИЯ
Произведем некоторую систематизацию знаний по органике.
Так, скажем, что в органической химии существует 3 вида частиц, в зависимости от заряда и атакованной группы атомов.
Радикал – атом или группа атомов, несущих 1 неспаренный электрон: метил (▪CH3), этил (▪C2H5), ▪ОН (гидроксигруппа), ▪NO2 ( нитрогруппа) и др.
Электрофил (E+) (“филия” – любить) – положительнозаряженный атом или группа атомов, атакующие отрицательно заряженные частицы.
Нуклеофил (Nu-) (“nucleo” – ядро, которое заряжено положительно), следовательно, атакующая группа должна быть отрицательно-заряженной, таким образом, нуклеофил – отрицательно заряженный атом или группа атомов, атакующие положительно-заряженные частицы.
Относительно типов реакций в органической химии, их тоже можно разделить на три группы: реакции присоединения, замещения и отщепления.
Переход вещества из твердого в газообразное состояние в химии называется сублимацией
Двое химиков в лаболатории:
-Вась, опусти руку в этот стакан.
-Опустил.
-Что-нибудь чувствуешь?
-Нет.
-Значит серная кислота в другом стакане.
И каждому из типов характерен тот или иной механизм, в зависимости от участвующей частицы.
Например, галогенирование алканов, состоящее из трех классических этапов радикального замещения: инициирование (или рост цепи), рост цепи (пролонгация) и обрыв цепи. Параллельно с основной реакцией протекает и побочные реакции, однако, их принято игнорировать.
Раритетные машины достаточно часто украшали хромом
17

В случае реакций, присущих алкенам, алкинам, алкадиенам наблюдаем скорее реакции электрофильного присоединения, поскольку в молекулах имеется электронное облако, возникшее в результате перекрывания р-орбиталей sp2 гибридизованных атомов С.
Карбокатион иначе называется σ – комплексом (теперь атомы, которые при двойной связи имели sp2-гибридизацию, меняют тип гибридизации на sp3).
Электрофильное замещение наблюдается у ароматических соединений (бензол и его гомологи). В зависимости от того какие функциональные группы входят в состав той или иной молекулы, в том числе, ароматического соединения, вещество проявит свойства и за счет присутствующей группы.
Урок химии. Учительница:
-Маша, какого цвета у тебя раствор?
-Красного.
-Правильно. Садись, пять.
-Катя, а у тебя?
-Оранжевого.
-Не совсем правильно. Четыре, садись.
-Вовочка, цвет твоего раствора?
-Черный.
-Два. Класс! Ложись!!!!
Рассмотрим общий механизм электрофильного замещения.
По такому механизму протекают реакции алкилирования (Х.р. Фриделя-Крафтса), галогенирования, нитрования и сульфирования ароматических соединений бензола и его гомологов.
Реакции идут в присутствии катализаторов, функция которых активировать молекулы реагирующих веществ, снизить энергию активации и выйти из реакции без затрат.
Так, при алкилировании и галогенировании используются так называемые кислоты Льюиса (такие соли как – хлорид алюминия, бромид железа (III)). Роль этих кислот Льюиса заключается в формировании электрофила, т.е. активной частицы, готовой к атаке ароматического кольца (метильного катиона, катиона нитрогруппы, катиона сульфогруппы и пр.). Далее электрофил готов к атаке бензольного кольца, с образованием вначале π-комплекса, а затем и карбкатиона,
Масса нашей планеты увеличилась на один миллиард тонн за последние пять столетий.
Организм человека выделяет приблизительно 1 кг углекислого газа в сутки
18
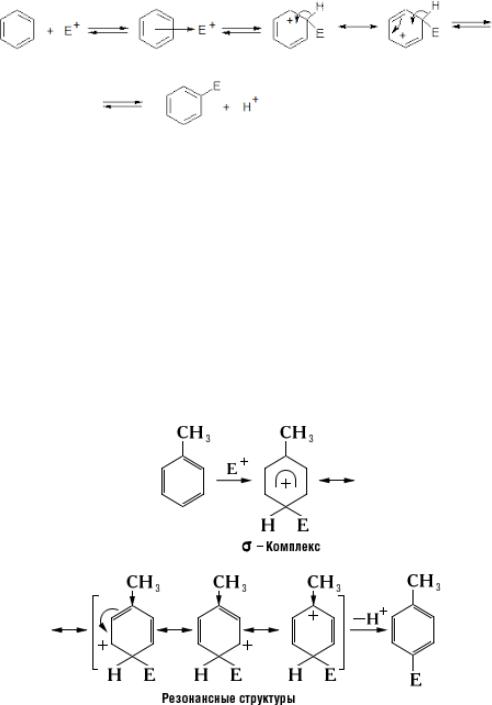
которые также называется σ-комплекс. Но, т.к. любая система стремится к устойчивости, так цикл замыкается с отщеплением катиона водорода. Образовавшийся Н+ соединяется с галогеном или другой группой, освобождая, в свою очередь, катализатор.
Джозеф Блэк открыл углекислый газ в
1754 году.
пи-комплекс сигма-комплекс
С другой стороны есть понятие ориентации в ароматическом кольце. Выделяют две группы ориентантов: орто-, па-
ра- и мета.
К орто- и пара-ориентантам (т.е. ориентантам первого рода) относятся доноры электронных пар такие как: алкильные радикалы ( CH3 метил, C2H5 этил, C3H7 пропипл и т.д.), гидроксигруппа (-OH), аминогруппа (-NH2), галогены (Hal), все без исключений и алкоксигруппа (-OR).
Приведем механизм электрофильной атаки толуола (метилбензол)
Оксид мышьяка издавна применялся для травли грызунов, поэтому название элемента в народной речи было образовано от слова «мышь».
Кроме ртути при комнатной температуре в жидкое вещество переходит франций и галлий.
С другой стороны, мета-ориентанты, к которым относятся все сильные акцепторы (-COOH (карбоксильная группа), -NO2 (нитрогруппа), -C≡N (цианогруппа), -CHO (альдегидная группа), -CH=CH2 (остаток этилена – винил)).
19

В случае атак молекул ароматических соединений, включающих эти функциональные группы, электрофил будет ориентирован в мета-положение.
Хлор может вызвать аллергические реакции органов дыхания.
В молодости Чарльз Дарвин был знаменит своими химическими открытиями.
Предлагаем несколько задач по органической химии разных типов.
1.Какими способами, используя в качестве исходного вещества кокс, можно синтезировать метилформиат и этилацетат? Напишите и объясните уравнения соответствующих реакций.
2.Анилин можно получить из хлорбензола, фенола или нитробензола.
А) Напишите уравнения реакции получения анилина на базе указанных веществ через ацетилен и бензол, беря за исходное вещество карбид кальция.
Б) Какие количества исходного сырья необходимы для получения 1 т анилина из карбида (через промежуточную стадию нитробензола), содержащего 95% CаC2, железа и 22% соляной кислоты? Выход анилина принять равным 60%.
Ответ: 1806.5 кг железа, 10706 кг 22%-ой соляной кислоты.
3. При производстве мыла из жира (с выходом 85%) получено 7898.2 кг глицерина. Какое количество жира было использовано для производства, если одна из спиртовых групп глицерина была этерифицирована пальмитиновой кислотой, а остальные – масляной ксилотой?
Ответ: из 858 кг указанного жира получается 1 кмоль глицерина, т.е. гидролизу было подвергнуто 86658 кг жира.
В Индонезии люди добывают серу из вулкана, что приносит им большую прибыль.
Геосмин – это вещество, которое вырабатывается на поверхности земли после дождя, вызывая характерный запах.
20
