Лекция №1
ВВЕДЕНИЕ
Технической термодинамикой называется наука, изучающая законы взамного превращения различных видов энергии в физических, химических и технических устройствах и аппаратах.
Основой термодинамики являются два закона – два Начала. Эти законы получены опытным путем. Они утверждают, что нельзя построить вечный двигатель первого и второго родов. Вечный двигатель первого рода это двигатель, который производил бы энергию из ничего. Таким образом, первый закон является частной формой всеобщего закона природы – закона сохранения и превращения энергии применительно к тепловым и механическим явлениям. Вечный двигатель второго рода – это двигатель, который мог бы работать при наличии только одного источника энергии. Чтобы преобразовать теплоту в работу, необходимо иметь не менее двух источников теплоты («горячего» и «холодного»). Второй закон термодинамики показывает направление протекающих в природе процессов и устанавливает границы взаимного превращения теплоты и работы.
Исторически термодинамика выделилась в отдельную научную дисциплину в результате анализа процессов превращения теплоты в работу в паровых машинах. Во второй половине XVIII в. появились первые паровые машины – двигатели, в которых механическая энергия получается за счёт теплоты, выделяющейся при сгорании топлива. Затем появились двигатели внутреннего сгорания, в которых сгорание топлива происходит внутри цилиндра машины, и позднее − паровые турбины (конец XIX начало XX вв.).
Появление тепловых двигателей позволило широко использовать громадные природные энергетические ресурсы (уголь, торф, нефть, сланцы, газ) для получения механической энергии. В последние годы получили развитие газовые турбины и реактивные двигатели, работа которых также описывается термодинамичесмкими методами. В связи с этим актуальность изучения термодинамики все более возрастает.
Термодинамика рассматривает вещество как сплошную среду и использует для его исследования макропараметры, такие как давление, удельный объем, температура, которые могут определяться прямыми измереними.
Термодинамика не использует какие-либо гипотезы или теории о микроскопическом строении вещества, поэтому её методы не зависят от новых открытий микрофизики.
Знание термодинамики, её исходных идей, её универсального метода, строгого и эффективного математического аппарата является необходимой предпосылкой подготовки инженера. Термодинамика играет важную роль в развитии научного мышления, в формировании мировоззрения и представлений о мироздании и дает возможность практического приложения изучаемого материала.
Глава 1. Общие положения
1.1. Основные параметры состояния
Преобразование тепловой энергии (теплоты) в механическую энергию (работу) осуществляется с помощью вспомогательного вещества, называемого рабочим телом.
Наиболее подходящим состоянием рабочего тела является газообразное, так как именно в этом состоянии оно характеризуется наибольшей способностью сжиматься и расширяться. При расширении газ совершает работу. Состояние рабочего тела (газа) определяется физическими величинами, которые называются параметрами состояния. Основные параметры состояния: абсолютная температура, абсолютное давление и удельный объем.
Температура определяет степень нагретости тела. В системе СИ (от англ. SI –system international) единицей измерения температуры является Кельвин (К); на практике широко применяется градус Цельсия (оС). Температура, выраженная в Kельвинах, обозначается символом Т, температура в градусах Цельсия – символом t, причем 1 К = 1оС.
Отличаются они началом отсчета: температурная шкала Кельвина отсчитывается от абсолютного нуля, равного –273,16 оС, шкала Цельсия – от температуры тройной точки воды, равной 0,01 оС (273,15 К): Т, К = t,оС + 273,15.
Термодинамическим параметром состояния является абсолютная температура Т, измеряемая в Кельвинах. В соответствии с молекулярно-кинетической теорией температура пропорциональна средней кинетической энергии поступательного движения молекул:
 ,
(1.1)
,
(1.1)
где
mм
– масса молекулы, кг;
 – средняя квадратичная скорость движения
молекулы, м/с; kБ
– постоянная Больцмана, равная
приблизительно 1,3810-23Дж/К;
– средняя квадратичная скорость движения
молекулы, м/с; kБ
– постоянная Больцмана, равная
приблизительно 1,3810-23Дж/К;
 −
средняя кинетическая энергия
поступательного движения молекулы.
−
средняя кинетическая энергия
поступательного движения молекулы.
Таким образом, температура тела тем выше, чем интенсивнее движение молекул.
Давление возникает в результате ударов молекул газа о стенки сосуда. Оно равно силе, действующей по нормали на площадь поверхности тела. Давление обозначается символом p, единицей измерения в системе СИ является паскаль (Па). 1 Па=1 Н/м2. В технике используются кратные и дольные единицы: килопаскаль, равный 103 Па (кПа), мегапаскаль, равный 106 Па (МПа) и другие, а также внесистемные единицы: бар (1 бар = 105 Па), кгс/см2 (1 кгс/см2 = 98,1 кПа).
Давление измеряют также высотой столба жидкости (ртути, воды и др.; p = 750 мм рт. ст. = 105 Па). Прибор для измерения атмосферного давления называется барометром, а измеряемое им давление барометрическим. Барометрическое давление обозначается символом В. Давление выше атмосферного называется манометрическим (pм) или избыточным (pизб) и измеряется манометром. Давление ниже атмосферного называется вакуумом (pвак) и измеряется вакуумметром.
Параметром
состояния является абсолютное давление
pабс.
Если давление выше атмосферного, то

Если
давление ниже атмосферного, то

Согласно
молекулярно-кинетической теории
 ,
Па где n – число молекул в единице объема.
,
Па где n – число молекул в единице объема.
Удельный
объем – это объем единицы массы вещества,
который обозначается символом
 :
:
 ,
, ,
,
где m, кг – масса вещества в объеме V; V, м3 – объем, занимаемый веществом массой m.
Величина,
обратная удельному объему, называется
плотностью и обозначается символом
 :
:
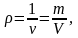
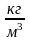 .
.
Удельный объем и плотность зависят от термодинамического состояния (в частности, от температуры и давления). Часто в теплофизических справочниках приводятся их значения для газов при нормальных физических условиях, то есть при давлении p = 101325 Па (760 мм рт. ст. ) и температуре Т= 273,15 К (t = 0оС).
Термодинамика рассматривает в первую очередь равновесные состояния и равновесные процессы изменения состояния. Если все параметры во всех точках системы одинаковы в каждый момент времени, то такое состояние называется равновесным. Равновесное состояние в координатах (p, v, T) изображается точкой. Для удобства обычно изображают проекцию этой точки в плоскости pv, pT, или vТ (чаще в плоскости pv).
Переход системы (рабочего тела) из состояния 1 (p1, v1, T1) в состояние 2 (p2, v2, T2) называется термодинамическим процессом изменения состояния (рис. 1.1).
Процесс изменения состояния рабочего тела может быть равновесным и неравновесным.
Равновесный – это такой процесс, который проходит через непрерывный ряд равновесных состояний. Равновесный процесс в координатах (p, v, T) изображается линией (pv – диграмма, рис. 1.1).
Реальные процессы неравновесны и могут только в той или иной степени приближаться к равновесным, а на диаграммах изображаются условно.
|
|
Рис. 1.1. Равновесный термодинамический процесс |
Рис. 1.2. Обратимый термодинамический процесс |
Равновесные процессы бывают обратимыми и необратимыми. Допустим, рабочее тело переходит из состояния 1 в состояние 2 через промежуточные состояния а, b, c, d (рис. 1.2).
Если, переходя в обратном направлении из состояния 2 в состояние 1, рабочее тело пройдет через те же промежуточные состояния d, c, b, a, не производя никаких изменений ни в рабочем теле, ни в окружающей среде, процесс будет обратимым. Если эти условия не выполняются, процесс будет необратимым.
Для того чтобы процесс был обратимым, он должен протекать без таких необратимых явлений как трение, теплообмен при конечной разности температур между источником теплоты и рабочим телом, диффузия. Например, в цилиндре с поршнем имеется газ. Если процесс сжатия газа протекает с трением, то за счет трения нагревается стенка и теплота уходит в окружающую среду. При прохождении процесса в обратном направлении теплота от окружающей среды к газу самопроизвольно не вернется. Следовательно, в результате сжатия в окружающей среде произошли изменения, а это значит, что процесс сжатия был необратимым.
Классическая термодинамика изучает в основном обратимые процессы, которые в реальных условиях не существуют, так как процессы в тепловых двигателях и аппаратах протекают при конечной разности температур между источником и рабочим телом. Однако, чем меньше эта разность температур, тем ближе действительный процесс приближается к обратимому.