
оип 19.09.22
.pdfснабжение производства всеми видами энергии, а также эксплуатацию и выполнение работ по ремонту теплосилового, электротехнического, сантехнического оборудования, средств связи и всех видов энергетических
сетей. http://prom-nadzor.ru/content/polozhenie-ob-otdele-glavnogo-energetika
Отдел контрольно-измерительные приборы и автоматика. Служба с одноименным названием выполняет следующие задачи и функции:
осуществление метрологического надзора техническое обслуживание, настройка и ремонт измерительного оборудования
внедрение новых систем автоматизации на предприятии, например, АСУ
Должностная инструкция Главного инженера фармацевтического предприятия вставляю статью где все четко расписано про главного инженера http://www.medbusiness.ru/upload/img/Spr15-8.pdf стр 4 из документа
Функции описаны на данном сайте под номером 3 http://prom-nadzor.ru/content/polozhenie-ob-inzhenernom-otdele
Документы регламентирующие деятельность ГОСТ 52249 приказ 916
10. Структура и функции отдела обеспечения качества промышленного фармацевтического предприятия.
Современная система качества на фармацевтическом производстве состоит из Отдела обеспечения качества (ООК) и Отдела контроля качества (ОКК).
Отдел обеспечения качества (ООК) гарантирует, что фармацевтическая компания придерживается требований GMP, а также является арбитром между отделом контроля качества, производственными подразделениями и техническими службами. Специалисты ООК проводят тренинги по системе GMP с персоналом на всех уровнях организации. При проведении всех
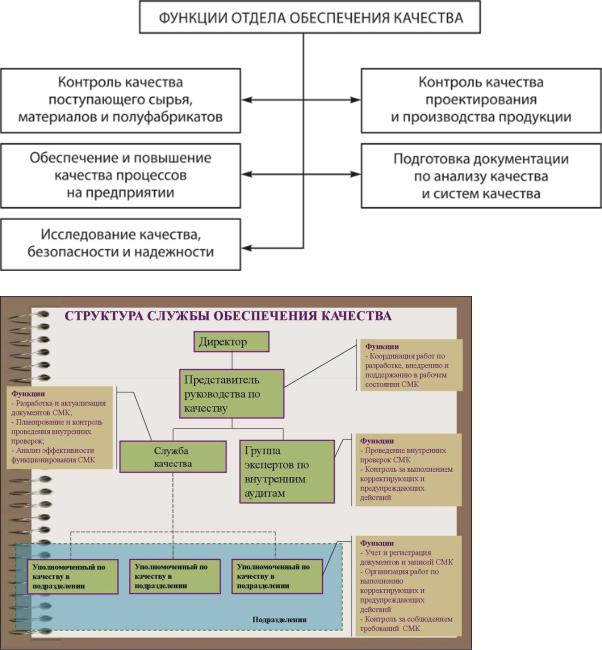
текущих задач ООК делает окончательные решения по качеству продукции и соответствию производства требованиям GMP, проводит расследование выявленных отклонений, несоответствий и жалоб, а также выполняет контроль над изменениями.
Проведенный анализ стандартов GMP показывает, что в целом они базируются на необходимости устранения негативных моментов в производственном процессе, в результате учета тех факторов, которые могут нанести ущерб готовой продукции. Правила GMP носят системный и предупреждающий характер.

СМК Система менеджмента качества — это набор специальных практик, внутренних политик, методик для работы компании, целью которых является удовлетворение покупателей товарами и услугами высокого качества на постоянной основе
Система обеспечения качества при производстве лекарственных средств
состоит из следующих элементов.
4.3.1 Информация о предприятии
"Информация о предприятии" - документ, содержащий основные данные о
предприятии в соответствии с подразделом 4.4.
4.3.2 Работа с материалами
Данный раздел включает в себя документацию, регламентирующую взаимоотношения с поставщиками исходных и упаковочных материалов,
порядок приема материалов, отбора проб, карантинного хранения и пр. от
заключения договоров (оформления заказов на поставку материалов) до выдачи материалов в производство в соответствии с разделом 5.
4.3.3 Организация производства
Данный раздел включает весь комплекс документации, регламентирующей производство лекарственных средств, от получения исходных материалов на складе материалов до сдачи продукции на склад и получения разрешения на реализацию готовой продукции в соответствии с разделом 6.
4.3.4 Контроль качества
Раздел содержит документацию по работе контрольных лабораторий, включая контроль материалов и готовой продукции в соответствии с разделом 7.
4.3.5 Анализ качества
Включает в себя проведение анализа рисков, случаев отклонения от спецификаций, рекламаций и организацию отзывов продукции с разработкой мер по повышению уровня работы в соответствии с разделами 7, 11.
4.3.6 Аудит
Проведение внешнего и внутреннего аудита позволяет своевременно обнаружить отклонения в производстве и связанные с ним факторы от установленных требований и принять необходимые меры в соответствии с разделом 13.
4.3.7 Подготовка производства
В понятие "подготовка производства" входят разработка проекта производства, строительство, оснащение оборудованием и приборами, разработка документации (методик аттестации критических помещений, оборудования и процессов, инструкций и пр.), проведение аттестации с оформлением протоколов, разработка планов организационно-технических мероприятий по обеспечению качества и развитию производства и пр.
4.3.8 Персонал
Разработка, реализация и контроль выполнения требований к
профессиональной подготовке персонала, системы обучения, инструкций по
поведению, личной гигиене и пр. в соответствии с разделом 9.
4.3.9 Система контроля исполнения
Содержит оформленный документально и реализованный организационно
порядок контроля исполнения и меры воздействия на нарушителей в соответствии с разделом 10.
Структура системы обеспечения качества приводится в "Информации о предприятии". Она должна быть доступной для восприятия и наглядной, так как сложные, запутанные и неясно изложенные предметы не воспринимаются, и к ним, как правило, относятся формально.

12. Структура и функции административного подразделения промышленного фармацевтического предприятия.
Административное подразделение – структурная единица компании,
осуществляющая документационное и административное обеспечение управления.
Цель подразделения – обеспечить эффективное управление путем поддержки и развития систем делопроизводства, информационного обмена, регламентации.
Административный аппарат:
Высшее руководство;
Исполнительный директор;
Директор по производству, директор по качеству, директор по развитию, директор по
науке, финансовый директор, технический директор;
Вподчинении директора по производству: главный технолог, начальники
производственных участков, заведующие складами;
Вподчинении директора по качеству: подразделение по обеспечению качества, подразделение по контролю качества;
Вподчинении директора по развитию: руководители научно-исследовательских
лабораторий, руководители подразделений по маркетинговому и экономическому
анализу, руководитель подразделения по связям с общественностью, руководитель PR-подразделений;
Вподчинении финансового директора: главный бухгалтер, начальник планового отдела, начальник коммерческого отдела, начальник отдела расчета заработной платы;
Вподчинении технического директора: главный инженер, начальник транспортно-логистического отдела, начальник отдела эксплуатации помещений и оборудования.
Функции административного подразделения промышленного фармацевтического предприятия:
1.Осуществляет системное руководство предприятием;
2.Определяет общую политику предприятия и её составляющих (кадровую, экономическую, финансовую политику, ассортиментную, PR-политику, политику качества и др.);
3.Формирует структуру предприятия;
4.Руководит ресурсным обеспечением предприятия.
13. Отличительные особенности мелкосерийного и крупносерийного фармацевтического производства
·Серия – кол-во ЛС, произведенного в результате 1-ого технологического цикла его производителем (из ФЗ 61)
·Серия (партия) - определенное количество исходного сырья, упаковочных материалов или продукции, подвергаемое обработке в одном или в ряде последовательных технологических процессов таким образом, что можно рассчитывать на однородность продукции в установленных пределах, при этом с точки зрения контроля готовой продукции серия
включает в себя совокупность единиц дозированной формы лекарственных средств (лекарственной формы), произведенных из одного объема исходного материала и прошедших единую последовательность производственных операций или единый цикл
стерилизации, а при непрерывном производстве - все единицы, произведенные в заданный интервал времени. Для завершения некоторых этапов производства иногда необходимо разделить серию на определенное
количество подсерий, которые позже объединяют для получения окончательной однородной серии. При непрерывном производстве
понятие серии должно относиться к определенной части продукции, характеризуемой однородностью. Размер серии в этом случае может
определяться либо фиксированным количеством, либо количеством, произведенным за определенный промежуток времени (из приказа 916)
Мелкосерийное производство характеризуется тем, что выпуск одноименной продукции систематически повторяется (через месяц,
квартал), т.е. нерегулярно при единичных или малых объёмах выпуска.
Для мелкосерийного производства лекарственных препаратов характерно
большое разнообразие номенклатуры производимой продукции,
многокомпонентное составов, широкое использование аптечной заготовки, номенклатура которой базируется на изучении часто повторяющихся прописей.
Работы ведутся по плану, учитывая сложность изготавливаемого препарата, в
специальных помещениях, где оборудование имеет групповое
расположение.
> Готовая продукция имеет ограниченный срок хранения.
Крупносерийное производство ЛС характеризуется высокой механизацией технологических процессов, оснащенностью современным оборудованием, узкой специализацией производства и ограниченной
номенклатурой лекарственных препаратов.
> Готовая продукция имеет длительный срок хранения
Крупносерийное производство отличается тем, что одноимен ная продукция
выпускается постоянно чередующимися партиями или идет непрерывно и носит постоянный характер.
Машины и аппараты располагаются по групповому признаку (а в мелкосерийном всё оборудование находится, грубо говоря, в одном месте)
Производственный процесс рассчитывается с большой точностью, и
изготавливаемая продукция движется непрерывно и последовательно через равные промежутки времени, от одного рабочего места к другому.
Готовая продукция выходит также непрерывно и ритмично.
Итого:
1. Мелкосерийное производство – много разной продукции
Крупносерийное – узкая специализация (одна какая-то продукция)

2.Мелкосерийное производство осуществляется редко в сравнение с крупносерийном, так как оно происходит непрерывно
3.Крупносерийное производство характеризуется высокой степенью технологического процесса, а также крутым оборудованием, когда как мелкосерийное заточено на часто повторяющихся процессах
4.Cрок хранения в мелкосерийном – ограниченно; в крупносерийном – длительный срок хранения продукции
5.Мелкосерийное производство выпускает единичные/ малые объёмы продукции, а крупносерийное характеризуется больших кол-во выпускаемой продукции
+на крупносерийном производстве образуются:
рабочие места
производственные участки
производственные цеха (это важно!!!!)
на мелкосерийном производстве действует бесцеховая структура
!!!!
+себестоимость на мелкосерийном производстве ниже,
чем на крупносерийном, так как задействовано
бОльшее кол-во ресурсов, персонала, большЕ трат на
сырьё итд
14.Система управления качеством: определение, общие принципы
качество (quality) – совокупность признаков, определяющих свойства готового продукта (услуги), его соответствие предназначенному применению и основным параметрам технологического процесса, включенным в регистрационные материалы.
Под управлением качеством (Quality Management) в фармацевтической промышленности понимают обеспечение надлежащего производства и контроля качества продукции в соответствии со стандартами качества исходя из назначения продукции и согласно
регистрационному досье, протоколу клинических испытаний или спецификации на продукцию.

на всех этапах процесса производства лекарственных препаратов.
ФСК фармацевтическая система качества : включает надлежащую производственную практику и управление рисками для качества лс.
Система должна быть полностью документирована, а ее эффективность постоянно контролируется
Документация ФСК
Руководство по качеству (Quality Manual) — это документ, излагающий политику в области качества и описывающий систему качества предприятия
Стандарты надлежащих практик — это требования, предъявляемые организациями здравоохранения на этапе разработки, исследований, производства и реализации лекарственных средств (ЛС). Руководства по надлежащим практикам устанавливают стандарты качества на различных этапах жизненного цикла ЛС.
Основные требования GMP
-все производственные процессы должны быть определены;
-критические стадии производственного процесса должны пройти валидацию;
-должен быть персонал с необходимой квалификацией;
-соответствующие помещения и оборудование;
-надлежащие материалы, контейнеры и этикетки;
-утвержденные методики и инструкции, которые изложены в виде распоряжений;
-необходимо протоколировать процесс производства; - все отклонения оценены;
-при дистрибуции не снижается качество продукции;
-системы отзывов и оценки рекламаций эффективны.
Документы излагающие правила gmp -ГОСТ 52-249
-Приказ Минпромторга России от 14.06.2013 № 916 «Об утверждении Правил организации производства и контроля качества лекарственных средств»
Контроль качества включает в себя: -отбор проб (контролеры)
-проведение испытаний (анализов) в контрольно-аналитической лаборатории -оформление соответствующей документации (протоколов, аналитический обзор)
Руководство:
1.Ген. директоротвечает за наличие эффективной фарм. системы менеджмента качества
2.директор по качеству - управление фарм системой качества
3.совет директоров : определяет политику в области качества , поддержка функционирования системы менеджмента
