

Отчет по лабораторной работе
Работа 1.2
УЧЕБНАЯ ПРАКТИКА ПО РАЗВИТИЮ ЦИФРОВЫХ КОМПЕТЕНЦИЙ
Вариант 1
Выполнил: студент гр. 2Д13
Чижова Анастасия
Васильевна
Бурдина Карина
Михайловна
Проверил: Липских Ольга
Ивановна
Томск, 2022г.
Цель работы: в рамках освоения ПО Origin провести построение зависимостей сигнала от внешних факторов и кривых кислотно-основного титрования и сделать выводы по полученным зависимостям.
Теоретическая часть
Титриметрический анализ – метод количественного химического анализа, основанный на точном измерении объема раствора известной концентрации (титранта), израсходованного на реакцию взаимодействия с определяемым веществом (А).
Титрование – это операция, когда титрант (B) добавляют к точно отмеренному объему анализируемого раствора небольшими порциями.
В основе титриметрического анализа могут лежать различные типы химических реакций:
реакции нейтрализации (кислотно-основное титрование);
окислительно-восстановительные реакции (окислительно-восстановительное титрование; например, перманганатометрия, иодометрия, хроматометрия, цериметрия, броматометрия, ванадатометрия);
реакции, протекающие с образованием малорастворимого соединения (осадительное титрование; например, аргентометрия, гексоцианоферратометрия, меркурометрия);
реакции, основанные на образовании прочных комплексных соединений (комплексонометрическое титрование, с комплексоном; например, ЭДТА).
Точка эквивалентности – это момент титрования, когда число эквивалентов добавляемого титранта эквивалентно или равно числу эквивалентов определяемого вещества в образце.
Титрант - это растор, имеющий точную концентрацию и вступающий во взаимодействие с определяемым веществом.
Титруемое вещество - это вещество, количество кототрого определяется непосредственно в процессе титрования.
Титрование раствором щелочи называется алкалиметрией, а титрование раствором кислоты — ацидиметрией.
При количественном определении кислот (алкалиметрия) — рабочим раствором является раствор щелочи NaOH или КОН, при количественном определении щелочи (ацидиметрия) рабочим раствором является раствор сильной кислоты (обычно НСl или H2SO4).
.
Конечная точка титрования определяется следующими способами:
визуальным — при помощи кислотно-основных индикаторов;
потенциометрически;
кондуктометрически;
спектрофотометрически.
Титриметрический метод анализа используется в следующих методиках:
ГОСТ 8.234-2013 12350-78. Стали легированные и высоколегированные. Методы определения хрома
ГОСТ 32186-2013 Битумы. Определение числа нейтрализации титрованием с цветным индикатором
ГОСТ 32333-2013 Нефтепродукты. Определение кислотного числа полумикрометодом титрования с цветным индикатором
ГОСТ Р 51468-99 Казеины. Метод определения свободной кислотности
ГОСТ 3624-92 Молоко и молочные продукты. Титриметрические методы определения кислотности
ГОСТ ISO 6495-1-2017 Корма для животных. Определение содержания водорастворимых хлоридов. Часть 1. Титриметрический метод
ГОСТ 32904-2014 (ISO 6490-1:1985) Корма, комбикорма. Определение содержания кальция титриметрическим методом
ГОСТ 30355.4-96 (ИСО 3704-76) Сера техническая. Определение кислотности. Титриметрический метод
РД 52.10.743-2010 Общая щелочность морской воды. Методика измерений титриметрическим методом
Кривые титрования представляют собой сигмоиды – нелинейные функции, имеющие «S»-образную форму.
Аналитический сигнал – это измерительный сигнал, регистрируемый в ходе анализа пробы вещества объекта анализа, содержащий количественную информацию о величине, функционально связанной с содержанием определяемого компонента (конкретных атомов, изотопов, ионов, молекул).
В данной работе будет рассмотрено влияние pH среды и температуры фонового раствора на токи электроокисления-электровосстановления (аналитический сигнал) в ходе вольтамперометрического анализа.
Ход работы
А. Построение кривой титрования
Импортировать данные из Excel, согласно варианту.
Построить график по импортированным данным. Для этого в меню Plot выбрать Scatter.
Провести аппроксимацию данных. Для этого открыть пункт меню Analysis и выбрать пункт Sigmoidal Fit. В открывшемся окне провести подбор функции, аппроксимирующей конкретные данные.
Построить график «S»-образной кривой. По своему усмотрению изменить цвет и форму маркеров, а также цвет полученной аппроксимирующей кривой.
Вставить в отчет график зависимости.
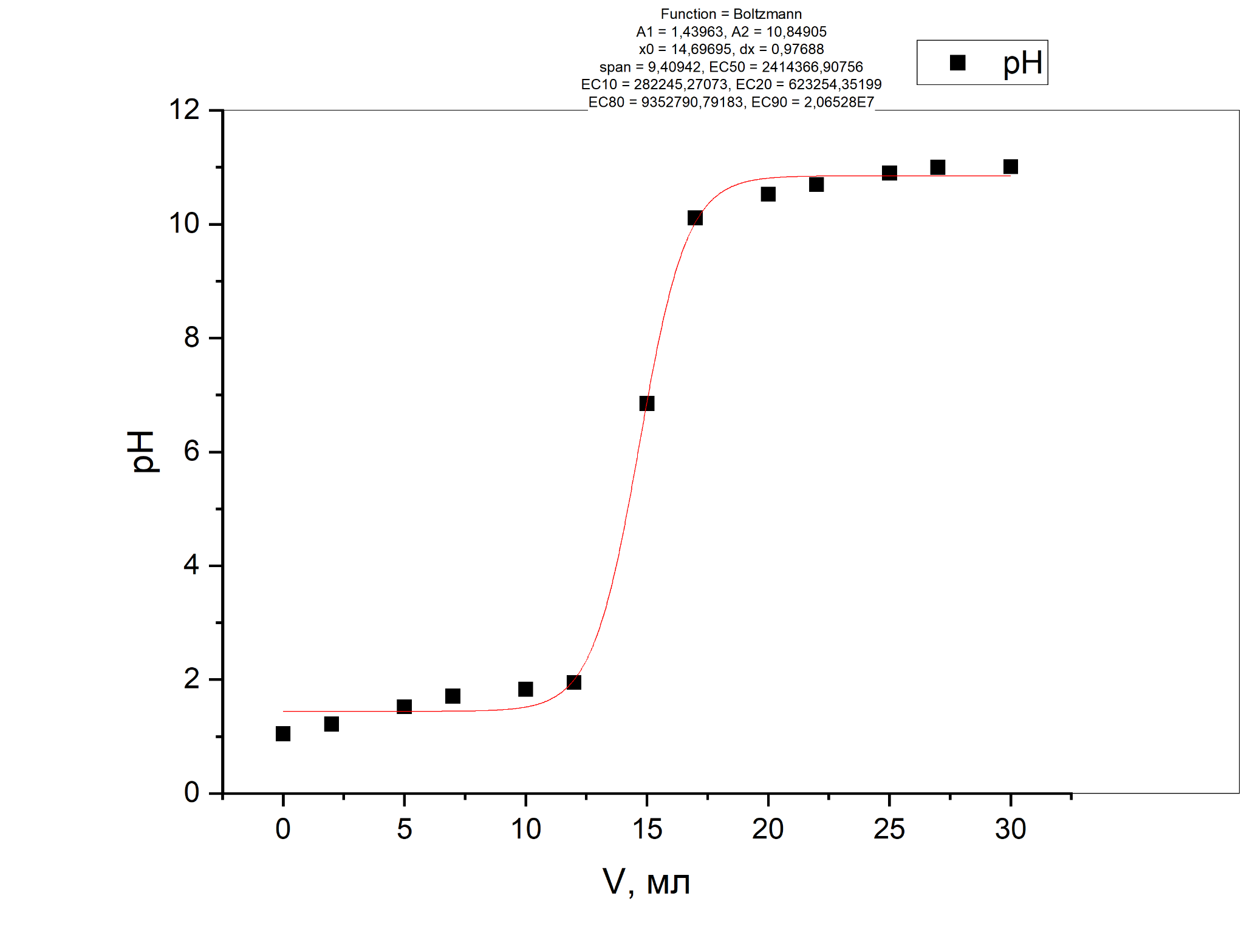
Сделать выводы по полученной зависимости (какой метод титрования использовался, что выступало в качестве титруемого вещества, а что в качестве титранта).
В. Построение графиков зависимостей аналитического сигнала от внешних факторов
В меню Column выбрать пункт Add column.
Импортировать данные из Excel, согласно варианту.
Построить график по импортированным данным. Для этого в меню Plot выбрать Multicurve plot и в данном пункте пункт Double Y curve.
Вставить полученные зависимости в отчет.
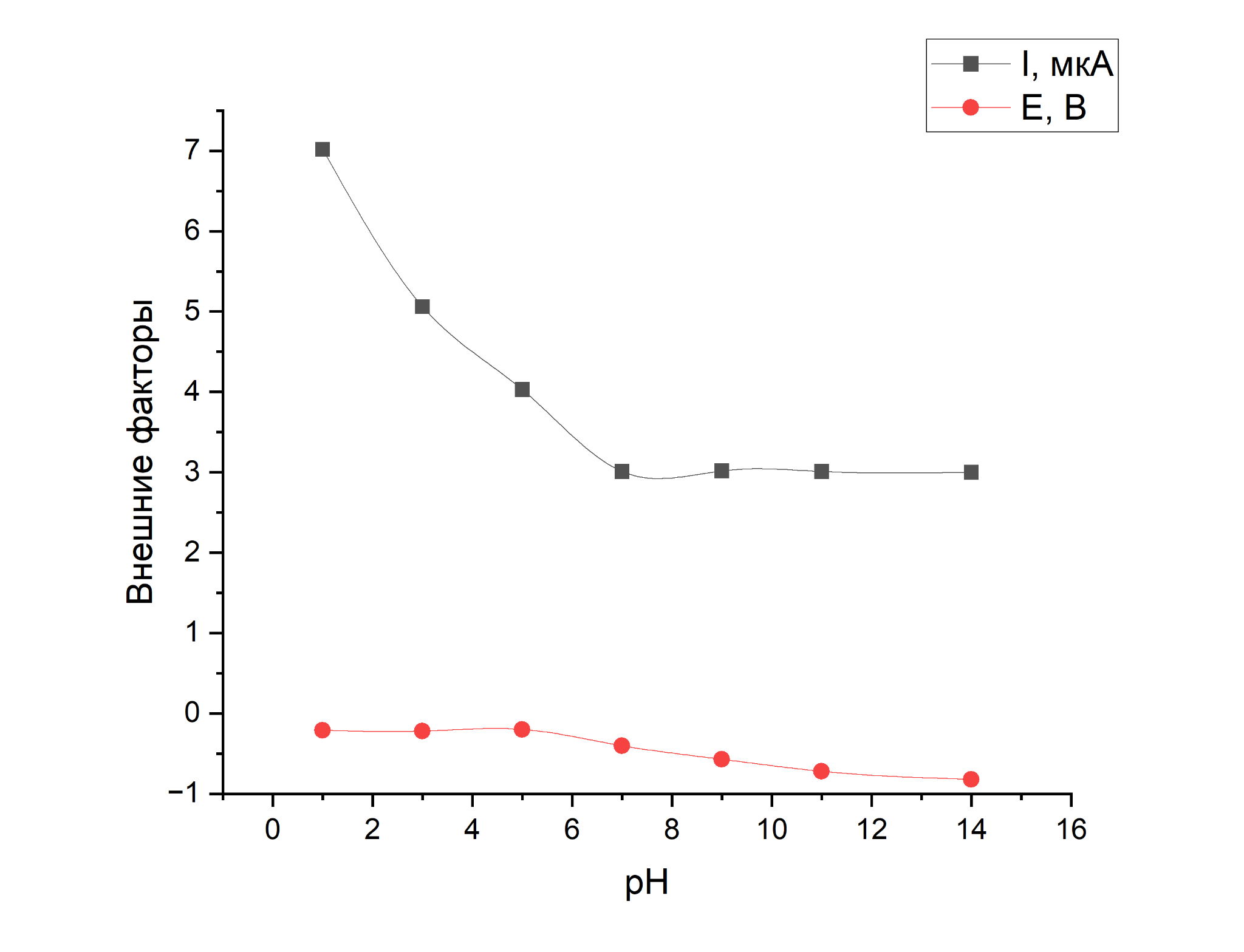
Сделать выводы по полученной зависимости (описать каким образом зависит получаемый сигнал от влияющих факторов, указать какие значения влияющих факторов соответствуют максимальному значению сигнала, а какие следует принять в качестве рабочих почему).
Выводы:
А. Построение кривой титрования:
Использовался метод «Кислотно-основного титрования» В виде титранта здесь выступало V, а в виде титрируемого вещества - pH
В. Построение графиков зависимостей аналитического сигнала от внешних факторов:
На величину сигнала влияют все факторы, от которых зависят значения рН: константа диссоциации титруемого вещества, концентрации титруемого вещества и титранта, температура, ионная сила. Максимальным значением сигнала является точка 14
В качестве рабочих точек сигналов можно принять все остальные точки.
