- •Итоговое занятие:
- •Вопросы для подготовки к письменному тест-контролю
- •Вопросы для подготовки к письменному контролю знаний:
- •Фаза первичной экзальтации
- •Фаза абсолютной рефрактерности
- •Фаза относительной рефрактерности
- •Фаза вторичной экзальтации (супернормальной возбудимости)
- •Фаза субнормальной возбудимости
- •Ситуационные задачи:
Фаза первичной экзальтации
Возникает в начале возбуждения, когда мембранный потенциал изменяется до критического уровня.
Соответствует латентному периоду потенциала действия (периоду медленной деполяризации). Характеризуется незначительным повышением возбудимости
Фаза абсолютной рефрактерности
Совпадает с восходящей частью пикового потенциала, когда мембранный потенциал изменяется от критического уровня до "спайка".
Соответствует периоду быстрой деполяризации. Характеризуется полной невозбудимостью мембраны (даже самый большой по силе раздражитель не вызывает возбуждение)
Фаза относительной рефрактерности
Совпадает с нисходящей частью пикового потенциала, когда мембранный потенциал изменяется от "спайка" к критическому уровню, оставаясь выше него. Соответствует периоду быстрой реполяризации. Характеризуется пониженной возбудимостью (возбудимость постепенно увеличивается, но остается ниже, чем в состоянии покоя).
В этот период может возникнуть новое возбуждение, но сила раздражителя должна превышать пороговую величину
Фаза вторичной экзальтации (супернормальной возбудимости)
Возникает в конце возбуждения, когда мембранный потенциал, минуя критический уровень, изменяется до величины потенциала покоя. Соответствует периоду следовой деполяризации. Характеризуется повышенной возбудимостью (мембрана может ответить новым возбуждением даже на действие подпорогового раздражителя)
Фаза субнормальной возбудимости
Возникает в конце возбуждения, когда изменение мембранного потенциала происходит ниже уровня потенциала покоя. Соответствует периоду следовой гиперполяризации.
характеризуется пониженной возбудимостью
9.
Закон "все или ничего": при допороговых раздражениях клетки ответной реакции не возникает, при пороговой силе раздражителя развивается максимальная ответная реакция, поэтому увеличение силы раздражения выше пороговой не сопровождается еѐ усилением. В соответствии с этим законом реагирует на раздражения одиночное нервное и мышечное волокно, сердечная мышца.
Закон силы: чем больше сила раздражителя, тем сильнее ответная реакция. Однако выраженность ответной реакции растет лишь до определенного максимума. Закону силы подчиняется целостная скелетная, гладкая мышца, так как они состоят из многочисленных мышечных клеток, имеющих различную возбудимость.
Закон длительности: чем сильнее раздражитель, тем меньшее время требуется для возникновения ответной реакции. Зависимость между пороговой силой и необходимой длительностью раздражения отражается кривой силы-длительности. По этой кривой можно определить ряд параметров возбудимости:
10.
При замыкании цепи постоянного электрического тока возбуждение возникает только под катодом, а при размыкании - только под анодом. Прохождение постоянного электрического тока через мембрану вызывает изменение мембранного потенциала покоя. Так, при замыкании цепи возле катода скапливается его "-" заряд, который уменьшает "+" заряд наружной поверхности мембраны. Разность потенциалов (между наружной и внутренней поверхностями мембраны) уменьшается, и мембранный потенциал изменяется в сторону уровня критической деполяризации, т.е. формируется деполяризация (возбудимость повышается). Достижение критического уровня приводит к возникновению пикового потенциала (потенциала действия) При замыкании цепи возле анода скапливается его "+" заряд. Он увеличивает "+" заряд мембраны и величину мембранного потенциала. Мембранный потенциал удаляется от критического уровня, превышает значение потенциала покоя и формирует гиперполяризацию (возбудимость уменьшается). При размыкании цепи, прекращение поступления дополнительного "+" заряда от анода приводит к уменьшению (восстановлению) заряда наружной поверхности мембраны. Мембранный потенциал, уменьшаясь, приближается к критическому уровню. Формируется деполяризация (возбудимость увеличивается). После достижения критического значения развивается пиковый потенциал (Поскольку размыкание происходит после замыкания, а, следовательно, на фоне гиперполяризации и пониженной возбудимости, то для возникновения ПД необходим раздражитель, превышающий по силе пороговый - это анодно-размыкательный эффект) При размыкании возле катода прекращается накопление его "-" заряда. Заряд наружной поверхности мембраны увеличивается (восстанавливается), мембранный потенциал, увеличиваясь, удаляется от критического уровня и возбуждение не возникает.
11.
Порог раздражения - наименьшая сила раздражителя способная вызвать распространяющийся потенциал действия
Хронаксия - наименьшее время действия на ткань постоянного электрического тока удвоенной пороговой силы, вызывающего возбуждение ткани
Лабильность - максимальное число импульсов, которое нервная клетка или функциональная структура может передать в единицу времени без искажений. (герцы)
Реобаза - минимальная сила постоянного тока, вызывающая ПД при неограниченно длительном действии
Полезное время – это время, в течение которого должен действовать раздражитель пороговой силы с тем чтобы вызвать возбуждение. Уменьшение времени действия раздражителя ниже критического значения приводит к тому, что раздражитель любой интенсивности не оказывает влияние.
12.
Нейро́н, или невро́н (от др.-греч. νεῦρον — волокно, нерв) — структурно-функциональная единица нервной системы. Нейрон — электрически возбудимая клетка, которая обрабатывает, хранит и передает информацию с помощью электрических и химических сигналов
Классификация:
1.В зависимости от нейромедиатора, используемого для передачи:
- холинергические – медиатор ацетилхолин (АХ);
- адренергические – норадреналин (НА);
- серотонинергические – серотонин (СТ);
- глицинергические – аминокислота глицин (ГЛИ);
- ГАМК-ергические – гамма-аминомасляная кислота (ГАМК);
- дофаминергические – дофамин (ДА);
- пептидергические – медиаторами являются нейропептиды (вещество Р, опиоидный пептид в-эндорфин и др.)
2. По форме (до 80 вариантов нейронов):
- звёздчатые
- пирамидальные,
- грушевидные
- веретеновидные
- паукообразные
- овальные
3. Функциональная (в зависимости от выполняемой функции и места в рефлекторной дуге):
- рецепторные (чувствительные, афферентные нейроны с помощью дендритов воспринимают воздействия внешней или внутренней среды, генерируют нервный импульс и передают его другим типам нейронов, встречаются только в спинальных ганглиях и чувствительных ядрах черепномозговых нервов)
- эффекторные (эфферентные нейроны передают возбуждение на рабочие органы, например, мышцы или железы, располагаются в передних рогах спинного мозга и вегетативных нервных ганглиях)
- вставочные (ассоциативные нейроны располагаются между рецепторными и эффекторными нейронами; по количеству их больше всего, особенно в ЦНС)
- секреторные (нейросекреторные клетки, специализированные нейроны, по своей функции напоминающие эндокринные клетки, синтезируют и выделяют в кровь нейрогормоны, расположены в гипоталамической области головного мозга, регулируют
4. По физиологической роли:
- возбуждающие
- тормозные
5. По количеству и характеру отростков:
- униполярные (имеющие один отросток)
- псевдоуниполярные (от тела отходит один отросток, который затем делится на 2 ветви)
- биполярные (2 отростка, один дендритоподобный, другой аксон)
- мультиполярные (имеют 1 аксон и много дендритов)
Физиологические функции:
1) возбудимость – способность приходить в состояние возбуждения в ответ на раздражение;
2) проводимость – способность передавать нервные возбуждение в виде потенциала действия от места раздражения по всей длине;
3) рефрактерность (устойчивость) – свойство временно резко снижать возбудимость в процессе возбуждения.
Нервная ткань имеет самый короткий рефрактерный период. Значение рефрактерности – предохранять ткань от перевозбуждения, осуществляет ответную реакцию на биологически значимый раздражитель;
4) лабильность – способность реагировать на раздражение с определенной скоростью. Лабильность характеризуется максимальным числом импульсов возбуждения за определенный период времени (1 с) в точном соответствии с ритмом наносимых раздражений.
13.
 На
рис. 31 показаны три состояния нейрона.
На
рис. 31 показаны три состояния нейрона.
Рис. 31. Три состояния нейрона. А. Нейрон в покое с ПП (-65 мВ);Б. Нейрон в состоянии возбуждения с ВПСП (-45 мВ) и с переходом его в ПД; В. Нейрон в заторможенном состоянии с ТПСП (-70 мВ) (Гайтон, 2008)
При возбуждении нейронов потребление кислорода возрастает. Источником энергии служит в основном глюкоза крови, собственных небольших запасов гликогена хватает лишь на 3-5 мин работы нейрона. Передача сигнала в химических синапсах ЦНС подобна таковой в нервно-мышечном синапсе, однако имеет ряд отличительных особенностей, основные из которых приводятся ниже.
Для возбуждения нейрона (возникновения ПД) необходимы потоки афферентных импульсов и их взаимодействие. Одна везикула (квант медиатора) содержит 1—10 тыс. молекул медиатора. Один ПД, пришедший в пресинаптическое окончание, обеспечивает выделение 200—300 квантов медиатора; при этом возникает небольшой ВПСП — около 0,05 мВ (миниатюрный ВПСП).
Необходимо учесть, что одновременно могут возникать не только возбуждающие, но и тормозные потенциалы. На нейронах одновременно присутствуют возбуждающие и тормозные синапсы (рис. 32).
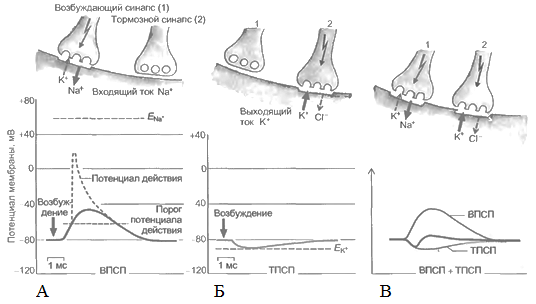
Рис. 32. А - Процессы освобождения медиатора, поступления ионов натрия и формирования ВПСП в возбуждающем синапсе и потенциала действия ПД; Б - Процесс формирования тормозного постсинаптического потенциала (ТПСП) в тормозном синапсе после поступления медиатора и выхода ионов калия или входа ионов хлора; В – Процесс суммации ТПСП и ВПСП на постсинаптической мембране нейрона. В верхней части рисунка показаны процессы, развивающиеся в синапсах (возбуждающий, тормозной), а в нижней – графическое отображение этих процессов (ВПСП,ТПСП и ПД) (Камкин, 2004)
Пороговый потенциал нейрона равен 5—10 мВ, поэтому ясно, что для возбуждения нейрона требуется некоторое множество импульсов. Выброс медиатора из нервного окончания обеспечивает входящий в деполяризованную терминаль Са2+, причем количество медиатора прямо пропорционально входу ионов Са2+, при этом четыре иона Са2+ обеспечивают выброс одного кванта медиатора. При поступлении импульсов к нейрону-мишени по входам в результате пространственной суммации ВПСП возникает ПД нейрона-мишени.
ВПСП возникает вследствие суммарного тока в клетку и из клетки через ионные каналы различных ионов согласно электрохимическому градиенту. Поступивший в пресинаптическое окончание Са2+ удаляется в среду с помощью Са-насоса.
Прекращение действия выделившегося в синаптическую щель медиатора осуществляется частично посредством обратного захвата его пресинаптическим окончанием, частично — с помощью разрушения специальными ферментами. Например, норадреналин расщепляется МАО и катехолметилтрансферазой, ацетилхолин гидролизуется ацетилхолинтрансферазой, имеющейся в синаптической щели и встроенной в постсинаптическую мембрану. Прекращение действия избытков медиатора на постсинаптическую мембрану предотвращает десенситизацию — снижение чувствительности постсинаптической мембраны к действующему медиатору.
В возникновении ПД в нейронах принимают участие ионы Сa2+, ток которых в клетку более медленный, чем ток Na+, играющий главную роль в формировании ПД-нейронов. В частности, в дендритах клеток Пуркинье мозжечка выявлены не только быстрые натриевые потенциалы, но и медленные кальциевые. В телах некоторых нервных клеток потенциал действия создается преимущественно за счет Са2+.
Место возникновения ВПСП, вызывающих ПД нейрона, — тело нейрона, поскольку постсинаптические мембраны этих синапсов располагаются в непосредственной близости от аксонного холмика, где начинается развитие ПД. Близость ВПСП, возникающих в теле нейрона, к аксонному холмику обеспечивает их участие в механизмах генерации ПД. Однако подавляющее большинство синапсов (в частности, в коре большого мозга, согласно расчетам, 98%) находится на дендритах. Площадь мембраны тела нейронов занята синапсами на 40%, дендритов — на 75%. Синапсов в коре большого мозга в 40 тыс. раз больше, чем самих нейронов.
Место возникновения ПД нейрона. Формирование ПД начинается на мембране аксонного холмика (генераторный пункт нейрона). Синапсы на нем отсутствуют, возбудимость мембраны аксонного холмика в 3—4 раза превосходит возбудимость мембраны тела нейрона, что объясняется более высокой (примерно в 7 раз) концентрацией Na- каналов на аксонном холмике (на нем отсутствует миелиновая оболочка). ВПСП, возникающие в любых участках сомы нейрона суммируются, их суммарное электрическое поле достигает аксонного холмика и вызывает его деполяризацию до КП, в результате чего начинает развиваться ПД на аксонном холмике. Это связано с тем, что постоянная длины мембраны тела нейрона (расстояние, на котором исходная амплитуда ВПСП уменьшается на 37%) составляет 1-2 мм, а диаметр тела нейрона — всего лишь 10-80 мкм. Поэтому электрическое поле начального возбуждения аксонного холмика обеспечивает деполяризацию тела нейрона до КП, в результате чего возникает ПД нейрона, который проводится по аксону к другой клетке.
На восходящей части ПД нейрона регистрируется перегиб на уровне 30— 40 мВ (задержка в развитии ПД), вследствие того, что возбудимость мембраны тела нейрона в 3—4 раза ниже возбудимости мембраны аксонного холмика, что также является подтверждением описанного механизма формирования ПД нейрона (рис. 33).
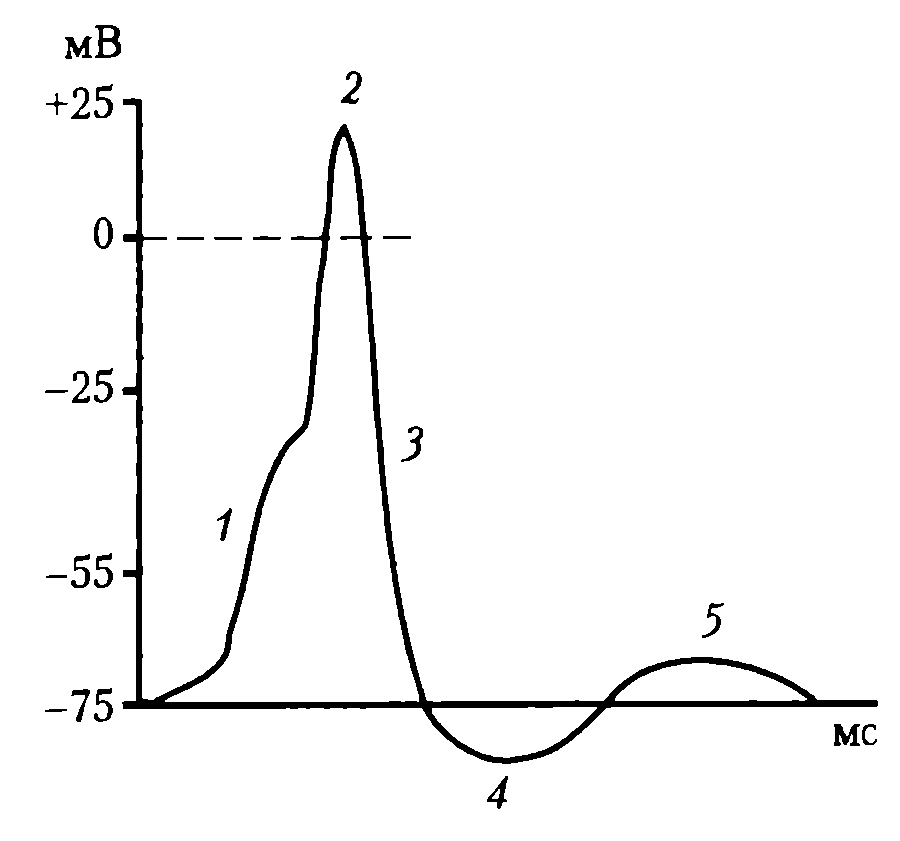 Рис.
33. Типичный ПД нейронов ЦНС: 1 –
деполяризация; 2 – инверсия; 3 –
реполяризация; 4 – следовая гиперполяризация;
5 – следовая деполяризация
Рис.
33. Типичный ПД нейронов ЦНС: 1 –
деполяризация; 2 – инверсия; 3 –
реполяризация; 4 – следовая гиперполяризация;
5 – следовая деполяризация
Таким образом, ПД нейрона — это единый одновременный процесс возбуждения аксонного холмика и тела нейрона.
Роль дендритов в возникновении возбуждения нейрона. Дендритные синапсы называют модуляторами. Это связано с тем, что они удалены на значительное расстояние от генераторного пункта нейрона — аксонного холмика. Поэтому суммарное электрическое поле их ВПСП не может вызвать достаточную деполяризацию аксонного холмика и обеспечить возникновение ПД, а определяет лишь возбудимость нейрона.
14.
Миелиновые волокна:
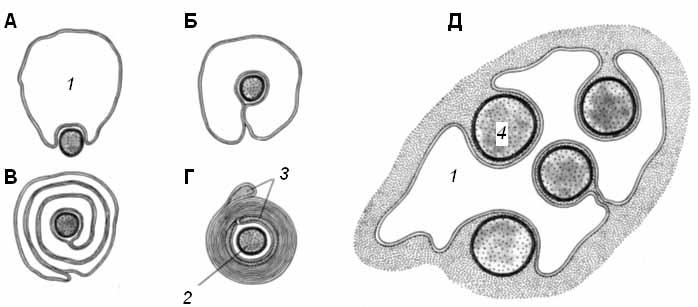
Часть нервных волокон в ходе эмбриогенеза подвергается миелинизации: леммоциты ( шванновские клетки ) сначала прикасаются к аксону, а затем окутывают его (рис. 1, А, Б). Мембрана леммоцита наматывается на аксон наподобие рулета, образуя многослойную спираль (миелиновую оболочку) (рис. 1, В, Г). Миелиновая оболочка не является непрерывной – по всей длине нервного волокна на равном расстоянии друг от друга в ней имеются небольшие перерывы (перехваты Ранвье). В области перехватов аксон лишен миелиновой оболочки.
|
Рис. 1. Формирование миелиновой оболочки вокруг аксона на разных стадиях его развития (А – Г); соотношение леммоцита и безмиелиновых волокон (Д) (по Судакову, 2000) 1 – леммоцит, 2 – миелиновое волокно, 3 – миелиновая оболочка, 4 – безмиелиновое волокно |
Безмиелиновые волокна:
Миелинизация других волокон заканчивается на ранних стадиях эмбрионального развития. В леммоцит погружается один или несколько аксонов; он полностью или частично окружает их, но не образует многослойной миелиновой оболочки (рис. 1, Д).
Механизм проведения возбуждения по безмиелиновым нервным волокнам:
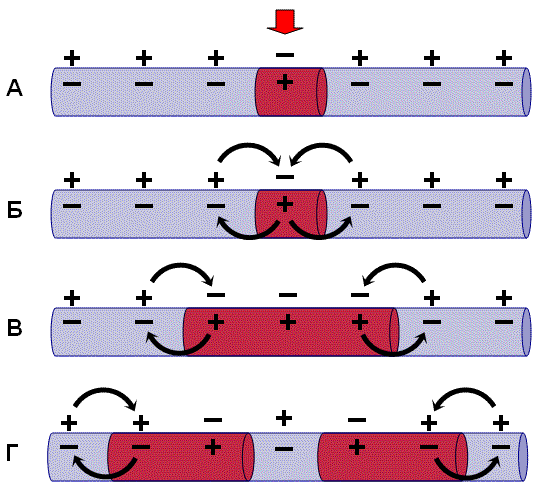
В состоянии покоя вся внутренняя поверхность мембраны нервного волокна несет отрицательный заряд, а наружная сторона мембраны – положительный. Электрический ток между внутренней и наружной стороной мембраны не протекает, так как липидная мембрана имеет высокое электрическое сопротивление.
Во время развития потенциала действия в возбужденном участке мембраны происходит реверсия заряда (рис. 2, А). На границе возбужденного и невозбужденного участка начинает протекать электрический ток (рис. 2, Б). Электрический ток раздражает ближайший участок мембраны и приводит его в состояние возбуждения (рис. 2, В), в то время как ранее возбужденные участки возвращаются в состояние покоя (рис. 2, Г). Таким образом, волна возбуждения охватывает все новые участки мембраны нервного волокна.
|
Рис. 2. Механизм распространения возбуждения по безмиелиновому нервному волокну. Объяснения – в тексте |
Механизм проведения возбуждения по миелиновым нервным волокнам:
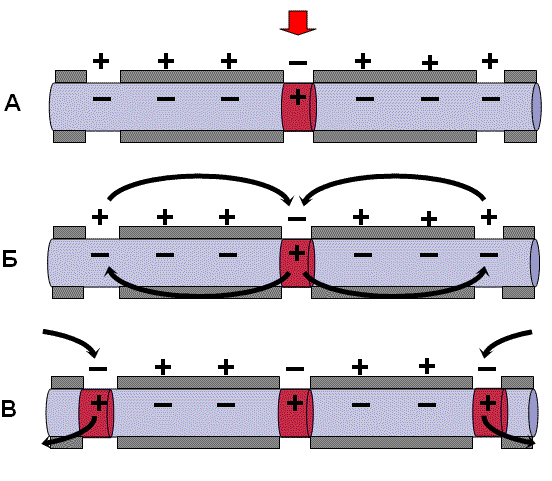
В миелинизированном нервном волокне участки мембраны, покрытые миелиновой оболочкой, являются невозбудимыми; возбуждение может возникать только в участках мембраны, расположенных в области перехватов Ранвье.
При развитии ПД в одном из перехватов Ранвье происходит реверсия заряда мембраны (рис. 3, А). Между электроотрицательными и электроположительными участками мембраны возникает электрический ток, который раздражает соседние участки мембраны (рис. 3, Б). Однако в состояние возбуждения может перейти только участок мембраны в области следующего перехвата Ранвье (рис. 3, В). Таким образом, возбуждение распространяется по мембране скачкообразно (сальтаторно) от одного перехвата Ранвье к другому.
|
Рис. 3. Механизм распространения возбуждения по миелиновому нервному волокну. Объяснения – в тексте |
15.
Нервные волокна (neurofibrae) – это отростки нервных клеток, окруженные оболочками из нейроглиальных клеток.
Существуют различные классификации нервных волокон.
По наличию (или отсутствию) миелиновой оболочки нервные волокна делят на миелиновые и безмиелиновые.
Классификация нервных волокон по Эрлангеру – Гассеру основана на исследовании составного потенциала действия смешанного периферического нерва (например, седалищного). После электрической стимуляции такого нерва регистрируется целый спектр потенциалов действия, отражающий наличие в нерве волокон с разными скоростями проведения импульса. Согласно этой классификации выделяют три основных типа волокон – А, В, С, соответствующие трем волнам составного потенциала действия. Волокна типа А подразделяются на 4 подтипа – α, β, γ, δ. Данная классификация учитывает как чувствительные, так и двигательные волокна.
Классификация нервных волокон по Ллойду – Ханту учитывает диаметр волокна и скорость проведения импульса, но применяется только для чувствительных волокон. Согласно этой классификации выделяют четыре класса волокон – I,II,III,IV. ВолокнаIкласса подразделяют на 2 группы – а иb. Эти классификации не противоречат друг другу и представлены в сводной таблице.
Тип волокна |
Тип волокна (только чувствительные) |
Диаметр волокна (мкм) |
Скорость (м/с) |
Функция, тип обслуживаемого рецептора |
Чувствительные нервные волокна |
||||
Аα |
Ia, Ib |
13 – 20 |
80 – 120 |
Первичные афферентные волокна мышечных веретен и от сухожильных органов Гольджи. |
Аβ |
II |
6 – 12 |
35 – 75 |
Вторичные афферентнфе волокна мышечных веретен, кожные механорецепторы |
Аδ |
III |
1 – 5 |
5 – 30 |
Кожные механорецепторы, терморецепторы, ноцицепторы |
С |
IV |
0,2 – 1,5 |
0,5 – 2 |
Кожные механорецепторы, терморецепторы, ноцицепторы (немиелинизированные волокна) |
Двигательные нервные волокна |
||||
Аα |
− |
12 – 20 |
72 – 120 |
Экстрафузальные волокна скелетных мышц |
Аγ |
− |
2 – 8 |
12 – 48 |
Интрафузальные мышечные волокна |
В |
− |
1 – 3 |
6 – 18 |
Преганглионарные вегетативные волокна |
С |
− |
0,2 – 2 |
0,5 – 2 |
Постганглионарные вегетативгые (немиелинизированные волокна) |
16.
Закон анатомо-физиологической целостности: проведение импульсов по нервному волокну возможно лишь в том случае, если не нарушена его целостность. При нарушении физиологических свойств нервного волокна путем охлаждения, применения различных наркотических средств, сдавливания, а также порезами и повреждениями анатомической целостности проведение нервного импульса по нему будет невозможно.
17.
Явление парабиоза открыто русским физиологом Н.Е.Введенским в 1901 г. при изучении возбудимости нервно-мышечного препарата. Состояние парабиоза могут вызвать различные воздействия – сверхчастые, сверхсильные стимулы, яды, лекарства и другие воздействия как в норме, так и при патологии. Н. Е. Введенский обнаружил, что если участок нерва подвергнуть альтерации (т. е. воздействию повреждающего агента), то лабильность такого участка резко снижается. Восстановление исходного состояния нервного волокна после каждого потенциала действия в поврежденном участке происходит медленно. При действии на этот участок частых раздражителей он не в состоянии воспроизвести заданный ритм раздражения, и поэтому проведение импульсов блокируется. Такое состояние пониженной лабильности и было названо Н. Е. Введенским парабиозом. Состояние парабиоза возбудимой ткани возникает под влиянием сильных раздражителей и характеризуется фазными нарушениями проводимости и возбудимости. Работы Н.Е.Введенского по парабиозу сыграли важную роль в развитии нейрофизиологии и клинической медицины, показав единство процессов возбуждения, торможения и покоя, изменили господствовавший в физиологии закон силовых отношений, согласно которому реакция тем больше, чем сильнее действующий раздражитель.
Выделяют 3 фазы
1) Примум (уравнительная - по И.П. Павлову; провизорная, трансформирующая - по Н.Е.Введенском): характеризуется снижением возбудимости и повышением лабильности. происходит уравнивание величины ответной реакции на частые и редкие раздражители. В нормальных условиях функционирования нервного волокна величина ответной реакции иннервируемых им мышечных волокон подчиняется закону силы: на редкие раздражители ответная реакция меньше, а на частые раздражители—больше. При действии парабиотического агента и при редком ритме раздражении (например, 25 Гц) все импульсы возбуждения проводятся через парабиотический участок, так как возбудимость после предыдущего импульса успевает восстановиться. При высоком ритме раздражении (100Гц) последующие импульсы могут поступать в тот момент, когда нервное волокно еще находится в состоянии относительной рефрактерности, вызванной предыдущим потенциалом действия. Поэтому часть импульсов не проводится. Если проводится только каждое четвертое возбуждение (т.е. 25 импульсов из 100), то амплитуда ответной реакции становится такой же, как на редкие раздражители (25Гц)—происходит уравнивание ответной реакции.
2) Оптимум (парадоксальная фаза): возбудимость достигает максимума, лабильность начинает снижаться. В третью фазу (пессимум) возбудимость и лабильность снижаются параллельно и развивается 3 стадии парабиоза. Характеризуется извращенным реагированием – сильные раздражения вызывают меньший ответ, чем умеренные. Происходит дальнейшее снижение лабильности. При этом на редкие и частые раздражители ответная реакция возникает, но на частые раздражители она значительно меньше, т. к. частые раздражители еще больше снижают лабильность, удлиняя фазу абсолютной рефрактерности. Следовательно, наблюдается парадокс— на редкие раздражители ответная реакция больше, чем на частые.
3) Тормозная фаза: лабильность снижается до такой степени, что и редкие, и частые раздражители не вызывают ответной реакции. При этом мембрана нервного волокна деполяризована и не переходит в стадию реполяризации, т. е. не восстанавливается ее исходное состояние. Ни сильные, ни умеренные раздражения не вызывают видимой реакции, в ткани развивается торможение. Парабиоз— явление обратимое. Если парабиотическое вещество действует недолго, то после прекращения его действия нерв выходит из состояния парабиоза через те же фазы, но в обратной последовательности. Однако, при действии сильных раздражителей за тормозной стадией может наступить полная потеря возбудимости и проводимости, а в дальнейшем – гибель ткани.
Медицинское значение: явление парабиоза лежит в основе медикаментозного локального обезболивания. Влияние анестезирующих веществ вязано с понижением лабильности и нарушением механизма проведения возбуждения по нервным волокнам.
18.
Закон двустороннего проведения возбуждения: нервное волокно проводит нервные импульсы в двух направлениях – центростремительно и центробежно. В живом организме возбуждение проводится только в одном направлении. Двусторонняя проводимость нервного волокна ограничена в организме местом возникновения импульса и клапанным свойством синапсов, которое заключается в возможности проведения возбуждения только в одном направлении.
19.
Закон изолированного проведения возбуждения:существует ряд особенностей распространения возбуждения в периферических, мякотных и безмякотных нервных волокнах. В периферических нервных волокнах возбуждение передается только вдоль нервного волокна, но не передается на соседние, которые находятся в одном и том же нервном стволе. В мякотных нервных волокнах роль изолятора выполняет миелиновая оболочка. За счет миелина увеличивается удельное сопротивление и происходит уменьшение электрической емкости оболочки. В безмякотных нервных волокнах возбуждение передается изолированно. Это объясняется тем, что сопротивление жидкости, которая заполняет межклеточные щели, значительно ниже сопротивления мембраны нервных волокон. Поэтому ток, возникающий между деполяризованным участком и неполяризованным, проходит по межклеточным щелям и не заходит при этом в соседние нервные волокна.
20.
Физиологические свойства поперечнополосатых мышц:
- возбудимость (ниже, чем в нервном волокне, что объясняется низкой величиной мембранного потенциала)
- низкая проводимость, порядка 10–13 м/с
- рефрактерность (занимает по времени больший отрезок, чем у нервного волокна)
- лабильность
- сократимость (способность укорачиваться или развивать напряжение)
Физиологические функции поперечнополосатых мышц:
- двигательная (динамическая и статическая)
- обеспечения дыхания
- мимическая
- рецепторная
- депонирующая
- терморегуляторная
21.
При световой микроскопии было замечено, что в момент сокращения ширина А-диска не уменьшается, а Iдиски и Н-зоны саркомеров суживаются. При электронной, микроскопии было установлено, что длина нитей актина и миозина в момент соскращения не изменяется. Поэтому Хаксли и Хэнсон разработали теорию скольжения нитей. Согласно этой теории, мышца укорачивается в результате движения тонких актиновых нитей в промежутки между миозиновыми. Это приводит к укорочению каждого саркомера, образующего миофибриллы. Скольжение же нитей обусловлено тем, что при переходе в активное состояние головки отростков миозина связываются с центрами актиновых нитей и вызывают их движение относительно себя (гребковые движения). Но это последний этап всего сократительного механизма.
Сокращение начинается с того, что в области концевой пластинки двигательного нерва возникает ПД. Он с большой скоростью распространяется по сарколемме и переходит с неѐ по, системе поперечных трубочек СР, на продольные трубочки и цистерны. Возникает деполяризация мембраны цистерн и из них в саркоплазму высвобождаются ионы кальция. На нитях актина расположены молекулы еще двух белков – тропонина и тропомиозина. При низкой (менее 10-8 моль) концентрации кальция, т.е. в состоянии покоя, тропомиозин блокирует присоединение мостиков миозина к нитям актина. Когда ионы кальция начинают выходить из СР, молекула тропонина изменяет свою форму таким образом, что освобождает активные центры актина от тропомиозина. К этим центрам присоединяются головки миозина и начинается скольжение за счет ритмического прикрепления и разъединения поперечных мостиков с нитями актина. При этом головки ритмически продвигаются по нитям актина к Z-мембранам. Для полного сокращения мышцы необходимо 50 таких циклов.
Передача сигнала от возбужденной мембраны к миофибриллам называется электромеханическим сопряжением. Когда генерация ПД прекращается и мембранный потенциал возвращается к исходному уровню, начинает работать Са-насос (фермент Са-АТФаза). Ионы кальция вновь закачиваются в цистерны саркоплазматического ретикулума и их концентрация падает ниже 10-8 моль. Молекулы тропонина приобретают исходную форму и тропомиозин вновь начинает блокировать активные центры актина. Головки миозина отсоединяются от них, и мышца за счет эластичности приходит в исходное расслабленное состояние.
22.
При нанесении на двигательный нерв или мышцу одиночного порогового или сверхпорогового раздражения, возникает одиночное сокращение. При его графической регистрации, на полученной кривой можно выделить три последовательных периода:
1) Латентный период: это время от момента нанесения раздражения до начала сокращения. Его длительность около 1-2 мс. Во время латентного периода генерируется и распространяется ПД, происходит высвобождение кальция из СР, взаимодействие актина с миозином и т.д.
2) Период укорочения: в зависимости от типа мышцы (быстрая или медленная) его продолжительность от 10 до 100 мсек.,
3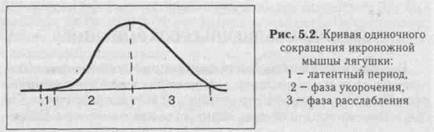 )
Период
расслаблени:
его длительность несколько больше, чем
укорочения (0,05-0.06 сек.)
)
Период
расслаблени:
его длительность несколько больше, чем
укорочения (0,05-0.06 сек.)
В режиме одиночного сокращения мышца способна работать длительное время без утомления, но его сила незначительна. Поэтому в организме такие сокращения встречаются редко, например, так могут сокращаться быстрые глазодвигательные мышцы, мышцы сгибателей пальцев. Чаще одиночные сокращения суммируются.
Суммация – это сложение двух последовательных сокращений при нанесении на нее двух пороговых или сверхпороговых раздражений, интервал между которыми меньше длительности одиночного сокращения, но больше продолжительности рефракторного периода.
Виды:
- неполная суммация: возникает в том случае, если повторное раздражение наносится на мышцу, когда она уже начала расслабляться
- полная возникает тогда, когда повторное раздражение действует на мышцу до начала периода расслабления, т.е. в конце периода укорочения.
Амплитуда сокращения при полной суммации выше, чем неполной. Если интервал между двумя раздражениями еще больше уменьшить, например, нанести второе в середине периода укорочения, то суммации не будет, потому что мышца находится в состоянии рефрактерности.
23.
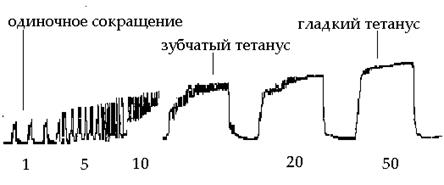
Тетанус – это длительное сокращение мышцы, возникающее в результате суммации нескольких одиночных сокращений, развивающихся при нанесении на нее ряда последовательных раздражений.
Формы
- зубчатый тетанус: наблюдается в том случае, если каждое последующее раздражение действует на мышцу, когда она уже начала расслабляться. Т.е. наблюдается неполная суммация.
- гладкий тетанус: возникает тогда, когда каждое последующее раздражение наносится в конце периода укорочения. Т.е. имеет место полная суммация отдельных сокращений. Амплитуда гладкого тетануса больше, чем зубчатого. В норме мышцы человека сокращаются в режиме гладкого тетануса. Зубчатый возникает при патологии, например, тремор рук при алкогольной интоксикации и болезни Паркинсона.
24.
Различают следующие режимы мышечного сокращения:
Изотонические сокращения. Длина мышцы уменьшается, а тонус не изменяется. В двигательных функциях организма не участвуют.
Изометрическое сокращения. Длина мышцы не изменяется, но тонус возрастает. Лежат в основе статической работы, например при поддержании позы тела.
Ауксотонические сокращения. Изменяются и длина, и тонус мышцы. С помощью их происходит передвижение тела и другие двигательные акты.
Максимальная сила мышц – это величина максимального напряжения, которое может развить мышца. Она зависит от строения мышцы, ее функционального состояния, исходной длины, а также пола, возраста, степени тренированности человека.
В зависимости от строения, выделяют мышцы с параллельными волокнами (например портняжная), веретенообразные (двуглавая мышца плеча), перистые (икроножная). У этих типов мышц различная площадь поперечного физиологического сечения – это сумма площадей поперечного сечения всех мышечных волокон, образующих мышцу. Наибольшая площадь поперечного физиологического сечения, а, следовательно, и сила, у перистых мышц. Наименьшая у мышц с параллельным расположением волокон.
При умеренном растяжение мышцы сила ее сокращения возрастает, но при перерастяжении уменьшается. При умеренном нагревании сила также увеличивается, а при охлаждении снижается. Сила мышц снижается при утомлении, нарушениях метаболизма и т.д. Максимальная сила различных мышечных групп определяется динамометрами (кистевым, становым и т.д.).
Для сравнения силы различных мышц определяют их удельную или абсолютную силу. Она равна максимальной силе, деленной на кв. см. площади поперечного сечения мышцы. Удельная сила икроножной мышцы человека составляет 62 кг/см2, трехглавой – 16,8 кг/см2, жевательных – 10 кг/см2.
Работу мышц делят на динамическую и статическую Динамическая выполняется при перемещении груза. При динамической работе изменяется длина мышцы и ее напряжение. Следовательно мышца работает в ауксотоническом режиме. При статической работе перемещения груза не происходит, т.е. мышца работает в изометрическом режиме.
Динамическая работа равна произведению веса груза на высоту его подъема или величину укорочения мышцы (А=М·h). Работа измеряется в кг·м, джоулях. Зависимость величины работы от нагрузки подчиняется закону средних нагрузок. При увеличении нагрузки работа мышц первоначально растет. При средних нагрузках она становится максимальной. Если увеличение нагрузки продолжается, то работа снижается. Такое же влияние на величину работы оказывает ее ритм. Максимальная работа мышцы осуществляется при среднем ритме. Особое значение в расчете величины рабочей нагрузки имеет определение мощности мышцы - это работа выполняемая в единицу времени (Р=А·Т). Единица измерения – ватт (Вт).
Динамометрия – методика измерения силы отдельной мышцы или группы мышц при помощи специальных приборов – динамометров. Показатель силы = сила мышц / масса тела * 100%
25.
Физиологические свойства гладких мышц:
- возбудимость (ниже, чем в нервном волокне, что объясняется низкой величиной мембранного потенциала)
- низкая проводимость, порядка 10–13 м/с
- рефрактерность (занимает по времени больший отрезок, чем у нервного волокна)
- лабильность
- сократимость (способность укорачиваться или развивать напряжение)
- нестабильный мембранный потенциал, который поддерживает мышцы в состоянии постоянного частичного сокращения – тонуса
- самопроизвольную автоматическую активность
- сокращение в ответ на растяжение
- пластичность (уменьшение растяжения при увеличении растяжения)
- высокую чувствительность к химическим веществам
Физиологические функции гладких мышц:
- поддержание давления в полых органах
- регуляция давления в кровеносных сосудах
- опорожнение полых органов и продвижение их содержимого
26.
Теория хемомеханического этапа мышечного сокращения была разработана О. Хаксли в 1954 г. и дополнена в 1963 г. М. Девисом. Основные положения этой теории:
1) ионы Ca запускают механизм мышечного сокращения;
2) за счет ионов Ca происходит скольжение тонких актиновых нитей по отношению к миозиновым.
В покое, когда ионов Ca мало, скольжения не происходит, потому что этому препятствуют молекулы тропонина и отрицательно заряды АТФ, АТФ-азы и АДФ. Повышенная концентрация ионов Ca происходит за счет поступления его из межфибриллярного пространства. При этом происходит ряд реакций с участием ионов Ca:
1) Ca2+ реагирует с трипонином;
2) Ca2+ активирует АТФ-азу;
3) Ca2+ снимает заряды с АДФ, АТФ, АТФ-азы.
Взаимодействие ионов Ca с тропонином приводит к изменению расположения последнего на актиновой нити, открываются активные центры тонкой протофибриллы. За счет них формируются поперечные мостики между актином и миозином, которые перемещают актиновую нить в промежутки между миозиновой нитью. При перемещении актиновой нити относительно миозиновой происходит сокращение мышечной ткани.
Итак, главную роль в механизме мышечного сокращения играют белок тропонин, который закрывает активные центры тонкой протофибриллы и ионы Ca.
27.
Синапс — это структурно-функциональное образование, обеспечивающее переход возбуждения или торможения с окончания нервного волокна на иннервирующую клетку.
Cтруктура синапса:
1) пресинаптическая мембрана (электрогенная мембрана в терминале аксона, образует синапс на мышечной клетке); 2) постсинаптическая мембрана (электрогенная мембрана иннервируемой клетки, на которой образован синапс);
3) синаптическая щель (пространство между пресинаптической и постсинаптической мембраной, заполнена жидкостью, которая по составу напоминает плазму крови).
Классификации:
По локализации:
- центральные синапсы;
- периферические синапсы.
По типу соединения с нейроном:
- аксосоматический, образованный аксоном одного нейрона и телом другого нейрона;
- аксодендритный, образованный аксоном одного нейрона и дендритом другого;
- аксоаксональный (аксон первого нейрона образует синапс на аксоне второго нейрона);
- дендродентритный (дендрит первого нейрона образует синапс на дендрите второго нейрона).
По функции:
- возбуждающие синапсы;
- тормозящие синапсы.
По механизму передачи возбуждения:
- химические;
- электрические.
По нейромедиатору (для химических):
- холинэргические (передача возбуждения при помощи ацетилхолина);
- адренэргические. (передача возбуждения при помощи трех катехоламинов);
- дофаминэргические (передача возбуждения при помощи дофамина);
- гистаминэргические (передача возбуждения при помощи гистамина);
- ГАМК-эргические (передача возбуждения при помощи гаммааминомасляной кислоты, т. е. развивается процесс торможения).
По строению и локализации (для периферических синапсов):
- мионевральный (нервно-мышечный), образованный аксоном мотонейрона и мышечной клеткой;
- нервно-эпителиальный, образованный аксоном нейрона и секреторной клеткой.
Физиологические свойства:
- клапанное свойство синапсов, т. е. способность передавать возбуждение только в одном направлении с пресинаптической мембраны на постсинаптическую;
- свойство синаптической задержки, связанное с тем, что скорость передачи возбуждения снижается;
- свойство потенциации (каждый последующий импульс будет проводиться с меньшей постсинаптической задержкой). Это связано с тем, что на пресинаптической и постсинаптической мембране остается медиатор от проведения предыдущего импульса;
- низкая лабильность синапса (100—150 имульсов в секунду).
28.
Медиатор, находящийся в пузырьках, выделяется в синаптическую щель с помощью экзоцитоза (пузырьки подходят к мембране, сливаются с ней и разрываются, выпуская медиатор). Его выделение происходит небольшими порциями – квантами. Каждый квант содержит от 1'000 до 10'000 молекул нейромедиатора. Небольшое количество квантов выходит из окончания и в состоянии покоя. Когда нервный импульс, т.е. ПД, достигает пресинаптического окончания, происходит деполяризация его пресинаптической мембраны.
Открываются ее кальциевые каналы и ионы кальция входят в синаптическую бляшку. Начинается выделение большого количества квантов нейромедиатора. Молекулы медиатора диффундируют через синаптическую щель к постсинаптической мембране и взаимодействуют с еѐ хеморецепторами. В результате образования комплексов медиатор-рецептор, в субсинаптической мембране начинается синтез так называемых вторичных посредников (в частности, цАМФ). Эти посредники активируют ионные каналы постсинаптической мембраны. Поэтому такие каналы называют хемозависимыми или рецепторуправляемыми. Т.е. они открываются при действии ФАВ на хеморецепторы. В результате открывания каналов изменяется потенциал субсинаптической мембраны. Такое изменение называется постсинаптическим потенциалом.
В ЦНС возбуждающими являются холин-, адрен-, дофамин-, серотонинергические синапсы и некоторые другие. При взаимодействии их медиаторов с соответствующими рецепторами, открываются хемозависимые натриевые каналы. Ионы натрия входят в клетку через субсинаптическую мембрану. Происходит ее местная или распространяющаяся деполяризация. Эта деполяризация называется возбуждающим постсинаптическим потенциалом (ВПСП).
Тормозными являются глицин- и ГАМК-ергические синапсы. При связывании медиатора с хеморецепторами, активируются калиевые или хлорные хемозависимые каналы. В результате ионы калия выходят из клетки через мембрану. Ионы хлора входят через нее. Возникает только местная гиперполяризация субсинаптической мембраны. Она называется тормозным постсинаптическим потенциалом (ТПСП).
Величина ВПСП и ТПСП определяется количеством квантов медиатора, выделившихся из терминали, а, следовательно, частотой нервных импульсов. Т.е. синаптическая передача не подчиняется закону "все или ничего". Если количество выделившегося возбуждающего медиатора достаточно велико, то в субсинаптической мембране может генерироваться распространяющийся ПД. ТПСП, независимо от количества медиатора не распространяется за пределы субсинаптической мембранеы.
После прекращения поступления нервных импульсов, выделившийся медиатор удаляется из синаптической щели тремя путями:
Разрушается специальными ферментами, фиксированными на поверхности субсинаптической мембраны. В холинергических синапсах это ацетилхолинэстераза (АХЭ). В адренергических, дофаминергических, серотонинергических – моноаминоксидаза (МАО) и катехол-О-метилтрансфераза (КОМТ).
Часть медиатора возвращается в пресинаптическое окончание с помощью процесса обратного захвата (значение в том, что синтез нового нейромедиатора – длительный процесс).
Небольшое количество уносится межклеточной жидкостью.
Особенности передачи возбуждения через химические синапсы:
Возбуждение передается только в одном направлении, что способствует его точному распространению в ЦНС.
Они обладают синаптической задержкой – это время, необходимое на выделения медиатора, его диффузию и процессы в субсинаптической мембране.
В синапсах происходит трансформация, т.е. изменение частоты нервных импульсов.
Для них характерно явление суммации. Т.е. чем больше частота импульсов, тем выше амплитуда ВПСП и ТПСП. 5. Синапсы обладают низкой лабильностью.
29.
Химический синапс:
Передача в синапсе имеет два главных этапа. 1. Преобразование электрического сигнала в химический (электросекреторное сопряжение). Потенциал действия (ПД), поступивший в пресинаптическое окончание, вызывает деполяризацию его мембраны, открывающую потенциалзависимые Са-каналы. Ионы кальция входят, согласно концентрационному и электрическому градиентам, внутрь клетки, что ведет к увеличению его содержания в цитозоле в 10—100 раз. Ионы кальция активируют фосфорилирование синаптосина, что ослабляет связь везикулы с цитоскелетом, и везикула перемещается вдоль микротрубочек на позицию у активной зоны. При контакте везикулы с пресинаптической мембраной происходит ферментативное «плавление» ее стенки, а также активация белка синаптопорина, формирующего канал, через который медиатор выходит в синаптическую щель посредством первично-активного транспорта — экзоцитоза. В нервно-мышечном синапсе медиатором является ацетилхолин, который образуется в пресинаптическом окончании из ацетилкоэнзима А и холина под действием фермента холинацетилтрансферазы. Впервые экспериментальное доказательство химического механизма передачи возбуждения в нервно-мышечном синапсе получил А.Ф.Самойлов (1924). Он показал, что скорость передачи возбуждения с нерва на мышцу в отличие от проведения возбуждения по нерву зависит от температуры в такой же степени, как и скорость химических реакций. Английский физиолог Г.Дейл (1934) установил, что медиатором нервно-мышечного синапса является ацетилхолин. Этот медиатор был обнаружен одним из первых − он был известен также как «вещество блуждающего нерва» из-за своего действия на сердце.
Выделение молекул медиатора из пресинаптического окончания пропорционально количеству поступившего туда Са2+ в степени n = 4. Следовательно, химическое звено пре-синаптического окончания работает как усилитель. Один из возможных механизмов усиления связан с тем, что поступивший в пресинаптическое окончание Са2+ активирует рианодиновые рецепторы в цистернах эндоплазматической сети, имеющие в своем составе Са-каналы, что приводит к дополнительному выделению Са2+в цитозоль из цистерн. Выделение ацетилхолина в синаптическую щель осуществляется квантами, каждый из которых в нервно-мышечном синапсе содержит от нескольких тысяч до 10 тыс. молекул. На один ПД из пресинаптического окончания нервно-мышечного синапса выделяется 200—300 квантов медиатора. В промежутках между ПД из пресинаптического окончания происходит спонтанное выделение 1—2 квантов медиатора в синаптическую щель в течение 1 с.
Молекулы медиатора, поступившие в синаптическую щель, диффундируют к пост-синаптической мембране и вступают во взаимодействие с ее рецепторами. В нервно-мышечном синапсе ацетилхолин действует на Н-холинорецепторы, которые способны активизироваться и под влиянием никотина, вследствие чего они и получили свое название. Н-холинорецептор имеет в своем составе Nа/К-канал и состоит из пяти очень сходных субъединиц (α)2, β, γ, δ) примерно одинакового размера, группирующихся вокруг центрального канала. Такого рода макробелок составляет основу рецепторов различных типов, а для ацетилхолинового рецептора установлена его полная аминокислотная последовательность. Молекулярная масса этого белка 258 000. Открывание каналов в химических синапсах происходит в результате связывания медиатора или его агониста с комплексом рецептор-канал.
Скорость диффузии молекул медиатора позволяет им пройти расстояние синаптической щели в течение 0,1—0,2 мс. Длительность действия медиатора на рецепторы постсинаптической мембраны, определенная по продолжительности открытия в ней ионных каналов, равна около 1 мс. Это значительно меньше периода полураспада медиатора и свидетельствует о его удалении из синаптической щели. Оно осуществляется путем диффузии ацетилхолина из щели в окружающую жидкость и разрушения его под действием ацетилхолинэстеразы.
Этот фермент выделяется миоцитом и прикрепляется к мукополисахаридному веществу в синаптической щели. Одна молекула ацетилхолинэстеразы может гидролизовать до ацетата и холина 10 молекул ацетилхолина в 1 мс, что обеспечивает его разрушение в синаптической щели в течение нескольких десятых долей миллисекунды. При этом большая часть (около 60 %) холина захватывается обратно пресинаптическим окончанием. Значительная доля высвобожденного ацетилхолина разрушается уже в ходе диффузии через синаптическую щель, не успевая достигнуть рецепторов, и через несколько миллисекунд его практически не остается: синапс вновь готов к передаче возбуждения. 2. Преобразование химического сигнала обратно в электрический. Этот этап осуществляется в постсинаптической мембране. Действие молекул медиатора на ее рецепторы ведет к открытию ионных каналов и перемещению ионов, имеющих высокий электрохимический градиент на протяжении канала. Присоединение двух молекул ацетилхолина к α-субъединицам Н-холинорецептора открывает канал. Открытое состояние сохраняется 1 мс, в течение которой через него проходит около 500 000 ионов. Один квант медиатора (десятки тысяч его молекул) создает на несколько миллисекунд около рецепторов его высокую концентрацию, которая затем быстро падает. Начальный подъем концентрации медиатора повышает вероятность открывания канала, причем его открытые состояния перемежаются кратковременными закрываниями. После такой вспышки открываний он окончательно закрывается, потому что концентрация медиатора становится слишком низкой. Серии открываний суммируются, так что квант тока складывается из нескольких сотен токов одиночных каналов. Поскольку квант медиатора почти всегда вызывает только одну вспышку открываний, постоянная времени спада синаптического тока тоже примерно соответствует средней продолжительности такой вспышки.
Канал на внутреннем суженном конце имеет диаметр 0,65 нм, хорошо проницаем для Nа+ и К+, плохо проницаем для Са2+. Поскольку канал имеет слабую избирательность в отношении Nа+ и К+, то ионные токи через канал зависят главным образом от электродвижущей силы (ЭДС) этих ионов.
ЭДС иона равна разности между мембранным потенциалом покоя и равновесным потенциалом данного иона (ЭДС = МПП - Еиона). Отрицательная величина ЭДС характеризует движение иона в клетку, положительная — из клетки.
В связи с этим входящий в клетку ток натрия (ЭДС = -140 мВ) резко преобладает над выходящим из клетки током калия (ЭДС = 14 мВ). Иными словами, ион Nа+ движется в клетку согласно концентрационному и электрическому градиенту (клетка внутри имеет положительный заряд), а ион К+ выходит из клетки только согласно концентрационному градиенту, причем вопреки электрическому (снаружи клетка имеет положительный заряд). Поэтому суммарный ток ионов Nа+ в клетку превосходит ток К+из клетки, что и приводит к деполяризации постсинаптической мембраны (концевой пластинки). Эта деполяризация называется возбуждающим постсинаптическим потенциалом (ВПСП), который в нервно-мышечном синапсе называют потенциалом концевой пластинки (ПКП). Особенностью нервно-мышечного синапса фазного мышечного волокна является то, что при одиночной его активации формирующийся ПКП имеет большую амплитуду (30—40 мВ), которая превышает критический уровень деполяризации и вызывает генерацию ПД в миоците. Тоническое мышечное волокно имеет 7—10 синапсов, принадлежащих, как правило, нескольким мотонейронам. При этом ПКП не вызывает генерации ПД, а непосредственно запускает мышечное сокращение.
Как было отмечено, в промежутках между передачей нервного импульса происходит спонтанное выделение 1—2 квантов медиатора в синаптическую щель. При этом в пост-синаптической мембране формируется деполяризация амплитудой 0,12—0,24 мВ, возникающая в среднем 1 раз в 1 с. Такие потенциалы, изученные в нервно-мышечном синапсе, были названы миниатюрными потенциалами концевой пластинки. Они, вероятно, поддерживают высокую возбудимость синапсов в условиях функционального покоя нервных центров. Кроме экзоцитоза медиатора, существует постоянная неквантовая утечка молекул медиатора в синаптическую щель. Предполагают, что неквантовая секреция играет трофическую роль. Саморегуляция в синапсе осуществляется с использованием функциональных обратных связей. Веществами, влияющими на эффективность синаптической передачи, могут быть медиаторы, продукты их распада. В нервно-мышечном синапсе ацетилхолин, выделившийся в небольшом количестве в синаптическую щель, может стимулировать более сильный выброс ацетилхолина из пресинаптического окончания по механизму обратной связи (самоусиление секреции). Высокие концентрации ацетилхолина в синаптической щели, напротив, угнетают секрецию его из пресинаптического окончания.
Показано, что холин (продукт гидролиза ацетилхолина) в концентрации 10-4—10-5 М тормозит выделение ацетилхолина из пресинаптического окончания.
Электрический синапс:
После того как концепция химической синаптической передачи стала общепринятой, примерно между 1930 и 1950 гг., к большому удивлению специалистов выяснилось, что межклеточная передача возбуждения может осуществляться и электрическим способом [Furshpan,Potter,1959]. Две соседние клетки прилегают друг к другу так тесно, что сопротивление двух их мембран протекающему через них электрическому току сравнимо с сопротивлением остальной, внесинаптической области мембраны. При возбуждении 1-ой клетки натриевый ток (INa) входит в нее через открытые Nа-каналы и выходит через пока невозбужденные участки мембраны; при этом часть тока входит через участок мембранного контакта во 2-ю клетку, вызывая ее деполяризацию. Разумеется, здесь уровень деполяризации гораздо ниже - скажем, в 10 раз, чем в 1-ой клетке, однако он может оказаться выше порога генерирования потенциала действия во 2-ой клетке. Часто такая деполяризация подпороговая, и тогда 2-ая клетка возбуждается только в результате суммации синаптических потенциалов, возникающих в результате химической или электрической передачи от других клеток.
Итак, перечислим основные характеристики, которые отличают химическую синаптическую передачу от электрической.
1. В химическом синапсе постсинаптический ток генерируется за счет открывания каналов в постсинаптической мембране и обусловлен ионными градиентами постсинаптической клетки. 2. В электрическом синапсе источник постсинаптического тока - мембрана пресинаптической клетки. Здесь нет химического медиатора, и все факторы, влияющие на его высвобождение и действие (например, снижение внеклеточной концентрации Са2+или устранение разрушающих медиатор ферментов), на передаче возбуждения не сказываются. Щелевые контакты. Ионы, переносящие электрические токи, не могут проходить через липидные мембраны, следовательно, для их транспорта в «мембранных контактах» между электрически сопряженными клетками необходимы канальные белки. Такие межклеточные связи называются нексусами, или «щелевыми контактами». В каждой из двух соседних клеточных мембран находятся регулярно распределенные через небольшие промежутки коннексоны, пронизывающие всю толщу мембраны; они расположены так, что в месте контакта клеток находятся друг против друга и их просветы оказываются на одной линии. У образованных таким образом каналов крупные диаметры и, значит, высокая проводимость для ионов: через них могут проходить даже относительно крупные молекулы с молекулярной массой до 1000 (около 1.5 нм в поперечнике). Коннексон состоит субъединиц числом до шести с молекулярной массой примерно 25000 каждая. Щелевые контакты обычны для ЦНС позвоночных и, как правило,соединяютгруппы синхронно функционирующих клеток. Такие контакты характерны также длябеспозвоночных. Функциональные синцитии. В тканях, не относящихся к нервной системе, клетки тоже очень часто соединены щелевыми контактами.
Говоря о передаче возбуждения, стоит, прежде всего, упомянуть миокард и гладкую мускулатуру, где эти контакты создают функциональный синцитий. Возбуждение здесь переходит от одной клетки к другой без заметной паузы или снижения амплитуды потенциала действия на границе.
Для таких органов важна регулируемость щелевых контактов; в самом деле, их каналы закрываются при снижении рН или повышении концентрации Са2+. Это неизбежно происходит в случае повреждения клеток или глубокого нарушения обмена. За счет такого механизма пораженные места изолируются от остальной части функционального синцития, и распространение патологии ограничивается (например, при инфаркте миокарда). Кроме этих возбудимых тканей существует и много других (в частности, все эпителии, печень), где клетки также соединены щелевыми контактами. В принципе такая связь присуща любой клетке на ранних стадиях эмбрионального развития, когда все клетки соединены между собой щелевыми контактами и сохраняют их до стадии дифференцировки органов.
Роль таких контактов у невозбудимых клеток неясна. Через них возможен обмен многими мелкими молекулами; не исключено, что это важно для метаболизма. Через щелевые контакты могли бы также диффундировать внутриклеточные вторые посредники, передавая по ткани сигналы, регулирующие клеточные процессы.
Учитывая широкое распространение щелевых контактов, кажется удивительным, почему в нервной системе они не используются для синаптической передачи повсеместно. Видимо, сложнее организованные химические синапсы обеспечивают настолько более высокую специфичность и регулируемость межклеточной коммуникации, что в значительной степени вытеснили электрические.
Тормозные электрические синапсы. Щелевой контакт наиболее распространенный тип электрического синапса. Однако существуют и другие. Например, электрическим путем может передаваться и торможение. В этом случае потенциал действия особым образом расположенных пресинаптических волокон генерирует во внеклеточном пространстве вокруг постсинаптического аксона местный положительный потенциал такой амплитуды, что деполяризация аксона не может достичь порогового уровня, и проведение по нему потенциала действия блокируется.
Свойства электрических и химических синапсов
Свойство |
Электрические синапсы |
Химические синапсы |
Проведение возбуждения |
двустороннее |
одностороннее |
Утомляемость |
низкая |
высокая |
Лабильность |
высокая |
низкая |
Синаптическая задержка |
короткая |
длинная |
Трансформация ритма ПД |
не происходит |
происходит |
Чувствительны к действию |
электромагнитных излучений |
химических агентов |
30.
Если кратко: слияние синаптических пузырьков с пресинаптической мембраной происходит, когда увеличивается концентрации Са2+ в цитозоле нервной терминали. Белок синаптического пузырька синаптотагмин связывается с Са2+ и тем самым принимает участие в регуляции экзоцитоза (в том числе реорганизуя примембранный цитоскелет).
Синапсины - белки, ассоциированные с везикулами, которые предположительно связывают синаптические пузырьки с цитоскелетом нервного окончания. Прикрепление, образование поры и опорожнение везикул осуществляются взаимодействиями (указаны стрелками) различных везикулярных и мембранных белков. Например, в образовании прикрепительного комплекса участвуют везикулярные белки (синаптотагмин и синаптобревины) и белки плазматической мембраны нервного окончания (синтаксины и нейрексины). Какие белки - плазматические или везикулярные образуют пору слияния до сих пор не ясно. Предположительно, это - синаптофизин (имеющий и другие функции) и белок плазматической мембраны физофилин. Rab-белки могут участвовать в транспорте везикул в клетке и в прикреплении их к мембране нервной клетки. Везикулярные транспортеры играют роль в аккумуляции нейромедиатора в синаптических пузырьках.
Одновременно Ca2+ начинает удаляться из цитоплазмы несколькими путями: связывание с белками, захват митохондриями и работа активного транспорта. Выход медиатора зависит от деполяризации терминали и составляет около 100 - 200 везикул, каждая из которых содержит одну порцию (квант), соответствующую приблизительно 104 молекул. Молекулы медиатора диффундируют к постсинаптической мембране, где взаимодействует с рецепторами постсинаптической мембраны, регулирующими состояние ионных каналов. Эта регуляция может быть прямой (как, например, в нервно-мышечном соединении скелетных мышц позвоночных), так и включать активацию систем вторичных внутриклеточных медиаторов ( G-белки, цАМФ).
А1 - медиатор, например, ацетилхолин (АХ) или глутамат, непосредственно действует на рецептор Na+/К+ - канала и открывает его (А2); Б1 - медиатор, например, серотонин (5-ГT), связывается с рецептором и стимулирует аденилатциклазу через соединяющий G- белок. При этом фосфорилируется связанный с G-белком ГДФ. Образующийся цАМФ активирует затем протеинкиназу, которая фосфорилирует (Ф) субcтратный белок (или сам канал, или регуляторный белок, контролирующий канал), в результате чего К+ -канал закрывается (Б2).
В первом случае осуществляется передача быстрых пусковых сигналов, во втором - осуществляются более медленные длительные воздействия. Направление изменения потенциала постсинаптической мембраны (деполяризация или гиперполяризация) зависит главным образом от того, открытием каких каналов управляют постсинаптические рецепторы. Часть молекул медиатора может взаимодействовать с пресинаптическими рецепторами, что приводит к изменению МП нервной терминали и, соответственно, количества выделяемого медиатора (обратная связь). Синаптическая щель очищается от медиатора различными путями: дезактивация, гидролиз, обратный захват в пресинаптическое окончание, диффузия, захват глиальными клетками. Основная часть синаптической задержки - времени от прихода нервного импульса до развития постсинаптического ответа (0,2-0,5 мс) приходится на процесс секреции медиатора. Химический синапс обеспечивает передачу сигнала только от пресинаптического нейрона к постсинаптическому.
При частой ритмической стимуляции в химических синапсах наблюдается сначала усиление (облегчение), а затем ослабление (депрессия) передачи, т.е. рост, а затем падение амплитуды постсинаптических потенциалов. Эти явления в основном определяются изменениями в пресинаптическом звене. Они имеют особое развитие в некоторых синапсах ЦНС, где выступают как факторы синаптической пластичности. Наличие различных типов рецепторов в постсинаптической мембране может обусловливать развитие этих явлений по отдельности, как, например, длительную потенциацию (рис.11) и длительную депрессию (рис.12).
Обычный ход возбуждающей синаптической передачи. Единичный ПД в нервном окончании высвобождает глутамат (Глу), который может связываться с постсинаптическими глутаматными рецепторами. Одни из них - AMPA / каинатные (А/К)- рецепторы, каналы которых открываются после связывания с глутаматом. При этом ионы Na+, K+ и Ca2+ проходят через эти каналы, вызывая ВПСП амплитудой, например, 20 мВ. Соединение глутамата с другим типом рецепторов (NMDA-рецепторы) не дает эффекта, т.к. их каналы блокированы ионами Mg2+, которые связаны с внутренними стенками поры при отрицательных значениях МП. Справа - серия ПД вызывает длительную потенциацию за счет большего количества высвобождаемого глутамата. Более сильная деполяризация в этом случае (за счет большего числа активированных А/К каналов) приводит к разблокированию NMDA-каналов путем удаления из них ионов Mg2+. Возникающий относительно сильный Ca2+ ток увеличивает внутриклеточную концентрацию этих ионов, что ведет к активации специфической ферментной системы, чье действие в шипиках длительно повышает реакцию на глутамат. Вероятно, катализируется также образование молекул NO, которые могут диффундировать к пресинаптическому окончанию как ретроградный медиатор и там стимулировать выброс новых квантов глутамата, тем самым, способствуя длительной потенциации.
31.
Нервно-мышечный синапс образован окончанием аксона моторного нейрона и мышечным волокном поперечно-полосатой мускулатуры.
Структурами, непосредственно образующими синапс, являются пресинаптическая мембрана аксонной терминали, синаптическая щель и постсинантическая мембрана, являющаяся частью плазматической мембраны (сарколеммы) постсинаптической мышечной клетки. Пресинаптической мембраной называют часть не покрытой миелином мембраны аксонной терминали, обращенной в синаптическую щель.
Пресинаптическая терминаль формируется тонкой веточкой аксона, которая, подходя к мышечному волокну, образует утолщение (пуговку, бляшку, бутон). В пресинаптической терминали находятся синаптические пузырьки (везикулы), содержащие запасы медиатора ацетилхолина. Везикул может быть до нескольких тысяч. Их диаметр около 40 им, и в каждой содержится несколько тысяч молекул медиатора. В отсутствие поступления нервных импульсов везикулы с помощью белка синапсина связаны с цитоскелетом и малоподвижны. В пресинаптической терминали имеются также митохондрии, обеспечивающие выработку АТФ, ацетил СоА, белки цитоскелета, микротрубочки и микронити, по которым в терминаль из тела нейрона перемещается фермент ацетилхолинтрансфсраза. При участии этого фермента из ацетил СоА и холина образуется ацетилхолин.
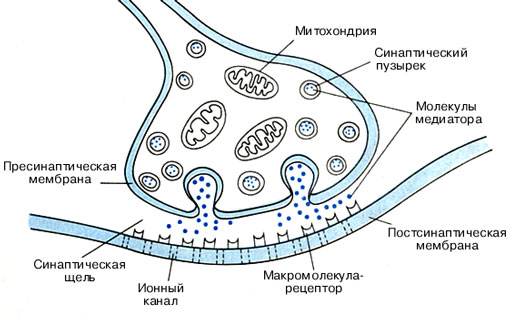
Рис. 1. Строение нервно-мышечного синапса
Отличает нервно-мышечный синапс от центрального синапса большая протяженность пресинаптической мембраны, что способствует экзоцитозу большего количества медиатора. Этого количества медиатора достаточно для того, чтобы один потенциал действия, пришедший по нервному волокну, вызвал возбуждение мышечного волокна. В пресинаптической мембране, уже не покрытой миелиновой оболочкой, содержатся потенциалзависимые кальциевые каналы, преимущественно локализованные вблизи мест расположения везикул с медиатором. Такая локализация кальциевых каналов позволяет, изменяя разность потенциалов на пресинаптической мембране (и тем самым состояние каналов), идеально контролировать зависящий от концентрации кальция процесс высвобождения медиатора.
Между пре- и постсинаптическими мембранами располагается синаптическая щель шириной 50-100 им. Она заполнена межклеточным веществом и содержит тяжи плотного вещества из мукополисахаридов, с которым связана ацетилхолинэстераза (АХЭ) — фермент, разрушающий выходящий в синаптическую щель ацетилхолин на холин и уксусную кислоту.
Постсинаптическую мембрану нервно-мышечного синапса называют также концевой пластинкой. На ней имеются многочисленные впячивания, которые увеличивают площадь этой мембраны и в ней может расположиться до 20 миллионов рецепторных белковых молекул к ацетилхолину. Их плотность достигает 10 000 на 1 нм2. Эти белки наряду с выполнением рецепторной функции формируют неселективные лигандзависимые каналы, через которые могут проходить ионы К+ и Na+. Рецепторы чувствительны также к никотину; их полное название — никотинчувствительные ацетилхолиновые рецепторы мышечного типа, или сокращенно н-ХРмт.
Когда нервный импульс, посланный моторным нейроном, распространяется по нервному волокну и достигает пресинаптической терминали, он вызывает деполяризацию ее мембраны.
Деполяризация приводит к открытию встроенных в мембрану потенциалзависимых кальциевых каналов, и ионы Са2+' из межклеточного пространства поступают внутрь пресинап- тичсской терминали. Ионы Са2 перемещаются в терминаль по градиенту концентрации, так как снаружи аксонной терминали содержание кальция в 10 000 раз больше, чем внутри. Содержание кальция в цитоплазме терминали повышается, и это приводит к запуску ряда событий, необходимых для высвобождения ацетилхолина в синаптическую щель. Среди них отшнуровывание везикул от эндосом, приближение их к преси- наптической мембране, слияние с мембраной и экзоцитоз квантов ацетилхолина в синаптическую щель (рис. 2).
При поступлении к аксонной терминали одного ПД в синаптическую щель выбрасывается ацетилхолин из десятков синаптических пузырьков. Количество выделяемого АЦХ пропорционально величине и продолжительности деполяризации пресинаптической мембраны, которая в свою очередь определяется частотой и количеством поступивших по аксону нервных импульсов.
Молекулы ацетилхолина за время около 0,2 мс диффундируют к постсинаптической мембране и связываются с н-холинорецепторами, которые выполняют роль ворот в несслек- тивных лигандзависимых ионных каналах, проницаемых для ионов Na+ и К+. Ворота открываются, и через ионные каналы внутрь мышечного волокна начинают входить ионы Na+, а из волокна выходить ионы КЛ Поток входящих ионов Na+ больше, чем поток выходящих ионов К+, так как ионы Na+ идут не только но градиенту концентрации, но и но градиенту электрического поля (на внутренней стороне мембраны отрицательный заряд до — 90 мВ).
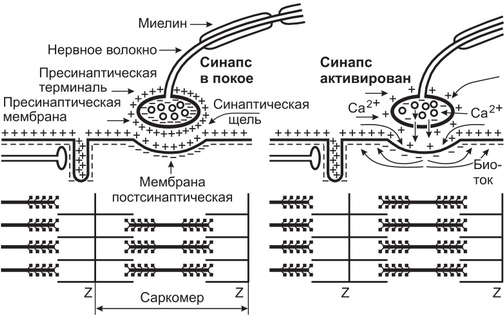
Рис. 2. Структура нервно-мышечного синапса в покое и при активации
Положительно заряженные ионы Na+, входящие в мышечное волокно, деполяризуют постсинаптическую мембрану, нейтрализуя часть отрицательных зарядов на ее внутренней стороне. Амплитуда деполяризации зависит от количества выделившегося АЦХ и, следовательно, от числа нервных импульсов, поступивших к мышечному волокну от иннервирующего его мотонейрона. Она может достигать 40-50 мВ, длиться около 1 мс и сменяется реполяризацией за счет выхода из постсинаптической клетки катионов К . Возникающая деполяризация не сопровождается перезарядкой постсинаптической мембраны и развитием на ней ПД.
Кратковременное (около 4 мс) уменьшение разности потенциалов (деполяризация) постсинаптической мембраны нервно-мышечного синапса называют потенциалом концевой пластанки (ПКП). По характеру влияния на постсинаптическую клетку он аналогичен ВПСП. Деполяризация постсинаптической мембраны приводит к возникновению локального кругового электрического тока между нею и сарколеммой, граничащей с синапсом. В сарколемме, прилежащей к синапсу, имеются потенциалзависимые селекгивные быстрые натриевые и медленные калиевые каналы. Под действием локальных токов сарколемма деполяризуется и, если уровень деполяризации достигает Ек, каналы открываются и на граничащем с синапсом участке сарколеммы возникает потенциал действия.
В естественных условиях при поступлении нервных импульсов и их успешном проведении через нервно-мышечный синапс, амплитуда возникающего ПКП всегда превышает пороговый уровень, необходимый для генерации ПД на сарколемме. Возникший ПД распространяется вдоль мышечного волокна по сарколемме и вглубь его по мембранам поперечных трубочек, пронизывающих волокно.
Почему же потенциал действия возникает на прилежащей к синапсу мембране, а не па постсинаптической мембране? Постсинаптическая мембрана не может генерировать ПД, так как на ней нет потенциалзави- симых натриевых каналов, которые обеспечивают быстрый вход ионов Na+ и перезарядку мембраны. Перезарядке противодействуют также выходящие из постсинаптической клетки ионы К+. В то же время вход натрия, движимый силами его концентрационного и электрического градиентов, опережает выход калия, который обусловлен действием только сил концентрационного градиента калия и осуществляется против сил электрического поля. Вход натрия в мышечное волокно, опережающий выход калия, создает условия для кратковременной деполяризации постсинаптической мембраны и последующей ее реполяризации, т.е. для возникновения ПКП.
Ионные каналы постсинаптической мембраны остаются открытыми, пока концентрация ацетилхолина в синаптической щели не понизится примерно до 10 нмолей. Снижение концентрации АЦХ в синаптической щели в нормальных условиях происходит под действием фермента ацетилхолинэстеразы (АХЭ). Значение АХЭ для нормальной работы нервно-мышечного синапса чрезвычайно велико. Для того чтобы идущие от мотонейронов друг за другом нервные импульсы могли оказывать на рецепторы постсинаптической мембраны активирующее действие, необходимо к моменту поступления очередного импульса удалить из синаптической щели предшествующую порцию медиатора главным образом путем разрушения.
Когда содержание медиатора понизится до уровня 10 нмолей, ацетилхолин диссоциирует из связи с рецептором, восстанавливается способность рецепторов связываться с новой порцией АЦХ и открывать лигандзависимые ионные каналы. Синапс становится готовым к передаче нового сигнала. В устранении молекул ацетилхолина из синаптической щели также имеют значение обратный захват продукта его расщепления (холина) пресинаптической мембраной в пресинаптическую терминаль, диффузия АЦХ в интерстициальнос пространство и далее в кровь. Время от момента прихода ПД к пресинаптической мембране до момента возникновения ПД на мембране мышечного волокна называют синаптической задержкой. В нервно-мышечном синапсе она составляет около 1 мс.
В состоянии покоя наблюдается спонтанное высвобождение (экзоцитоз) ацетилхолина в синаптическую щель. Объем экзоцитируемого медиатора составляет около 1 кванта в секунду, что эквивалентно количеству АЦХ, высвобождаемого из одной везикулы. Выход медиатора в этом объеме способен вызвать лишь малую (0,1-0,2 мВ) деполяризацию постсинап- тической мембраны (миниатюрный потенциал концевой пластинки), и его недостаточно для инициации сокращения мышцы. Однако считается, что спонтанный выход этого небольшого количества медиатора имеет важное значение для трофического влияния АЦХ на постсинаптичсскую мышечную клетку: стимуляции синтеза каналообразующих рецепторных белков, регуляции обменных процессов в клетке, поддержания ее тканевой специфичности.
Таким образом, в нервно-мышечном синапсе сигнал электрической природы (нервный импульс) преобразуется в химический сигнал — высвобождение нейромедиатора АЦХ, который через цепочку последовательных событий на постсинаптической мембране вновь обеспечивает возникновение электрического потенциала на мембране мышечного волокна в виде ПД. Этот потенциал является непосредственной причиной инициирования сокращения постсинаптической мышечной клетки.
Имеется много факторов, способных влиять на состояние синаптической передачи сигналов к скелетным мышцам. Это влияние можно наблюдать в условиях патологии, например, при отравлении ботулиническим токсином С — одним из продуктов метаболизма анаэробного микроорганизма Clostridium botuinum, другими ядами растительного и животного происхождения. При попадании в организм ботулинического токсина он накапливается в аксонных терминалях нервно-мышечных синапсов и, обладая свойствами фермента цинкзависимой эндопептидазы, разрушает белки, участвующие в эк- зоцитозе ацетилхолина. Нейромышечная передача команд моторных нейронов к мышцам становится неэффективной или прекращается. Это может вести к развитию парезов, параличей скелетных мышц, нарушению глотания, дыхания и в случаях тяжелого отравления — к остановке дыхания.
С другой стороны, ряд веществ, способных влиять на различные этапы синаптической передачи, используется в качестве лекарственных. Так, если ботулинический токсин (ботокс) ввести в низких концентрациях в мышцу с повышенным тонусом, развившемся вследствие ее избыточной активации нервными импульсами, часто поступающими от мотонейронов, то дозированное снижение эффективности синаптической передачи может помочь снизить повышенный тонус, восстановить координацию движений. В настоящее время ботокс применяют для снижения степени тонического напряжения наружных глазных и других поперечно-полосатых мышц, например при косоглазии, кривошее, других спастических состояниях мышц.
Следующий способ воздействия на синаптическую передачу также связан с влиянием на количество ацетилхолина в синаптической щели через управление скоростью его расщепления под действием фермента АХЭ. Он реализуется с помощью применения веществ, ингибирующих ферментативную активность АХЭ. Ими являются вещества, обратимо ингибирующие активность АХЭ (лекарственные вещества эзерин, прозерин, галангамин, физостигмин и др.). Эти вещества, блокируя активность АХЭ, способствуют снижению скорости расщепления АЦХ и его накоплению в синаптической щели, пролонгированию и усилению действия АЦХ во всех холинергических, в том числе и нервно-мышечных, синапсах. Применение (в небольших дозах) блокаторов активности АХЭ обратимого действия позволяет облегчить передачу сигналов к мышце, повысить ее тонус и усилить сокращение. Их введение в организм в небольших дозах улучшает синаптическую передачу и оказывает лечебный эффекг при многих неврологических заболеваниях, в частности при миастении (myastenia gravis).
Однако передозировка этих веществ или применение веществ, необратимо ингибирующих АХЭ — инсектицидов, боевых отравляющих веществ нервно-паралитического действия (соединения фосфорорганической природы — зарин, зоман), сопровождается накоплением в синапсе большого количества АЦХ. Это ведет к десенситизации н-холинорецепторов, развитию стойкой, продолжительной деполяризации постсинаптической мембраны, невозможности дальнейшей генерации ПД на мембране мышечного волокна, блокаде передачи сигналов к скелетным мышцам, их расслаблению, парезам, нарушению или остановке дыхания.
Ряд веществ может легко связываться с никотинчувствительными холинорецепторами и блокировать при этом открытие лигандзависимых ионных каналов. Это, например, такие вещества, как кураре, D-тубокурарин, и вещества, входящие в состав ядов — кобратоксин, а-бунгаротоксин. Примененние кураре и курареподобных веществ позволяет, заблокировав взаимодействие АЦХ с холинорецепторами постсинаптической мембраны, вызывать блокаду передачи сигнала от мотонейронов к мышечным волокнам, расслабление мышц во время хирургических операций (миорелаксация) или при повышении их тонического напряжения при спастичесих состояних.
При некоторых аутоиммунных заболеваниях, например при myastenia gravis, в организме вырабатываются антитела к ацетилхолиновым рецепторам постсинаптической мембраны нервно-мышечных синапсов. Антитела могут блокировать рецепторы и разрушать их. В этих условиях даже при высвобождении достаточного количества АЦХ из нервного окончания амплитуда постсинаптичсского потенциала часто не достигает величины, необходимой для генерации ПД на мембране мышечного волокна. Вследствие длительного нарушения нервно-мышечной передачи развиваются слабость и повышенная утомляемость мышц. Введение больным миастенией ботокса или блокаторов АХЭ обратимого действия, улучшающих нервно-мышечную передачу, даже при сниженном количестве рецепторов приводит к повышению силы сокращения и работоспособности мышц.
Если кратко: Механизмы передачи возбуждения в синапсах на примере мионеврального синапса
Мионевральный (нервно-мышечный) синапс — образован аксоном мотонейрона и мышечной клеткой.
Нервный импульс возникает в тригерной зоне нейрона, по аксону направляется к иннервируемой мышце, достигает терминали аксона и при этом деполяризует пресинаптическую мембрану. После этого открываются натриевые и кальциевые каналы, и ионы Ca из среды, окружающей синапс, входят внутрь терминали аксона. При этом процессе броуновское движение везикул упорядочивается по направления к пресинаптической мембране. Ионы Ca стимулируют движение везикул. Достигая пресинаптическую мембрану, везикулы разрываются, и освобождается ацетилхолин (4 иона Ca высвобождают 1 квант ацетилхолина). Синаптическая щель заполнена жидкостью, которая по составу напоминает плазму крови, через нее происходит диффузия АХ с пресинаптической мембраны на постсинаптическую, но ее скорость очень мала. Кроме того, диффузия возможна еще и по фиброзным нитям, которые находятся в синаптической щели. После диффузии АХ начинает взаимодействовать с хеморецепторами (ХР) и холинэстеразой (ХЭ), которые находятся на постсинаптической мембране.
Холинорецептор выполняет рецепторную функцию, а холинэстераза выполняет ферментативную функцию. На постсинаптической мембране они расположены следующим образом:
ХР—ХЭ—ХР—ХЭ—ХР—ХЭ.
ХР + АХ = МПКП — миниатюрные потенциалы концевой пластины.
Затем происходит суммация МПКП. В результате суммации образуется ВПСП — возбуждающий постсинаптический потенциал. Постсинаптическая мембрана за счет ВПСП заряжается отрицательно, а на участке, где нет синапса (мышечного волокна), заряд положительный. Возникает разность потенциалов, образуется потенциал действия, который перемещается по проводящей системе мышечного волокна.
ХЭ + АХ = разрушение АХ до холина и уксусной кислоты.
В состоянии относительного физиологического покоя синапс находятся в фоновой биоэлектрической активности. Ее значение заключается в том, что она повышает готовность синапса к проведению нервного импульса. В состоянии покоя 1—2 пузырька в терминале аксона могут случайно подойти к пресинаптической мембране, в результате чего вступят с ней в контакт. Везикула при контакте с пресинаптической мембраной лопается, и ее содержимое в виде 1 кванта АХ поступает в синаптическую щель, попадая при этом на постсинаптическую мембрану, где будет образовываться МПКН.
32.
Нервный центр — это совокупность нейронов, необходимых для осуществления определенного рефлекса или регуляции определенной функции.
Основными клеточными элементами нервного центра являются многочисленные нейроны, скопление которых формирует нервные ядра. В состав центра могут входить нейроны, рассеянные за пределами ядер. Нервный центр может быть представлен структурами мозга, располагающимися на нескольких уровнях центральной нервной системы (например, центры регуляции дыхания, кровообращения, пищеварения).
Любой нервный центр состоит из ядра и периферии.
Ядерная часть нервного центра представляет собой функциональное объединение нейронов, в которое поступает основная информация от афферентных путей. Повреждение этого участка нервного центра приводит к повреждению или существенному нарушению осуществления данной функции.
Периферическая часть нервного центра получает небольшую порцию афферентной информации, и ее повреждение вызывает ограничение или уменьшение объема выполняемой функции (рис. 1).
Функционирование центральной нервной системы осуществляется благодаря деятельности значительного числа нервных центров, представляющих собой ансамбли нервных клеток, объединенных с помощью синаптических контактов и отличающихся огромным разнообразием и сложностью внутренних и внешних связей.
Рис. 1. Схема общего строения нервного центра
В нервных центрах выделяют следующие иерархические отделы: рабочие, регуляторные и исполнительные (рис. 2).
Рис. 2. Схема иерархического подчинения разных отделов нервных центров
Рабочий отдел нервного центра ответствен за осуществление данной функции. Например, рабочий отдел дыхательного центра представлен центрами вдоха, выдоха и пневмотаксиса, расположенными в продолговатом мозге и варолиевом мосту; нарушение этого отдела вызывает остановку дыхания.
Регуляторный отдел нервного центра - это центр, расположенный в коре больших полушарий мозга и регулирующий активность рабочего отдела нервного центра. В свою очередь, активность регуляторного отдела нервного центра зависит от состояния рабочего отдела, который получает афферентную информацию, и от внешних стимулов среды. Так, регуляторный отдел дыхательного центра расположен в лобной доле коры больших полушарий и позволяет произвольно регулировать легочную вентиляцию (глубину и частоту дыхания). Однако эта произвольная регуляция небезгранична и зависит от функциональной активности рабочего отдела, афферентной им пульсации, отражающей состояние внутренней среды (в данном случае рН крови, концентрации углекислого газа и кислорода в крови).
Исполнительный отдел нервного центра - это двигательный центр, расположенный в спинном мозге и передающий информацию от рабочего отдела нервного центра к рабочим органам. Исполнительный отдел дыхательного нервного центра расположен в передних рогах грудного отдела спинного мозга и транслирует приказы рабочего центра к дыхательным мышцам.
С другой стороны, одни и те же нейроны головного и спинного мозга могут участвовать в регуляции разных функций. Например, клетки центра глотания участвуют в регуляции не только акта глотания, но и акта рвоты. Этот центр обеспечивает все последовательные стадии акта глотания: движение мышц языка, сокращение мышц мягкого неба и его поднятие, последующее сокращение мышц глотки и пищевода при прохождении пищевого комка. Эти же нервные клетки обеспечивают сокращение мышц мягкого нёба и его поднятие во время акта рвоты. Следовательно, одни и те же нервные клетки входят и в центр глотания, и в центр рвоты.
33.
Одностороннее проведение возбуждение в нервном центре: возбуждение в ЦНС проводится в одном направлении с аксона на дендрит или тело клетки следующего нейрона. Основу этого свойства составляют особенности морфологической связи между нейронами.
Одностороннее проведение возбуждения зависит от строения синапса и гуморальной природы передачи в нем импульса: медиатор, осуществляющий передачу возбуждения, выделяется только в пресинаптическом окончании, а рецепторы, воспринимающие медиатор, расположены на постсинаптической мембране;
34.
Задержка в проведение возбуждения (центральная задержка): в системе рефлекторной дуги медленнее всего проводится возбуждение в синапсах ЦНС. В связи с этим центральное время рефлекса зависит от количества вставочных нейронов.
Чем сложнее рефлекторная реакция, тем больше центральное время рефлекса. Его величина связана со сравнительно медленным проведением возбуждения через последовательно включенные синапсы. Замедление проведения возбуждения создается вследствие относительной длительности осуществляющихся в синапсах процессов: выделения медиатора через пресинаптическую мембрану, его диффузии через синаптическую щель, возбуждения постсинаптической мембраны, возникновения возбуждающего постсинаптического потенциала и его перехода в потенциал действия;
35.
Пространственная и временная суммация:
Временная суммация возникает, как и в синапсах вследствие того, что чем больше поступает нервных импульсов, тем больше выделяется нейромедиатора в них, тем выше амплитуда возбуждения постсинаптических потенциалов (ВПСП). Поэтому рефлекторная реакция может возникать на несколько последовательных подпороговых раздражений.
Пространственная суммация наблюдается тогда, когда к нервному центру идут импульсы от нескольких рецепторных нейронов. При действии на них подпороговых стимулов, возникающие постсинаптические потенциалы суммируются и в мембране нейрона генерируется распространяющийся ПД.
36.
Трансформация ритма возбуждения: нервные центры способны изменять ритм поступающих к ним импульсов. Они могут отвечать на одиночные раздражители серией импульсов или на раздражители небольшой частоты — возникновением более частых потенциалов действия. В результате ЦНС посылает к рабочему органу количество импульсов, относительно независимое от частоты раздражений.
Это связано с тем, что нейрон является изолированной единицей нервной системы, к нему в каждый момент приходит множество раздражений. Под их влиянием происходит изменение мембранного потенциала клетки. Если создается небольшая, но продолжительная деполяризация (длительный возбуждающий постсинаптический потенциал), то один стимул вызывает серию импульсов (рис. 3);
Рис. 3. Схема трансформации ритма возбуждения
37.
Рефлекторное последействие - способность сохранять возбуждение после окончания действия раздражителя, т.е. афферентных импульсов нет, а эфферентные продолжают действовать еще некоторое время.
Последействие объясняется наличием следовой деполяризации. Если следовая деполяризация длительна, то на ее фоне в течение нескольких миллисекунд могут возникать потенциалы действия (ритмическая активность нейрона), вследствие чего сохраняется ответная реакция. Но это дает сравнительно короткий эффект последействия.
Более длительное последействие связано с наличием кольцевых связей между нейронами. В них возбуждение как бы само себя поддерживает, возвращаясь по коллатералям к первоначально возбужденному нейрону (рис. 4);
Рис. 4. Схема кольцевых связей в нервном центре (по Лоренто де Но): 1 — афферентный путь; 2-промежуточные нейроны; 3 — эфферентный нейрон; 4 — эфферентный путь; 5 — возвратная ветвь аксона
38.
Тонус нервных центров - состояние постоянной повышенной активности. Он обусловлен постоянным поступлением к НЦ нервных импульсов от периферических рецепторов, возбуждающим влиянием на нейроны продуктов метаболизма и других гуморальных факторов. Например, проявлением тонуса соответствующих центров является тонус определенной группы мышц
39.
Утомляемость нервного центра: нервный центр обладает малой лабильностью. Он постоянно получает от множества высоколабильных нервных волокон большое количество стимулов, превышающих его лабильность. Поэтому нервный центр работает с максимальной загрузкой и легко утомляется.
Исходя из синаптических механизмов передачи возбуждения утомление в нервных центрах может объясняться тем, что по мере работы нейрона истощаются запасы медиатора и становится невозможной передача импульсов в синапсах. Кроме того, в процессе деятельности нейрона наступает постепенное снижение чувствительности его рецепторов к медиатору, что называется десенситизацией;
40.
Чувствительность нервных центров к кислороду и некоторым фармакологическим веществам: в нервных клетках осуществляется интенсивный обмен веществ, для чего необходимы энергия и постоянный приток нужного количества кислорода.
Особенно чувствительны к недостатку кислорода нервные клетки коры больших полушарий головного мозга, после пяти-шести минут кислородного голодания они погибают. У человека даже кратковременное ограничение мозгового кровообращения приводит к потере сознания. Недостаточное снабжение кислородом легче переносят нервные клетки мозгового ствола, их функция восстанавливается через 15-20 мин после полного прекращения кровоснабжения. А функция клеток спинного мозга восстанавливаются даже после 30 мин отсутствия кровообращения.
По сравнению с нервным центром нервное волокно малочувствительно к недостатку кислорода. Помешенное в атмосферу азота, оно только через 1,5 ч прекращает проведение возбуждения.
41.
Проявление и осуществление рефлекса возможно только при ограничении распространения возбуждения с одних нервных центров на другие. Это достигается взаимодействием возбуждения с другим нервным процессом, противоположным по эффекту процессом торможения.
Почти до середины XIX века физиологи изучали и знали только один нервный процесс - возбуждение.
Явления торможения в нервных центрах, т.е. в центральной нервной системе были впервые открыты в 1862 году И.М.Сеченовым ("сеченовское торможение”). Это открытие сыграло в физиологии не меньшую роль, чем сама формулировка понятия рефлекса, так как торможение обязательно участвует во всех без исключения нервных актах. И.М.Сеченов обнаружил явление центрального торможения при раздражении промежуточного мозга теплокровных. В 1880 году немецкий физиолог Ф.Гольц установил торможение спинальных рефлексов. Н.Е. Введенский в результате серий опытов по парабиозу вскрыл интимную связь процессов возбуждения и торможения и доказал, что природа этих процессов едина.
Торможение - местный нервный процесс, приводящий к угнетению или предупреждению возбуждения. Торможение является активным нервным процессом, результатом которого служит ограничение или задержка возбуждения. Одна из характерных черт тормозного процесса- отсутствие способности к активному распространению по нервным структурам.
В настоящее время в центральной нервной системе выделяют два вида торможения: торможение центральное (первичное), являющееся результатом возбуждения (активации) специальных тормозных нейронов и торможение вторичное, которое осуществляется без участия специальных тормозных структур в тех самых нейронах в которых происходит возбуждение.
Центральное торможение (первичное) - нервный процесс, возникающий в ЦНС и приводящий к ослаблению или предотвращению возбуждения. Согласно современным представлениям центральное торможение связано с действием тормозных нейронов или синапсов, продуцирующих тормозные медиаторы (глицин, гаммааминомасляную кислоту), которые вызывают на постсинаптической мембране особый тип электрических изменений, названных тормозными постсинаптическими потенциалами (ТПСП) или деполяризацию пресинаптического нервного окончания, с которым контактирует другое нервное окончание аксона. Поэтому выделяют центральное (первичное) постсинаптическое торможение и центральное (первичное) пресинаптическое торможение.
Постсинаптическое торможение (лат. post позади, после чего-либо + греч. sinapsis соприкосновение, соединение) - нервный процесс, обусловленный действием на постсинаптическую мембрану специфических тормозных медиаторов (глицин, гаммааминомаслянная кислота), выделяемых специализированными пресинаптическими нервными окончаниями. Медиатор, выделяемый ими, изменяет свойства постсинаптической мембраны, что вызывает подавление способности клетки генерировать возбуждение. При этом происходит кратковременное повышение проницаемости постсинаптической мембраны к ионам К+ или CI, вызывающее снижение ее входного электрического сопротивления и генерацию тормозного постсинаптического потенциала (ТПСП). Возникновение ТПСП в ответ на афферентное раздражение обязательно связано с включением в тормозной процесс дополнительного звена - тормозного интернейрона, аксональные окончания которого выделяют тормозной медиатор. Специфика тормозных постсинаптических эффектов впервые была изучена на мотонейронах млекопитающих (Д. Экклс, 1951). В дальнейшем первичные ТПСП были зарегистрированы в промежуточных нейронах спинного и продолговатого мозга, в нейронах ретикулярной формации, коры больших полушарий, мозжечка и таламических ядер теплокровных животных.
Известно, что при возбуждении центра сгибателей одной из конечностей центр ее разгибателей тормозится и наоборот. Д. Экклс выяснил механизм этого явления в следующем опыте. Он раздражал афферентный нерв, вызывающий возбуждение мотонейрона, иннервирующего мышцу - разгибатель.
Нервные импульсы, дойдя до афферентного нейрона в спинномозговом ганглии, направляются по его аксону в спинном мозге по двум путям: к мотонейрону, иннервирующему мышцу - разгибатель, возбуждая ее и по коллатерам к промежуточному тормозному нейрону, аксон которого контактирует с мотонейроном иннервирующим мышцу - сгибатель, вызывая таким образом торможение антагонистической мышцы. Этот вид торможения был обнаружении в промежуточных нейронах всех уровней центральной нервной системы при взаимодействии антагонистических центров. Он был назван поступательным постсинаптическим торможением. Этот вид торможения координирует, распределяет процессы возбуждения и торможения между нервными центрами.
Возвратное (антидромное) постсинаптическое торможение (греч. antidromeo бежать в противоположном направлении) - процесс регуляции нервными клетками интенсивности поступающих к ним сигналов по принципу отрицательной обратной связи. Он заключается в том, что коллатерали аксонов нервной клетки устанавливают синаптические контакты со специальными вставочными нейронами (клетки Реншоу), роль которых заключается в воздействии на нейроны, конвергирующие на клетке, посылающей эти аксонные коллатерали (рис. 87). По такому принципу осуществляетсяторможение мотонейронов.
Возникновение импульса в мотонейроне млекопитающих не только активирует мышечные волокна, но через коллатерали аксона активирует тормозные клетки Реншоу. Последние устанавливают синаптические связи с мотонейронами. Поэтому усиление импульсации мотонейрона ведет к большей активации клеток Реншоу, вызывающей усиление торможения мотонейронов и уменьшение частоты их импульсации. Термин "антидромное” употребляется потому, что тормозной эффект легко вызывается антидромными импульсами, рефлекторно возникающими в мотонейронах.
Чем сильнее возбужден мотонейрон, чем больше сильные импульсы идут к скелетным мышцам по его аксону, тем интенсивнее возбуждается клетка Реншоу, которая подавляет активность мотонейрона. Следовательно, в нервной системе существует механизм, оберегающий нейроны от чрезмерного возбуждения. Характерная особенность постсинаптического торможения заключается в том, что оно подавляется стрихнином и столбнячным токсином (на процессы возбуждения эти фармакологические вещества не действуют).
В результате подавления постсинаптического торможения нарушается регуляция возбуждения в цнс, возбуждение разливается ("диффундирует”) по всей цнс, вызывая перевозбуждение мотонейронов и судорожные сокращения групп мышц (судороги).
Торможение ретикулярное (лат. reticularis - сетчатый) - нервный процесс, развивающийся в спинальных нейронах под влиянием нисходящей импульсации из ретикулярной формации (гигантское ретикулярное ядро продолговатого мозга). Эффекты, создаваемые ретикулярными влияниями, по функциональному действию сходны с возвратным торможением, развивающимся на мотонейронах. Влияние ретикулярной формации вызывают стойкие ТПСП, охватывающие все мотонейроны независимо от их функциональной принадлежности. В этом случае, так же, как и при возвратном торможении мотонейронов происходит ограничение их активности. Между таким нисходящим контролем со стороны ретикулярной формации и системочй возвратного торможения через клетки Реншоу существует определенное взаимодействие, и клетки Реншоу находятся под постоянным тормозящем контролем со стороны двух структур. Тормозящее влияние со стороны ретикулярной формации являются дополнительным фактором в регуляции уровня активности мотонейронов.
Первичное торможение может вызываться механизмами иной природы, не связанными с изменениями свойств постсинаптической мембраны. Торможение в этом случае возникает на пресинаптической мембране (синаптическое и пресинаптическое торможение).
Синаптическое торможение (греч. sunapsis соприкосновение, соединение) - нервный процесс, основанный на взаимодействии медиатора, секретируемого и выделяемого пресинаптическими нервными окончаниями, со специфическими молекулами постсинаптической мембраны. Возбуждающий или тормозной характер действия медиатора зависит от природы каналов, которые открываются в постсинаптической мембране. Прямое доказательство наличия в цнс специфических тормозящих синапсов было впервые получено Д. Ллойдом (1941).
Данные относительно электрофизиологических проявлений синаптического торможения: наличие синаптической задержки, отсутствие электрического поля в области синаптических окончаний дали основание считать его следствием химического действия особого тормозящего медиатора, выделяемого синаптическими окончаниями. Д. Ллойд показал, что если клетка находится в состоянии деполяризации, то тормозной медиатор вызывает гиперполяризацию, в то время как на фоне гиперполяризации постсинаптической мембраны он вызывает ее деполяризацию.
Пресинаптическое торможение (лат. praе -впереди чего-либо + греч. sunapsis соприкосновение, соединение) - частный случай синаптических тормозных процессов, проявляющихся в подавлении активности нейрона в результате уменьшения эффективности действия возбуждающих синапсов еще на пресинаптическом звене путем угнетения процесса высвобождения медиатора возбуждающими нервными окончаниями. В этом случае свойства постсинаптической мембраны не подвергаются каким-либо изменениям. Пресинаптическое торможение осуществляется посредством специальных тормозных интернейронов. Его структурной основой являются аксо-аксональные синапсы, образованные терминалиями аксонов тормозных интернейронов и аксональными окончаниями возбуждающих нейронов.
При этом окончание аксона тормозного нейрона является пресимпатическим по отношению к терминали возбуждающего нейрона, которая оказывается постсинаптической по отношению к тормозному окончанию и пресинаптической по отношению к активируемой им нервной клетки. В окончаниях пресинаптического тормозного аксона освобождается медиатор, который вызывает деполяризацию возбуждающих окончаний за счет увеличения проницаемости их мембраны для CI. Деполяризация вызывает уменьшение амплитуды потенциала действия, приходящего в возбуждающее окончание аксона. В результате происходит угнетение процесса высвобождения медиатора возбуждающими нервными окончаниями и снижение амплитуды возбуждающего постсинаптического потенциала.
Характерной особенностью пресинаптической деполяризации является замедленное развитие и большая длительность (несколько сотен миллисекунд), даже после одиночного афферентного импульса.
Пресинаптическое торможение существенно отличается от постсинаптического и в фармакологическом отношении. Стрихнин и столбнячный токсин не влияют на его течение. Однако наркотизирующие вещества (хлоралоза, нембутал) значительно усиливают и удлиняют пресинаптическое торможение. Этот вид торможения обнаружен в различных отделах цнс. Наиболее часто оно выявляется в структурах мозгового ствола и спинного мозга. В первых исследованиях механизмов пресинаптического торможения считалось, что тормозное действие осуществляется в точке, отдаленной от сомы нейрона, поэтому его называли "отдаленным” торможением.
Функциональное значение пресинаптического торможения, охватывающего пресинаптические терминали, по которым поступают афферентные импульсы, заключается в ограничении поступления к нервным центрам афферентной импульсации. Пресинаптическое торможение в первую очередь блокирует слабые асинхронные афферентные сигналы и пропускает более сильные, следовательно, оно служит механизмом выделения, вычленения более интенсивных афферентных импульсов из общего потока. Это имеет огромное приспособительное значение для организма, так как из всех афферентных сигналов, идущих к нервным центрам, выделяются самые главные, самые необходимые для данного конкретного времени. Благодаря этому нервные центры, нервная система в целом освобождается от переработки менее существенной информации.
Вторичное торможение- торможение осуществляющееся теми же нервными структурами, в которых происходит возбуждение. Этот нервный процесс подробно изложен в работах Н.Е. Введенского (1886, 1901г.г.).
Торможение реципрокное (лат. reciprocus - взаимный) - нервный процесс, основанный на том, что одни и те же афферентные пути, через которые осуществляется возбуждение одной группы нервных клеток, обеспечивают через посредство вставочных нейронов торможение других групп клеток. Реципрокные отношения возбуждения и торможения в цнс были открыты и продемонстрированы Н.Е. Введенским: раздражение кожи на задней лапке у лягушки вызывает ее сгибание и торможение сгибания или разгибания на противоположной стороне. Взаимодействие возбуждения и торможения является общим свойством всей нервной системы и обнаруживается как в головном, так и в спинном мозге. Экспериментально доказано, что нормальное выполнение каждого естественного двигательного акта основано на взаимодействии возбуждения и торможения на одних и тех же нейронах цнс.
Общее центральное торможение - нервный процесс, развивающийся при любой рефлекторной деятельности и захватывавающий почти всю цнс, включая центры головного мозга. Общее центральное торможение обычно проявляется раньше возникновения какой-либо двигательной реакции. Оно может проявляться при такой малой силе раздражения при которой двигательный эффект отсутствует. Такого вида торможение было впервые описано И.С. Беритовым (1937). Оно обеспечивает концентрацию возбуждения других рефлекторных или поведенческих актов, которые могли бы возникнуть под влиянием раздражений. Важная роль в создании общего центрального торможения принадлежит желатинозной субстанции спинного мозга.
При электрическом раздражении желатинозной субстанции у спинального препарата кошки происходит общее торможение рефлекторных реакций, вызываемых раздражением сенсорных нервов. Общее торможение является важным фактором в создании целостной поведенческой деятельности животных, а также в обеспечении избирательного возбуждения определенных рабочих органов.
Парабиотическое торможение развивается при патологических состояниях, когда лабильность структур центральной нервной системы снижается или происходит очень массивное одновременное возбуждение большого числа афферентных путей, как, например, при травматическом шоке.
Некоторые исследователи выделяют еще один вид торможения - торможение вслед за возбуждением. Оно развивается в нейронах после окончания возбуждения в результате сильной следовой гиперполяризации мембраны (постсинаптической).
42.
Дивергенция и конвергенция: способность нейрона устанавливать многочисленные синаптические связи с различными нервными клетками в пределах одного или разных нервных центров называется дивергенцией. Например, центральные окончания аксонов первичного афферентного нейрона образуют синапсы на многих вставочных нейронах. Благодаря этому одна и та же нервная клетка может участвовать в различных нервных реакциях и контролировать большое число других нейронов, что приводит к иррадиации возбуждения.
Схождение различных путей проведения нервных импульсов к одному и тому же нейрону получило название конвергенции. Простейшим примером конвергенции является замыкание на одном двигательном нейроне импульсов от нескольких афферентных (чувствительных) нейронов. В ЦНС большинство нейронов получают информацию от разных источников благодаря конвергенции. Это обеспечивает пространственную суммацию импульсов и усиление конечного эффекта.
Явление конвергенции было описано Ч. Шеррингтоном и получило название воронки Шеррингтона, или эффекта общего конечного пути. Данный принцип показывает, как при активации различных нервных структур формируется конечная реакция, что имеет первостепенное значение для анализа рефлекторной деятельности;
43.
Иррадиация: при возбуждении нервного центра нервные импульсы распространяются на соседние центры и приводят их в деятельное состояние. Это явление получило название иррадиации. Степень иррадиации зависит от количества вставочных нейронов, степени их миелинизации, силы раздражителя. Со временем в результате афферентной стимуляции только одного нервного центра зона иррадиации уменьшается, происходит переход к процессу концентрации, т.е. ограничению возбуждения только в одном нервном центре. Это является следствием уменьшения синтеза медиаторов во вставочных нейронах, в результате чего биотоки не передаются из данного нервного центра на соседние (рис. 7 и 8).

Рис. 7. Процесс иррадиации возбуждения в нервных центрах: 1, 2, 3 — нервные центры
Рис. 8. Процесс концентрации возбуждения в нервном центре
Выражением данного процесса является точная координированная двигательная реакция в ответ на раздражение рецептивного поля. Формирование любых навыков (трудовых, спортивных и т.д.) обусловлено тренировкой двигательных центров, основу которых составляет переход от процесса иррадиации к концентрации;
44.
Принцип общего конечного пути разработан Ч. Шеррингтоном. В основе его лежит явление конвергенции. Согласно этому принципу на одном эфферентном мотонейроне могут образовывать синапсы нескольких афферентных, входящих в несколько рефлекторных дуг. Этот нейрон называется общим конечным путем и участвует в нескольких рефлекторных реакциях. Если взаимодействие этих рефлексов приводит к усилению общей рефлекторной реакции, такие рефлексы называются союзными. Если же между афферентными сигналами происходит борьба за мотонейрон – конечный путь, то антагонистическими. В результате этой борьбы второстепенные рефлексы ослабляются, а жизненно важным освобождается общий конечный путь.
45.
Окклюзия – явление противоположное облегчению. Когда рефлекторная реакция на два или более сверхпороговых раздражителя меньше, чем ответы на их раздельное воздействие. Оно связано с конвергенцией нескольких возбуждающих импульсов на одном нейроне.
46.
Явление центрального облегчения - это усиление рефлекторной реакции при действии ряда последовательных раздражителей или одновременном их воздействии на несколько рецептивных полей. Объясняется явлением суммации в нервных центрах.
47.
Принцип доминанты открыт А.А. Ухтомским. Доминанта – это преобладающий очаг возбуждения в ЦНС, подчиняющий себе другие НЦ. Доминантный центр обеспечивает комплекс рефлексов, которые необходимы в данный момент для достижения определенной цели. При некоторых условиях возникают питьевая, пищевая, оборонительная, половая и др. доминанты. Свойствами доминантного очага являются повышенная возбудимость, стойкость возбуждения, высокая способность к суммации, инертность. Эти свойства обусловлены явлениями облегчения, иррадиации, с одновременным повышением активности вставочных тормозных нейронов, которые тормозят нейроны других центров.
48.
Пластичность нервных центров - это их способность изменять функциональные свойства. При этом центр приобретает возможность выполнять новые функции или восстанавливать старые после повреждения. В основе пластичности НЦ лежит пластичность синапсов и мембран нейронов, которые могут изменять свою молекулярную структуру.
49.
Реципрокная иннервация обнаружена Ч. Шеррингтоном. Это явление торможения одного центра в результате возбуждения другого. Т.е. в этом случае тормозится антагонистический центр. Например, при возбуждении центров сгибания левой ноги, по реципрокному механизму тормозятся центры мышц разгибателей этой же ноги и центры сгибателей правой. В реципрокных взаимоотношениях находятся центры вдоха и выдоха продолговатого мозга, центры сна и бодрствования и т.д.
50.
Обратная афферентация: результаты рефлекторного акта воспринимаются нейронами обратной афферентации и информация от них поступает обратно в нервный центр. Там они сравниваются с параметрами возбуждения и рефлекторная реакция корректируется.