
- •Ферменты. Номенклатура. Классификация ферментов
- •6 Билет
- •3. Пигмент билирубин????
- •3) Молекулярные механизмы патогенеза острого панкреатита.
- •14 Билет
- •2) Функции сосудистого эндотелия, субэндотелия, тромбоцитов.
- •3) Диагностика панкреатита.
- •16 Билет.
- •3 Метаболические механизмы алкоголизма.
- •3) Моногенные заболевания.
- •3) Полиморфизм гена апобелка е, клиническое значение.
- •21 Билет
- •2. Особенности метаболизма и энергетического обмена в клетках поперечно-полосатой мускулатуры и миокарда.
- •2) Характеристика и роль фибриллярных и регуляторных белков в процессе мышечного сокращения. Механизм мышечного сокращения, этапы. Роль ионов кальция в реализации механизма мышечного сокращения.
- •2. Кальцитриол: химическая природа, этапы синтеза, механизм действия, органы-мишени, биологические эффекты. Представление о заболевании «рахит».
- •26 Билет
- •2) Адреналин- химическая природа, органы мишени, биологические эффекты.
- •3) Моноклональные антитела, препараты на их основе против опухолей.
- •27 Билет
- •1. Понятие о процессах катаболизма и анаболизма. Функции клеточного метаболизма. Стадии генерирования энергии по Кребсу.
- •2. Ферментативные системы антирадикальной защиты. Катализируемые реакции.
- •3. Вектор иммуноконъюгата. Вещества, используемые в качестве векторов адресной доставки.
- •2.Типы переваривания*. Функции жкт как пищеварительно-транспортного конвейера*. Функции слюны*. Функции жёлчных кислот*.
- •3.Эпидермальнвй фактор роста и а-фетопротеин : их использование в качестве векторов.
- •1) Биосинтез триацилглицеринов (таг): последовательность реакций, субстраты, ферменты. Особенности синтеза в печени, жировой ткани, энтероцитах. Регуляция процесса.
- •3) Понятие о рекомбинантных днк.
- •2) Неферментативные системы антирадикальной защиты и их физиологическое значение.
- •2. Действие первичных и вторичных продуктов перекисного окисления на мембраны и другие структуры.
- •3. Действие наркотиков. Дофаминовая система.
- •1. Разобщители цпэ.
- •2. Пути обезвреживания аммиака.
- •3. Теломеразная активность.
- •38 Билет
1) Биосинтез триацилглицеринов (таг): последовательность реакций, субстраты, ферменты. Особенности синтеза в печени, жировой ткани, энтероцитах. Регуляция процесса.
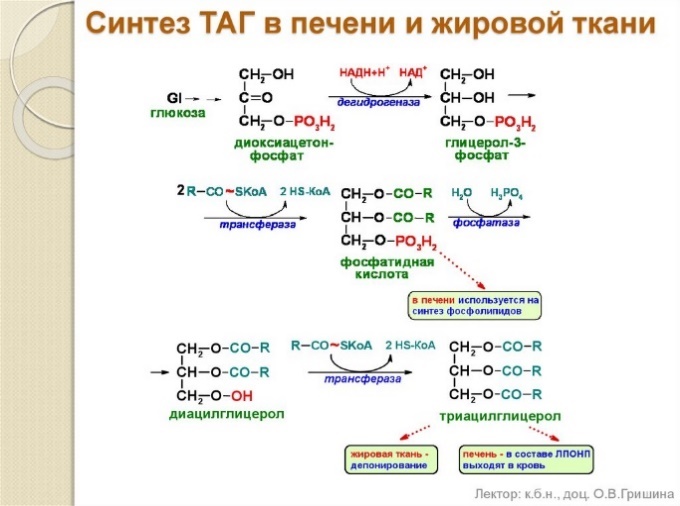 Синтез
ТАГ происходит в абсорбтивный период
в печени и жировой ткани. Но если жировая
ткань – только место депонирования
жира, то печень выполняет важную роль
превращения части углеводов, поступающих
с пищей, в жиры, которые затем секретируются
в кровь в составе ЛПОНП и доставляются
в другие ткани. Непосредственными
субстратами в синтезе жиров являются
ацил-КоА и глицерол-3-фосфат.
Синтез
ТАГ происходит в абсорбтивный период
в печени и жировой ткани. Но если жировая
ткань – только место депонирования
жира, то печень выполняет важную роль
превращения части углеводов, поступающих
с пищей, в жиры, которые затем секретируются
в кровь в составе ЛПОНП и доставляются
в другие ткани. Непосредственными
субстратами в синтезе жиров являются
ацил-КоА и глицерол-3-фосфат.
Печень – основной орган, где идет синтез жирных кислот из продуктов гликолиза. В гладком эндоплазматическом ретикулюме гепатоцитов жирные кислоты активируются и сразу же используются для синтеза ТАГ, взаимодействуя с глицерол-3-фосфатом. Синтезированные жиры упаковываются в ЛПОНП и секретируются в кровь.
В жировой ткани для синтеза ТАГ используются в основном жирные кислоты, освободившиеся при гидролизе жиров ХМ и ЛПОНП. Жирные кислоты поступают в адипоциты, превращаются в производные КоА и взаимодействуют с глицерол-3-фосфатом. Кроме жирных кислот, поступающих в адипоциты из крови, в этих клетках идет и синтез жирных кислот из продуктов распада глюкозы. Молекулы ТАГ в адипоцитах объединяются в крупные жировые капли, не содержащие воды, и поэтому являются наиболее компактной формой хранения топливных молекул.
** В абсорбтивный период при увеличении соотношения инсулин/глюкагон активируется синтез ТАГ в печени. В жировой ткани индуцируется синтез липопротенлипазы (ЛПЛ), т.е в этот период активируется поступление жирных кислот в адипоциты. Одновременно инсулин активирует белки-переносчики глюкозы – ГЛЮТ-4, что ведет к увеличению поступления глюкозы в адипоциты и активации там гликолиза. В результате образуются необходимые для синтеза жиров глицерол-3-фосфат и активированные жирные кислоты. В печени в результате действия инсулина увеличивается количество и активность регуляторных ферментов гликолиза, пируватдегидрогеназного комплекса, а также ферментов, участвующих в синтезе жирных кислот из ацетил-КоА. Итогом этих изменений является увеличение синтеза ТАГ и секреция их в кровь в составе ЛПОНП. ЛПОНП доставляют жиры в капилляры жировой ткани, где действие ЛПЛ обеспечивает быстрое поступление жирных кислот в адипоциты, где они депонируются в составе ТАГ.
Мобилизация жиров, т.е. гидролиз до глицерола и жирных кислот, происходит в постабсорбтивный период, при голодании и активной физической работе. Процесс осуществляется под действием гормончувствительной ТАГ-липазы. Этот фермент отщепляет одну жирную кислоту у первого углеродного атома глицерола с образованием диацилглицерола, а затем другие липазы гидролизуют его до глицерола и жирных кислот, которые поступают в кровь. Глицерол как водорастворимое вещество транспортируется кровью в свободном виде, а жирные кислоты – в комплексе с белком плазмы альбумином.
2) Химический состав мочи: органические и неорганические компоненты мочи в норме и их происхождение. Патологические компоненты мочи и их происхождение. Клиническое значение биохимического анализа мочи.
Основной компонент мочи — это вода (1-2 л/сут), в которой растворен сухой остаток (60 г/сут). Сухой остаток представлен органическими и неорганическими соединениями.
Химический состав мочи может изменяться при различных патологиях, определение этих изменений может иметь диагностическое значение. Мочевина выделяется с мочой от 12 до 36 г/сут. Увеличение наблюдается при белковой диете, при ускоренном распаде белков в результате голодания, при ожогах, травмах, лихорадке, опухолях, гипертиреозе, диабете. Снижается при тяжелых поражениях печени, нарушении фильтрации плазмы в клубочках почек, при избытке инсулина. Креатинин. У мужчин около 1-2 г/сут. У женщин 0,8-1,8г/сут. Выделение отражает мышечную массу и скорость почечного кровотока.
Аминокислоты выделяются с мочой около 1,1г/сут. Среди них преобладает глицин, и гистидин, немного меньше глутамина, аланина и серина. Рост их содержания наблюдается при наследственных и приобретенных нарушениях обмена АК, заболеваниях паренхимы печени, при тяжелых инфекционных заболеваниях, опухолях, травмах, миопатии, коме, гипертиреозе, при нефротическом синдроме.
Молочная, пировиноградная, щавелевая, янтарная, уксусная, пропионовая, валериановая и другие кислоты. Их выделение с мочой не превышает 1г/сут. Увеличение их концентрации наблюдается при интенсивной мышечной нагрузке, гипоксии, сахарном диабете, голодании. Мочевая кислота (0,2-1,2г/сут). Содержание в моче растет при употреблении пищи, богатой нуклеотидами, при лейкемии, гепатитах, подагре, полицитемии, избытке стероидов.
Гиппуровая кислота выделяется с мочой около 0,7г/сут. Образуется при соединении глицина и бензойной кислоты. Повышается приупотреблении растительной пищи. Аммонийные соли выделяются с мочой около 1г/сут. Их количество повышается при ацидозах, снижается при алкалозах и поражениях дистальных канальцев, где протекают процессы аммониогенеза.
Минеральные соли (5-7 г/сут). Моча содержит натрий (3-6г/сут), хлор (3,6-9г/сут), калий (1,5-3,2г/сут), кальций (0,1-0,25г/сут), магний (0,1-0,2г/сут), неорганический фосфор (0,9-1,3г/сут), сульфаты (1,8 г/сут).
Выделение NaCl(норма 8-15г/сут) снижается при хронических нефритах, диарее, остром суставном ревматизме. Выведение NaC lувеличивается при введении гипертонических растворов.
Уровень бикарбонатов в моче повышается при алкалозе, снижается при ацидозе. Выделение фосфатов возрастает при ацидозе, гиперфункции паращитовидной железы, снижается при избытке витамина Д3. С мочой из организма выделяются различные ядовитые вещества, после их обезвреживания в печени путем конъюгации с серной или глюкуроновой кислотами.
Патологические компоненты мочи. Протеинурия (наличие белка в моче) наблюдается после тяжелой физической работы, при нефритах, гломерулонефритах, нефротическом синдроме, амилоидозе, острых инфекциях, отравлениях и т д. Патологическая глюкозурия - при сахарном диабете, почечном диабете, избытке стероидов, остром панкреатите, отравлении морфином, стрихнином, фосфором, хлороформом. Кетонурия (наличие кетоновых тел в моче) появляется при сахарном диабете, голодании, кахексии, гиперинсулинизме, тиреотоксикозах, послеоперационный период, гликогенозах (I,II,IV), акромегалиях, инфекциях, интоксикациях. Гемоглобинурия появляется после переохлаждении, при гемолитических анемиях, при сепсисе, ожогах, отравлениях сульфаниламидами, ядами грибов. Гематурия появляется при остром нефрите, гломерулонефрите, пиелонефрите мочекаменной болезни, циститах, инфаркте почек, ишемии почек, опухоли почек, амилоидозе почек, аденоме простаты, лихорадке.
