
- •Общая фармакология
- •Предмет и задачи фармакологии. Место ее среди других медицинских и биологических дисциплин
- •Основные исторические этапы развития отечественной фармакологии. Работы и.П.Павлова, н.П. Кравкова, м.Н. Николаева, н.В. Вершинина, а.И. Черкеса, и.С. Цитовича, с.В.Аничкова, в.В. Закусова.
- •Определение понятий лекарственное средство (лекарство), лекарственное вещество, лекарственный препарат, лекарственная форма, лекарственное сырье. Что такое пролекарство?
- •Что такое фармакокинетика лекарственных веществ? Основные фармакокинетические параметры (период полувыведения, объем распределения, клиренс).
- •Какие физико-химические факторы определяют проникновение лекарственных веществ через биологические мембраны? Пассивный и активный транспорт, фильтрация. Ускоренная или обменная диффузия.
- •Характеристика путей введения и поступления лекарственных веществ в организм. Примеры различий всасывания лекарственных веществ. Биодоступность лекарств. Ее зависимость от рН среды и рК лекарства
- •Особенности метаболизма лекарственных веществ у новорожденных и грудных детей. Экскреция лекарственных веществ, пути выведения лекарственных препаратов.
- •Явления, наблюдаемые при повторном применении лекарственных средств: кумуляция, привыкание, пристрастие, тахифилаксия, сенсибилизация.
- •Комбинированное действие лекарственных веществ: синергизм и его виды (суммированный, потенцированный, физиологический), примеры.
- •Антагонизм и его виды: физико-химический, химический, конкурентный, физиологический, одно- и двусторонний; примеры. Понятие о синерго-антагонизме, примеры.
- •Значение индивидуальных особенностей организма и его состояния для проявления действия лекарственных средств (возраст, пол, генетический фактор, суточные ритмы).
- •Виды лекарственной терапии: этиотропная, патогенетическая, симптоматическая, профилактическая, заместительная.
- •Взаимодействие лекарственных веществ в организме, классификация. Понятие фармакологического и фармацевтического взаимодействия. Примеры.
- •Общие принципы лечения острых отравлений лекарственными средствами.
- •Средства, влияющие на афферентную иннервацию
- •Нейротропные средства
- •Структура и функционирование холинергического синапса. Структура холинергического рецептора. Классификация и локализация холинергических рецепторов.
- •Классификация лекарственных веществ, действующих на холинергическую иннервацию. М- , н-холиномиметики. Вещества. Механизм действия, фармакологические эффекты.
- •Соединения группы атропина. Механизм действия. Фармакологические эффекты. Сравнительная характеристика препаратов группы атропина.
- •Синтетические холиноблокирующие вещества. Препараты. Фармакологические эффекты, показания и противопоказания к применению. Сравнительная характеристика.
- •Центральные холиноблокаторы. Препараты. Фармакологические эффекты. Особые показания и противопоказания к применению. Сравнительная характеристика.
- •Структура адренергического синапса и адренорецепторов. Синтез, депонирование, выделение и обратный захват медиатора.
- •Адреналин и норадреналин. Химическое строение. Механизм действия. Фармакологические эффекты, показания к применению, противопоказания. Побочные эффекты.
- •Бета-адреноблокаторы. Классификация. Препараты. Механизм формирования основных фармакологических эффектов. Показания к применению, противопоказания. Побочные эффекты.
- •Средства, влияющие на функции цнс
- •По количеству используемых препаратов
- •По применению на разных этапах операции
- •По факторам, влияющим на цнс
- •По способу введения препарата
- •Стадия анальгезии
- •Стадия возбуждения
- •Стадия хирургического наркоза
- •IV. Агональная стадия
- •Спирт этиловый. Действие на цнс, жкт, ссс, печень. Применение в медицинской практике. Острое отравление этиловым спиртом. Меры помощи. Хронический алкоголизм. Лечение.
- •Принципы организации и строения системы проведения и регуляции боли. Опиатные рецепторы и их эндогенные лиганды. Возможные механизмы опиоидной анальгезии.
- •Опиоидные анальгетики. Определение.Классификация. Основные показания к клиническому применению опиоидных анальгетиков. Ограничения, противопоказания и возможные осложнения.
- •Природные опиоиды-агонисты. Сравнительная характеристика. Морфин. Основные эффекты. Особенности клинического применения.
- •Транквилизаторы (анксиолитики). Определение группы. Основные фармакологические эффекты. Механизм действия. Основное клиническое применение
- •Анксиолитики, производные бензодиазепинов. Возможные механизмы действия. Характеристика представителей этой группы. Клиническое применение, противопоказания. Побочные эффекты.
- •Анксиолитики, производные других химических групп. Возможные механизмы действия. Характеристика представителей этой группы. Клиническое применение, противопоказания. Побочные эффекты.
- •Антидепрессанты. Определения группы. Современная классификация. Основные фармакологические эффекты. Возможные механизмы действия. Показания к клиническому применению.
- •Антидепрессанты-ингибиторы обратного нейронального захвата. Классификация. Особенности механизмы действия. Показания к клиническому применению.
- •Антидепрессанты-ингибиторы моноамнооксидазы (мао). Классификация. Особенности механизмы действия. Показания к клиническому применению. Токсичность.
- •2.Ингибиторы мао обратимого и избирательного действия:
- •Особенности применения антидепрессантов в клинике психиатрии и в соматической медицине. Взаимодействие с другими лекарственными веществами.
- •Средства, влияющие на процессы тканевого обмена
- •Гормональные препараты. Источники получения. Виды гормонотерапии. Препараты гормонов гипоталамуса. Применение.
- •Препараты гормонов гипофиза. Механизм действия, фармакологические эффекты. Показания к применению. Побочные эффекты.
- •Препараты гормонов щитовидной железы. Антитиреоидные средства. Кальцитонин. Их применение.
- •Антитиреоидные средства
- •Препараты иодидов - Тиреостатическое действие связано с перегрузкой клеток щ/ж йодом, при которой его концентрация внутри клетки превышает внеклеточную более чем в 1.000 раз.
- •Препараты гормонов поджелудочной железы. Инсулин. Влияние на обмен. Получение, методы очистки. Препараты инсулина. Дозирование. Применение. Побочные эффекты. Понятие толерантности к инсулину.
- •Инсулин
- •Синтетические антидиабетические средства. Механизм действия. Основные группы. Препараты. Применение. Побочные эффекты.
- •Сульфаниламиды
- •4) Гкс для местного применения
- •5) Гкс для ингаляционного применения
- •Преднизолон
- •Метилпреднизолона ацепонат
- •Дексаметазон (дексазон)
- •Триамцинолон (полкортолон)
- •Известны и антагонисты глюкокортикоидов.
- •Минералокортикоиды. Влияние на обмен. Препараты. Применение. Антагонисты минералокортикоидов.
- •Существуют антагонисты минералокортикоидов.
- •Препараты половых гормонов. Препараты женских половых гормонов. Эстрогенные и антиэстрогенные препараты. Гестагенные и антигестагенные препараты.
- •А) Эстрогенные и антиэстрогенные препараты
- •Б) Гестагенные (прогестагенные) и антигестагенные препараты
- •Прогестерон
- •Прегнин (этистерон)
- •Противозачаточные (контрацептивные) средства для энтерального применения. Механизм действия. Показания и противопоказания к применению.
- •Препараты гормонов мужских половых желез (андрогены) и антиандрогенные средства. Препараты, механизм действия. Показания и противопоказания к применению. Побочные реакции.
- •Ципротерона ацетат
- •Анаболические стероиды. Препараты. Механизм действия. Показания и противопоказания к применению. Побочные реакции.
- •Витамин е. Препараты. Суточная потребность. Фармакодинамика и фармакокинетика. Применение витамина е с профилактической и лечебной целями.
- •Нестероидные противовоспалительные средства - производные салициловой и антраниловой кислот. Основные фармакодинамические эффекты. Показания и противопоказания к применению. Побочные эффекты.
- •Нестероидные противовоспалительные средства - производные пиразолона и оксикамов. Основные фармакодинамические эффекты. Показания и противопоказания к применению. Побочные эффекты.
- •Нестероидные противовоспалительные средства – производные индолуксусной, фенилуксусной и нафтилпропионовой кислот. Показания и противопоказания к применению. Побочные эффекты.
- •Средства, влияющие на функции исполнительных органов
- •Антигипертензивные средства. Классификация. Механизм действия, фармакодинамика, фармакокинетика, показания к применению и побочные эффекты средств, понижающих тонус вазомоторных центров.
- •Локализации действия в области нефрона:
- •По влиянию на обмен ионов калия:
- •3) По влиянию на кислотно-щелочное равновесие:
- •Умеренные салуретики. Механизм действия и эффекты тиазидных и тиазидоподобных диуретиков. Показания к клиническому применению. Побочные эффекты и противопоказания.
- •Слабые салуретики (диакарб, эуфиллин). Механизмы действия. Особенности фармакодинаики. Показания к клиническому применению. Побочные эффекты и противопоказания.
- •Калийсберегающие диуретики. Механизмы действия и фармакологические эффекты. Показания к клиническому применению. Побочные эффекты и противопоказания.
- •Осмотические диуретики. Отличительные особенности фармакодинамики и фармакокинетики. Показания к клиническому применению. Побочные эффекты и противопоказания.
- •Аналептики и стимуляторы дыхания. Определение понятия и классификация. Возможные механизмы действия. Характеристика препаратов. Клиническое применение. Побочные эффекты.
- •Противокашлевые и отхаркивающие средства. Характеристика препаратов. Клиническое применение. Предосторожности при применении средств центрального действия. Муколитические средства.
- •Средства применяемые при отеке легких. Характеристика основных групп препаратов: их механизм действия и фармакодинамика при отеке легких.
- •Средства, влияющие на аппетит: стимулирующие и снижающие (анорексигенные). Классификация анорексигенных средств. Показания и противопоказания к применению.
- •Средства, применяемые при нарушении функции желудка. Средства, усиливающие секрецию желез желудка. Средства заместительной терапии.
- •Средства, понижающие секрецию желез желудка. Основные группы препаратов и их механизм действия. Показания и противопоказания к применению.
- •Антацидные средства. Понятие о системных и несистемных антацидах.
- •Гастропротекторы, деление на группы, характеристика препаратов. Показания и противопоказания к применению.
- •Рвотные и противорвотные средства. Препараты. Показания и противопоказания к применению.
- •Желчегонные средства, деление на группы по механизму действия. Препараты. Показания и противопоказания к применению. Гепатопротекторы. Препараты. Показания к применению.
- •Средства, влияющие на функции поджелудочной железы: стимуляторы секреции (секретин, холецистокинин), средства заместительной терапии (панкреатин), средства угнетающие секрецию (контрикал).
- •Прокоагулянты. Классификация. Фармакологические эффекты. Механизм действия. Показания и противопоказания к применению. Побочные эффекты. Передозировка антикоагулянтов – симптоматика, лечение.
- •Стимуляторы фибринолиза. Классификация. Механизм действия. Сравнительная характеристика основных фибринолитических средств. Показания и противопоказания к применению. Побочное действие.
- •Ингибиторы фибринолиза. Препараты. Механизм действия. Показания и противопоказания к применению. Побочные эффекты.
- •Стимуляторы эритропоэза. Средства, применяемые при гиперхромных анемиях. Механизм действия, фармакодинамические свойства. Показания и противопоказания к применению. Побочные реакции.
- •Стимуляторы лейкопоэза. Препараты. Механизм действия. Показания и противопоказания к применению. Побочные эффекты.
- •Химиотерапевтические средства
- •Антисептические и дезинфицирующие средства (противомикробные средства неизбирательного действия). Классификация. Основные механизмы действия препаратов по группам. Их применение.
- •Бета-лактамные антибиотики, полусинтетические пенициллины. Классификация, механизм действия. Спектр противомикробной активности. Показания к применению. Побочное действие пенициллинов.
- •Бета-лактамные антибиотики. Цефалоспорины. Классификация. Механизм действия. Спектр противомикробной активности по поколениям. Применение. Побочные эффекты.
- •Бета-лактамные антибиотики: карбапенемы и монобактамы. Препараты, механизм действия, спектр активности. Применение. Побочные эффекты. Тиенам (циластатин).
- •Комбинированные пенициллины. Принципы комбинации. Особенности действия. Применение. Возможные побочные эффекты.
- •Макролиды. Классификация. Механизм действия. Спектр противомикробной активности по группам.Особенности азалидов (новые макролиды). Применение. Побочные эффекты.
- •Препараты биосинтетических и полусинтетических тетрациклинов. Механизм действия и спектр противомикробной активности. Особенности фармакокинетики. Применение. Побочные эффекты
- •Гликопептиды. Препараты. Механизм действия. Применение. Побочные эффекты
- •Левомицетин. Механизм действия и особенности фармакокинетики. Спектр противомикробной активности. Применение. Побочные эффекты.
- •Антибиотики группы линкозамидов. Механизм действия. Спектр активности (дать отличия в группе). Применение. Побочные эффекты.
- •Полимиксины. Препараты. Механизм действия. Спектр противомикробной активности. Фармакокинетика. Показания к применению. Побочные эффекты.
- •Производные хинолонкарбоновой кислоты: группа налидиксовой кислоты, палина и фторхинолоны. Механизмы действия, спектр активности, особенности фармакокинетики. Побочные эффекты.
- •Производные нитрофурана. Механизм действия. Спектр противомикробной активности. Особенности фармакокинетики. Возможные побочные эффекты.
- •Синтетические антибактериальные средства из группы 8-оксихинолинов и хиноксалина. Спектр активности. Клиническое применение. Побочные эффекты.
- •Антибактериальные препараты – производные имидазола. Особенности механизма действия. Спектр активности. Клиническое применение. Побочные эффекты.
- •Вещества противосифилитического действия. Группы препаратов. Преимущества и недостатки препаратов каждой группы. Побочные эффекты.
- •Противотуберкулезные средства II и III групп. Препараты. Механизм туберкулостатического действия. Показания к применению. Побочные эффекты.
- •Противовирусные препараты. Классификация по влиянию на этапы репродукции вируса. Интерфероны: препараты, механизм действия, клиническое применение. Понятие об интерфероногенах.
- •Противовирусные средства, нарушающие синтез ранних вирусных белков и нуклеозидов. Особенности механизма действия, обеспечивающие избирательность, клиническое применение. Побочные эффекты.
- •Средства для лечения вич-инфекции: механизм действия, применение, возможные побочные эффекты.
- •Средства применяемые при лечении амебиаза. Классификация по направленности действия на амебиаз различной локализации. Характеристика препаратов.
- •Средства применяемые при лечении лямблиоза, трихомонадоза, токсоплазмоза, лейшманиозов.
- •Средства для лечения микозов. Классификация по химической природе и клиническому применению. Механизм действия полиеновых антибиотиков. Препараты. Особенности фармакокинетики. Побочные эффекты.
- •Средства для резорбтивного и местного лечения дерматомикозов. Механизм действия производных имидазола. Препараты. Побочные эффекты. Тербинафин. Особенности применения.
- •Средства для лечения кандидомикозов. Препараты полиеновых антибиотиков, макролидов, производных имидазола. Особенности применения.
- •Противоглистные (антигельминтные) средства. Деление на группы по механизму действия. Средства применяемые для лечения кишечных и внекишечных гельминтозов. Возможные побочные реакции.
- •Алкилирующие противоопухолевые средства. Классификация по химическому строению. Механизм действия. Спектр действия. Побочные реакции.
- •Противоопухолевые средства группы антиметаболитов и антибиотиков с противоопухолевой активностью. Препараты. Возможные механизмы действия. Спектр действия. Побочные реакции.
Опиоидные анальгетики. Определение.Классификация. Основные показания к клиническому применению опиоидных анальгетиков. Ограничения, противопоказания и возможные осложнения.
Опиоидными анальгетиками называют ЛС, которые оказывают центральное, дозазависимое, обратимое анальгетическое действие без выключения сознания. Они избирательно подавляют боль, повышают ее переносимость, уменьшают эмоциональную окраску и вегетативное сопровождение боли. К опиоидным анальгетикам относят опиаты и собственно опиоиды.
Опиатами – называют анальгетики на основе природных алкалоидов мака снотворного и их полусинтетические производные. Опиоидами – называют синтетические соединения, имитирующие действие морфина.
Классификация опиоидных анальгетиков по происхождению:
Опий - высушенный млечный сок из надрезов недозревших коробочек снотворного мака - Papaver Somniferum. алколоиды опия: а) фенантренового ряда (морфин, кодеин, тебаин) - вызывают обезболивающий эффект б) изохинолинового ряда (папаверин, наркотин, нарцеин) – вызывают спазмолитический эффект.
1. галеновые препораты опия - настойка и экстракт. 2. новогаленовый препарат опия- омнопон (содержит все 20 алколоидов опия и очищен от баластных веществ- сапонинов).
3. полусинтетические аналоги морфина (этилморфин, гидрокодон), у которых фенолвивит гидроксил замещен другим радикалом. 4. синтетические заменители морфина 1) фенантрена – морфин, кодеин, гидрокодон, нальбуфин, бупренорфин, налорфин, налоксон, налтрексон 2) фенилпиперидина – промедол, фентанил, суфентанил, альфентфнил 3) фенилгептиламина – метадон, проксифен 4) морфина - леворфанол , буторфанол, леваллорфан 5) бензоморфина - пентазоцин
Классификация по принципу взаимодействия опиоидных анальгетиков с опиоидными рецепторами
- Агонисты опиоидных рецепторов - Агонисты-антагонисты опиоидных рецепторов - Частичные агонисты опиоидных рецепторов - Антагонисты опиоидных рецепторов
Агонисты опиоидных рецепторов
- Морфина гидрохлорид - Морфилонг - Кодеин - Омнопон - Тримепиридин (промедол) - Фентанил - Суфентанил - Алфентанил - Пиритрамид
Агонисты-антагонисты опиоидных рецепторов
- Буторфанол - Налбуфин - Пентазоцин - Налорфин - Лоперамид
Частичные агонисты опиоидных рецепторов - Бупренорфин
Антагонисты опиоидных рецепторов
- Налоксон - Налтрексон
Природные опиоиды-агонисты. Сравнительная характеристика. Морфин. Основные эффекты. Особенности клинического применения.
Морфина гидрохлорид -Хлористоводородная соль природного алкалоида, содержащегося в опии (до 10%), которая представляет собой застывший на воздухе млечный сок, вытекающий из надрезов головок сонного мака. Морфин связывается с μ - и κ -рецепторами опиоидных пептидов и стимулирует их. В итоге повышается активность антиноцицептивной системы и усиливаются ее тормозящие влияния на функции ноцицептивной системы. Активация опиоидных рецепторов на мембране нейронов ноцицептивной системы приводит к повышению активности аденилатциклазы и образованию в клетке цАМФ. Под действием цАМФ-зависимых протеинкиназ происходит инактивация кальциевых каналов и открытие калиевых каналов.
Нарушение поступления ионов Ca через пресинаптическую мембрану снижает выделение медиаторов и затрудняет передачу импульсов в синапсах ноцицептивной системы. Нарушение поступления ионов Ca через постсинаптическую мембрану, в сочетании с выходом ионов K приводит к гиперполяризации мембраны и снижению возбудимости нейронов (затруднению восприятия импульсов).
Угнетение процесса межнейроной передачи болевых импульсов центральной части нервного пути 1. Стимуляция пресинаптических ОР Блокируются кальциевые каналы Уменьшается выделение медиаторов передающих боль (субстанция Р, глютамат, нейрокининов) 2.Стимуляция постсинаптических ОР Активируются калиевые каналы Развивается гиперполяризация постсинаптической мембраны, что препятствует действию медиаторов Нарушается передача болевых импульсов в высшие центры (таламус – коллектор боли). 3. Супраспинальное действие — стимуляция ОР в нейронах антиноцицептивной системы — активация. Центральные эффекты морфина:
- Анальгетический эффект. Ослабляет чувство боли, изменяет восприятие боли. В итоге, человек лучше переносит боль, они становится менее дискомфортной для него. Связывают с его влиянием на процесс передачи импульсов на спинальном и супраспинальном уровнях, а также со снижением активности периферических ноцицепторов. Эффект сохраняется 4-5 часов.
- Седативный эффект. Оказывает общеуспокаивающее действие, снижает активность психических процессов, двигательную активность. Постепенно переходит в чуткий, поверхностный, богатый яркими приятными сновидениями сон.
- Эйфория. Возникает только в том случае, если морфин поступает в организм с высокой скоростью и исходное состояние человека близко к комфортному. Эйфория характеризуется иллюзорным восприятием окружающей действительности. Возникает койнестопатия (исчезновение ощущения своего тела, «невесомость»), мория (патологически повышенное настроение со склонностью к дурашливости, неуместным шуткам). Внизу живота, в области промежности и половых органов возникают ощущения близкие к оргазму.
- Противокашлевой эффект – связан с угнетением кашлевого центра под влиянием морфина.
- Миоз (сужение зрачка). Возникает за счет стимуляции ядра глазодвигательного нерва и увеличения тем самым парасимпатических влияний на глаз. Зрачок под влиянием морфина может достигать размера булавочной головки. - Эндокринологические эффекты. Усиливает секрецию пролактина, СТГ и АДГ, понижает выделение кортико- и гонадолиберинов (что вызывает снижение содержания в крови уровней АКТГ, ФСГ, ЛГ, кортизола, эстрогенов и прогестерона, тестостерона). - В высоких дозах морфин тормозит термоустановочный центр гипоталамуса и несколько снижает температуру тела. - Влияние на рвотный центр. Морфин, связываясь с опиоидными рецепторами рвотного центра вызывает его торможение, но в то же время, морфин способен активировать дофаминовые D2-рецепторы триггерной зоны рвотного центра, которые оказывают на него стимулирующее действие. Поскольку триггерная зона лежит кнаружи от ГЭБ, то она активируется раньше, чем начнется торможение рвотного центра, поэтому при первом введении морфина (у 20-40% пациентов) может возникать тошнота и рвота, которая сменяется быстрым угнетением рвотного рефлекса. - Морфин повышает тонус мышц и усиливает рефлексы, которые замыкаются на уровне спинного мозга. Это связано с выключением тормозящих влияний на спинной мозг ретикулярной фармации головного мозга.
Влияние на ЦНС Морфин оказывает мозаичное влияние на различные функции ЦНС. Это проявляется угнетающим действием в отношении отдельных центров и стимулирующим в отношении других центров.
Угнетающее действие морфина - Дыхательного центра (снижение чувствительности к СО2) - Центра кашлевого рефлекса - Гипоталамического центра теплопродукции (снижение основного обмена, гипотермия) - Сосудодвигательного центра (при передозировке, возможна ортостатическая гипотензия, дополнительно связанная с высвобождением гистамина) - Десинхронизирующих структур мозга (гипно – седативное действие)
|
Стимулирующее действие морфина - Некоторых эмоциогенных зон лимбической системы (эйфория) - Центров глазодвигательного нерва (миоз – важный диагностический признак, свидетельствующий о применении морфиноподобных анальгетиков - В отношении этого эффекта практически не развивается толерантность) - Центров блуждающего нерва (брадикардия, увеличение тонуса гладкой мускулатуры внутренних органов) - Вазопрессин – содержащих нейронов паравентрикулярного гипоталамуса (усиление секреции вазопрессина – снижение диуреза) - Специальных центров, управляющих тонусом скелетной мускулатуры (ригидность, мышц туловища) |
Периферические эффекты морфина:
- Влияние на ССС. Морфин стимулирует ядра блуждающего нерва (ПСНС), что приводит к возникновению брадикардии. Вызывает расширение сосудов малого круга кровообращения, поэтому при его применении снижается преднагрузка на миокард и давление в сосудах легких. Вызывает дилятацию внутричерепных сосудов и приводит к некоторому повышению внутричерепного давления, поэтому его не рекомендуется применять для обезболивания у лиц с ЧМТ.
- Влияние на дыхательную систему. Морфин вызывает выброс гистамина из тучных клеток, что совместно с повышением тонуса блуждающего нерва может спровоцировать развитие бронхоспазма.
- Влияние на ЖКТ. Обстипационный эффект (запор). Этот эффект связывают с несколькими механизмами. Стимуляция морфином μ -рецепторов кишечника и желудка приводит к угнетению выделения ацетилхолина, PgE2 и нейропептида Y в сплетениях метасимпатической нервной системы кишечника. Эти медиаторы необходимы для обеспечения моторики, их недостаток приводит к повышению тонуса гладких мышц и сфинктеров ЖКТ и сегментации кишечника с исчезновением пропульсивных движений. Кроме того, морфин приводит к снижению секреции кишечного сока и увеличению абсорбции воды из каловых масс. За счет стимуляции ядер блуждающего нерва и прямого действия на гладкие мышцы, морфин повышает тонус моче - и желчевыводящих путей, что может спровоцировать колику у чувствительных лиц.
Показания
1. Болевой синдром при: - Травмах - Инфаркте миокарда (нельзя пентазоцин и буторфанол) - Ожогах - Почечной и печеночной - Онкопатологии (наркотические анальгетики здесь наиболее эффективны, т.к хронические боли у онкобольных во многом зависят от процессов суммации афферентных болевых импульсов в таламусе) - Родах (применяются редко из – за опасности угнетения дыхательного центра у плода, предпочтительно применять тримеперидин)
2. Премедикация (введение в преднаркозный период – потенцирование действия средств для наркоза)
3. Нейролептанальгезия (фентанил, суфентанил, алфентанил)
4. Кашель (предпочтительно кодеин)
5. Сердечная астма и отек легких (иногда используют морфин для подавления дыхательного центра и снижения потребности в кислороде)
Противопоказания: Обезболивание у лиц с ЧМТ. Морфин повышает внутричерепное давление, оказывает седативное действие и вызывает миоз, не позволяя оценить реакцию зрачка на свет. Уровень сознания и реакция зрачка на свет - Обезболивание у пациентов с почечной и печеночной коликой. Повышает тонус желче - и мочевыводящих путей, что может парадоксально усилить колику. Кроме того, заброс желчи при закрытом сфинктере Одди в протоки поджелудочной железы приводит к активации панкреатических ферментов в ткани железы и развитию панкреонекроза.
Нецелесообразно назначать морфин для обезболивания родов, т.к. он вызывает снижение тонуса матки и способствует тем самым удлинению родов. Кроме того, проникая через плаценту морфин приводит к угнетению дыхания у новорожденного ребенка
Нежелательные эффекты
- Угнетение дыхательного центра. Снижает чувствительность дыхательного центра к изменению уровня СО2 и рН крови и поддержание дыхания происходит за счет работы периферических рецепторов каротидных клубочков, возникает дыхание Чейна-Стокса. Вначале дыхание становится редким и глубоким, по мере выведения СО2 дыхание еще более урежается и становится поверхностным, а затем прекращается совсем. Во время паузы происходит накопление СО2 и развитие ацидоза, которые активируют рецепторы каротидных клубочков и дыхание возобновляется постепенно нарастая по глубине. Затем процесс повторяется. При увеличении дозы морфина возможен полный паралич дыхательного центра.
- Толерантность – постепенное ослабление фармакологических эффектов при повторном введении в одной и той же дозе. Для получения прежнего эффекта требуется вводить все большие и большие дозы. Толерантность носит перекрестный характер, т.е. при использовании одного опиоидного анальгетика она развивается ко всем средствам из этой группы. Толерантность никогда не развивается к миотическому, обстипационному эффектам и способности морфина повышать тонус скелетных мышщ.
- Лекарственная зависимость. Морфин вызывает быстрое формирование психической и физической зависимости. Психическая зависимость – непреодолимое, неконтролируемое (компульсивное) стремление к повторным введениям морфина связано с его способностью вызывать эйфорию. При длительном применении вызывает перестройку нейроэндокринных функций и по механизму отрицательной связи тормозит синтез собственных эндогенных опиопептидов. Это приводит к формированию физической зависимости, при которой прекращение регулярного введения в организм морфина вызывает болезненное состояние – синдром лишения или абстинентный синдром.
Абстинентный синдром - проявляется развитием эффектов обратных тем, которые наблюдаются при введении морфина. Возникают тревога, бессонница, сильные мышечные и суставные боли, ринорея, слезотечение, мидриаз, тошнота и рвота, резкие колебания АД, гипертермия с ознобом, дыхание становится учащенным и неритмичным. Возникает через 6-10 часов после выполнения последней инъекции и достигает максимума ко 2 суткам, после чего ослабевает к 5-7 дню.
Острое отравление морфином. Возникает при введении в вену свыше 30 мг морфина (лица с наркотической зависимостью могут переносить инъекции 200-500 мг морфина без каких-либо последствий). Возникает эйфория переходящая в ступор и кому, полная анальгезия, гипотермия, гипотензия. Зрачки резко сужены, наблюдается задержка мочи и запор, дыхание по типу Чейна-Стокса. Смерть наступает от паралича дыхательного центра и острой дыхательной недостаточности. Патогномоничными симптомами морфиновой комы является сочетание миоза, дыхания Чейна-Стокса при сохраненных и даже усиленных сухожильных рефлексах. Меры помощи: ИВЛ с положительным давлением на вдохе. Наиболее критическими являются первые 10-12 часов в течение которых необходимо обеспечить непрерывную ИВЛ. Повторные промывания желудка через зонд взвесью активированного угля и 0,05% раствором KMnO4. Данное мероприятие следует проводить даже в случае парентерального введения морфина, поскольку морфин подвергаясь энтерогепатической циркуляции выделяется через слизистую оболочку ЖКТ, где он может быть окислен перманганатом или связан активированным углем. Ведение антидотов – антагонистов опиоидных рецепторов.
Синтетические опиоиды-агонисты. Классификация. Сравнительная характеристика. Особенности клинического применения и побочные эффекты. СМ выше
Опиоиды агонисты-антагонисты. Сравнительная характеристика. Особенности фармакологической активности. Клиническое применение и возможные побочные эффекты.
СМ выше
Опиоиды-антагонисты. Механизм действия и основные показания к применению. Острое отравление опиоидами, клиническая картина, меры помощи.
СМ выше
Хроническое отравление опиоидами. Механизм возникновения зависимости. Клиника опиоидной наркомании. Лечение. Меры предупреждения наркомании: социальные и медицинские аспекты наркомании.
СМ выше
Снотворные средства. Классификация снотворных средств. Бензодиазепиновые снотворные средства Возможные механизмы действия. Влияние на структуру сна. Особенности их фармакологического действия.
Снотворные средства (гипнотики) - относят вещества, вызывающие сон близкий по структуре к физиологическому, облегчающие процесс засыпания и обеспечивающие необходимую продолжительность и глубину сна Основные требования к снотворным средствам: - должны восстанавливать физиологический или максимально близкий к таковому сон; - метаболизироваться в течение времени сна и не вызывать последующей сонливости и заторможенности (резидуальный эффект); - быть эффективными и безопасными для разных групп больных; - оказывать быстрый эффект; - обеспечивать оптимальную длительность сна; - не должны вызывать развитие зависимости. Идеального препарата не существует, но некоторые средства из новых групп: бензодиазепинов и т.н. Z-группы отвечают этим требованиям.
Нарушения сна
Нарушения сна (гипосомния, инсомния) - патология, проявляющаяся в виде: - Расстройства засыпания; этой формой страдают чаще молодые легко возбудимые и эмоционально-лабильные субъекты; - Укороченный сон или преждевременное пробуждение - чаще встречается у лиц пожилого и старческого возраста;
- Пробуждение ночью или поверхностный сон - встречается в любом возрасте при различных невротических состояниях, а также как синдром при некоторых соматических заболеваниях.
Классификация снотворных средств
- Производные бензодиазепинов: нитразепам, мидозалам, флунитразепам, триазола - Производные барбитуровой кислоты: Барбитал, эстимал, этаминал-натрия - Средства Z-группы: Зопиклон, золпидем, залеплон - Прочие снотворные средства: Рамелтеон, мелотонин, донормин и пр.
Нейрохимические и нейрофизиологические механизмы сна
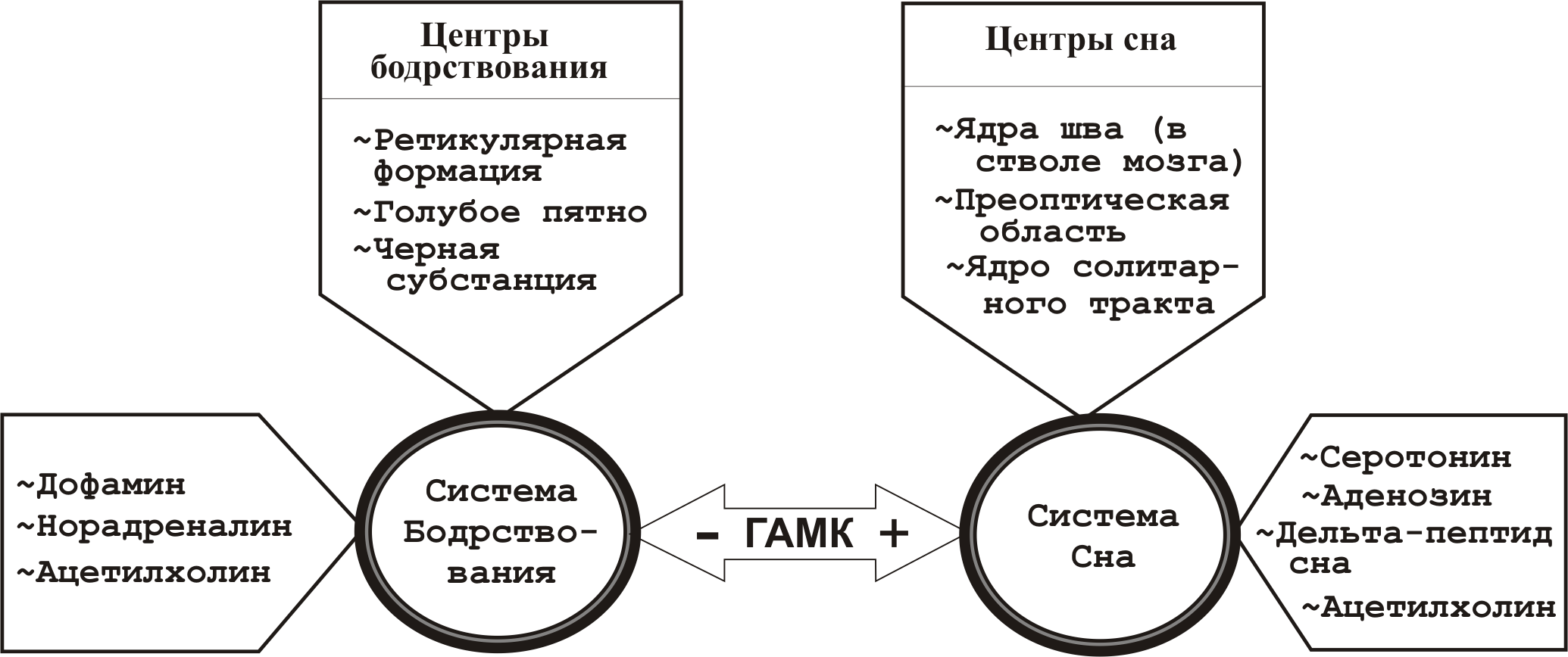
Классификация по механизму действия -Агонисты ГАМК-бензодиазепиновых рецепторов: нитразепам, мидозалам, флунитразепам, зопиклон, золпидем - Агонисты ГАМК-баритуратовых рецепторов: барбитал, эстимал, этаминал-натрия; - Агонист MT1 и MT2 мелатониновых рецепторов: рамелтеон, мелатонин;
Снотворные, производные бензодиазепинов.
Все транквилизаторы группы бензодиазепинов оказывают седативно-снотворное действие и способствуют наступлению сна. Существенным для различных представителей этой группы веществ является интенсивность и соотношение различных компонентов фармакологической активности, свойственных БДЗ-транквилизаторам и связанных с дозой препарата: седативного, анксиолитического и миорелаксирующего. Снотворное действие БДЗ обусловлено их взаимодействием с БДЗ-рецепторами или наличия у некоторых из них серотонинергической активности. Возможна и комбинация этих гипотез или что-то иное. Ообенностью является то, что они не влияют на нормальную структуру сна, не блокируют фазу быстрого сна, т.е. вызывают сон близкий к естественному сну. Их могут использоваться в тех случаях, когда нет собственно нарушения сна, а просто затруднен процесс засыпания. Это может наблюдаться у эмоционально-лабильных субъектов, на фоне негативных или сильных положительных эмоций, переживаемых человеком. В этом случае можно использовать препараты не обладающие выраженным снотворно-седативным действием и к снотворным средствам не относящихся: элениум, сибазон - в обычных, анксиолитических дозах
Показания к приему снотворных средств: расстройства засыпания; Укороченный сон или преждевременное пробуждение - чаще встречается у лиц пожилого и старческого возраста; Пробуждение ночью или поверхностный сон - встречается в любом возрасте при различных невротических, пограничных и депрессивных состояниях, а также как синдром при некоторых соматических заболеваниях.
Отравления снотворными препаратами: характеризуется коматозным состоянием, не имеющим явных специфических симптомов. Наиболее надежным способом диагностики отравления барбитуратами является анализ крови экспресс-методом на их наличие. Для выведения из коматозного состояния необходимо предотвратить всасывание яда из ЖКТ. Для этого промывают желудок через зонд, дают адсорбенты, вводят солевые слабительные, делают сифонные промывания. Для форсированного выведения барбитуратов из крови капельно вводят плазмозамещающих растворов, назначают мочегонные средства, проводят гемодиализ. При тяжелых отравлениях переводят на искусственное дыхание. Вводить средства, возбуждающие ЦНС (аналептики), не рекомендуется, особенно при глубокой коме и нарушении функции внешнего дыхания. Для лечение отравлений показано применение специфических антагонистов (флюмазенил),
Барбитуратовые снотворные средства. Возможные механизмы действия барбитуратов. Влияние на структуру сна. Сравнительная характеристика барбитуратов и бензодиазепинов как снотворных средств. Возможность развития лекарственной зависимости.
Барбитураты усиливают ингибирующее действие ГАМК во многих областях ЦНС. Взаимодействуя с аллостерическим участком БАРБ-БДЗ-ГАМК-рецепторного комплекса они повышают аффинитет ГАМК к ГАМК-А рецепторам, что приводит к более длительному открытию хлорных ионофоров. Действие менее селективно, поскольку барбитураты, взаимодействуя с мембраной нейронов, нарушают трансмембранный ионный ток и функции других ионных каналов. Угнетают действие нейротрансмиттеров возбуждения и вызывают несинаптические мембранные эффекты параллельно с их эффектами на ГАМК нейропередачу.
Подобная множественность точек приложения действия объясняет их способность вызывать полноценный хирургический наркоз, но и способность вызывать угнетающее действие на ЦНС Различные барбитураты отличаются по скорости наступления эффекта и продолжительности действия, которые зависят от их физико-химических свойств, в частности от способности растворяться в липидах, связываться с белками плазмы и проникать через гистогематические барьеры. В качестве снотворных средств применялись барбитураты средней продолжительности действия (4-6 часов) и длительного (7-8 часов).
Характеристика снотворных средств других химических групп. Сравнениеих с бензодиазепиновыми и барбитуратовыми снотворными средствами. Острое отравление снотворными средствами, меры помощи, специфические антагониста бензодиазепинов и барбитуратов.
Механизмы гипнотического эффекта Z-препаратов
Z-препараты представляют новое поколение гипнотиков с избирательным действием на определенный подтип рецепторов ГАМК-А рецепторного комплекса. Существует три основных семейства субъединиц ГАМК-А рецептора: α, β и γ. ГАМК связывается с β-субъединицей, способствуя открытию хлорного канала, что приводит к гиперполяризации мембраны и снижению нейронной активности. Гипнотики благодаря связыванию с α-субъединицей (а точнее с ω(омега)-бензодиазепиновыми рецепторами α-субъединицы) облегчают открытие хлорных каналов в ответ на связывание ГАМК с β-субъединицей, что обусловливает повышение частоты открытия в цитоплазматической мембране нейронов каналов для входящих токов ионов хлора, в результате происходит усиление тормозного влияния ГАМК. Отличается наибольшей степенью селективности в отношении ω-бензодиазепинового рецептора; поскольку их биологическим «субстратом» действия являются подтипы ω1 и ω2 бензодиазепинового рецептора, которые с современными представлениями непосредственно связаны с появлением «чистого» гипнотического эффекта.
Противоэпилептические средства. Возможные механизмы действия. Общие принципы лечения эпилепсии. Выбор препаратов с учетом клинической формы эпилепсии. Средства для купирования эпилептического статуса.
Противопаркинсонические средства. Представления о патогенезе паркинсонизма. Классификация по принципу действия. Сравнительная оценка эффективности отдельных препаратов. Основные побочные эффекты. Клиническое применение.
Психотропные средства. Определение. Краткая история психофармакологии. Современная классификация психотропных средств. Общая характеристика основных классов психотропных средств.
Антипсихотические средства (нейролептики). Определение понятия. Основные фармакологические эффекты. Механизм действия. Фармакологическая коррекция основных побочных эффектов.
Антипсихотические средства (нейролептики) - психотропные средства, предназначенные для лечения психозов – т.е. синдрома для которого характерны тяжелые качественные формы нарушения психики, сопровождающиеся нарушением восприятия, мышления, поведения, влечений и памяти.
Симптомы психоза и шизофрении
Положительные или продуктивные симптомы - Бред; - Галлюцинации; - Искаженность и избыточность речевой продукции; - Дезорганизованная речь; - Дезорганизованное поведение; - Кататоническое поведение; - Ажитация
|
Негативные симптомы - Уплощенный аффект; - Эмоциональная отгороженность; - Коммуникационная ограниченность; - Асоциальность; - Нарушение абстрактного мышления; - Нарушение внимания; - Агедония - Аволиция – снижение мотивации, желаний; ограничения в целенаправленном поведении |
Основные дофаминовые пути в мозге
- Мезолимбический дофаминовый путь (положительные симптомы шизофрении) представляет проекцию от дофаминергических нейронов черной субстанции к аксонным терминалям одной из лимбических областей мозга. Возможно это связано с гиперактивностью и избытком дофамина. Предполагается, что этот путь играет важную роль в некоторых аспектах эмоционального поведения, включая положительные симптомы психоза, такие как мании и галлюцинации. Важен для мотивации, удовольствия и вознаграждения. Мезокортикальный путь и когнитивные, негативные, и аффективные симптомы шизофрении. Считают, что негативные, когнитивные и аффективные симптомы симптомы шизофрении, могут быть связаны с дефицитом активности дофамина в мезокортикальной проекции на дорсолатеральную и мезокортикальной префронтальную кору.
- Нигростриатный дофаминовый путь является частью экстрапирамидальной нервной системы и участвует в двигательной активности. Дофаминовая недостаточность приводит к нарушениям движения, включая болезнь Паркинсона, характеризующуюся ригидностью, акинезией/брадикинезией и тремором.
- Тубероинфундибулярный дофаминовый путь. Дофаминовые нейроны, которые проецируются от гипоталамуса до переднего гипофиза относятся к тубероинфундибулярному пути. Обычно они активны и ингибируют высвобождение пролактина. Если функционирование снижается в результате приема ЛС, уровень пролактина может повышаться. Повышенный уровень пролактина связан с галактореей, аменореей, с другими проблемами, такими как сексуальная дисфункция. Такие проблемы могут возникнуть после лечения многими антипсихотическими препаратами, которые блокируют D2‑рецепторы.
- Таламический дофаминовый путь. Относительно недавно был описан дофаминовый путь, который иннервирует таламус у приматов. Его функция все еще исследуется, но он может быть задействован в механизмах сна и пробуждения путем передачи информации, проходящей через таламус в кору и другие области мозга. На данный момент нет доказательств аномального функционирования этого пути при шизофрении.
Нейролептики фенотиазинового ряда. Классификация. Возможные механизмы действия. Характеристика групп. Фармакологические эффекты аминазина, трифтазина, этаперазина, фторфеназина. Побочные эффекты представителей фенотиазинового ряда.
Нейролептики фенотиазинового ряда делят на 3 группы в зависимости от их химического строения.
Алифатические соединения фенотиазина - соединения, содержащие при атоме азота фенотиазинового ядра диалкиламиноалкильную цепь - алифатические производные (аминазин, пропазин, левомепромазин. Обладают выраженной седативной активностью, способны вызывать вялость, интеллектуальную и моторную заторможенность, при их длительном применении развиваются экстрапирамидные нарушения.
Аминазин - индивидуальные свойства выражаются в сильном затормаживающем действии, обуславливающем сильный седативный эффект, со слабым антипсихотическим действием. После приема замедляются психические процессы, движения и речь, нарастает вялость, безинициативность, нивелируются эмоциональные реакции, появляется однообразие мимики и моторики, индифферентное отношение к собственным переживаниям и окружающему миру. Этот симптомокомплекс не зависит от клинической картины и возможен у здоровых людей. Обладает периферическим адреноблокирующим действием: устраняет артериальную гипертонию, но не влияет на адреналиновую гипергликемию. Оказывает тормозящее действие на центральные и периферические холинореактивные структуры. Обладает слабым антигистаминовым действием. Угнетает интероцептивные рефлексы, уменьшает проницаемость капилляров, оказывает противовоспалительное и выраженное гипотермическое действие. Потенцирует эффекты наркотических, снотворных, анальгезирующих и противосудорожных средств.
Показания. Для купирования возбуждения и показан при синдромах с преобладанием возбуждения. Однако при ступоре, апатикоабулических явлениях и других синдромах с заторможенностью, аминазин противопоказан. Применение: шизофрения, хронических параноидальных и галлюцинаторно-параноидальных состояниях; при маниакальном возбуждении у больных МДП. В детской психиатрии применяется при возбуждении у олигофренов, при галлюцинациях, импульсивных и агрессивных приступах..
Побочное действие. В зависимости от дозы, способа введения и длительности приема возникают побочные эффекты и осложнения со стороны нервной системы и внутренних органов.
1. Тахикардия, снижение АД (антиадренергический компонент). Существует опасность ортостатического коллапса. 2. Сухость кожи, уменьшение саливации, вялость реакции зрачков на свет и прочие реакции, обусловленные холинолитическим компонентом аминазина. 3. Экстрапирамидные расстройства в виде паркинсонической симптоматики, сопровождающиеся чувством внутреннего беспокойства и тревоги, нарушением ночного сна, появляются суетливость, назойливость. 4. Токсический гепатит, при котором аминазин немедленно отменяют. Реже встречаются агранулоцитоз и тромбофлебиты.
Противопоказания. Поражения печени, почек, нарушение функции кроветворных органов, язва желудка и 12-пк в период обострения, тромбоэмболическая болезнь, миокардиодистрофии, коматозные состояния, связанные с отравлениями снотворными, алкоголем, наркотиками; для купирования возбуждения при острых травмах мозга.
Пропазин. По седативным свойствам уступает аминазину, но переносится лучше, реже вызывает побочные эффекты. Токсичность на печень и другие паренхиматозные органы намного меньше.
Левомепромазин (тизерцин). По способности потенцировать действие наркотических и анальгезирующих средств, а также по гипотермическому действию тизерцин в 3-4 раза активнее аминазина. Cчитается одним из наименее токсичных фенотиазинов, абсолютных противопоказаний к его применению нет.
Пиперазиновые производные. Соединения, содержащие в боковой цепи ядро пиперазина -пиперазиновые производные (этаперазин, трифтазин, фторфеназин) наряду с сильным антипсихотическим действием обладают растормаживающим и активирующим компонентом, вызывают тяжкие экстрапирамидные расстройства, в картине которых преобладают гиперкинетические явления.
Трифтазин (стелазин). Проявляет сильное антипсихотическое действие, чем аминазин, что позволяет применять его в дозах в 10 раз меньших. По седативному, холинолитическому, адренолитическому, гипотензивному и потенцирующему эффектам трифтазин уступает аминазину. Не обладает противогистаминной, спазмолитической и противосудорожной активностью. Обладает сильным противорвотным действием.
Осложнения и побочное действие. Экстрапирамидные неврологические расстройства в виде паркинсонизма, гиперкинезии и дискинезии, которые проявляются в виде чувства моторного беспокойства со стремлением менять положение тела, неусидчивостью, непреодолимой потребностью двигаться и ощущением внутренней тревоги. Токсическое действие на печень и кроветворную систему выражено мало. Не вызывает снижения АД, ортостатического коллапса и других вегетативных нарушений. Аллергические реакции практически не наблюдаются.
Противопоказания. Как и у аминазина.
Этаперазин. По седативному действию этаперазин в 5 раз превосходит аминазин, по противорвотному и антиамфетаминовому действию в 10 раз активнее. Показания. Применяется в психиатрии. Является одним из сильнейших противорвотных средств! В акушерской, хирургической и терапевтической практике, а также при рентгено- и химиотерапии, острой лучевой болезни применяется как сильное противорвотное средство в минимальных дозах для купирования неукротимой рвоты.
Флуфеназин (модитен). По химическому строению представляет соединение фторсодержащего фенотиазинового ядра трифтазина с боковой пиперазиновой цепью этаперазина. В 20 раз активнее аминазина и в два-три раза сильнее трифтазина при относительно меньшей токсичности. Применение эффективно в тех случаях когда клиническая картина характеризуется наличием возбуждения, агрессивности, обусловленных продуктивной симптоматикой. Отличием является еще то, что он, обладая большей силой терапевтического действия, не вызывает серьезные экстрапирамидные расстройства и соматических осложнений как аминазин или трифтазин.
Пиперидиновые производные. Соединения, содержащие в боковой цепи ядро пиперидина (тиоридазин, периацизин) обладают меньшей антипсихотической активностью, не оказывают выраженного седативного действия и редко вызывают экстрапирамидные расстройства.
Тиоридазин (меллерил, сонапакс)- является пиперидиновым производным фенотиазина. Это своеобразное нейролептическое средство, обладающее только ему присущим спектром психотропной активности.Его основной характеристикой является сочетание седативного и стимулирующего компонента при относительно небольшом антипсихотическом влиянии. Наиболее эффективен при психических и эмоциональных расстройствах, сопровождающихся страхом, напряжением, возбуждением. Показан при неврастениях, повышенной раздражительности, беспокойстве, старческих психозах, неврогенных функциональных нарушениях желудочно-кишечного тракта и CCC, хронических нарушениях сна, при предменструальном нервном напряжении и климактерических расстройствах. Практически не вызывает у больных выраженных экстрапирамидных расстройств.
Нейролептики, производные бутирофенона, тиоксантена. Фармакологическая характеристика представителей этих групп. Возможные механизмы действия. Клиническое применение, противопоказания. Побочные эффекты и их фармакологическая коррекция.
Бутирофенонами называют производные масляной кислоты, с замещением гидроксильной группы фенильным радикалом.
Галоперидол является сильным прямым блокатором дофаминовых рецепторов ЦНС. По антиапоморфиновому действию он в 50 раз сильнее аминазина. В клинике оказывает сильнейшее антипсихотическое действие, является сильным противорвотным средством. Потенцирует и пролонгирует эффекты барбитуратов, опиатных анальгетиков и наркотических средств. Не обладает гипотензивными свойствами и мало влияет на функции вегетативной нервной системы. Хорошо всасывается и быстро выделяется с мочой и калом в виде метаболитов в неизменном виде. Показания. Является эффективным средством для купирования возбуждения, при маниакальных со-стояниях, остром бреде, лечении шизофрении Не вызывает вялости и апатии, оказывает активирующее действие. Осложнения и побочное действие. неврологические расстройства в виде акинето-гипертонического синдрома и кризов моторного возбуждения. В этих случаях следует прекращать наращивать дозы, начинать применять корректоры и назначать витамины группы "B". Иногда наблюдаются кожные реакции, фотосенсибилизация, бессонница. Противопоказания. Вызывает неврологические нарушения, особенно на фоне органических поражений мозга. Перенесенные в прошлом или имеющиеся к моменту назначения, заболевания ЦНС; особенно при наличие пирамидных и экстрапирамидных патологических симптомов. В этих случаях побочные явления быстро приобретают осложненный характер.
Дроперидол - нейролептическое средство из группы бутирофенонов. Мощный блокатор центральных дофаминовых рецепторов. По своей нейролептической активности в 200-300 раз превосходит аминазин. Обладает сильной каталептической активностью. Потенцирует действие анальгетиков и снотворных средств. Обладает выраженным противошоковым и противорвотным действием. Оказывает выраженное адренолитическое действие, понижает АД; оказывает антиаритмическое действие.Оказывает сильное, быстрое, но непродолжительное дей-ствие. Эффект при введении в вену проявляется через 2-5 мин, достигает максимума через 20-30 минут. Действие продолжается до 2-х часов. В силу особенностей своей фармакологической активности и фармакокинетических параметров
Производные тиоксантена (хлорпротиксен, сординол ) По химическому строению близки к фенотиазинам. В зависимости от структуры боковой цепи тиоксантены, как и фенотиазины, образуют алифатические (хлорпротиксен), пиперазиновые (сординол) и пиперидиновые (тримарил) производные. Последнее соединение - тримарил - нашло применение в качестве антипаркинсонического средства и не рассматривается как нейролептик.
Хлорпротиксен (труксал). По фармакологическим свойствам имеет много общего с аминазином. Так по адренолитическим свойствам близок к аминазину, а по холинолитической, антисеротониновой и нейролептической - гораздо сильнее аминазина. В спектре его психотропной активности присутствует умеренное антидепрессивное (тимоаналептическое) действие. Не вызывает выраженный побочный экстрапирамидный синдром. Не оказывает токсическое действие на кровь, печень и другие паренхиматозные органы. Применяют при психозах и психоневротических состояниях, сопровождающихся беспокойством, страхом, психомоторным возбуждением, агрессивностью, также в рамках МДП. Препарат эффективен при лечении острых алкогольных психозов. Противопоказан при отравлении алкоголем и снотворными, при склонности к коллапсу, при эпилепсии, паркинсонизме, нарушениях кроветворения и поражениях печени.
Нейролептики, производные дибензодиазепина и бензамида. Фармакологическая характеристика представителей этих групп. Возможные механизмы действия. Клиническое применение, противопоказания. Побочные эффекты и их фармакологическая коррекция.
Производные дибензодиазепина
Клозапин (лепонекс, азалептин). По химической структуре является трициклическим соединением, имеющим элементы сходства с трициклическими антидепрессантами и с бензодиазепиновыми транквилизаторами. Характерными фармакологическими особенностями являются: сильное антипсихотическое действие в сочетании с седативным компонентом; выраженное центральное и периферическое антихолинергическое действие; периферическое альфа-адреноблокирующее действие; не обладает каталептогенным эффектом. Влияет на D1- и D4-рецепторы по сравнению с классическими нейролептиками, действующими в основном на D2-рецепторы. При использовании отсутствуют экстрапирамидные побочные расстройства. Применяют при галлюцинаторно-бредовых состояниях и состояниях психомоторного возбуждения при шизофрении, при маниакальном синдроме в рамках МДП, при психопатиях у возбужденных больных. Эффективен при резистентности к лечению другими нейролептиками. Показание - лечение психических заболеваний с церебрально-органической этиологией, на фоне пирамидной и экстрапирамидной симптоматики. Переносится хорошо. Осложнение при длительной терапии - гранулоцитопения до агранулоцитоза, что требует постоянного контроля за картиной крови. Противопоказан больным с изменениями картины крови, при токсических (алкогольных) психозах, эпилепсии, тяжелых заболеваниях печени и почек, ССС, глаукоме, атонии кишечника и беременности. Профессиональные ограничения в амбулаторной практике.
Замещенные бензамиды ( сульпирид , тиаприд )
Сульпирид (эглонил, топрал) является производным сульфонилбензамида. По строению и свойствам близок к противорвотному средству метоклопрамиду. Оказывает умеренное антисеротониновое и каталептогенное действие. Является специфическим блокатором дофаминовых D2/D3-рецепторов, а также серотониновых рецепторов. Клинически характеризуется как вещество с "регулирующим" действием на ЦНС, у которого умеренная антипсихотическая активность сочетается с антидепрессивным и стимулирующим свойствами. Он оказался высокоэффективным прежде всего в отношении острых маниакальных и маниакльно-бредовых состояний при эндогенных психозах. Эффективен при патологии, сопровождающейся вялостью, заторможенностью и депрессиях. Применяют при язвенной болезни желудка и 12-ти перстной кишки. Побочные явления: слабый экстрапирамидный синдром, нарушения сна, повышение АД, нарушения менструального цикла, описаны случаи галактореи и гинеко-мастии.
