
Учебники 80270
.pdf
функционален, молекула полимера растет в двух направлениях и имеет элементарное звено
CH2 CH .
Cl
Задача 2. Разберите механизм цепной полимеризации пропилена, используя в качестве инициатора перекись водорода, а в качестве регулятора – диметиламин NH(CH3)2.
Решение. Перекись водорода сравнительно легко в условиях проведения процесса распадается на свободные радикалы:
H2O2 или H – O – O – H → 2 HO• ,
которые и будут выступать в качестве инициатора процесса радикальной цепной полимеризации пропилена.
Зарождение цепи:
|
|
|
|
|
HO.+ CH2 |
|
|
CH |
|
HO |
|
CH2 |
|
|
CH . |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
инициатор |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
мономер |
|
|
|
активный центр . |
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
Рост цепи: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
HO |
|
CH |
|
|
CH . |
+ |
CH2 |
|
|
CH |
HO |
|
CH |
|
CH |
|
|
CH |
|
CH |
.+CH |
|
|
CH |
... |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
2 |
|
|
|
2 |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
CH |
|
|
|
|
|
CH |
|
|
|
CH |
|
|
|
|
CH |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
3 |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
CH |
|
|
||||
Образуется полимерный радикал с элементарным звеном |
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
||
Обрыв цепи – это поглощение активного центра и прекращение роста полимерной молекулы:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
HO |
|
CH |
|
CH |
( |
CH |
|
CH |
) |
CH |
|
CH |
+ NH |
|||||||||||
|
|
|
|
|||||||||||||||||||||
|
|
2 |
|
|
|
2 |
|
|
|
n |
2 |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
CH |
|
|
|
|
CH |
|
|
|
|
CH |
|
CH3 |
||||||
|
|
|
|
|
3 |
|
|
3 |
|
|
|
|
3 |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
регулятор |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
HO |
|
|
CH |
|
|
CH |
( |
CH |
|
|
CH |
) |
|
CH |
|
|
CH + N |
|||||||
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
2 |
|
|
|
|
2 |
|
|
|
|
n |
|
2 |
|
|
|
2 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
CH3 |
|
CH3 |
|
|
|
|
CH3 |
CH3 |
||||||||||
активный радикал
Процесс полимеризации не прекращается, так как образующийся радикал диметиламина активен и служит инициатором зарождения новой цепи.
111
Задача 3. Рассмотрите химические особенности поливинилового спирта, представьте схемы возможных превращений и их влияние на свойства
вновь образующихся продуктов. |
|
|
||||||
|
|
Решение. |
Макромолекулы |
поливинилового |
спирта |
|||
|
( |
CH2 |
|
CH(OH) |
)n |
имеют в своем составе большое количество свободных |
||
|
|
|||||||
групп –OH, которые придают полимеру свойства спиртов. Это реакции образования алкоголятов, простых и сложных эфиров, дегидратации, окисления:
|
|
|
|
|
|
|
|
|
+ RBr |
... |
|
|
CH2 |
|
|
CH |
|
|
|
... + H O + NaBr |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
+ NaOH |
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
... |
|
CH2 |
|
|
|
CH |
|
... |
|
|
|
|
|
|
|
|
OR |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
OH |
+ |
RCOOH ... |
|
|
CH |
|
|
CH |
|
|
|
|
... + H O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
H2SO4 |
|
|
2 |
|
|
|
|
|
|
|
|
2 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OCOR |
|
|||||
Приведенные реакции не влияют на строение полимера и не меняют его степень полимеризации, изменяется его функциональная группа, следовательно меняются его химические и физические свойства. Это реакции звеньев цепи, которые позволяют изменять свойства полимера и вероятные области его применения.
Но если воздействовать на поливиниловый спирт двухосновной кислотой в присутствии небольших количеств серной кислоты при нагревании, то возможно образование межмолекулярных сложных эфиров, что приведет к переходу линейного полимера в сетчатый, к резкому возрастанию его молекулярной массы, потере растворимости, плавкости, пластичности. Это будет макромолекулярная реакция:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OC |
|
CO |
|
... |
|
|||||||||||||||
... |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
... |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
CH2 |
|
|
|
CH |
|
|
CH2 |
|
|
|
|
CH |
|
|
... |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
... |
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
CH CH2 |
|
CH |
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
HOOC |
|
H2SO4 |
(конц.) |
|
|
|
|
O |
|
OC |
|
+ 2 n H2O |
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
+ n |
|
|
|
|
|
O |
|
|
OC |
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
OH |
|
HOOC |
|
|
... |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
... |
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
... |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
... |
|
|
CH2 |
|
|
CH |
|
|
|
CH2 |
|
|
|
|
|
CH |
|
|
|
|
|
|
... |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OC |
|
CO |
|
||||||||||||||||||||||||
|
|
CH2 |
|
|
|
CH |
|
|
|
CH2 |
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Для решения контрольных задач воспользуйтесь табл. 6.1.
112
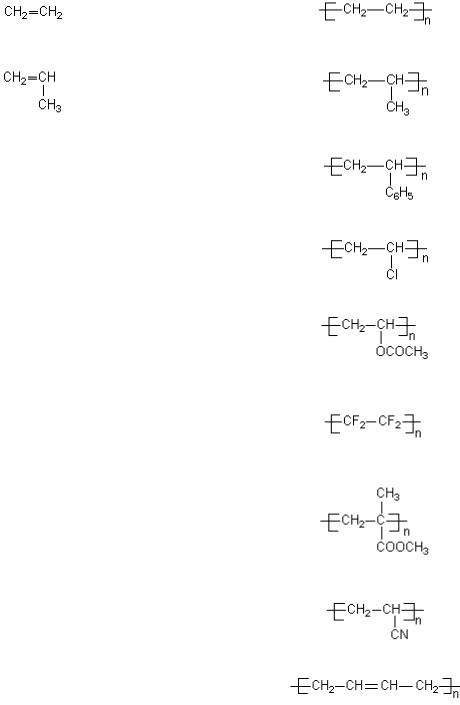
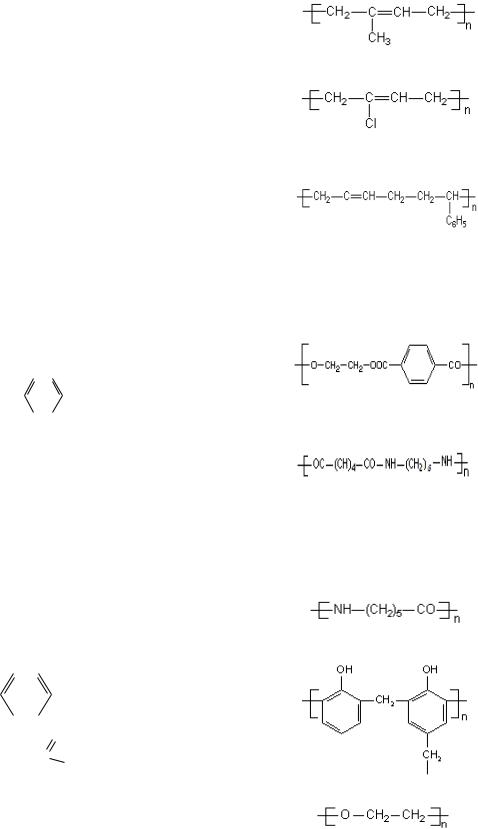
Таблица 6.1 Формулы и названия наиболее распространенных полимеров
и их исходных мономеров
|
Формула |
Название мономера |
Формула полимера |
Название |
|||||||||||||||||
|
мономера |
полимера |
|||||||||||||||||||
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Полимеризационные полимеры |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Этилен |
|
Полиэтилен |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Пропилен |
|
Полипропилен |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Винилбензол |
|
Поливинилбен- |
|
CH2 |
|
|
|
CH |
|
зол |
||||||||||||||
|
|
|
|
|
|||||||||||||||||
|
|
|
|
(стирол) |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(полистирол) |
|
|
|
|
|
|
|
|
|
|
|
|
C6H5 |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
CH |
Хлорэтилен |
|
Поливинил- |
||||||||||
|
|
|
|
||||||||||||||||||
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(винилхлорид) |
|
хлорид (ПВХ) |
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
CH2 |
|
|
|
CH |
Винилацетат |
|
Поливинилаце- |
||||||||||||||
|
|
|
|
||||||||||||||||||
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тат (ПВА) |
|
|
|
|
|
|
|
|
OCOCH3 |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Политетра- |
|
|
CF2 |
|
|
|
|
CF2 |
Тетрафторэтилен |
|
фторэтилен |
|||||||||||
|
|
|
|
|
|
|
(тефлон, |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
фторопласт) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Метиловый эфир |
|
|
CH2 |
|
|
|
C |
|
|
|
|
|
|
CH3 |
метакриловой |
|
Полиметилме- |
|||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
кислоты |
|
такрилат (плек- |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
COOCH3 |
|
||||||||||||
|
|
|
|
|
|
|
|
(метилметакрилат) |
|
сиглас) |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Нитрил акриловой |
|
Полиакрило- |
|
|
CH2 |
|
|
|
|
|
CH |
кислоты |
|
|||||||||||
|
|
|
|
|
|
|
|
нитрил |
|||||||||||||
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
CN |
(акрилонитрил) |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(нитрон) |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
CH2 |
|
CH |
|
|
|
|
|
|
|
CH |
|
CH2 |
Бутадиен-1,3 |
|
Полибутадиен |
||||||
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(дивинил) |
|
(каучук СКБ) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
113
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Продолжение табл. 6.1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
Формула |
|
|
|
Название мономера |
|
Формула полимера |
Название |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
мономера |
|
полимера |
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Полиизопрен |
CH2 |
|
|
|
|
C |
|
|
CH |
|
|
|
|
|
|
CH2 |
2-метилбутадиен-1,3 |
|
|
(натуральный |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(изопрен) |
|
|
каучук) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
CH2 |
2-хлорбутадиен-1,3 |
|
|
Полихлоропрен |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(хлоропрен) |
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
CH2 |
|
|
|
Полибута- |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
диенстирол |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Бутадиен + стирол |
|
|
(бутадиен- |
|
CH2 |
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
стирольный |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C6H5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
каучук) |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Поликонденсационные полимеры |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
CH2 |
|
|
|
|
|
OH |
Этиленгликоль + |
|
|
Полиэфир – |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
полиэтилен- |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
терефталевая |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
терефталат |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
HOOC |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
кислота |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(лавсан) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HOOC |
|
|
|
|
|
|
(CH)4 |
|
|
|
|
|
COOH |
Адипиновая |
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
кислота + гекса- |
|
|
Полиамид |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
метилендиамин |
|
|
(найлон) |
||||||||||||
NH2 |
|
|
|
|
|
|
|
(CH2)6 |
|
|
|
|
|
|
NH2 |
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
Формула |
|
|
|
Название |
|
Формула полимера |
Название |
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
мономера |
|
|
|
мономера |
|
полимера |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Полиамино- |
NH2 |
|
|
|
|
|
(CH2)5 |
|
|
COOH |
Аминокапроновая |
|
|
капроновая |
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислота |
|
|
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(капрон) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Фенолофор- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
мальдегидные |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
Фенол + |
|
|
смолы: |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
формальдегид |
|
|
новолак, резол, |
|||||
|
|
|
|
|
|
|
|
H |
|
|
|
|
C |
|
|
|
|
|
H |
|
|
|
|
|
|
резит |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(фенопласты) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
CH2 |
|
|
|
|
OH |
|
|
|
Полиэфир – |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Этиленгликоль |
|
|
полиэтилен- |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
гликоль |
114
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Окончание табл. 6.1. |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
Формула |
|
Название мономера |
Формула полимера |
|
|
Название |
||||||||||||||||||||||||||||||||||||||||
|
мономера |
|
|
|
полимера |
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
nClCH2 |
|
|
|
CH |
|
|
|
|
CH2 |
Эпихлоргидрин + |
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
[ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
] |
|
Эпоксидная |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
+ |
|
O |
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
O |
|
CH2 CH |
|
CH2 |
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2,2-дифенилол- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
OH |
|
|
смола |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
OH |
|
|
|
|
|
|
|
C |
|
OH |
пропан |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Кремний- |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
Si |
|
|
OH |
|
Диалкилсиландиол |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
органический |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
полимер |
||
|
|
|
|
|
|
|
|
R' |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Задачи для самостоятельного решения
301.Что понимают под элементарным звеном и степенью полимеризации макромолекул полимера? Укажите элементарное звено следующих полимеров: полистирола, новолака, полиэфира.
302.Рассмотрите три физических состояния аморфного полимера. Какое из них и почему свойственно только высокомолекулярным соединениям? Приведите примеры высокоэластичных материалов и условия потери этого свойства.
303.В чем отличие реакции полимеризации от реакции поликонденсации? Разберите на примерах. Какая реакция лежит в основе получения синтетического каучука и плексигласа?
304.Какие вещества используются в качестве мономеров? Как влияет функциональность мономера на строение получаемых из них полимеров? Ответ иллюстрируйте соответствующими уравнениями реакций.
305.Какие полимерные материалы называют фенопластами? Каково их применение в строительной практике? Приведите схему и условия получения термо- и реактопластов на их основе.
306.Приведите схему реакции получения полистирола. Разберите механизм цепной полимеризации стирола, используя в качестве инициатора пе-
рекись бензоила (C6H5CO – O – O – OCC6H5), а в качестве регулятора метилмеркаптан (CH3SH). Дайте полную классификацию этого полимера.
307.Приведите схему реакции получения полиэфира. Дайте полную классификацию этого полимера, укажите основные направления его практического применения и главную реакцию старения.
308.Что такое пластмассы? Назовите главные составляющие пластмасс. Какие свойства пластмасс отличают их от других материалов и оказываются наиболее ценными в процессе их эксплуатации. Ответ иллюстрируйте конкретными примерами.
115

309.Приведите пример реакции сополимеризации при получении синтетического каучука. Какой процесс используют для улучшения физикомеханических свойств каучука? Приведите схемы соответствующих реакций.
310.Приведите схему реакции получения эпоксидного полимера. Укажите возможность и условия его использования.
311.Опишите процесс растворения полимеров. Как он зависит от состава и строения полимера? Какие вещества называются пластификаторами,
вчем суть их действия и когда они применяются? Назовите пути использования растворов полимеров.
312.Что понимают под старением полимеров? Какие процессы происходят при старении полимера? Рассмотрите процесс на примере резины. Каковы методы борьбы со старением?
313.Напишите схемы реакций получения карбамидоформальдегидного
полимера:
n NH2 – CO – NH2 |
+ m CH2O → … |
карбамид |
формальдегид |
При каком соотношении n и m будет получаться линейный или сетчатый полимер и в каком случае полимер будет термопластичным, а в каком термореактивным? Укажите возможные направления их использования.
314.Какие реакции протекают при отверждении термореактивных полимеров и какое влияние они оказывают на строение и свойства полимеров? Ответ проиллюстрируйте на примере резола, мочевиноформальдегидного полимера.
315.Напишите схему уравнения реакции поликонденсации глицерина
CH2 |
|
CH |
|
CH2 |
|
|
|
|
|
COOH |
||||
|
|
и ортофталевой кислоты |
|
|
|
|
|
COOH . Охарактеризуйте об- |
||||||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
OH |
|
OH |
OH |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|||||||
разующийся полимер и укажите область его применения.
316.Опишите способы проведения реакций поликонденсации и полимеризации. Укажите их достоинства, недостатки и области использования получаемых продуктов.
317.Отметьте принципиальную разницу между макрореакциями и реакциями звеньев цепи полимера на примере полибутадиена. Где нашли применение эти реакции? Ответ иллюстрируйте схемами соответствующих уравнений реакций.
318.К какому классу полимеров относится полиацетатное волокно? Каким методом оно получается? Запишите схему происходящей химической реакции.
319.Что обозначают такие понятия как мономер, олигомер, полимер? Какова средняя степень полимеризации полипропилена, имеющего среднюю
молярную массу M = 28000 г/моль?
320. Какие полимеры называются стереорегулярными? Какие особые свойства они имеют по сравнению с другими полимерами того же состава? Напишите структурные формулы натурального, синтетического каучуков. В каких условиях образуются стереорегулярные полимеры?
116
Раздел 7. ХИМИЧЕСКАЯ ИДЕНТИФИКАЦИЯ
7.1. КАЧЕСТВЕННЫЙ И КОЛИЧЕСТВЕННЫЙ ХИМИЧЕСКИЙ АНАЛИЗ
Содержание материала для самостоятельного изучения
Качественный химический анализ: алгоритм идентификации; качественный анализ анионов и катионов и его применение для идентификации строительных материалов. Количественный химический анализ: гравиметрический и титриметрический методы исследования, их использование для изучения свойств конструкционных материалов, используемых в строительстве.
Литература: [1 – гл. 16, §§ 16.1, 16.2].
Основные теоретические положения
Идентификация катионов и анионов неорганических веществ
Методы химического качественного анализа базируются на ионных реакциях, которые позволяют идентифицировать элементы в форме тех или иных ионов. В ходе реакций образуются труднорастворимые соединения, окрашенные комплексные соединения, происходит окисление или восстановление с изменением цвета раствора. Такие аналитические реакции называются качественными. Вещества, которые используют для проведения аналитических реакций, называются реактивами или реагентами.
Реактивы, дающие общие реакции, могут быть групповыми и служить для отделения одной группы ионов от другой. Селективными (избирательными) являются такие реактивы, которые взаимодействуют с небольшим числом ионов. Специфические реактивы реагируют только с одним ионом. Такие реактивы позволяют обнаружить искомый ион в присутствии других ионов. Примером может служить щелочь, применяемая для обнаружения ионов аммония, а также крахмал, позволяющий обнаруживать йод.
Качественные реакции на некоторые катионы приведены в табл. 7.1, на анионы – в табл. 7.2.
Таблица 7.1
|
Качественные реакции на катионы |
||
|
|
|
|
Катион |
Воздействие |
Наблюдаемая реакция |
|
или реактив |
|||
|
|
||
|
|
|
|
Н+ |
лакмус |
красное окрашивание |
|
(кислая |
метиловый |
|
|
среда) |
оранжевый |
розовое окрашивание |
|
Li+ |
пламя |
карминово-красное окрашивание |
|
Na+ |
пламя |
желтое окрашивание |
|
117
|
|
|
|
|
Продолжение табл. 7.1 |
|
|
|
|
|
|
||
Катион |
Воздействие |
Наблюдаемая реакция |
||||
или реактив |
||||||
|
|
|
|
|||
K+ |
пламя |
фиолетовое окрашивание |
||||
|
|
|
|
|
появляется запах аммиака, посинение лакму- |
|
NH4+ |
щелочь, нагрев |
совой бумажки в парах: |
||||
|
|
|
|
|
NH4+ + ОН‾ → NH3↑ + Н2О |
|
|
|
|
(NH4) 2CO3 |
образуется белый аморфный осадок: |
||
|
|
|
|
|
2Mg2+ + 2CO32‾+ Н2О →(MgOH)2CO3↓ + CO2↑ |
|
|
|
|
гидрофосфат |
образуется белый кристаллический осадок: |
||
Mg |
2+ |
натрия Na2HPO4 |
||||
|
|
|
||||
|
в присутствии |
Mg2++ HPO42‾+ NH3→ MgNH4PO4↓ |
||||
|
|
|
||||
|
|
|
NH4OH и NH4Cl |
|
||
|
|
|
NaOН |
образуется белый аморфный осадок: |
||
|
|
|
Mg2+ + 2OН‾→ Mg(OH)2↓ |
|||
Аg |
+ |
Cl‾ |
|
выпадает белый осадок: |
||
|
|
Аg+ +Cl‾→AgCl↓ |
||||
|
|
|
пламя |
кирпично-красное окрашивание |
||
|
|
|
|
|
|
|
|
|
|
(NН4) 2СО3 |
образуется белый осадок: |
||
Са2+ |
Ca2+ + CO32‾ → СаСО3↓ |
|||||
|
|
|
оксалат аммония |
образуется белый осадок: |
||
|
|
|
(NH4)2C2O4 |
Cа2+ + C2O42‾→ CaC2O4↓ |
||
|
|
|
|
|
||
|
|
|
пламя |
желто-зеленое окрашивание |
||
|
|
|
|
|
|
|
Ва |
2+ |
|
|
выпадает белый осадок, нерастворимый ни в |
||
|
|
|
||||
|
|
SО42‾ |
щелочах, ни в кислотах: |
|||
|
|
|
||||
|
|
|
|
|
Ва2+ + SО42‾→ BaSО4↓ |
|
|
|
|
I‾ |
|
выпадает золотисто-желтый осадок: |
|
Рb2+ |
(KI) |
Pb2+ + 2I‾ → PbI2 ↓ |
||||
2 |
|
выпадает белый осадок, растворимый в ще- |
||||
|
|
|
|
|||
|
|
|
SО4 |
‾ |
лочах: Pb 2+ + SО42‾→ PbSО4↓ |
|
Zn |
2+ |
H2S |
|
образуется белый осадок: |
||
|
|
|
Zn2+ + H2S → ZnS↓ + 2H+ |
|||
|
|
|
вода |
гидратированные ионы Сu2+ имеют голубую |
||
|
|
|
окраску |
|||
|
|
|
|
|
||
|
|
|
|
|
||
|
|
|
избыток |
образуется темно-синий раствор аммиаката |
||
Сu2+ |
аммиака NH3 |
меди |
||||
гексацианоферрат |
|
|||||
|
|
|
|
|||
|
|
|
(II) калия (желтая |
образуется красно-коричневый осадок: |
||
|
|
|
кровяная соль) |
2Cu2+ + [Fe(CN)6]4‾→Cu2[Fe(CN)6]↓ |
||
|
|
|
K4[Fe(CN)6] |
|
||
118
|
|
|
|
|
|
Окончание табл. 7.1 |
|
|
|
|
|
|
|
Катион |
Воздействие |
|
|
Наблюдаемая реакция |
||
или реактив |
|
|
||||
|
|
|
|
|
||
|
|
гексацианоферрат |
выпадает темно-синий осадок (турнбулева |
|||
|
|
(III) калия (крас- |
||||
Fe2+ |
синь): |
|||||
|
|
ная кровяная |
|
2+ |
3 |
|
|
|
соль) K3[Fe(CN)6] |
3Fe |
|
+ 2[Fe(CN)6] ‾→ Fe3[Fe(CN)6]2 |
|
Zn |
2+ |
H2S |
|
образуется белый осадок: |
||
|
|
Zn2+ + H2S → ZnS↓ + 2H+ |
||||
|
|
I‾ |
|
выпадает золотисто-желтый осадок: |
||
Рb2+ |
(KI) |
Pb2+ + 2I‾ → PbI2 ↓ |
||||
2 |
|
выпадает белый осадок: |
||||
|
|
|
||||
|
|
SО4 |
‾ |
Pb 2+ + SО42‾→ PbSО4↓ |
||
|
|
избыток |
выпадает осадок гидроксида алюминия: |
|||
Al3+ |
Al3++3OH‾→ Al(OH)3↓, который при даль- |
|||||
|
|
щелочи NaOH |
нейшем приливании щелочи растворяется |
|||
|
|
|
|
|||
|
|
гексацианоферрат |
выпадает темно-синий осадок (берлинская |
|||
Fe3+ |
(II) калия (желтая |
лазурь): |
||||
|
|
кровяная соль) |
4 Fe3+ + 3[Fe(CN)6]4‾ → Fe4[Fe(CN)6]3↓ |
|||
|
|
K4[Fe(CN)6] |
|
|
|
|
|
|
SCN‾ |
появляется ярко-красное окрашивание: |
|||
|
|
(роданид калия |
||||
|
|
Fe3+ + 3CNS ‾ → Fe(CNS)3 |
||||
|
|
KCNS) |
|
|
|
|
Таблица 7.2
Качественные реакции на анионы
Анион |
Реактив |
Наблюдаемая реакция |
||
|
|
|
||
ОН‾(ще- |
лакмус |
синее окрашивание |
||
лочная |
|
|
|
|
фенолфталеин |
малиновое окрашивание |
|||
среда) |
||||
|
|
|
|
|
Cl‾ |
Аg |
+ |
выпадает белый творожистый осадок: |
|
|
Аg++CI‾→ AgCl↓ |
|||
Br‾ |
Аg |
+ |
выпадает светло-желтый творожистый оса- |
|
|
док: Ag+ + Br‾→AgBr↓ |
|||
I‾ |
Аg+ |
выпадает желтый творожистый осадок: |
||
|
|
|
Аg+ + I‾ →АgI↓ |
|
NO3– |
дифениламин |
образуется вещество интенсивного синего |
||
|
(C6H5)2NH |
цвета |
||
2 |
ацетат свинца |
образуется черный осадок: |
||
S ‾ |
Pb(CH3COOH)2 |
Pb2++S2‾→ PbS↓ |
||
119

|
|
|
|
|
Окончание табл. 7.2 |
|
|
|
|||
Анион |
Реактив |
Наблюдаемая реакция |
|||
|
|
|
|
|
|
SО42‾ |
Ва |
2+ |
выпадает белый мелкокристаллический оса- |
||
|
|
док: |
|||
|
|
(BaCl2) |
Ва2+ + SО42‾→ BaSО4 |
||
2 |
|
H+ |
выделяется углекислый газ: |
||
СО3 |
‾ |
(HCl) |
2Н+ + CO32‾→ Н2О + CО2↑ |
||
|
|
|
|
|
появляется гель кремниевой кислоты белого |
SiO32‾ |
Н+ |
цвета: |
|||
|
|
|
|
|
2Н+ + SiO32‾ → Н2SiO3↓ |
|
|
Ag |
+ |
выпадает светло-желтый осадок: |
|
|
|
|
3Аg+ + РО43‾→ Аg3РО4 |
||
РО43‾ |
магнезиальная |
|
|||
|
|
смесь |
образуется белый кристаллический осадок: |
||
|
|
MgCI2+NH4CI+ |
PO43‾+Mg2+ +NH4+→MgNH4PO4↓ |
||
|
|
NH4OH |
|
||
Количественный анализ – определение содержания (массы, концентрации и т.п.) или количественных соотношений компонентов в анализируемом образце.
Все методы количественного анализа делят на химические и инструментальные. Это разделение условное, так как многие инструментальные методы основаны на использовании химических законов и свойств веществ. В данном пособии рассмотрены только химические методы анализа: гравиметрический и титриметрический.
Гравиметрический метод (гравиметрия) − основан на измерении мас-
сы определяемого компонента, выделенном в чистом виде либо в виде соединения определённого состава. Соединение, в виде которого осаждается определяемый элемент, называется осаждаемой формой, а соединение, в виде которого взвешивается определяемое вещество, − гравиметрической (ве-
совой) формой.
Сущность титриметрического анализа (титриметрии) состоит в оп-
ределении концентрации веществ, проводимом титрованием.
Титрование осуществляется путём прибавления к точно измеренному объёму исследуемого раствора одного вещества по каплям из бюретки стандартного раствора другого вещества. Раствор, концентрация которого определяется, называется исследуемым, а второй, концентрация которого точно известна, − рабочим или титрантом. Титрование ведется до точки эквивалентности. В точке эквивалентности количества эквивалентов реагирующих веществ равны.
Если индексом «1» обозначить раствор исследуемого вещества, а индексом «2» − рабочий раствор, то в точке эквивалентности
сэ(1)  V(1) = сэ(2)
V(1) = сэ(2) 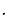 V(2),
V(2),
120
