- •Федеральное агеНтСтво по образованию
- •Кафедра химии
- •Оглавление
- •Введение
- •Тема 1. Теория строения органических соединений. Органическое сырьё и пути его переработки
- •Контрольные задания
- •Классификация органических соединений, их применение
- •Тема 2. Углеводороды
- •2. 1. Насыщенные углеводороды (алканы)
- •Характеристика алканов
- •Литература /1, с. 39 - 60; 2, с. 42 - 62/ Контрольные задания
- •Перечень насыщенных углеводородов в соответствии с вариантом задания
- •2.2. Ненасыщенные углеводороды (алкены,
- •Характеристика ненасыщенных углеводородов (состав, строение, номенклатура, характерные реакции)
- •Контрольные задания
- •2.3. Ароматические углеводороды
- •Характеристика ароматических углеводородов (состав, строение, номенклатура, характерные реакции)
- •Контрольные задания
- •Тема 3. Производные углеводородов
- •3.1. Спирты и фенолы
- •Характеристика спиртов и фенолов
- •Контрольные задания
- •3.2. Альдегиды и кетоны. Углеводы
- •Характеристика альдегидов и кетонов
- •Контрольные задания
- •3.3. Карбоновые кислоты и их производные. Поверхностно -активные вещества
- •Характеристика кислот
- •Контрольные задания
- •Тема 4. Высокомолекулярные соединения (вмс)
- •ККонтрольные задания
- •Тема 5. Превращения органических
- •Библиографический список рекомендуемой литературы
2.2. Ненасыщенные углеводороды (алкены,
алкины)
Гомологические ряды этиленовых и ацетиленовых углеводородов: строение, изомерия, номенклатура. Химические свойства ненасыщенных углеводородов: реакция присоединения, окисления, полимеризации. Механизм реакции присоединения по двойной и тройной связи. Правило В. В. Марковникова. Получение и полимеризация винильных мономеров. Подвижность атомов водорода у углерода с тройной связью. Сравнение свойств этиленов и ацетиленов, и их связь со строением молекулы углеводорода. Промышленное использование ненасыщенных углеводородов (табл. 4).
Таблица 4
Характеристика ненасыщенных углеводородов (состав, строение, номенклатура, характерные реакции)
Характеристика |
Ряд этилена (алкены) |
Алкадиены |
Ряд ацетилена (алкины) |
Общая формула гомологического ряда |
Сn H2n |
Cn H2n-2 |
Cn H2n-2 |
Первые члены ряда |
С2H4 |
С4 H6 |
С2 H2 |
Систематическая номенклатура |
-ен |
-диен |
-ин |
Структура |
С = С |
С = С – С =С |
С ≡ С |
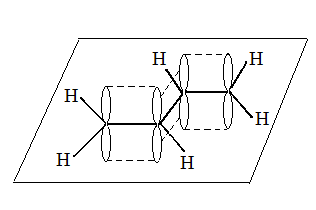
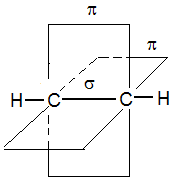
Состояние гибридизации |
sp2 π – связь локализована
|
sp2 - sp2 π – связь (сопряженная связь) |
sp π – связь |
Геометрическая форма молекулы, угол связи между ядрами атомов
|
|
120o |
180o |
Характерные реакции |
Присоединения, окисления, полимеризации |
||
|
замещения, конденсации |
||
Литература /1, с. 61- 89; 2, с. 62-99/
Контрольные задания
41. Приведите уравнения реакций, подтверждающих сходство и различие в химических свойствах этилена и ацетилена. Ответ мотивируйте электронным строением двойной и тройной связи.
42. Приведите уравнения реакций, лежащих в основе промышленных методов получения пропена из сырьевых источников. Охарактеризуйте химические свойства пропена.
Дайте сравнительную энергетическую характеристику углерод - углеродных π- и σ- связей. Приведите уравнения реакций галогенирования, гидрирования, гидрогалогенирования 1 – бутена. Рассмотрите механизм реакций присоединения по двойной связи.
Напишите уравнения реакций присоединения брома и хлористого водорода к пропену, укажите механизм реакций, сформулируйте правило Марковникова.
Какие реакции называются реакциями полимеризации? Приведите уравнения реакций полимеризации этилена и 1,3 - бутадиена. Укажите области применения продуктов полимеризации в технике и строительной практике.
Напишите уравнения реакций окисления пропена в различных условиях. Назовите продукты окисления. Объясните причину достаточно легкого окисления алкенов на основании электронного строения двойной связи.
Дайте сравнительную характеристику химических свойств бутена и бутана. В чем причина высокой реакционной способности одного из них? Приведите уравнения реакций, укажите их механизм.
Рассмотрите процесс получения 1,3 – бутадиена из этилового спирта (по С. В. Лебедеву) и схему полимеризации указанного алкадиена. Назовите полученный полимер и укажите области его применения.
Напишите уравнения реакций присоединения серной кислоты к 1- бутену и 1,3 – бутадиену. Какой из названных углеводородов является более активным в реакциях электрофильного присоединения? Ответ поясните на основе эффекта сопряжения.
Приведите уравнения реакций, лежащих в основе промышленного получения 1,3 - бутадиена, 2-метил-1,3 – бутадиена и полимеризации этих алкадиенов. Укажите основную область использования полимеров.
Напишите уравнения реакций, лежащих в основе получения ацетилена из природного сырья (газа, нефти) и из карбида кальция. Охарактеризуйте физические свойства ацетилена. Приведите уравнение реакции окисления ацетилена и обоснуйте использование этой реакции в сварке.
Что общего в строении этиленовых и ацетиленовых углеводородов, и как это отражается на их свойствах? Ответ подтвердите уравнениями реакций.
На основании электронного строения тройной связи объясните возможность протекания реакции нуклеофильного присоединения для алкинов. Приведите уравнения реакций присоединения к ацетилену воды, синильной кислоты (НСN), бутанола. Укажите нуклеофильные атакующие группы. Назовите класс образующихся соединений и основные направления их использования.
С помощью каких химических реакций можно отличить этан, этилен, ацетилен? Ответ проиллюстрируйте уравнениями соответствующих реакций.
Объясните особое отношение алкинов к реакциям полимеризации. Приведите уравнения реакций образования ди-, три- и тетрамеров ацетилена и укажите условия их проведения.
Какие особенности строения ацетилена способствуют появлению кислотных свойств? Ответ подтвердите, написав уравнения реакций образования ацетиленидов различных металлов.
Для какого из трех углеводородов - этана, этилена или ацетилена – характерны реакции конденсации? Ответ обоснуйте электронным строением простой, двойной и тройной связи. Приведите уравнения конденсации соответствующего углеводорода с формальдегидом и ацетоном, укажите области использования полученных продуктов реакции.
Приведите уравнения реакций, с помощью которых можно отличить 3-метил–1-гексин от 3-метил–1–гексена. Ответ мотивируйте строением двойной и тройной связи.
Напишите уравнения химических реакций, лежащих в основе промышленного использования этилена, пропилена, бутадиена, ацетилена, винилацетилена.
Напишите уравнения реакций бромирования, окисления ацетилена, образование ацетиленида. Сравните поведение ацетилена с этиленовыми углеводородами и объясните их различие особенностями электронного строения тройной связи.

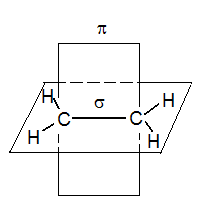 120o
120o