
ОТВЕТЫ К ЭКЗУ
.pdfГемодинамика. Во время систолы происходит постоянный обратный ток крови из левого желудочка в левое предсердие. Мышца левого предсердия из-за перегрузки гипертрофируется. В дальнейшем происходит дилатация полости левого желудочка и гипертрофия его мышцы. Далее происходит повышение давление в левом предсердии и в малом круге кровообращения. Повышение нагрузки на правый желудочек приводит к его гипертрофии. В последнюю очередь происходит дилатация и гипертрофия правого предсердия.
Недостаточность митрального клапана проходит несколько стадий формирования - от минимальной до максимальной, в зависимости от степени выраженности порока сердца. Особенность - при умеренной степени недостаточности может длительно сохраняться состояние компенсации митрального клапана.
Клиника
I степень недостаточности митрального клапана клинически характеризуется: расширением границ относительной сердечной тупости влево и вверх
Аускультативно:
•определяется ослабление I тона
•дующий систолический шум органического характера, р. max. – на верхушке сердца.
Клиника при II и III степени
Аускультативно:
•I тон приглушен
•II тон на легочной артерии акцентуирован
•при развитии сердечной недостаточности может выслушиваться III тон При перкуссии:
•выраженное расширение всех трех границ относительной сердечной тупости
•усиление и смещение верхушечного толчка влево и вниз.
Диагностика
•ЭхоКГ – (золотой стандарт диагностики порока) позволяет выявить степень недостаточности митрального клапана, морфологические изменения его клапанов.
•ЭКГ – признаки перегрузки и гипертрофии различных отделов сердца, аритмии: экстрасистолию, фибрилляцию предсердий.
•Рентгенография – расширение всех границ относительной сердечной тупости,
Осложнения: фатальные аритмии при декомпенсации порока и инфекционный эндокардит. При тяжелом поражении митрального клапана проводят клапаносохраняющую операцию – аннулопластику с использованием полужесткого искусственного кольца.
Митральный стеноз – склеивание, а затем срастание соприкасающихся между собой створок митрального клапана. Порок чаще всего формируется при атипичном течении РЛ. Створки утолщаются, становятся плоскими, укорачиваются. Также происходит утолщение и укорочение подкапанных структур. Клапан приобретает вид воронки, которая суживается у выходного отдела левого желудочка и расширяется в полости левого предсердия
171
Гемодинамические нарушения
•возникают при уменьшении площади митрального отверстия в 2-3 раза
•резко затрудняется продвижение крови в диастолу из левого предсердия в левый желудочек, левое предсердие гипертрофируется.
•Повышенное давление в левом предсердии способствует повышению давления в малом круге кровообращения.
•легочная гипертензия ведет к гипертрофии правого желудочка, далее к его дилатации и формированию правожелудочковой недостаточности.
Клиника
•ранний клинический симптом: одышка, особенно при физической нагрузке, из-за развития гипертензии в малом круге кровообращения
•при физической нагрузке могут возникать сухой кашель, иногда с примесью крови
•жалобы ребенка на выраженные боли в области сердца, сердцебиение
Объективно:
•верхушечный толчок ослаблен, в третьем-четвертом межреберье слева от грудины возможно диастолическое дрожание
•I тон на верхушке громкий, хлопающий, «пушечный», диастолический шум на верхушке.
•II тон резко усилен или раздвоен на легочной артерии.
•границы относительной сердечной тупости расширены вправо и вверх
•САД снижено, снижено пульсовое АД, пульс малого наполнения и напряжения.
Диагностика
•ЭхоКГстепень стеноза, дилатацию и гипертрофия правого желудочка, левого предсердия
•Рентгенограмма– кардиомегалия за счет увеличения левого предсердия и правого желудочка, выбухание дуги легочной артерии, признаки легочной гипертензии.
•ЭКГ – ЭОС отклонена вправо, признаки гипертрофии левого предсердия и правого желудочка. Ранний признак стеноза - изменение зубца Р: вначале он высокий и широкий, позже он расщепляется в I, II стандартных отведениях и в AVL, в отведениях V1 и V2 зубец Р двухфазный (+,-).
Прогноз серьезен, так как адаптационные механизмы левого предсердия и правого желудочка значительно ограничены. При прогрессировании стеноза митрального клапана проводится оперативная коррекция в виде баллонной вальвулопластики или митральной комиссуротомии.
Недостаточность аортального клапана
•Изменения гемодинамики связаны с обратным током крови из аорты в левый желудочек в период диастолы из-за неполного смыкания створок аортального клапана.
•При ревматическом поражении клапана аорты створки его уплотняются, сморщиваются и в диастолу становится невозможным их полное смыкание.
•В левом желудочке происходит так называемая «тоногенная» дилатация его полости.
•При прогрессировании порока высокое диастолическое давление в левом желудочке приводит к застою крови в левом предсердии и повышении в нем ДАД. Это, в свою очередь, ведет к формированию гипертензии в малом круге кровообращения.
172
•Застойные явления в легких вначале приводят к усиленной работе правого желудочка и далее к недостаточности правых отделов сердца и застою в большом круге кровообращения. При выраженной декомпенсации порока может возникнуть острая левожелудочковая недостаточность.
Клиника
•На первом этапе компенсации порока (за счет усиленной работы левого желудочка), пациент жалоб не предъявляет, нет периферических симптомов.
•Определяется некоторое усиление верхушечного толчка и небольшое расширение левой границы относительной сердечной тупости.
•Аускультативно в V точке выслушивается нежный, льющийся диастолический шум аортальной недостаточности.
Клиника при прогрессировании аортальной недостаточности (компенсация порока за счет усиленной работы правого желудочка):
•жалобы на одышку (из-за гипертензии в малом круге кровообращения)
•сердцебиение
•боли в области сердца сжимающего характера (недостаточность коронарного кровообращения).
•выраженные головные боли, головокружения, обмороки (из-за значительного уменьшения кровоснабжения головного мозга).
•периферические симптомы: псевдокапиллярный пульс (симптом Квинке), высокий и быстрый пульс, феномен «бесконечного» пульса, над бедренной артерией определяется феномен двойного патологического шума Дюрозье.
•Отмечается пульсация сонных артерий - «пляска каротид».
•Может появиться симптом Мюссе – ритмичное покачивание головой синхронно с пульсом.
•Кожные покровы бледные. При декомпенсации цвет кожи приобретает пепельный оттенок.
•Верхняя граница артериального давления повышается, а нижняя граница падает вплоть до нуля
•на н\к САД может быть значительно выше, чем на в\к.
•Верхушечный толчок усилен, разлитой, смещен влево и вниз.
•Границы относительной сердечной тупости значительно расширены влево.
Аускультативно:
•Во II межреберье справа - диастолический шум аортальной недостаточности, может выслушиваться грубый систолический шум относительного стеноза аорты
•На верхушке – систолический шум относительной недостаточности митрального клапана, иногда – диастолический шум Флинта.
Диагноз
•Рентгенография органов грудной полости - выявление «аортальной» конфигурации сердца, с подчеркнутой талией.
•ЭхоКГ - подтверждает диагноз недостаточности аортального клапана.
•ЭКГ - отклонение ЭОС влево, признаки гипертрофии миокарда левого желудочка без его систолической перегрузки.
Прогноз. Отличительная способность – порок у детей и подростков может быть длительно компенсированным, без возникновения жалоб. В более старшем возрасте, при появлении жалоб у
173
пациента, без хирургического лечения продолжительность жизни может составить 3-5 лет. Протезирование аортального клапана проводится в более ранние сроки аортальной недостаточности; хорошие результаты хирургического лечения у 75% больных сохраняются до 10 лет.
Аортальный стеноз. При ОРЛ изолированный стеноз аорты - крайне редко, чаще происходит присоединение стеноза аорты к уже имеющейся недостаточности аортального клапана. В 3-4 раза чаще встречается у лиц мужского пола, чем у женского.
Гемодинамика: в результате сращения между собой полулунных створок аортального клапана в области комиссур, создается препятствие оттоку крови из левого желудочка в аорту во время систолы. Развивается концентрическая гипертрофия левого желудочка с незначительным расширением его полости, между аортой и полостью левого желудочка возникает градиент давления, который может достигать 50 мм. рт. ст. и более. Компенсаторно возникает удлинение систолы левого желудочка и брадикардия. Порок может оставаться компенсированным до 15-20 лет, из-за мощной сократительной способности гипертрофированного левого желудочка. Признаки коронарной недостаточности возникают задолго до развития сердечной недостаточности. При декомпенсации возникает снижение сократительной способности левого желудочка, его дилатация, недостаточность кровообращения в малом круге кровообращения, левожелудочковая сердечная недостаточность. При имеющейся выраженной левожелудочковой сердечной недостаточности, при значительном расширении фиброзного кольца митрального клапана возникает недостаточность митрального клапана, так называемая «митрализация» аортального порока, что еще в большей степени вызывает легочную гипертензию. С момента возникновения левожелудочковой недостаточности гибель пациента может наступить в течение 2-3-х лет из-за прогрессирования СН и/или развития фатальной аритмии.
Клиника. Долгое время у пациента отсутствуют жалобы. Жалобы появляются при значительном сужении аортального устья:
•быстрая утомляемость и слабость при умеренной физической нагрузке
•головокружение, обмороки при нагрузке или быстрой перемене положения тела
•боли в сердце (из-за коронарной недостаточности)
•одышка, сначала при физической нагрузке, а затем в покое.
Объективно
•Кожа бледная («аортальная» бледность) – из-за сниженного сердечного выброса и компенсаторной вазоконстрикторной реакции периферических сосудов.
•При выраженном стенозе аортального клапана пульс слабого наполнения и напряжения.
•АД: САД - понижено, ДАД – повышено, пульсовое давление – уменьшено.
•При усиленном сокращении левого желудочка у пациентов может наблюдаться «двойной» верхушечный толчок, в дальнейшем он усилен, но и смещен влево и вниз.
•На основании сердца определяется систолическое дрожание; граница относительной сердечной тупости смещена влево.
•Аускультативно – тоны сердца ослаблены, во II межреберье справа от грудины выслушивается грубый громкий систолический шум органического характера, проводится на сосуды шеи и спину (Иногда этот систолический шум приобретает «дистанционный» характер, по шкале Levin – 5 - 6 степени интенсивности, т.е. слышен на расстоянии от больного).
174

Диагностика
•ЭКГ – отклонение ЭОС влево, признаки гипертрофии левого желудочка, иногда признаки полной или неполной блокады левой ножки пучка Гиса.
•Рентгенография органов грудной полости: в стадии декомпенсации определяется «аортальная» конфигурация сердца, с выраженной талией сердца и постстенотическим расширением аорты, при легочной гипертензии – признаки застоя крови в легких по венозному и артериальному руслу.
•ЭХоКГ – выявляет все признаки, характерные для стеноза аорты.
Прогноз. При тяжелом течении порока 25% больных умирают на первом году жизни (у взрослых). Неблагоприятными прогностическими признаками являются такие клинические проявления как, обмороки, боли в сердце ишемического характера, левожелудочковая недостаточность. При появлении этих признаков необходима хирургическая коррекция порока. При протезировании механическими клапанами необходим пожизненный прием антикоагулянтов, при протезировании биологическими протезами – повторная операция по замене клапана показана через 12-15 лет
11. Врожденные пороки сердца. Классификация. Пороки бледного типа (дефект межжелудочковой перегородки, открытый артериальный проток, дефект межпредсердной перегородки): сроки выявления, особенности гемодинамических нарушений, клинические проявления, показания к хирургической коррекции, исходы. Пороки синего типа (Тетрада Фалло): анатомические составляющие порока, сроки выявления, клинические проявления, диагностика, купирование одышечно-цианотических приступов, показания к кардиохирургической коррекции. Пороки с препятствием кровотоку (коарктация аорты): гемодинамические нарушения, клинические проявления, диагностика, сроки хирургического лечения.
Врожденный порок сердца – дефект в структуре сердца и (или) крупных сосудов, присутствующий с рождения. Большинство пороков нарушают ток крови внутри сердца или по большому и малому кругам кровообращения.
Эпидемиология
•30% от всех пороков
•средняя частота 5-8 на 1000 живорожденных
•в России ежегодно рождается 20-22 тыс. детей с ВПС
•мальчики более подвержены этой патологии, чем девочки (57% и 43% соответственно)
Частота ВПС:
•дефект межжелудочковой перегородки (ДМЖП) – 15-23%
•транспозиция магистральных сосудов (ТМС) – 9- 20%
•тетрада Фалло (ТФ) – 8-14%
•коарктация аорты – 6-15%
•открытый артериальный проток (ОАП) – 6-18%
•открытый атриовентрикулярный канал – 2-5%
•дефект межпредсердной перегородки (ДМПП) – 2,5-16%
•аномальный дренаж лѐгочных вен – 0,5-2%
•стеноз устья аорты – 2-7%
175
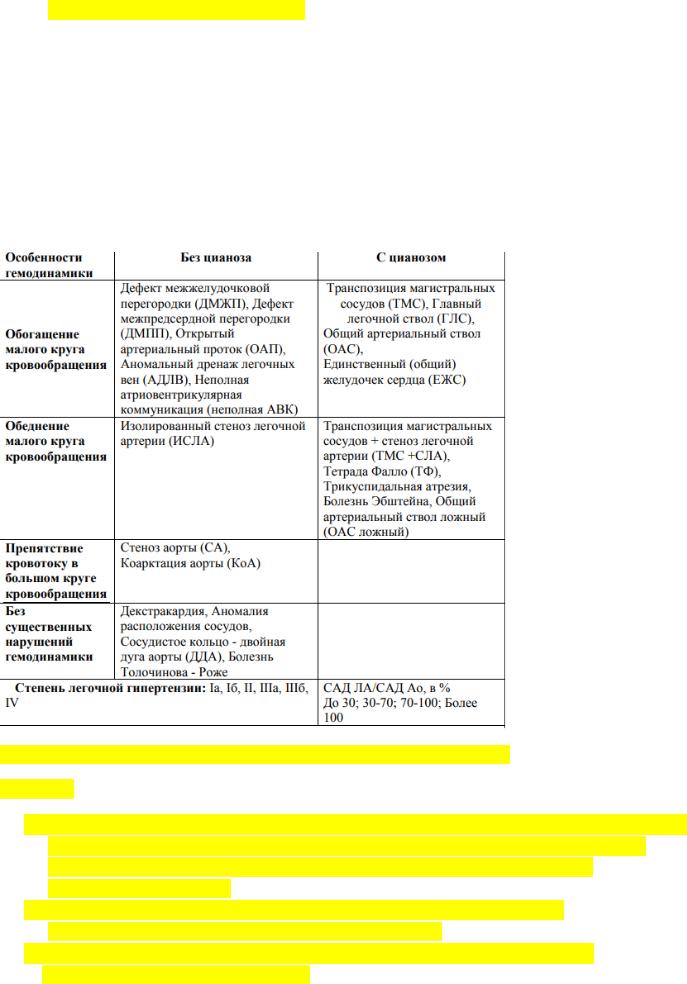
•стеноз лѐгочной артерии – 6,8-9%
Классификация: разработана в институте сердечно-сосудистой хирургии им. А.Н. Бакулева основана на распределении ВПС с учетом их анатомических особенностей и гемодинамических нарушений.
1.ВПС бледного типа с артериовенозным шунтом – дефект межжелудочковой перегородки, дефект межпредсердной перегородки, открытый артериальный проток, атриовентрикулярная коммуникация.
2.ВПС синего типа с веноартериальным шунтом – транспозиция магистральных сосудов, тетрада Фалло, триада Фалло, атрезия трикуспидального клапана.
3.ВПС без сброса, но с препятствием на пути кровотока из желудочков – стенозы легочной артерии и аорты, коарктация аорты.
Эмбриогенез сердца приходится на период с 3 по 9 неделю беременности.
Этиология
Аномалии анатомического развития сердца и крупных сосудов формируются на 2-8-й неделе внутриутробного развития (обусловлены как наследственными (генные, хромосомные, геномные, зиготические мутации), так и средовыми факторами, влияющими на развивающийся зародыш).
90% ВПС наследуются многофакторно - результат сочетания генетической предрасположенности и воздействия средовых факторов.
воздействие на плод и организм матери некоторых неблагоприятных факторов:
o радиация, алкоголизм, наркомания,
176

o эндокринные заболевания (сахарный диабет, тиреотоксикоз),
oвирусные и другие инфекции, перенесенные в I триместре беременности (краснуха, грипп, гепатит В),
oприем лекарственных средств (препараты лития, варфарин, талидамид, антиметаболиты, антиконвульсанты).
o инфекции, перенесенные плодом внутриутробно.
o инфекционные агенты (вирус краснухи, цитомегаловирус, вирус простого герпеса, вирус
гриппа, энтеровирус, вирус Коксаки В и др);
o наследственные факторы – в 57% случаев ВПС обусловлены генетическими нарушениями, которые могут встречаться как изолированно, так и в составе множественных врожденных пороков развития; наиболее известные причины ВПС – точечные генные изменения либо хромосомные мутации в виде делеции или дупликации сегментов ДНК;
oсоматические заболевания матери, и в первую очередь – сахарный диабет – приводят к развитию гипертрофической кардиомиопатии и ВПС;
oпрофессиональные вредности и вредные привычки матери (хронический алкоголизм, компьютерное излучение, интоксикации ртутью, свинцом, воздействие ионизирующей радиации и т.д.).
Факторы риска рождения ребенка с ВПС:
•возраст матери;
•токсикоз и угроза прерывания I триместра беременности;
•мертворожденные в анамнезе;
•наличие детей с врожденными пороками развития у ближайших родственников;
•количественно оценить риск рождения ребенка с ВПС в семье может только генетик;
•у большинства детей с изолированными ВПС семейный анамнез не отягощен и набор хромосом не изменен!
Патогенез
•нарушение формирования структур сердца и диспластические изменения в его каркасе
•происходит неполное, неправильное или несвоевременное закрытие перегородок между предсердиями и желудочками, дефектное формирование клапанов, недостаточный поворот первичной сердечной трубки с образованием аплазированных желудочков и неправильным расположением магистральных сосудов, сохраняются отверстия, свойственные плодному кровообращению.
•Гемодинамика плода при этом не страдает, и ребенок рождается хорошо развитым.
•Компенсация может сохраняться и некоторое время после рождения. В таком случае ВПС проявляется только через несколько недель или месяцев, а иногда и на 2-3 году жизни.
Периодичность течения ВПС: три фазы
1)1)Первичная адаптация. После рождения организм ребенка приспосабливается к нарушениям гемодинамики, вызванным ВПС. Недостаточные возможности компенсации, нестабильное состояние ребенка в раннем возрасте иногда приводят к тяжелому течению заболевания и даже летальному исходу;
2)Относительная компенсация. Наступает на 2-3-м году жизни и может продолжаться несколько лет. Состояние ребенка и его развитие улучшаются за счет гипертрофии и гиперфункции миокарда разных отделов сердца;
177

3)Терминальная (необратимая). Связана с постепенно развивающимися дистрофией миокарда, кардиосклерозом, снижением коронарного кровотока.
Взависимости от состояния кругов кровообращения в организме больного ВПС развиваются следующие патологические изменения:
•– при наличии увеличенного кровотока в легких (пороки сердца бледного типа с артериовенозным шунтом) – гиперволемия и гипертензия малого круга кровообращения, переполнение которого способствует возникновению острой, а затем и хронической патологии органов дыхания;
•– при наличии обедненного кровотока в лѐгких (пороки сердца синего типа с веноартериальным шунтом) – недостаточное насыщение венозной крови кислородом, приводящее к постоянной гипоксемии и цианозу;
•– при пороках сердца с обеднением большого круга кровообращения выше места сужения
– гипертензия, распространяющаяся на сосуды головы, плечевого пояса, верхних конечностей. Сосуды нижней половины тела получают мало крови. Развивается хроническая левожелудочковая недостаточность, часто с нарушениями мозгового и коронарного кровообращения
После рождения ребенка ВПС следует заподозрить при:
•отставании его в физическом развитии
•появлении одышки при движениях и кормлении,
•при бледности (аортальные пороки) или цианотичной окраске кожного покрова
•выраженном акроцианоза (стеноз легочной артерии, тетрада Фалло).
•при осмотре грудной клетки может выявляться «сердечный горб»
•при пальпации области сердца – систолическое (при высоком ДМЖП) или систолодиастолическое (при ОАП) дрожание.
•при перкуссии обнаруживается увеличение размеров и/или изменение конфигурации сердца.
•при аускультации расщепление тонов, акцент II тона на аорте или легочной артерии.
•при большинстве пороков может выслушиваться систолический грубый, иногда скребущий шум. Он нередко проводится в межлопаточное пространство и обычно не изменяется при смене положения тела и нагрузке.
Общая схема лечения.
Обязательные мероприятия: хирургическое лечение ВПС, лечение недостаточности кровообращения.
Вспомогательное лечение: оксигенотерапия, диета, режим, витаминотерапия, кардиотрофики, санация очагов хронической инфекции.
Показания для госпитализации: необходимость углубленного обследования, декомпенсация ВПС, развитие жизнеугрожающих состояний (аритмии, легочная гипертензия).
Лечение недостаточности кровообращения. При развитии недостаточности кровообращения показано ограничение соли, покой. Медикаментозное лечение: сердечные гликозиды, мочегонные. Строфантин детям до 2-х лет назначаются в дозе насыщения 0,01 мг/кг, а детям старше 2-х лет - в дозе 0,007 мг/кг. Доза насыщения для коргликона детям до 2-х лет равна 0,013 мг/кг, а детям старше 2-х лет - 0,01 мг/кг. Поддерживающая доза для строфантина и коргликона равна разовой дозе. Доза
178
насыщения для дигоксина детям до 2-х лет равна 0,06-0,07 мг/кг (внутрь) и 0,04 мг/кг (внутривенно). Детям старше 2-х лет доза насыщения равна 0,05-0,06 мг/кг (внутрь) и 0,03-0,04 мг/кг (внутривенно). Поддерживающая доза для дигоксина детям до 2-х лет составляет ¼-1/5 от дозы насыщения, а детям старше 2-х лет - 1/5-1/6.
Противопоказаниями для применения сердечных гликозидов являются брадикардия, АВ-блокада, желудочковая пароксизмальная тахикардия, анурия, коарктация и стеноз аорты, тетрада Фалло.
Допамин (с кардиотоническим эффектом) – 4 мкг/кг/мин и более в течение 4-48 часов и добутамин в дозе 2-10 мкг/кг/мин. При легочном сердце: оксигенотерапия, эуфиллин, блокаторы кальциевых каналов (верапамил, нифедипин, амлодипин), а при любой этиологии недостаточности – ингибиторы АПФ или антагонисты ангиотензина 2 (вальсартан, кандесартан). При задержке натрия и воды – мочегонные (альдактон, фуросемид, гипотиазид и др.).
При ВПС, сопровождающихся уменьшением легочного кровотока применяют: миотропные спазмолитики (дротаверин), β -адреноблокаторы (пропранолол, метопролол, бисопролол).
При недостаточности кровообращения показана оксигенотерапия через «усы» или носоглоточный катетер; при отеке легкого применяется оксигенотерапия в сочетании с пеногасителями.
Дефект межжелудочковой перегородки (ДМЖП) – врожденный дефект перегородки, возникший вследствие недоразвития межжелудочковой перегородки (МЖП) на различных еѐ уровнях, в результате чего формируется сообщение между левым и правым желудочками.
Гемодинамика зависит от величины ДМЖП, количества, расположения, продолжительности заболевания, степени легочной гипертензии, степени компенсаторной гипертрофии миокарда правого и левого желудочков сердца, соотношения сосудистых сопротивлений большого и малого кругов кровообращения.
После рождения, при малых дефектах (0,2–1,0 см) и физиологически высоком сопротивлении сосудов малого круга кровообращения, сброс крови слева-направо небольшой, и осуществляется только в систолу, легочный кровоток превышает системный только в 1,2–1,5 раза. Диастолическая перегрузка левого желудочка, вызывает его гипертрофию.
При средних и больших дефектах (2–3 см) величина сброса крови зависит от разницы сопротивлений в большом и малом кругах кровообращения. Обычно развивается гипертрофия левого желудочка. Повышение давления в левом предсердии и легочных венах благодаря нейрогуморальному механизму (рефлекс Китаева) ведет к спазму легочных сосудов, предохраняющего легкие от «затопления» их кровью. Увеличение легочного сосудистого сопротивления вызывает систолическую перегрузку правого желудочка. Правый желудочек, позже и правое предсердие гипертрофируются.
Анамнез, клиника. При малых дефектах МЖП физическое развитие ребенка не страдает. Систолический шум выслушивается при интеркурентных заболеваниях или случайно в III-IV межреберьях слева от грудины, иррадиирует вправо и влево от грудины, и на спину.
При средних и больших дефектах дети отстают в физическом развитии, у них возникает гипотрофия; у большинства пациентов в анамнезе затяжные и рецидивирующие пневмонии, бронхиты. С первых недель жизни отмечаются признаки недостаточности кровообращения: затруднения при сосании, возникновение одышки, бледности, потливости (за счет выделения кожей задержанной жидкости),
179
перорального цианоза. У детей с большим ДМЖП (из-за гиперволемии малого круга кровообращения) возникает постоянная одышка, усиливающаяся при кормлении, плаче, перемене положения тела.
При физикальном обследовании визуально определяется сердечный «горб», за счет увеличения правого желудочка (грудь Дэвиса). Верхушечный толчок разлитой, усиленный, определяется патологический сердечный толчок, у 2/3 больных - систолическое дрожание в 3-4 межреберье слева от грудины, свидетельствующее о сбросе крови в правый желудочек. Границы относительной сердечной тупости расширены в обе стороны, особенно влево. Выслушивается грубый скребущего тембра интенсивный систолический шум, максимально в 3-4 межреберье слева от грудины и у мечевидного отростка. Характерна иррадиация шума влево и вправо от грудины и на спину. Спонтанное закрытие дефекта наблюдается часто у детей до года и значительно реже после двух лет.
Диагноз ДМЖП основывается на выявлении органического шума максимально в 3-4 межреберье слева от грудины и у мечевидного отростка, признаков недостаточности кровообращения, кардиомегалии, наличия рецидивирующих бронхолегочных заболеваний.
•ЭКГ. Отклонение ЭОС вправо, признаки комбинированной гипертрофии желудочков.
•Рентгенологически выявляется гиперволемия по малому кругу кровообращения, увеличение размеров сердца за счет обоих желудочков и предсердий. Отмечается выбухание дуги легочной артерии по левому контуру сердца.
•ДЭхоКГ. Позволяет определить размер и локализацию ДМЖП. С помощью допплерографии дополнительно получают гемодинамические показатели: давление в правом желудочке, давление в легочной артерии, межжелудочковый градиент.
Показаниями к хирургической коррекции порока являются сердечная недостаточность, задержка физического развития, повторные респираторные инфекции. В этих случаях операцию проводят, начиная с первого полугодия жизни. У детей старше года хирургическое вмешательство показано при соотношении легочного и системного кровотоков 2:1 и более. При больших дефектах без сердечной недостаточности, но с повышением легочного артериального давления по данным допплерографии необходима как можно более ранняя радикальная операция в возрасте до 1-го года.
Осложнения. При средних и больших дефектах МЖП гиперволемия малого круга кровообращения сопровождается компенсаторным спазмом сосудов легких и повышением давления в легочной артерии. Длительная легочная гипертензия и гиперволемия малого круга кровообращения приводит к морфологическим изменениям в стенке легочных артериол, сосудов мелкого и среднего калибра. Развивается хронический артериит, фиброз и склероз стенок сосудов, их запустевание. В конечной склеротической стадии легочной гипертензии происходит расширение ствола легочной артерии, давление в легочной артерии может превышать 60-70% от системного артериального давления. Давление в правом желудочке повышается и становится больше, чем в левом. Сброс крови через дефект становится перекрестным, а затем право-левым, развивается синдром Эйзенменгера – осложнение терминальной фазы течения ДМЖП средних и больших размеров в перимембранозной части. Для него характерны:
•- тяжелая легочная гипертензия с высоким общелегочным сопротивлением;
•- веноартериальный сброс крови через дефект («смена шунта») с появлением цианоза;
•- расширение ствола легочной артерии и запустевание периферических сосудов малого круга кровообращения; обеднение периферического легочного рисунка на рентгенограмме
180
