
- •Федеральное государственное бюджетное образовательное учреждение высшего образования «Уральский государственный медицинский университет» Минздрава России
- •КС в водных растворах: истинные растворы, КДС, ГДС.
- •Лигандообменные равновесия:
- •Лигандообменные и гетерогенные равновесия:
- •Гетерогенные процессы и лигандообменные равновесия в организме
- •Значение ПР и растворимость некоторых солей, образующихся в организме в норме и при
- •Содержание аминокислот в мочевых камнях: 1 – оксалаты, 2 – фосфаты, 3 –
- •Задача 1 Содержание кальция в моче составляет 4-11 ммоль/л, а магния 3-6 ммоль/л.
- •Задача 2
- •ПРОИЗВЕДЕНИЯ РАСТВОРИМОСТИ МАЛОРАСТВОРИМЫХ ВЕЩЕСТВ (25оС)
- •Теория гетерогенных равновесий.

Федеральное государственное бюджетное образовательное учреждение высшего образования «Уральский государственный медицинский университет» Минздрава России
КОНСУЛЬТАЦИЯ по теме
Лигандообменные и гетерогенные равновесия
зав.кафедрой общей химии Белоконова Надежда Анатольевна
1

КС в водных растворах: истинные растворы, КДС, ГДС.
Истинные растворы, содержащие комплексные соединения – диссоциируют как сильные электролиты между ионом
внешней сферы и комплексным ионом:
[Ag(NH3)2]Cl = [Ag(NH3)2]+ + Cl–
K4 [Cd(CN)6] = 4K+ + [Cd(CN)6]4-
Комплексный ион диссоциирует как слабый электролит в несколько стадий, каждая из которых имеет свое значение Кн
1 ступень Кн(1): |
[Ag(NH3)2]+ [Ag(NH3)]+ + NН3 |
|
||||
2 ступень Кн(2): : |
[Ag(NH3)]+ Ag+ + NН3 |
|
|
|||
Обобщенное уравнение: |
[Ag(NH3)2]+ Ag+ + 2NН3 |
характеризуется |
||||
обобщенной константой, которая записывается К(1-2) или просто |
||||||
Кн |
|
[Ag ][NH3]2 |
|
|
||
|
|
|
8 |
|||
|
K |
|
|
|
6 10 |
|
|
н |
|
|
|
||
|
|
|
[[Ag(NH3)2] ] |
|
|
|
В справочнике приведены усредненные значения Кн
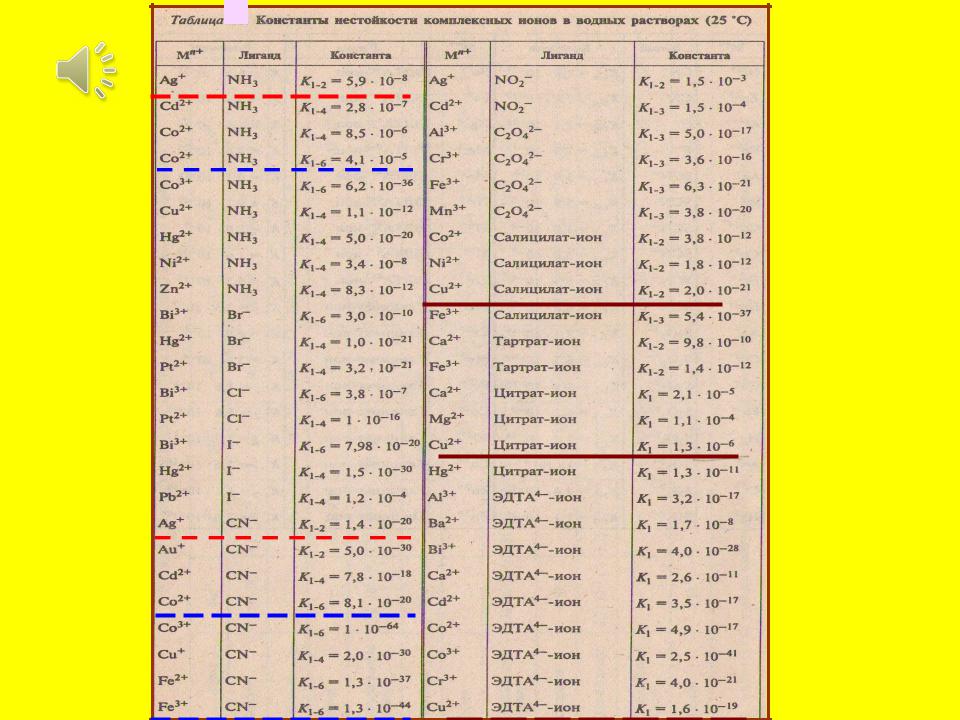
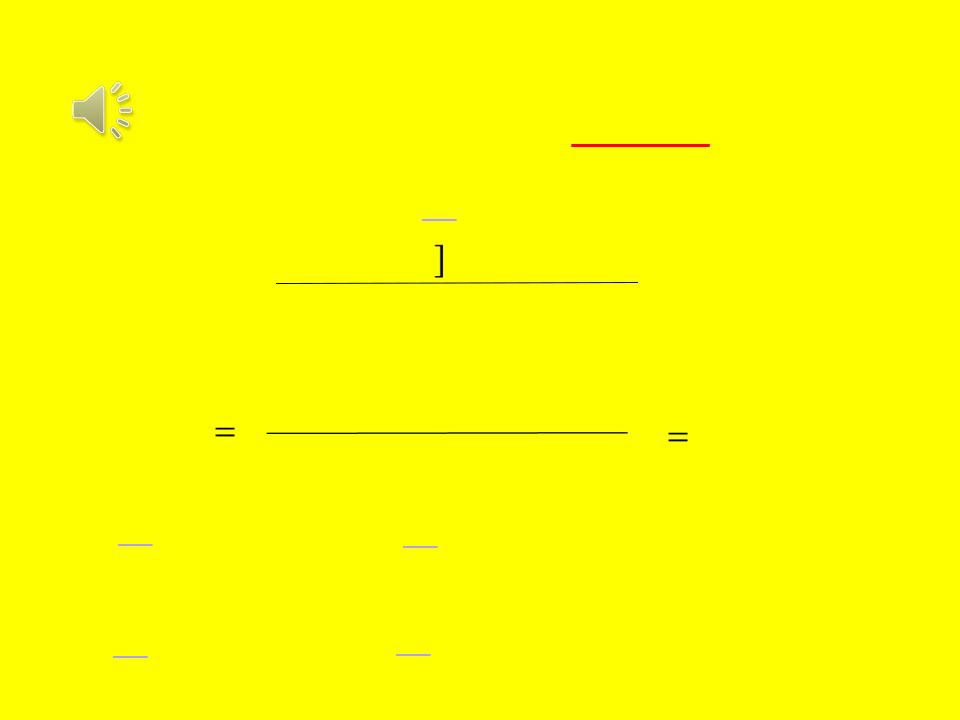
Лигандообменные равновесия:
|
|
[Ag(NH3)2]Cl = [Ag(NH3)2]+ + Cl– |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
K4 [Cd(CN)6] = |
4K+ |
+ [Cd(CN)6]4- |
|
|
|
|
|
|
|||||||
1) |
[Ag(NH3)2]+ |
+ 2CN– |
[Ag(CN)2]+ + 2NН3 |
|
|
6 |
8 |
|||||||||
|
|
|
||||||||||||||
|
|
|
|
|
|
[[ Ag(CN)2 |
] |
[NH3 ]2 |
g+] |
|
|
|||||
|
|
K равн |
|
|||||||||||||
|
|
|
Ag ( NH |
] ][CN]2 |
g+] |
|
|
|||||||||
|
|
|
|
|
|
|
[[ |
|
3)2 |
|
|
|
|
|
||
|
|
|
|
|
Кн ([Ag(NH3)2]+) |
|
|
|
|
|
|
|||||
|
|
|
|
|
Кн ([Ag(CN)2]+) |
|
|
|
|
|
|
4,2*1012 |
|
|||
2) |
[Cd(CN)6]4- |
+ Ni2+ |
[Ni(CN)6]4- |
|
+ Cd2+ |
|
|
|
|
|||||||
|
|
|
|
|
|
|
Кравн = 7,8*1013 |
|
|
|
||||||
2) |
[Ni(CN)6]4- |
+ Cd2+ [Cd(CN)6]4- |
|
+ Ni2+ |
|
|
|
|
||||||||
Кравн = 1,3*10-12

Лигандообменные и гетерогенные равновесия:
[Fe (ССК) ]+ |
|
|
|
Fe3+ + ССК2- |
|
|
|||
|
|
|||
(pH = 2-2,5) |
|
|
|
Кн = 10-14,05 |
|
|
|
[Fe (ССК)2 ]- |
|
|
|
Fe3+ + 2ССК2- |
|
|
|||
|
|
|||
(pH = 4-8) |
|
|
|
Кн = 10-24,33 |
|
|
|
[Fe (ССК)3 ]3- |
|
|
Fe3+ + 3ССК2- |
|
|
|
|||
|
|
|||
(pH = 8-11,5) |
|
|
||
|
|
|||
Кн = 10-33,1 |
||||

|
|
Расчет К |
|
|
|
|
равн |
[Fe (ССК)3 ]3- + 3ОН- |
3ССК2- + Fe(OH)3 |
||
|
|
|
|
ПР = [Fe3+] * [OH-]3 = 5* 10-27 |
(200C) |
||
[Fe (ССК)3]3- 
 Fe3+ + 3ССК3-
Fe3+ + 3ССК3-
н[Fe3+] * [ССК3-]3 [[Fe (ССК)3]3-]
[ССК2- ]3 [Fe3+] [OH-]3 * [[Fe(ССК2-)3]3-] [Fe3+]
Кравн = Кн/ПР = 10-33,1 / 5*10-27 Кр < 1

Гетерогенные процессы и лигандообменные равновесия в организме
Содержание кальция в крови 2,25 – 2,75 ммоль/л
• |
40% (с белками) 14%(лактаты, цитраты) |
• |
46% Ca2+ |

Значение ПР и растворимость некоторых солей, образующихся в организме в норме и при патологии
|
|
|
|
|
|
|
|
Соль |
|
|
|
|
|
|
|
|
|
|
ПР |
S, г/л |
|||||||||||||||||||||||
|
СаСО3 |
3,8·10-9 |
6,2·10-3 |
||||||||||||||||||||||||||||||||||||||||
|
СаС2О4 |
2,3·10-9 |
6,1·10-3 |
||||||||||||||||||||||||||||||||||||||||
|
Са(Н2РО4)2 |
1·10-3 |
14,7 |
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7,1·10-2 |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2,7·10-7 |
2,0·10-4 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5,4·10-5 |
|
|
СаНРО4 |
1,3·10-47 |
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2,2·10-4 |
|||||||||||||||||
|
Са4Н(РО4)3 |
1,6·10-58 |
8,6·10-3 |
||||||||||||||||||||||||||||||||||||||||
|
Са5(РО4)3ОН |
2,0·10-29 |
|
||||||||||||||||||||||||||||||||||||||||
|
2,5·10-13 |
|
|||||||||||||||||||||||||||||||||||||||||
|
Са3(РО4)2 |
|
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
NH4MgPO4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||

Содержание аминокислот в мочевых камнях: 1 – оксалаты, 2 – фосфаты, 3 – ураты
О.А. Голованова
ОСОБЕННОСТИ ПАТОГЕННОГО МИНЕРАЛООБРАЗОВАНИЯ В ОРГАНИЗМЕ ЧЕЛОВЕКА
Задача 1 Содержание кальция в моче составляет 4-11 ммоль/л, а магния 3-6 ммоль/л. В почечных камнях идентифицируется 11 соединений.
Наиболее часто встречается СаС2О4 (ПР = 2,3*10-9 ) и СаНРО4 (ПР = 2,7*10-7 ).
а)Объясните почему не встречаются соединения магния? MgС2О4 (ПР = 8,6*10-5 )
б)Могут ли повлиять на кристаллизацию АК, если
АК |
Гли |
Асп |
Глу |
Кн (Са2+) |
4,17* 10-2 |
2,51* 10-2 |
8,91* 10-3 |
Кн(Mg2+) |
3,54* 10-7 |
3,72* 10-5 |
1,26* 10-2 |
