
- •1. Основные газовые законы. Определение молекулярных масс газообразных веществ.
- •2. Основные стехиометрические законы.
- •3. Понятие о химическом эквиваленте и эквивалентной массе простых и сложных веществ. Закон химических эквивалентов.
- •5. Принцип Паули. Емкость энергетических уровней и подуровней атомов элементов.
- •4. Волновые свойства электрона. Квантовые числа,s-, p-,d-,f-состояния электронов. Электронные орбитали.
- •6. Связь периодического закона со строением электронных оболочек атома. Правило Клечковского. Энергетические ячейки. Правило Хунда.
- •7.Периодический закон д.И.Менделеева и периодическая система: ряды, периоды, группы, подгруппы и порядковый номер.
- •8. Периодическое изменение свойств химических элементов. Радиус атомов, сродство электрону,
- •9. Образование химической связи. Энергия связи и длина связи.
- •10. Ковалентная (атомная) связь. Метод валентных связей. Возбужденные состояния атомов. Валентность.
- •11. Направленность ковалентной связи. Сигма и пи-связи. Гибридизация атомных орбиталей.
- •12. Ионная связь.
- •13. Полярность связи. Полярность молекул и их дипольный момент.
- •14. Донорно-акцепторный механизм ковалентной связи. Комплексные соединения.
- •15. Межмолекулярное взаимодействие. Водородная связь.
- •16. Система. Фаза. Компонент. Параметры. Функции состояния: внутренняя энергия и энтальпия. Стандартные условия.
- •17. Теплота. Работа. Теплоемкость.
- •18. Первое начало термодинамики. Закон Гесса. Термохимические расчеты.
- •19. Стандартная энтальпия образования. Следствия из закона образования.
- •20. Зависимость теплового эффекта реакции от температуры (закон Кирхгоффа).
- •21. Второе начало термодинамики. Понятие об энтропии. Расчет энтропии.
- •23. Условия самопроизвольного протекания химических реакций.
- •24. Константа химического равновесия. Расчет Кр и Кс.
- •25. Принцип Ле-Шателье.
- •27. Молекулярность и порядок реакции.
- •28. Кинетическая классификация по степени сложности. Обратимые и необратимые реакции.
- •29. Зависимость скорости реакции от температуры. Правило Вант-Гоффа. Уравнение Аррениуса.
- •30. Энергия активации химической реакции. Аналитический и графический метод расчета.
- •35. Растворимость газов в жидкостях. Закон Генри. Закон Дальтона. Закон распределения.
- •31. Скорость гетерогенной химической реакции.
- •32. Катализ. Гомогенный и гетерогенный катализ.
- •33. Растворы. Растворимость. Способы выражения концентраций растворов.
- •34. Физические и химические процессы при при растворении. Растворимость твердых тел и жидкостей в жидкостях.
- •36. Законы Рауля.
- •39.Сильные электролиты. Понятие активности и коэффициента активности.
- •37. Электролитическая диссоциация. Степень диссоциации. Слабые электролиты.
- •40.Электролитическая диссоциация воды. Ионное произведение воды. Водородный показатель. Понятие об индикаторах.
- •38. Константа диссоциации. Закон разведения Оствальда.
- •41. Гидролиз солей. Константа и степень гидролиза.
- •42. Овр. Ионно-электронный метод подбора коэффициентов в овр.
- •43.Возникновение скачка потенциала на границе “металл-раствор”. Равновесный электродный потенциал.
- •44. Медно-цинковый гальванический элемент Якоби-Даниеля. Процессы на электродах. Понятие об эдс.
- •46. Стандартный водородный электрод. Формула Нернста. Стандартный потенциал. Ряд напряжений.
- •45.Зависимость эдс гальванического элемента от природы реагирующих веществ, температуры и концентрации. Стандартная эдс.
- •50.Химическая и концентрационная поляризация при электролизе. Перенапряжение.
- •47. Типы электродов и цепей. Окислительно-восстановительные электроды и цепи.
- •49. Законы Фарадея. Выход по току.
- •48.Электролиз. Последовательность разряда ионов на катоде и аноде.
- •51.Классификация химических источников тока.
- •52. Коррозия металлов. Химическая и электрохимическая коррозия.
- •53. Основные методы борьбы с коррозией.
- •54. Кристаллическое состояние вещества. Химическая связь в кристаллах.
- •5. Смешанная связь.
- •55. Составные части системы и компоненты. Правило фаз.
- •57.Диаграмма состояния однокомпонентной системы на примере воды.
- •56.Сущность термографического анализа. Кривые нагревания и охлаждения.
- •58.Основные принципы построения диаграммы плавкости бинарных систем.
- •1. Принцип непрерывности.
- •2. Принцип соответствия.
- •59. Эвтектическая диаграмма плавкости (без образования твердых растворов).
- •64. Адгезия, когезия, сорбция (адсорбция и абсорбция).
- •60.Диаграмма плавкости непрерывно твердых растворов. Правило рычага.
- •61. Диаграмма плавкости бинарной системы с ограниченными твердыми растворами.
- •62. Диаграмма плавкости бинарной системы с образованием химических соединений.
- •65. Физическая адсорбция и хемосорбция.
- •66. Величина и механизм адсорбции.
- •67. Поверхностное натяжение твердых тел. Принцип Гиббса-Кюри.
- •68. Поверхностное натяжение растворов. Изотерма адсорбции Лэнгмюра. Уравнение Фрейндлиха.
- •63. Дальтониды и бертоллиды.
62. Диаграмма плавкости бинарной системы с образованием химических соединений.
Диаграмма состояния системы - диаграмма, указывающая, в каких фазовых состояниях находится система в зависимости от условий: температура, давление и состав.
Диаграммы плавкости – частный вид диаграмм состояния.
Устойчивое, плавящееся без разложения хим.соединение АmВn проявляется на диаграмме в виде max. Чем круче мах,тем устойчивее хим.соединение.
Систему А-В можно представить как бы состоящей из 2 простейших эвтектических диаграмм,где роль одного из компонентов играет устойчивое хим.соединение АmВn .
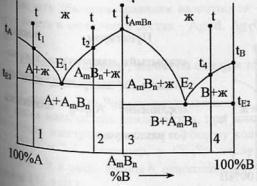
Кривые охлаждения четырех сплавов.

Хим.соединение АmВn разлагается ниже t пл. Имеются 2 точки нонвариантного равновесия-Р и Е.Пунктиром показан “скрытый” мах- так выглядела бы диаграмма, если бы хим.соединение АmВn плавилось без разложения.

Кривые охлаждения 3 сплавов-1,2,3.
Кривая охлаждения сплава1:первоначально при t1 выпадают кристаллы компонента А,жид.фаза меняет свой состав в интервале t1-tP по линии t1Р; при достижении жид.фазой состава Р получает развитие перитектическая реакция,в результате чего жид.фаза исчезает.
Для сплава2 при tP по перитектической реакции исчезают кристаллы компонента А,далее в интервале tP-tЕ из жид.фазы выпадают кристаллы АmВn ,а при достижении жид.фазы состава Е происходит кристаллизация эвтектики АmВn +В.На кривой охлаждения сплава 2 наблюдается 2 площадли- при tP и tЕ .
На кривой охлаждения сплава3 наблюдаются перегиб при t3 – начало выделения кристаллов компонента В и площадка при tЕ - кристаллизация эвтектики В+ АmВn.
65. Физическая адсорбция и хемосорбция.
Сорбция – процесс поглощения одного вещества поверхностью или всем объемом другого вещества. Поглощаемое вещество – сорбат, поглотитель – сорбент (часто твердое тело).
Поглощение может происходить только поверхностью (адсорбция) или всем объемом (абсорбция).
Физическая адсорбция – адсорбат и адсорбент связаны лишь слабыми силами межмолекулярного взаимодействия.
Хемосорбция – процесс, при котором поглощаемое вещество химически взаимодействуют с поглотителем.
В результате проявления сил химической связи на поверхности адсорбента образуется новое химическое соединение.
В научной и производственной практике наибольшее значение имеет адсорбция (нежели абсорбция).
Адсорбционная
способность
адсорбента определяется по удельной
площади поверхности


 степень дисперсности
адсорбента.
степень дисперсности
адсорбента.
Адсорбционная способность тем выше, чем меньше размеры частиц, на которые раздроблен адсорбент.
66. Величина и механизм адсорбции.
Сорбция – процесс поглощения одного вещества поверхностью или всем объемом другого вещества. Поглощаемое вещество – сорбат, поглотитель – сорбент (часто твердое тело).
Поглощение может происходить только поверхностью (адсорбция) или всем объемом (абсорбция).
Величина адсорбции
– способность адсорбента поглощать
адсорбат – это избыток массы адсорбата,
отнесенный к единице поверхности
адсорбента

Механизм адсорбции.
Адсорбция связана с особым энергетическим состоянием частиц на поверхности адсорбента в отличие от энергетического состояния частиц, находящихся в объеме.
Молекулы жидкости верхнего (первого) слоя обладают избытком энергии по сравнению с молекулами нижнего (второго) слоя.
Силы, действующие на первый слой, стремятся втянуть молекулы внутрь слоя и сократить величину поверхности раздела.
Нескомпенсированность сил у молекул верхнего слоя выражается как некий избыток энергии поверхностного слоя.
Поверхностное
натяжение
– избыток свободной энергии в
поверхностном слое, отнесенный к
 поверхности поглощающего тела.
поверхности поглощающего тела.

Поверхностное натяжение представляет собой максимальную полезную работу, затрачиваемую на образование единицы поверхностим т.е. фактически удельный потенциал поверхности.
За счет этой избыточной энергии и происходит притяжение поверхностью молекул газов и растворенных веществ.
