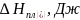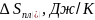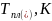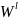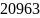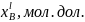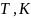ЛР_2
.docxМИНОБРНАУКИ РОССИИ
Санкт-Петербургский государственный
электротехнический университет
«ЛЭТИ» им. В.И. Ульянова (Ленина)
Кафедра микро- и наноэлектроники
отчет
по лабораторной работе №2
по дисциплине «Физико-химические основы технологии изделий электроники и наноэлектроники»
Тема: Моделирование диаграмм состояния с ограниченной растворимостью компонентов (полупроводник- примесь)
Студент гр. 8204 |
|
Овсянников А.И. |
Преподаватель |
|
Максимов А.И. |
Санкт-Петербург,
2020
Цель работы.
Изучение фазовых равновесий в бинарной системе полупроводник (Si, Ge) – примесь методом компьютерного моделирования; расчёт параметров межатомного взаимодействия; выбор моделей растворов, адекватно описывающих экспериментальные T-x диаграммы состояния; расчёт спинодалей и определение областей устойчивого и метастабильного состояния твёрдых растворов в заданной системе.
ИСХОДНЫЕ ДАННЫЕ
Ge-Pb
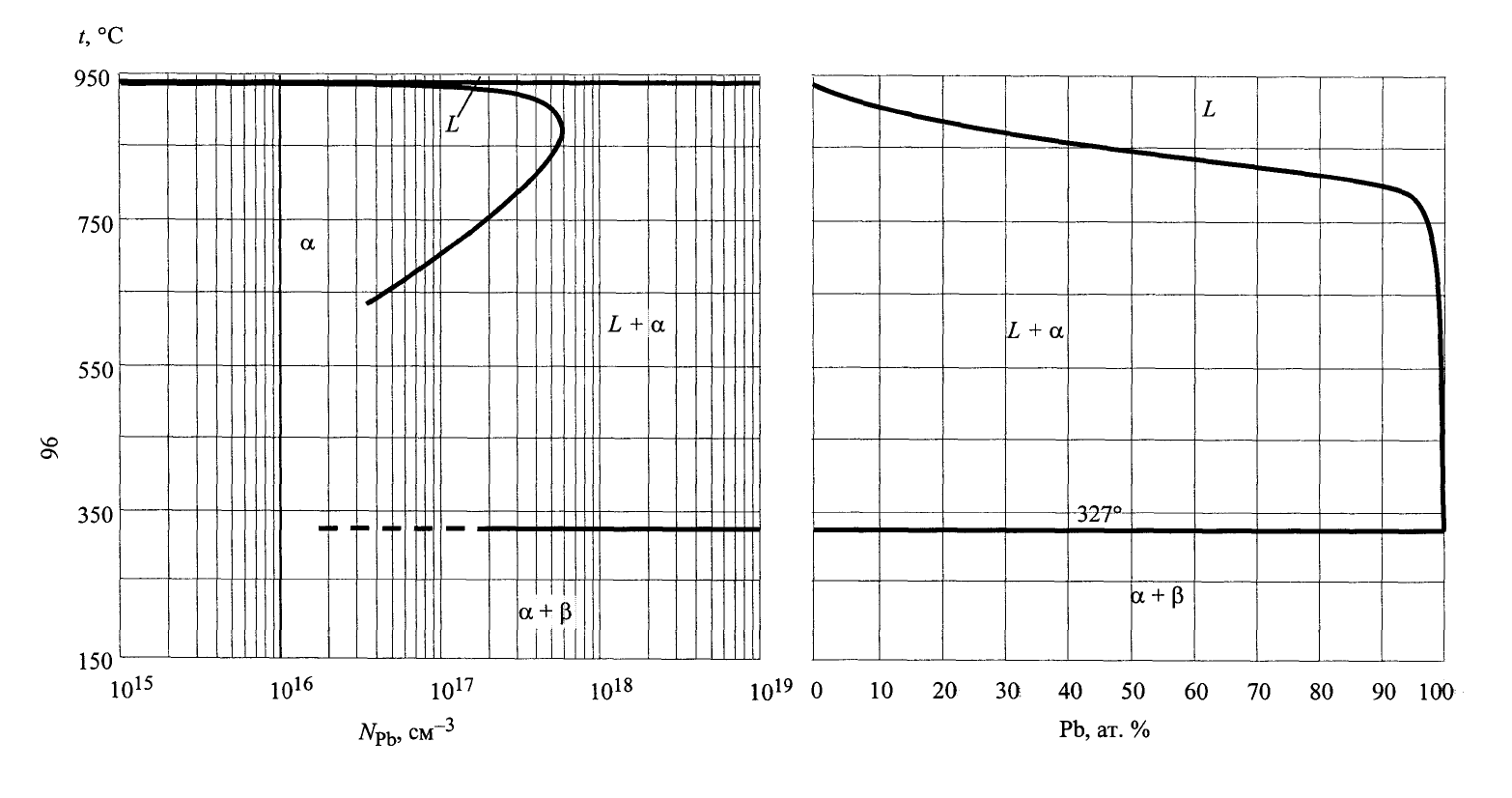
Рис. 1. Характер фазового равновесия в системе германий - свинец.
Таблица 1. Справочные данные по фазовым переходам.

Экспериментальные результаты.
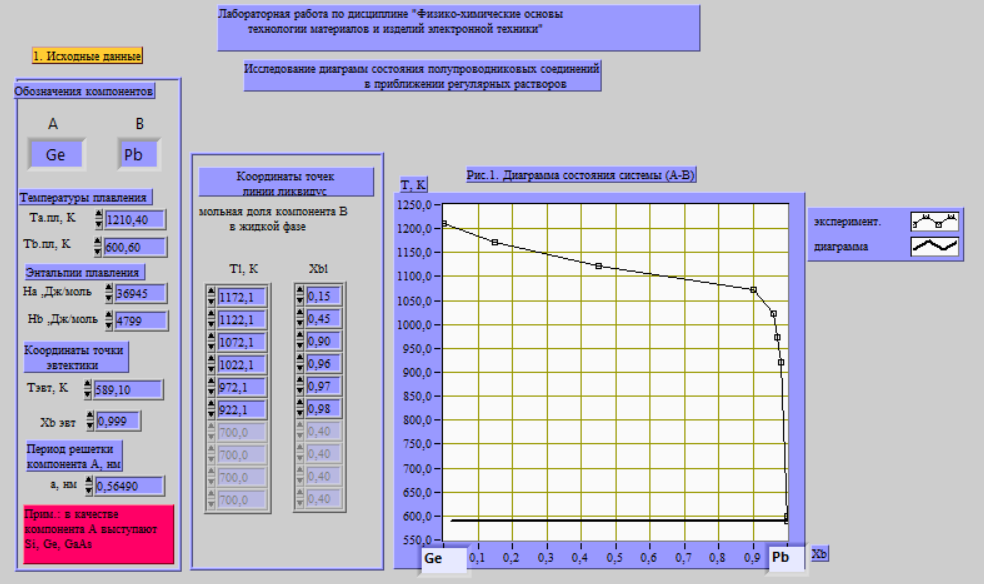
Рис. 2. Исходные данные для линии ликвидуса.
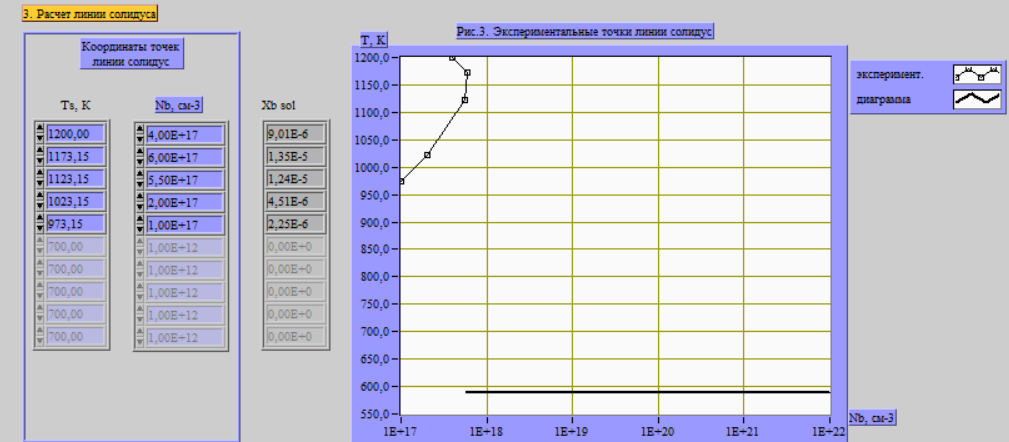
Рис. 3. Исходные данные для линии солидуса.
Обработка результатов
T-x-проекции (в обычном и полулогарифмическом масштабах) с подобранными оптимальными параметры межатомного взаимодействия
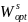 и
и
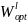 .
.
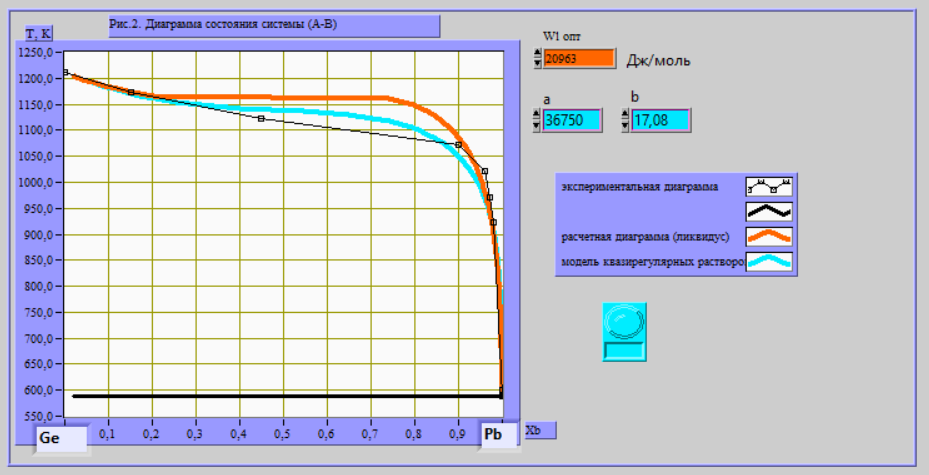
Рис. 4. Диаграмма состояния Ge-Pb.
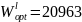
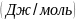 .
.
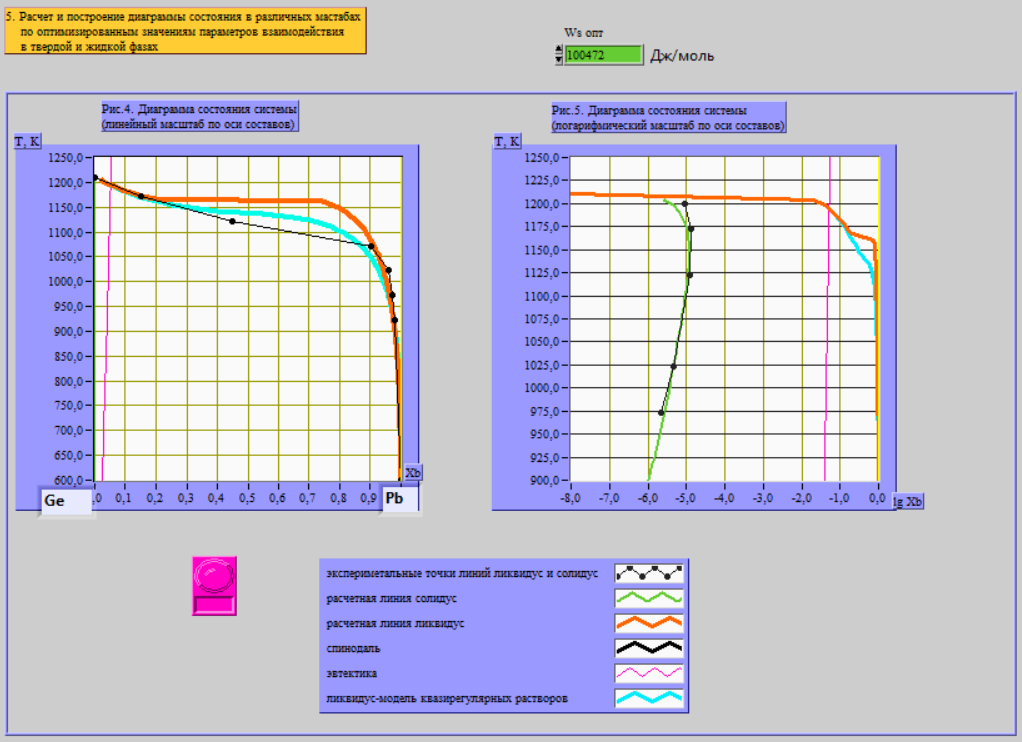
Рисунок 5. Две диаграммы состояния Ge-Pb в двух масштабах.
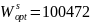 .
.
Рассчитать и построить линию ликвидуса в рамках модели идеального жидкого раствора. Сравнить линии ликвидуса, построенные в рамках модели идеальных, регулярных и квазирегулярных растворов, с экспериментальной приведённой на Т-х проекции.
Так
как
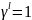 для идеального раствора, то
для идеального раствора, то
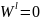

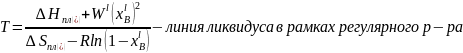
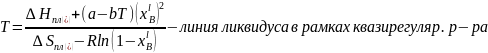
Таблица 1. Данные, входящие в расчёты.
|
|
|
a |
b |
|
36945 |
30,523 |
1210,4 |
36750 |
17,08 |
|
Таблица 2. Расчёт для трёх моделей раствора.
|
Для идеальн. р-ра |
Для регуляр. р-ра |
Для квазирег. р-ра |
|
|
|
|
0 |
1210,40 |
1210,40 |
1210,40 |
0,15 |
1159,11 |
1173,91 |
1147,01 |
0,45 |
1040,97 |
1160,58 |
938,08 |
0,9 |
744,00 |
1085,94 |
413,31 |
0,96 |
645,08 |
982,41 |
311,88 |
0,97 |
619,23 |
949,83 |
291,30 |
0,98 |
586,13 |
905,54 |
267,77 |
Пример расчёта
для
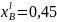 :
:
Для идеального раствора:
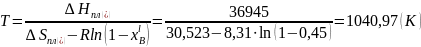
Для регулярного раствора:
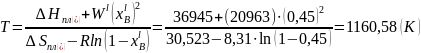
Для квазирегулярного раствора:
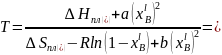
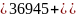
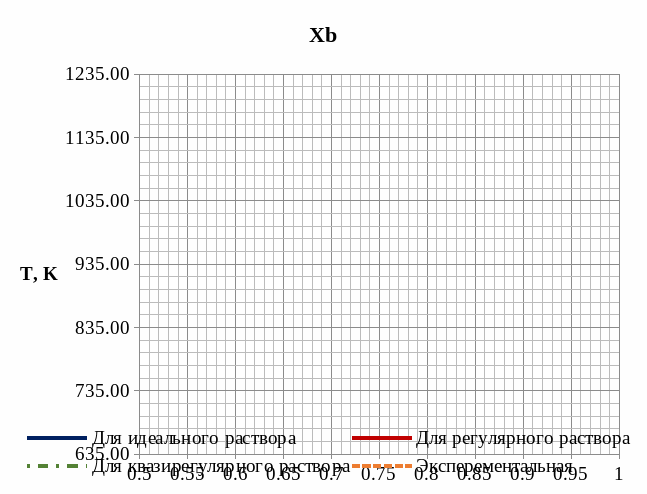
Рис. 6. Линии ликвидуса в рамках идеального, регулярного и квазирегулярного ликвидуса.
Рассчитать и построить концентрационные зависимости коэффициентов активностей компонентов в твёрдом растворе при
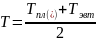 в пределах области растворимости, а
также жидком растворе во всём диапазоне
составов от
в пределах области растворимости, а
также жидком растворе во всём диапазоне
составов от
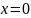 до
до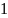 при
при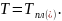 На них построить модели идеальных
растворов. + доп. концентрационные
зависимости активностей компонентов.
На них построить модели идеальных
растворов. + доп. концентрационные
зависимости активностей компонентов.
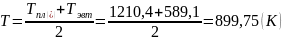
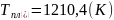

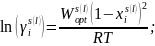
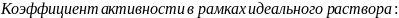
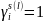 ;
;
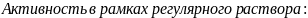
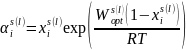 ;
;
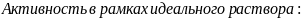
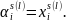
Таблица 3. Коэффициенты
активности и активности для Ge-Pb
в твёрдом регулярном растворе при
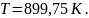
lgX(Pb) |
X(Pb) |
X(Ge) |
a(Ge) |
Y(Ge) |
a(Pb) |
Y(Pb) |
lnY(Pb) |
-8 |
1E-08 |
1 |
1 |
1 |
5,53 |
552901933 |
20,13069 |
-7,41 |
3,907E-08 |
1 |
1 |
1 |
21,60 |
552901286 |
20,13069 |
-6,48 |
3,298E-07 |
1 |
1 |
1 |
182,33 |
552894815 |
20,13068 |
-6,32 |
4,751E-07 |
1 |
1 |
1 |
262,69 |
552891579 |
20,13067 |
-6,25 |
5,62E-07 |
0,999999 |
0,999999 |
1 |
310,91 |
552889638 |
20,13067 |
Пример расчёта для первой строчки:

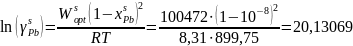
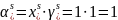
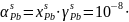 552901933
552901933
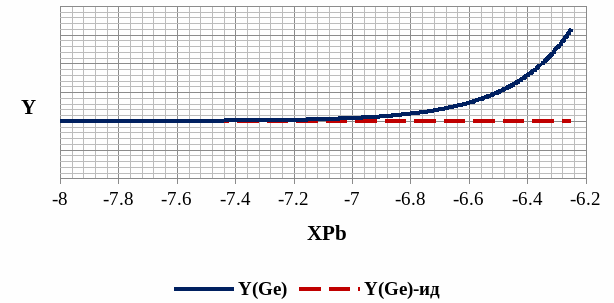
Рис. 7. Концентрационная зависимость коэффициента активности Ge в твёрдом растворе, области растворимости.
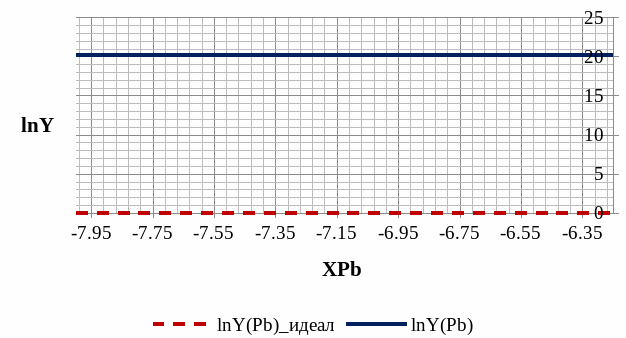
Рис. 8. Концентрационная зависимость коэффициента активности Pb в твёрдом растворе, области растворимости.
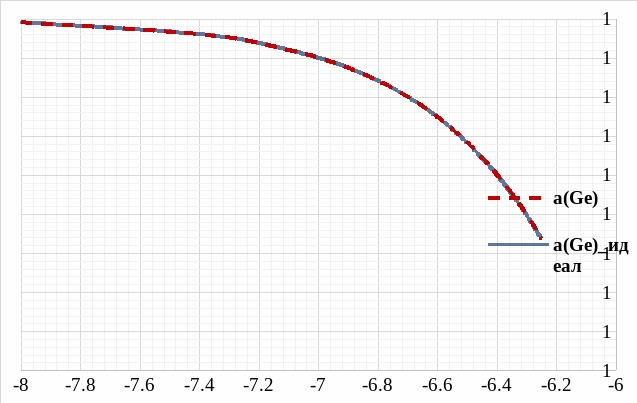
Рис. 9. Концентрационная зависимость активности Ge в твёрдом растворе, области растворимости.
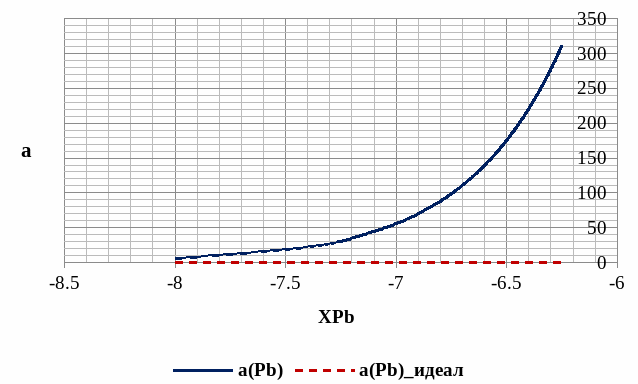
Рис. 10. Концентрационная зависимость активности Pb в твёрдом растворе, области растворимости.
Таблица 4. Коэффициенты
активности и активности для Ge-Pb
в жидком регулярном растворе при
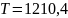 .
.
X(Pb) |
X(Ge) |
a(Ge) |
Y(Ge) |
a(Pb) |
Y(Pb) |
0 |
1 |
1 |
1 |
0 |
8,037545 |
0,1 |
0,9 |
0,918954 |
1,02106 |
0,5409411 |
5,409411 |
0,2 |
0,8 |
0,869551 |
1,086938 |
0,75911748 |
3,795587 |
0,3 |
0,7 |
0,844421 |
1,206316 |
0,83297455 |
2,776582 |
0,4 |
0,6 |
0,837473 |
1,395789 |
0,84704099 |
2,117602 |
0,5 |
0,5 |
0,841881 |
1,683763 |
0,8418813 |
1,683763 |
0,6 |
0,4 |
0,847041 |
2,117602 |
0,83747336 |
1,395789 |
0,7 |
0,3 |
0,832975 |
2,776582 |
0,84442124 |
1,206316 |
0,8 |
0,2 |
0,759117 |
3,795587 |
0,86955073 |
1,086938 |
0,9 |
0,1 |
0,540941 |
5,409411 |
0,91895394 |
1,02106 |
1 |
0 |
0 |
8,037545 |
1 |
1 |
Пример расчёта для пятой строчки:
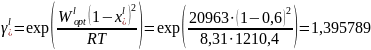
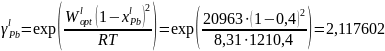
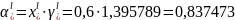
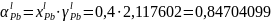
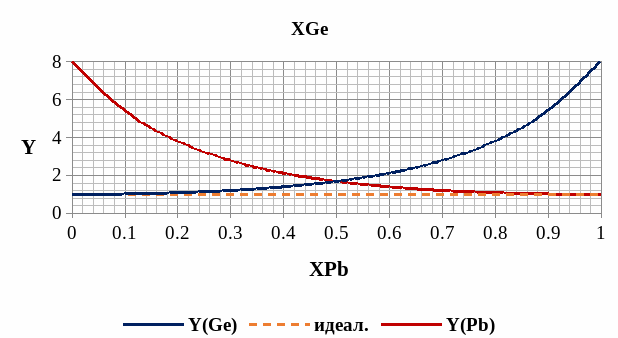
Рис. 11. Концентрационная зависимость коэффициента активности Ge-Pb в жидком растворе.
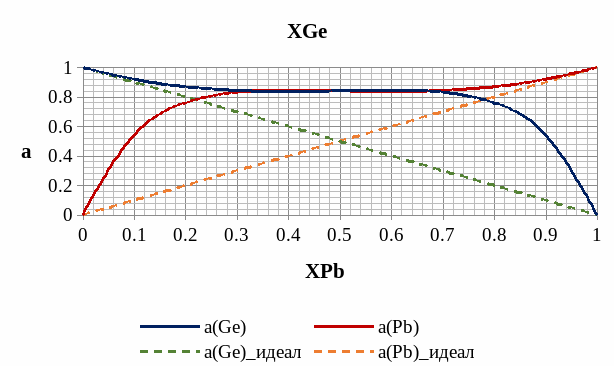
Рис. 12. Концентрационная зависимость активности Ge-Pb в жидком растворе.
Используя Т-х проекцию диаграммы состояния рассчитать равновесный коэффициент распределения компонента Pb (примесь) при .
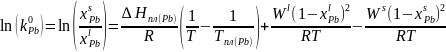
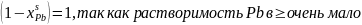
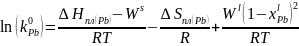
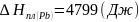
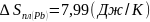
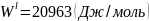
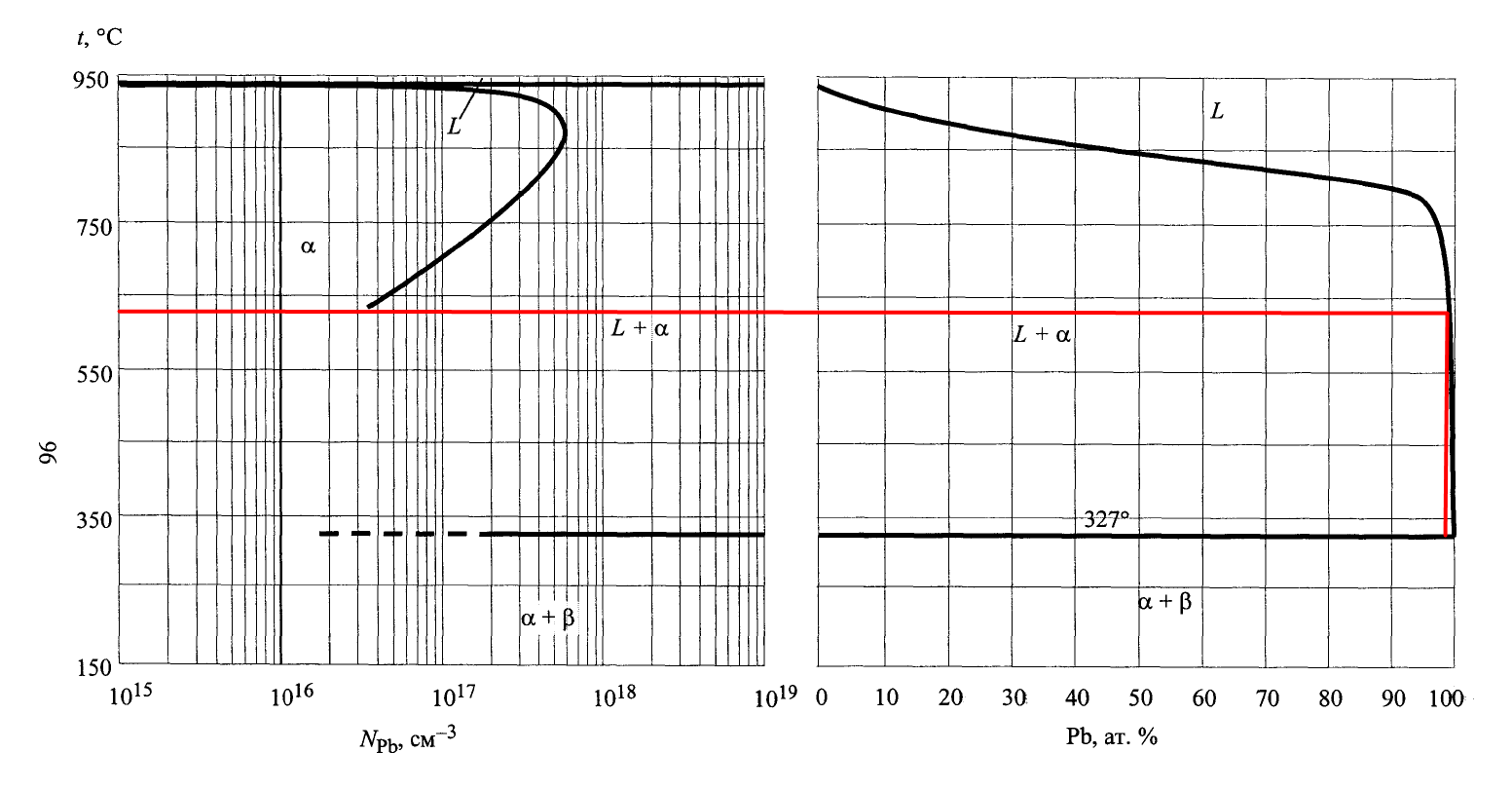
Рис. 13. Определение равновесного коэффициента.
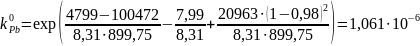
Рассчитать и построить спинодали при температурах от
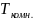 до
до
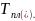 Показать на крупномасштабной Т-х-
диаграмме заданной системы области
стабильных, метастабильных и абсолютно
неустойчивых твёрдых растворов.
Показать на крупномасштабной Т-х-
диаграмме заданной системы области
стабильных, метастабильных и абсолютно
неустойчивых твёрдых растворов.
Уравнение химической спинодали:
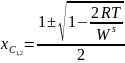
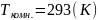
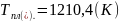
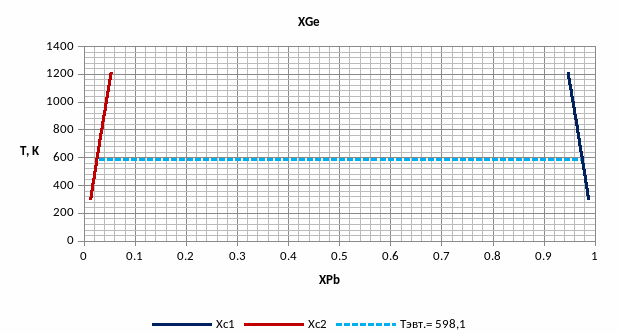
Рис. 14. Спинодали (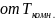 до
до
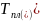 .
.
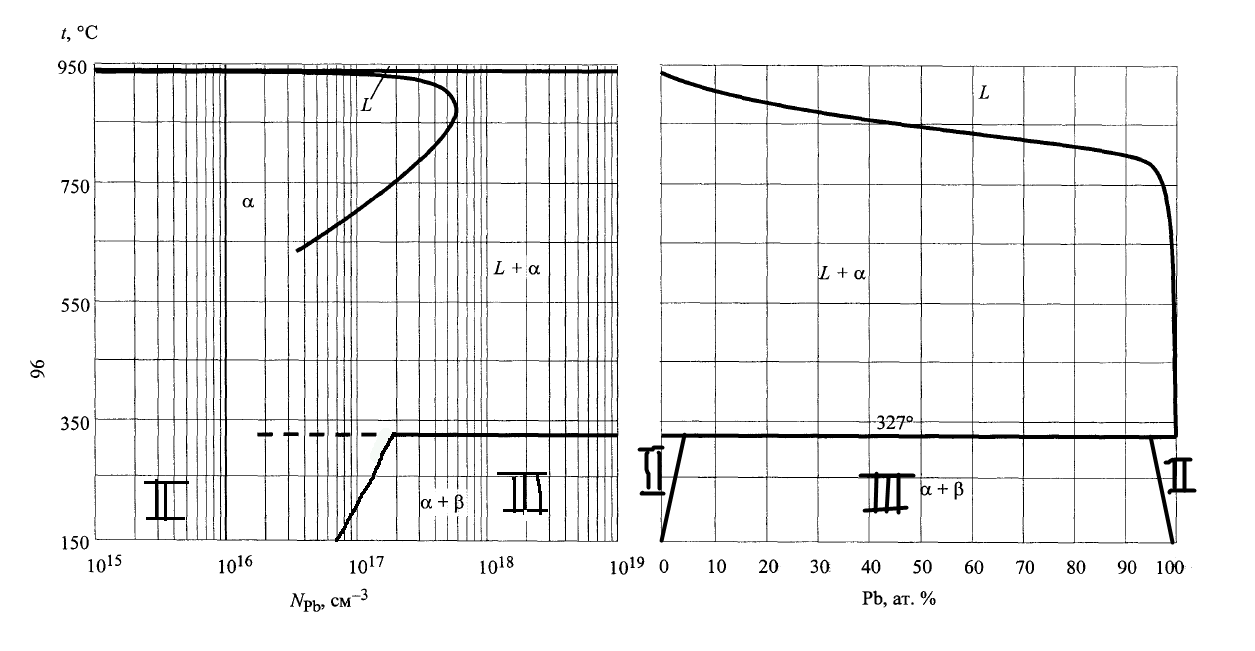
Рис. 14.T-x проекции, где область II - метастабильное состояние и область III- абсолютно неустойчивое, построенные по спинодалям.
Вывод.
Исходя из построенных Т-х проекций ликвидуса (рис. 6.) видно, что модель идеальных раствором подходит для описания только при очень малой доли компонента b, в то время как модели регулярных и квазирегулярных растворов оказываются достаточно точными на всей области проекции.
На построенной зависимости активности Ge в твёрдом растворе (рис. 9.) можно увидеть, что активность практически не отличается от идеальной из-за малой доли примеси Pb в растворе.
В зависимости активности и коэффициента активности (рис. 12.) для жидкого раствора можно увидеть достаточные отклонения от идеальной зависимости, однако есть тенденция роста точности, когда состав раствора становится «чистым» и приближается к одному из компонентов.
Также
был рассчитан равновесный коэффициент
распределения Pb
в полупроводнике Ge
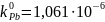 .
Коэффициент имеет очень малое значение,
что отображает очень низкую растворимость
примеси в полупроводнике.
.
Коэффициент имеет очень малое значение,
что отображает очень низкую растворимость
примеси в полупроводнике.