- •3. Закон химических эквивалентов. Молярные массы эквивалентов сложных веществ.
- •4. Волновые свойства электрона. Квантовые числа, s-,p-,d-,f-состояния электрона. Электронные орбитали.
- •5. Принцип Паули. Емкость энергетических уровней и подуровней атомов элементов.
- •6. Связь периодического закона со строением электронных оболочек атомов. Правило Клечковского. Энергетические ячейки. Правило Гунда.
- •7. Периодический закон д.И.Менделеева и периодическая система элементов: ряды, периоды, подгруппы, порядковый номер.
- •8. Периодическое изменение свойств химических элементов. Радиус атомов, сродство к электрону, энергия ионизации, электроотрицательность.
- •9. Образование химической связи. Энергия связи и длина связи.
- •10. Ковалентная (атомная) связь. Метод валентных связей. Возбужденные состояния атомов. Валентность.
- •11. Направленность ковалентной связи. Сигма и п-связи. Гибридизация атомных орбиталей.
- •12. Ионная (электронная) связь.
- •13. Представление о методе молекулярных орбиталей.
- •14. Полярная связь. Полярность молекул и их дипольный момент.
- •15. Донорно-акцепторный механизм ковалентной связи. Комплексные соединения.
- •16. Межмолекулярное взаимодействие. Водородная связь.
- •17. Система. Фаза. Компонент. Параметры. Функции состояния: внутренняя энергия и энтальпия. Стандартные условия.
- •18. Первое начало термодинамики. Закон Гесса как следствие 1-го начала термодинамики.
- •19. Стандартная энтальпия образования. Следствие из закона Гесса. Термохимические расчеты.
- •20. Зависимость теплового эффекта реакции от температуры.
- •21. Второе начало термодинамики. Понятие об энтропии. Расчет энтропии.
- •22. Объединенная формула 1 и 2 начала термодинамики. Свободная энергия Гиббса и Гельмгольца.
- •23. Условия самопроизвольного протекания химических реакций.
- •24. Изотерма химической реакции. Стандартное изменение свободной энергии.
- •25. Константа химического равновесия. Расчет Кр и Кс. Изотерма химической реакции.
- •26. Зависимость константы химического равновесия от температуры (изобара и изохора химической реакции).
- •27. Принцип подвижного равновесия (принцип Ле-Шателье).
- •28. Скорость химической реакции. Закон действующих масс. Константа скорости.
- •29. Кинетическая классификация по степени сложности. Обратимые и необратимые реакции.
- •30. Зависимость скорости реакции от температуры. Правило Вант-Гоффа. Уравнение Аррениуса.
- •31. Энергия активации химической реакции. Аналитический и графический метод расчета.
- •32. Скорость гетерогенной химической реакции.
- •33.Иницирование химической реакции. Катализ. Сущность гомогенного и гетерогенного катализа.
- •34.Дисперсные системы. Коллоидные растворы.
- •36. Физические и химические процессы при растворении. Растворимость твердых тел и жидкостей в жидкостях.
- •37. Растворимость газов в жидкостях. Закон Генри-Дальтона. Закон распределения.
- •38. Законы Рауля.
- •39.Электролитическая диссоциация. Степень диссоциации. Слабые электролиты.
- •40. Константы диссоциации. Закон разведения.
- •41. Сильные электролиты. Понятие активности и коэффициента активности.
- •42. Электролитическая диссоциация воды. Ионные произведения воды. Водородный показатель. Понятие об индикаторах.
- •43. Гидролиз солей.
- •44. Окислительно-восстановительные реакции. Ионно-электронный метод подбора коэффициентов в окислительно-восстановительных реакциях.
- •45. Возникновение скачка потенциала на границе раздела «металл-раствор». Равновесный электродный потенциал.
- •46. Медно-цинковый гальванический элемент. Процессы на электродах. Эдс.
- •47. Зависимость эдс гальванического элемента от природы реагирующих веществ, температуры и концентрации. Стандартная эдс.
- •48. Стандартный водородный электрод. Формула Нернста. Стандартный потенциал. Ряд напряжения.
- •49. Типы электродов и цепей. Окислительно-восстановительные электроды и цепи.
- •50. Электролиз. Последовательность разряда ионов на катоде и аноде.
- •51. Законы Фарадея. Выход по току.
- •52. Коррозия металлов. Химическая и электрохимическая коррозия.
- •53. Основные методы борьбы с коррозией.
- •54. Кристаллическое состояние вещества. Химическая связь в кристаллах.
- •55. Сущность физико-химического анализа. Правило фаз. Диаграмма состояния воды.
- •56.Основные принципы построения диаграммы плавкости бинарных систем. Термографический анализ. Кривая нагревания и охлаждения.
- •57.Диаграмма плавкости однокомпонентной системы на примере воды.
- •58. Поверхностные явления. Понятие поверхностного натяжения.
- •59. Адсорбция и абсорбция
- •60. Поверхностное натяжение растворов. Изотерма адсорбции.
- •Описание
- •61. Полимеры. Методы получения.
- •62. Материалы, получаемые на основе полимеров
59. Адсорбция и абсорбция
Адсорбция— это, в широком смысле, процесс изменения концентрации у поверхности раздела двух фаз, а в более узком и употребительном — это повышение концентрации одного вещества (газ, жидкость) у поверхности другого вещества (жидкость, твердое тело).
Поглощаемое вещество, ещё находящееся в объёме фазы, называют адсорбтив, поглощённое — адсорбат. В более узком смысле под адсорбцией часто понимают поглощение примеси из газа или жидкости твёрдым веществом (в случае газа и жидкости) или жидкостью (в случае газа) — адсорбентом. При этом, как и в общем случае адсорбции, происходит концентрирование примеси на границе раздела адсорбент-жидкость либо адсорбент-газ. Процесс, обратный адсорбции, то есть перенос вещества с поверхности раздела фаз в объём фазы, называется десорбция.
Абсо́рбция (лат. absorptio от absorbere — поглощать) — поглощение сорбата всем объёмом сорбента. Является частным случаем сорбции.
В технике и химической технологии чаще всего встречается абсорбция (поглощение, растворение) газов жидкостями. Но известны и процессы абсорбции газов и жидкостей кристаллическими и аморфными телами (например, абсорбция водорода металлами, абсорбция низкомолекулярных жидкостей и газов цеолитами, абсорбция нефтепродуктов резинотехническими изделиями и т.п.).
60. Поверхностное натяжение растворов. Изотерма адсорбции.
Изотерма адсорбции (англ. adsorption isotherm) — зависимость количества адсорбированного вещества (величины адсорбции) от парциального давления этого вещества в газовой фазе (или концентрации раствора) при постоянной температуре.
Описание
Экспериментальные изотермы адсорбции являются наиболее распространенным способом описания адсорбционных явлений. Методы получения адсорбционных данных для построения изотерм адсорбции основаны на измерении количества газа (жидкости), удаленного из газовой (жидкой) фазы при адсорбции, а также на различных способах определения количества адсорбата (адсорбированное вещество) на поверхности адсорбента (адсорбирующее вещество), например, волюметрический метод, гравиметрический метод и др.
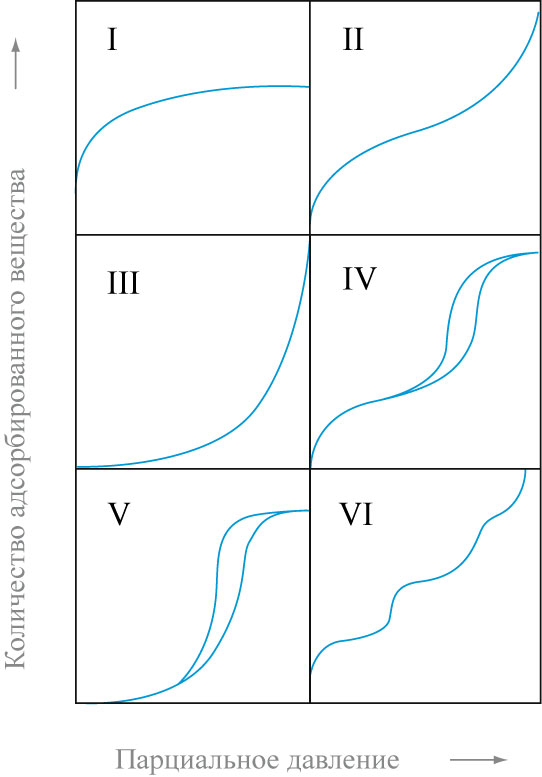
Различают шесть основных типов изотерм адсорбции (см. рис.). Тип I характерен для микропористых твердых тел с относительно малой долей внешней поверхности. Тип II указывает на полимолекулярную адсорбцию на непористых или макропористых адсорбентах. Тип III характерен для непористых сорбентов с малой энергией взаимодействия адсорбент-адсорбат. Типы IV и V аналогичны типам II и III, но для пористых адсорбентов. Изотермы типа VI характерны для непористых адсорбентов с однородной поверхностью.
Изотермы адсорбции используются для расчета удельной поверхности материалов, среднего размера пор или среднего размера нанесенных частиц, распределения пор или частиц по размерам.
Существует несколько методов математического выражения изотерм адсорбции, различающихся моделями, использованными для описания процесса адсорбции. При малых степенях покрытия поверхности адсорбатом для однородной поверхности уравнение изотермы адсорбции имеет вид уравнения Генри: a = Kp, где a — величина адсорбции, p — давление газа, K — константа. При средних степенях покрытия может быть применено эмпирическое уравнение Фрейндлиха: a = kpn, где k и n — константы.
Строгая теория изотермы адсорбции была предложена И. Ленгмюром для модели монослойной адсорбции на однородной поверхности, в которой можно пренебречь силами притяжения между молекулами адсорбата и их подвижностью вдоль поверхности. Уравнение изотермы Ленгмюра имеет вид: a = ambp/(1 + bp), где b — адсорбционный коэффициент, зависящий от энергии адсорбции и температуры; am — емкость монослоя.
Дальнейшее развитие теории состояло в исключении того или иного допущения, использованного Ленгмюром. Так, С. Брунауэром, П. Эмметом и Э. Теллером была предложена теория полимолекулярной адсорбции (метод БЭТ); Т. Хилл и Я. де Бур разработали теорию, учитывающую взаимодействие между адсорбированными молекулами (изотерма Хилла–де-Бура), и т. д.