
- •Антимикробные химиотерапевтические препараты История антибиотикотерапии
- •Классификация антимикробных препаратов
- •Синтетические химиотерапевтические препараты;
- •Ингибиторы синтеза белка:
- •Ингибиторы синтеза нуклеиновых кислот:
- •Продуценты антибиотиков
- •По происхождению (продуценту) антибиотики подразделяются на 3 группы:
- •Принципы получения антибиотиков
- •Перспективные биотехнологические разработки получения антибиотиков:
- •Причины поиска и разработки новых антибиотиков:
- •Требования, предъявляемые к антимикробным препаратам
- •Определение чувствительности бактерий к антибиотикам
- •Антибиотикорезистентность микроорганизмов
- •Приобретенная резистентность:
- •Генетические основы приобретенной резистентности:
- •Нарушение проницаемости
- •Обходной путь
- •Насос выброса
- •Пути борьбы с антибиотикоустойчивыми бактериями:
- •Характеристика антимикробных препаратов
- •А. Антибактериальные препараты:
- •Пенициллины:
- •Полусинтетические пенициллины:
- •Цефалоспорины.
- •Б. Противотуберкулезные препараты:
- •В. Противогрибковые препараты:
- •Г. Противовирусные препараты:
- •Д. Противопротозойные препараты:
- •Осложнения и побочные действия антимикробной терапии
- •Вопросы для контроля усвоения материала
- •Тренировочные тесты
Цефалоспорины.
Цефалоспорины продуцируются плесневым грибом Cephalosporium acremonium. Цефалоспорины не инактивируются пенициллиназой, поэтому они эффективны против грамположительных микробов, устойчивых к пенициллину. Эти
антибиотики применяются для лечения пневмонии, сепсиса, менингита и других инфекций. Цефалоспорины подразделяются на 5 групп, отличающихся между собой по спектру антимикробного действия:
цефалоспорины первого поколения: цефалотин, цефазолин, цефалексин, цефаклор, цефадроксил;
цефалоспорины второго поколения: цефуроксим, цефаклор, цефметазол, цефотиам, цефамандол, цефокситин;
цефалоспорины третьего поколения: цефотаксим, цефтриаксон, цефтазидим, цефтизоксим, цефиксим;
цефалоспорины четвертого поколения: цефпиром, цефепим;
цефалоспорины пятого поколения – цефтобипрол, цефтаролин.
Общая структура и один из цефалоспоринов представлены на рисунке 13.27.


Рисунок 13.27 - Общая структура цефалоспоринов и готовая лекарственная форма цефотаксима.
Цефалоспорины I поколения проявляют активность преимущественно в отношении грамположительных микроорганизмов: Streptococcus spp. и метициллиночувствительных Staphylococcus spp. Обладают невысокой активностью в отношении грамотрицательных бактерий. К цефалоспоринам I поколения чувствительны большинство анаэробов, за исключением B. fragilis. Эти антибиотики применяют преимущественно для лечения инфекций кожи и мягких тканей легкой и средней степени тяжести.
Цефалоспорины II поколения несколько уступают препаратам I поколения по активности в отношении грамположительных кокков, но превосходят в отношении грамотрицательных микроорганизмов. К препаратам II поколения чувствительны Е. coli, Salmonella spp., Proteus mirabilis, Klebsiella spp., Proteus vulgaris, Citrobacter diversus.
Цефалоспорины III поколения проявляют высокую устойчивость к β- лактамазам грамотрицательных микроорганизмов. Они активны в отношении менингококков, гонококков, Н. influenzae и М. catarrhalis, а также всех представителей семейства Enterobacteriaceae. Цефотаксим, цефтриаксон и цефтазидим хорошо проникают через гематоэнцефалический барьер, обеспечивая терапевтические концентрации в ликворе.
Цефалоспорины IV поколения близки к цефалоспоринам III поколения. Однако они лучше проникают через цитоплазматическую мембрану грамотрицательных бактерий и обладают высокой устойчивостью к гидролизу
хромосомными β-лактамазами. В результате этого они могут проявлять активность в отношении P. aeruginosa и неферментирующих грамотрицательных бактерий, резистентных к цефтазидиму. Цефепим также активен в отношении Enterobacter spp., Citrobacterfreundii, Serratia spp., Morganella morganii и др. Препарат показан для лечения тяжелых заболеваний разной локализации, вызванных полирезистентной микрофлорой, а также инфекций на фоне иммунодефицитных состояний.
Монобактамы (азтреонам). Из-за узкого спектра антибактериальной активности его используют в качестве препарата резерва для лечения поражений, вызванных аэробной грамотрицательной флорой, в том числе микроорганизмами семейства Enterobacteriaceae и P. aeruginosa, включая штаммы, устойчивые к аминогликозидам, уреидопенициллинам и цефалоспоринам (рисунок 13.28).

Рисунок 13.28 – Препарат азтреабол, содержащий азтреонам.
Карбапенемы (меропенем или меронем, имипинем) обладают широким спектром антибактериальной активности и высокой устойчивостью к бактериальным β-лактамазам. Они высокоэффективны при полимикробных, в том числе аэробно-анаэробных инфекциях. Карбапенемы применяются при тяжелых поражениях различной локализации преимущественно в качестве препаратов резерва. Общая структура и примеры карбапенемов представлены на рисунке 13.29.
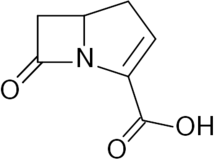


Рисунок 13.29 - Общая структура и готовые лекарственные формы карбапенемов.
Гликопептиды (ванкомицин, тейкопланин) обладают относительно узким спектром действия на грамположительные аэробные и анаэробные микроорганизмы: стафилококки (в том числе метициллинрезистентные), стрептококки, пневмококки, энтерококки, пептострептококки, коринебактерии, клостридии. В отношении большинства микроорганизмов они оказывают бактерицидный эффект, связанный с нарушением синтеза клеточной стенки. На энтерококки, некоторые стрептококки и коагулазонегативные стафилококки действуют бактериостатически. Гликопептиды -
это препараты выбора при инфекциях, вызванных метициллинрезистентными стафилококками, энтерококками, устойчивыми к ампициллину и аминогликозидам. Ванкомицин обладает ото- и нефротоксичностью. Общая структура и пример гликопептидов представлены на рисунке 13.30.
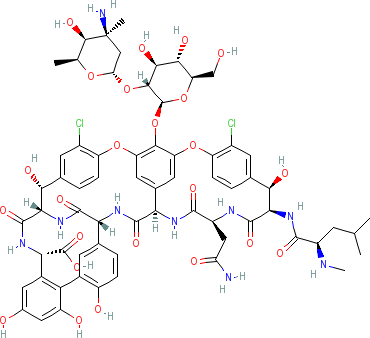

Рисунок 13.30 – Ощая структура и готовая лекарственная форма ванкомицина.
Полипептиды (грамицидин, бацитрацин, ристомицин, полимиксины). Грамицидин - это полипептид, продуцируемый В. brevis. Этот антибиотик обладает активностью в отношении стафилококков, стрептококков, сальмонелл, кишечной палочки, бацилл, клостридий и других бактерий. Бацитрацин – это антибиотик, продуцируемый B. subtilis. Наибольшую активность он проявляет по отношению к грамположительным бактериям. Используется при лечении инфицированных ран. Оказывает токсическое действие на почки. Ристомицин – антибиотик, продуцируемый Proactinomyces fructiveri. Подавляет развитие стафилококков, стрептококков, листерий, бацилл, клостридий. Полимиксины (полимиксин В, полимиксин Е или колистин, полимиксин М) – группа антибиотиков, образуемых некоторыми штаммами B. polymyxa. Антибиотики этой группы проявляют активность в отношении грамотрицательных бактерий (синегнойной палочки, кишечной палочки, сальмонелл, пастерелл и других бактерий). К полимиксинам резистентны кокки, микобактерии, протей. В обычно применяемых дозах антибиотики этой группы оказывают бактериостатическое действие, а в высоких концентрациях только бактерицидное. Полимиксины токсичны, поэтому чаще всего применяются местно.
Макролиды (эритромицин, азитромицин, кларитромицин, спирамицин, рокситромицин и другие) - антибиотики, обладающие бактериостатическим действием и преимущественной активностью в отношении грамположительных кокков (кроме энтерококков) и внутриклеточных возбудителей (хламидии, микоплазмы, кампилобактеры). Макролиды относятся к числу наименее токсичных антибиотиков. Их назначают при инфекциях дыхательных путей, кожи, мягких тканей и мочеполовой системы. На рисунке 13.31 представлена основа химической структуры и пример макролидов.
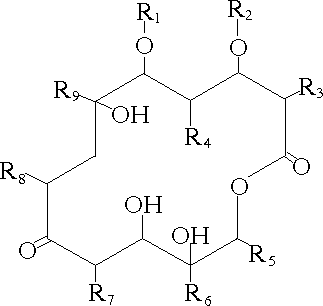

Рисунок 13.31 - Основа макролидов – макроциклическое лактамовое кольцо и готовая лекарственная форма эритромицина.
Тетрациклины - группа антибиотиков широкого спектра действия. Они активны в отношении кокков, клостридий, кишечной палочки, трепонем, бактероидов, микоплазм, риккетсий, хламидий, бруцелл. Тетрациклины подразделяют на природные (хлортетрациклин, окситетрациклин, тетрациклин) и полусинтетические (доксициклин, метациклин, морфоциклин). Все тетрациклины имеют одинаковый спектр активности. У микроорганизмов тетрациклины подавляют синтез белка. Хлортетрациклин (биомицин) выделен из Act. aureofaciens. Антибиотик применяют при салмонеллезах, бруцеллезе и других инфекциях. Тетрациклин вначале был получен химическим путем из хлортетрациклина путем удаления из его молекулы атома хлора. Позже этот антибиотик был получен путем биосинтеза из актиномицета. Препарат вызывает меньше побочных явлений, чем хлортетрациклин. Окситетрациклин (террамицин) образуется Act. rimosus. По своим свойствам он близок к хлортетрациклину. В отличие от хлортетрациклина в его формуле атом хлора заменен гидроксильной группой (ОН). Морфоциклин - синтетический препарат, полученный из тетрациклина, в котором один атом водорода в карбоксильной группе замещен группой метилморфина. Этот антибиотик действует на те же микробы, что и тетрациклин, но более активен в отношении микоплазм. Его токсичность ниже других тетрациклинов. Разрушается в кислой и щелочной средах, поэтому не применяется перорально.
Тетрациклины вызывают нарушения функций желудочно-кишечного тракта и аллергические реакции, обладают гепатотоксичностью. Основу тетрациклинов составляет четырехциклическая система (рисунок 13.32).



Рисунок 13.32 - Основа тетрациклинов – четырехциклическая система и готовые лекарственные формы тетрациклинов.
Аминогликозиды (стрептомицин, гентамицин, амикацин, тобрамицин, канамицин) - это группа антибиотиков широкого спектра действия. Они подразделяются на три поколения.
Аминогликозиды I поколения (стрептомицин, неомицин и канамицин) в настоящее время имеют ограниченное применение. Стрептомицин синтезируется Act. streptomycini. Он подавляет рост грамположительных и грамотрицательных микробов (стафилококков, стрептококков, салмонелл, шигелл, возбудителя туберкулеза). Антибиотик действует на микробы бактерицидно. Стрептомицин не подавляет рост анаэробных бактерий, грибов, риккетсий. К стрептомицину быстро вырабатывается резистентность, поэтому он применяется часто в сочетании с други- ми антибиотиками. При длительном парентеральном применении стрептомицина отмечается поражение органа слуха. Стрептомицин обладает общим нейротоксическим действием: угнетает дыхание, нарушает выделительную функцию почек.
Неомицин - антибиотик, продуцируемый Act. fradiae. Его антибактериальная активность выше, чем у стрептомицина, но он более токсичен. Вызывает потерю слуха и поражение почек, в связи с чем используют редко.
Канамицин выделен из культуральной жидкости Act. kanamyceticus. По биологическим свойствам он сходен со стрептомицином и неомицином.
Аминогликозиды II поколения (гентамицин) и III поколения (сизомицин, тобрамицин, амикацин, нетилмицин) активны в отношении микроорганизмов семейства Enterobacteriaceae, неферментирующих грамотрицательных бактерий (P. aeruginosa, Acinetobacter spp.), стафилококков. Аминогликозиды обладают ототоксичностью и нефротоксичностью. Представители аминогликозидов представлены на рисунке 13.33.
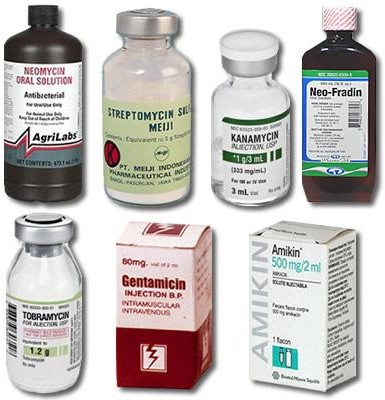
Рисунок 13.33 – Готовые лекарственные формы аминогликозидов.
Ансамицины (рифамицин, рифампицин, рифабутин). Рифампицин обладает широким спектром антимикробной активности. Действует бактерицидно. Рифампицин является противотуберкулезным препаратом. Применяют для лечения стафилококковых инфекций, атипичных микобактериозов, бруцеллеза. К
рифампицину у бактерий быстро развивается резистентность. Наиболее частым побочным эффектом являются гепатотоксические реакции. Химическая структура и представитель ансамицинов представлены на рисунке 13.34.

Рисунок 13.34 – Химическая структура и готовая лекарственная форма рифампицина.
Хинолоны и фторхинолоны являются производными хинолин- карболовой кислоты. Среди хинолонов выделяют нефторированные препараты (налидиксовая кислота, оксолиновая кислота, пипемидиевая кислота) и фторированные препараты. Клиническое применение нефторированных хинолонов ограничивается лечением инфекций мочевыводящих путей и кишечника, что обусловлено их узким спектром активности. Эти препараты ингибируют активность ДНК-гиразы, что препятствует спирализации молекулы ДНК. В группе фторхинолонов выделяют 3 поколения препаратов:
I поколение - ципрофлоксацин, энрофлоксацин, офлоксацин, пефлоксацин, норфлоксацин, ломефлоксацин;
II поколение - левофлоксацин;
III поколение - моксифлоксацин.
Структура хинолонов и фторхинолонов представлена на рисунке 13.35.


Рисунок 13.35 – Структура хинолонов и фторхинолонов и готовая лекарственная форма ципрофлоксацина.
Фторированные хинолоны отличаются широким спектром антимикробного действия, высокой бактерицидной активностью и хорошей фармакокинетикой, что позволяет применять их для лечения инфекций различной локализации. Для фторхинолонов разработаны лекарственные формы для внутривенного введения. Фторхинолоны активны в отношении большинства штаммов грамотрицательных и ряда грамположительных аэробных бактерий. Наиболее распространенные
побочные реакции при использовании фторхинолонов - расстройства со стороны желудочно-кишечного тракта, аллергические реакции, нарушения со стороны центральной нервной системы. Фторхинолоны хорошо сочетаются с другими антибиотиками (аминогликозидами, пенициллинами, цефалоспоринами и др.)
Линкозамиды - группа антибиотиков, включающая линкомицин и клиндамицин (рисунок 13.36). Они обладают узким спектром антимикробной активности: оказывают бактериостатическое действие на стафилококки, стрептококки, пневмококки и неспорообразующие анаэробы. К ним быстро развивается резистентность, особенно у стафилококков. При их применении развиваются тромбоцитопения и аллергические реакции.


Рисунок 13.36 – Линкозамиды.
Амфениколы (хлорамфеникол или левомицетин). Хлорамфеникол выделен из актиномицета (Act. venezuelae). Он является антибиотиком широкого спектра действия. Обладает активностью в отношении большинства грамотрицательных и грамположительных микроорганизмов. После установления химического состава антибиотик был получен синтетическим путем. Синтетическим аналогом хлорамфеникола является левомицетин (рисунок 13.37).


Рисунок 13.37 – химическая структура и готовая лекарственная форма левомицетина.
Сульфаниламиды (сульфадимезин, сульфадиметоксин, сульфаметоксазол) – это группа химических веществ, производных пара- аминобензолсульфамида. Сульфаниламиды по структуре схожи с парааминобензойной кислотой (ПАБК), необходимой для синтеза фолиевой кислоты. В процессе развития вместо ПАБК бактерии включают в метаболизм сульфаниламидные препараты, в результате чего вместо фолиевой кислоты синтезируются ее нефункциональные аналоги. Они оказывают бактериостатическое действие. Спектр активности сульфаниламидов включает грамположительные (стрептококки, стафилококки) и грамотрицательные микроорганизмы
(энтеробактерии), а также грибы. Сульфаниламиды обладают высокой токсичностью, вызывают нарушение функций ЦНС, почек, печени.
Нитрофурановые препараты (фурагин, фуразолидон, нитрофурантоин)
это антимикробные препараты, производные фурана (пятичленного гетероциклического соединения), у которого атом водорода замещен нитрогруппой. Они тормозят дыхание микробной клетки, одновременно блокируя несколько ферментных систем. Оказывают бактерицидное действие. Используются для лечения ран, острых неосложненных инфекций мочевыводящих путей (нитрофурантоин, фуразидин) и кишечных инфекций (фуразолидон). Они обладают токсичностью: могут нарушать функции желудочно-кишечного тракта, печени, нервной системы, вызывать аллергические реакции.
Нитроимидазолы (метронидазол, тинидазол, орнидазол, секнидазол) – группа синтетических антимикробных препаратов. Проявляют бактерицидный эффект в отношении грамотрицательных анаэробных бактерий. Механизм действия заключается в нарушении репликации ДНК и синтеза белка.
Производные хиноксалина (диоксидин, хиноксидин) – это группа синтетических противомикробных препаратов, оказывающих бактерицидное действие в результате нарушения синтеза ДНК. Эти соединения обладают активностью в отношении вульгарного протея, синегнойной палочки, кишечной палочки, сальмонелл, стафилококков, стрептококков и других бактерий. Применяются при лечении тяжелых гнойных воспалительных процессов.
Пиримидины (триметоприм, пириметамин) – химические антибактериальные препараты, механизм действия которых связан с ингибированием синтеза фолиевой кислоты. Это приводит к нарушению синтеза нуклеиновых кислот и белка в бактериальной клетке. Эти препараты обладают активностью против грамотрицательных и некоторых грамположительных бактерий. Их применяют при инфекциях желудочно-кишечного тракта и мочеполовой системы. Комбинация триметоприма с сульфаметоксазолом (бисептол) оказывает бактерицидное действие, хотя оба компонента - бактериостатики.
Оксазолидиноны. Единственный представитель группы оксазолидинонов - линезолид. Он ингибирует биосинтез белка на этапе связывания тРНК с бактериальной рибосомой. Линезолид проявляет высокую активность к большинству грамположительных бактерий. Используется для лечения инфекционных заболеваний кожи, мягких тканей, пневмонии.
Группа защищенных антибиотиков. В связи с увеличением числа бактерий, продуцирующих β-лактамазу, и возрастанием их роли в патологии человека были разработаны препараты, состоящие из двух компонентов: бета- лактамного антибиотика и ингибитора бета-лактамаз. Первоначально такие препараты назывались потенцированными пенициллинами, в настоящее время их объединяют в группу защищенных антибиотиков. Ингибиторы – это вещества бета- лактамной природы, которые обладают низкой антибактериальной активностью. Однако, связываясь с бета-лактамазами они ингибируют их активность. Таким способом ингибиторы защищают антибиотик от гидролиза. В качестве ингибиторов используются клавулановая кислота, сульбактам и тазобактам. В группу защищенных антибиотиков включены комбинация ампициллина с сульбактамом, амоксициллина с клавулановой кислотой (панклав).
