
1 курс 1 семестр / Химия / Biochemisry.Obmen_veschestv
.pdf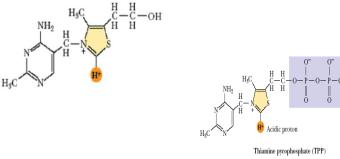
(биотин -антисеборейный,факторростабактери), |
|
|
В9 или |
Вс фол( кислотаевая |
- |
||
антианемический), |
В12 кобаламин( |
|
-антианемический), |
С (аскорбиноваякислота |
- |
||
антискорбутный), |
Р витамин( проницаемости,рутин). |
|
|
|
|
||
Длякровнеобходимытворенияфолкислотациев янкобалам,дляэнергетическогон |
|
|
|
|
|||
обмена –тиамин,рибофлавин,никотинамид,пантот |
|
еноваякислота,пиридоксин,биотин. |
|
|
|||
- |
жирорастворимые:витамины |
А ретинол( |
-антиксерофтальмический), |
D |
|||
(кальциферол -антирахитический), |
Е (α -токоферол -витразмножениямин), |
К (филлохинон – |
|||||
антигеморрагический, |
F (смесьполиненасыщенныхвысшжирныхк сл |
|
от:линолевой, |
|
||
линоленоварахидоновой, ). |
|
|
|
|
|
|
Водорастворимыевитаминыявляютсясубстрадлясинтезакоферментовами |
|
–важных |
||||
регулятоферментовактивн.ИсключениеостисоставляеттольковитаминС,егодействие |
|
|
|
|||
органинесвязаменоимодействиемферментами. |
|
|
|
|
|
|
Коферменпринимаютучастиевмодификацииысубстфератовре,нтативныхакцийпри |
|
|
|
|||
этомсамодифицируют |
ся – принимают« насебя»функциональныегруппыорганических |
|
|
|||
молекул (метильные,карбоксильные,гидроксильные,сульфг,ам )дрильныеногруппы |
|
.Сразу |
||||
жепослезавбиохиршенияреакции,мическойодифицированныекоферпомощьюенты |
|
|
|
|||
специальферментоввосстых |
|
анавлдосвоихваютсясходныхформ.Такимобр, ждыйзом |
|
|
|
|
коферментвитамин()будетиспользоватьсямног,чтокрегоеделяетатномалую |
|
|
|
|||
потребностьворганизме. |
|
|
|
|
|
|
Такиеважныефункциикоферментоввитаминов( ),естественно,могутбытьобеспечены |
|
|
|
|||
толькопри |
налунихунчи,узнаваемойикальной« »ферментструктуры.Нижерисункахми |
|
|
|
||
приведеформулыхимичнекскиеводораствторыхвитаминовсо тветствующихримых |
|
|
|
|||
имкоферментов. |
|
|
|
|
|
|
Водорастворимыевитамины. |
|
|
|
|
|
|
Табл.4.1 |
|
|
|
|
|
|
Витамин |
|
Коферменты |
Биологическаяроль |
Дефицит |
|
|
|
|
|
|
|
витаминаего |
|
|
|
|
|
|
проявление |
|
|
|
|
Ворганизметиамин |
Реакция |
Придефиците |
|
|
|
|
преобразуетсяв |
окислительного |
(несбалансированн |
|
) |
|
|
кофермент - |
декарбоксилирования |
оепитание, |
|
|
|
|
|
кетокислотпирува( , |
алкоголизм) |
|
|
|
|
(ТПФ): |
α-кетоглутарат). |
накапливаются |
|
|
|
|
|
Транскетолазная |
недоокисленные |
|
|
|
|
|
реакцияпревращения |
(токсические) |
|
|
|
|
|
пентоз |
продукты |
|
|
|
|
|
(пентозофосфатный |
углеводного |
|
|
|
|
|
путьокисления |
обмена.Бери |
-бери |
|
|
|
|
глюкозы). |
(полиневриты, |
|
|
|
|
|
|
поражения |
|
|
|
|
|
|
сердечно- |
|
|
|
|
|
|
сосудистой |
|
|
|
|
|
|
сис,отеи мыки |
|
|
|
|
|
|
мышечная |
|
|
|
|
|
|
атрофия)Синдром. |
|
|
|
|
|
|
Вернике-Корсакова |
|
|
|
|
|
|
(алкоголь). |
|
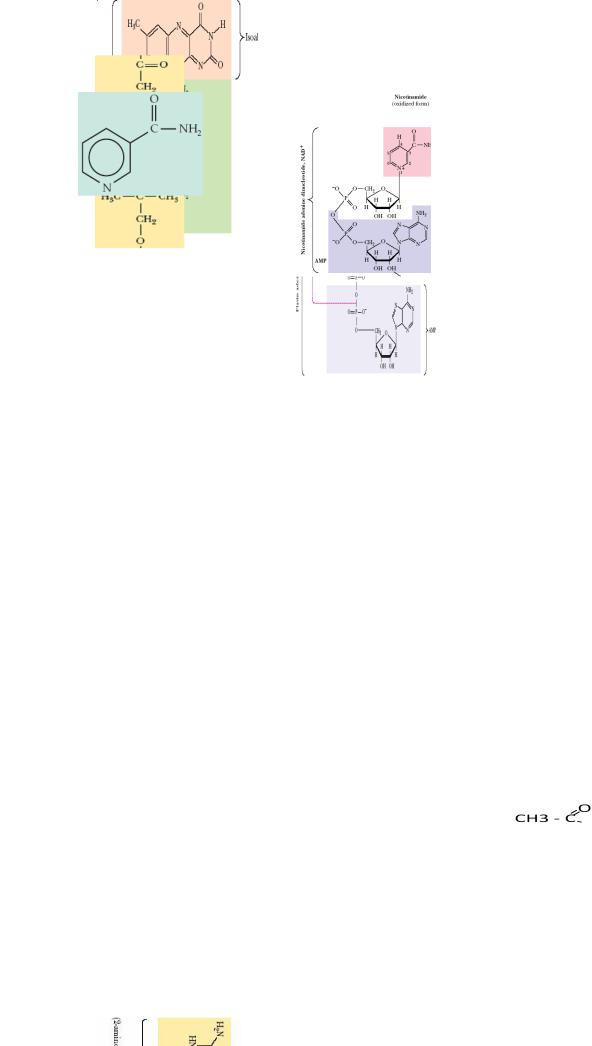
Рибофлавин |
|
Структурный |
Окислительно- |
Дефицит |
|
|
(В 2,витаминроста) |
|
элемент |
восстановительные |
снижает |
|
|
|
|
|
(предшественник)двух |
реакции.Перенос |
сопротивляемость |
|
|
|
|
важныхкоферментов |
атомовН. |
организма, |
|
|
|
|
оксидоредуктаз: |
ФМНпереносит |
вызывает |
|
21
|
|
|
Структурный |
|
Окислительно- |
Дефицит |
|
||
(В 2, |
|
|
элемент |
|
восстановительные |
снижает |
|
|
|
|
|
|
(предшественник)двух |
|
реакции.Перенос |
сопротивляемость |
|||
|
|
|
важныхкоферментов |
|
атомовН. |
|
организма, |
|
|
|
|
|
оксидоредуктаз: |
|
ФМНпереносит |
вызывает |
|
||
|
|
|
|
|
атНодругогомыт |
расстройства |
|
||
|
|
|
( )и |
|
коферментаНАД(). |
нервнойсистемы |
|
||
|
|
|
|
|
ФАДпереносит |
пищеварения |
|
||
|
|
|
тида( |
|
атомыводородаот |
(колиты |
|
|
|
|
|
|
|
|
восстановленных |
гастриты),кожн е |
|
||
|
|
|
|
|
субстратов. |
заболевания |
|
||
|
|
|
|
|
|
|
(трещины, |
|
|
|
|
|
|
|
|
|
изъязвлениявокруг |
|
|
|
|
|
|
|
|
|
ноздрейирта), |
|
|
|
|
|
|
|
|
|
поврежденияглаз |
|
|
|
|
|
|
|
|
|
(кератиты, |
|
|
|
|
|
|
|
|
|
катаракта), |
|
|
|
|
|
|
|
|
|
возникает |
|
|
|
|
|
|
|
|
|
непереносимость |
||
|
|
|
|
|
|
|
яркогосвета |
|
|
|
|
|
|
|
|
|
(фотофобия). |
|
|
|
|
|
|
|
|
||||
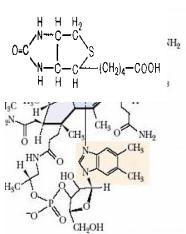
НикотинамидВ( |
5), |
Никотинамидаденин |
ПереноситатомыН |
Дефицит |
|
||||
витаминРР( |
Preventive |
-динуклеотидНАД(), |
|
вокислительно - |
приводитк |
|
|||
Pellagra), |
|
|
никотинамидадениндин |
восстановительных |
развитиюпеллагры |
||||
противопеллагрический |
уклеотидфосфат |
|
реакциях. |
(отитал. |
Pelle |
|
|||
|
|
|
(НАДФ): |
|
|
|
agraшершавая |
|
|
|
|
|
|
|
|
|
кожа)Пеллагра. |
– |
|
|
|
|
|
|
|
|
болезнь«3Д»: |
|
|
|
|
|
|
|
|
|
агрессивный |
|
|
|
|
|
|
|
|
|
Дерматит(1), |
|
|
|
|
|
|
|
|
|
фонтанирующая |
||
|
|
|
|
|
|
|
Диар(2),неярвно |
- |
|
|
|
|
|
|
|
|
психические |
|
|
|
|
|
|
|
|
|
расстройства |
|
|
|
|
|
|
|
|
|
форме Деменции |
||
|
|
|
|
|
|
|
(3). |
|
|
|
|
|
|
|
|
|
|
||
Пантотеноваякислота |
|
Входитвсостав |
|
Переносрадикалов: |
Дефицит |
|
|||
(В 3,антидерматитный |
коферментаАКоА( |
SH) |
ацетила( |
) |
|
||||
витамин) |
|
|
–учавсехтника |
|
иацила( |
R-COO): |
развиваетсяпри |
|
|
|
|
|
реацилированиякций: |
|
участиев |
хронических |
|
||
|
|
|
|
|
метаболизмежирных |
заболеваниях, |
|
||
|
|
|
|
|
алколизме. |
|
|||
|
|
|
|
|
кислот,холестерина |
|
|||
|
|
|
|
|
Характерны |
|
|||
|
|
|
|
|
егопроизводных: |
|
|||
|
|
|
|
|
поражения |
|
|||
|
|
|
|
|
стергормонов,идных |
|
|||
|
|
|
|
|
периферической |
||||
|
|
|
|
|
желчныхкислот, |
||||
|
|
|
|
|
нервнойсистемы |
|
|||
|
|
|
|
|
|
|
|
||
ФолиеваякислотаВ( |
9, |
Преобразуетсяв |
|
1)Перенос |
Мегалобластная |
||||
В ,антианемический |
кофермсинтезант |
|
одноуглеродных |
анемия. |
|
22 |
|||
ЦианкобаламинВ( |
12, |
Необходимдля |
Реакциипереноса |
Дефицитв |
|
|
антианемическийвитамин |
|
образованиядвух |
метильнойгруппы. |
продуктахпитания |
|
|
|
|
коферментов: |
Реакции |
илинарушение |
|
|
|
|
дезоксиаденозилкобала |
превращения |
всасывания |
|
|
|
|
мина |
рибонуклеотидов |
витаминаприводит |
|
|
|
|
метилкобаламина. |
дезоксирибонуклеоти |
краз |
витию |
|
|
|
Принимаетучастиев |
ды. |
пернициознойот( |
||
|
|
превращении |
В12 принимает |
лат. |
Perniciosus- |
|
|
|
метилмалонила. |
частиевпревращении |
губительный) |
|
|
|
|
|
ВЖК,аминокислот, |
анемии. |
|
|
|
|
|
азотистыхоснований. |
Придефиците |
|
|
|
|
|
|
В12 накапливается |
||
|
|
|
|
ВЖКс |
|
|
|
|
|
|
разветвленной |
||
|
|
|
|
цепьюи |
|
|
|
|
|
|
нарушается |
|
|
|
|
|
|
структумембран |
|
|
|
|
|
|
нервныхтканей. |
|
|
|
|
|
|
Приэтом |
|
|
|
|
|
|
вывбодитсяльшое |
|
|
|
|
|
|
количество |
|
|
|
|
|
|
метилмалоновой |
||
|
|
|
|
кисло.Теснаты |
|
|
|
|
|
|
авитаминозВ |
12. |
|
Биотинвитамин( Н, |
|
Коферментная |
Участиев |
Дефицит |
|
|
антисеборейный) |
|
форма – |
реакциях,связанных |
биотинавозникает |
|
|
|
|
карбоксибиотин. |
присоединением |
очредко,нь |
|
|
|
|
|
диоксидауглерода. |
характеризуется |
||
|
|
|
Входитвсостав |
дерматитом |
|
|
|
|
|
пируваткарбоксилазы, |
воспалением |
|
|
|
|
|
ацетил-КоА- |
сальныхжелез |
|
|
|
|
|
карбоксилазы, |
(себореей), |
|
|
|
|
|
пропионил-КоА- |
выпадениемволос, |
|
|
|
|
|
карбоксилазы. |
поражением |
|
|
|
|
|
Необходимдля |
ногтей,депре |
ссией. |
|
|
|
|
глюконеогенеза, |
|
|
|
|
|
|
синтезавысших |
|
|
|
|
|
|
жирныхкислот, |
|
|
|
|
|
|
образования |
|
|
|
|
|
|
оксалоацетата, |
|
|
|
|
|
|
окисления |
|
|
|
|
|
|
пропкислотыоновой |
|
|
|
|
|
|
вциклеКребса. |
|
|
|
Витамин 6, |
|
|
Кофермент |
Низкийуровень |
|
|
пиридоксин,пиридоксаль, |
|
|
ферментовобмена |
всывороткепри |
|
|
пиридоксамин, |
|
|
аминокислотв |
беременности |
||
антидермитный |
|
|
реакциях |
приемеоральных |
|
|
|
|
|
трансаминированияи |
контрацептивов. |
||
|
|
|
декарбоксилирования |
Антагонисты – |
||
|
|
|
|
изиниазид, |
|
|
|
|
|
|
пеницилламин |
||
|
|
|
|
другие |
|
|
23

|
|
|
|
|
|
Кофермент |
Низкийуровень |
|
|
|
|
|
|
|
ферментовобмена |
всывороткепри |
|
|
|
|
|
|
|
аминокислотв |
беременности |
|
|
|
|
|
|
|
реакциях |
приемеоральных |
|
|
|
|
|
|
|
трансаминированияи |
контрацептивов. |
|
|
|
|
|
|
|
декарбоксилирования |
Антагонисты – |
|
|
|
|
|
|
|
|
изиниазид, |
|
|
|
|
|
|
|
|
пеницилламин |
|
|
|
|
|
|
|
|
другие |
|
|
|
|
|
|
|
|
лекарственные |
|
|
|
|
|
|
|
|
средства. |
|
|
|
|
|
|
|
|
||
Аскорбиноваякислота |
|
|
Неизвестны |
|
Коферментв |
Цинга (анемия, |
||
(витаминС) |
|
|
|
|
|
реакциях |
плохоезаживление |
|
|
|
|
|
|
|
гидроксилирования |
ран,поражение |
|
|
|
|
|
|
|
пролинализина |
кровоточивость |
|
|
|
|
|
|
|
(синтезколлагена), |
десен,потеря |
|
|
|
|
|
|
|
антиоксидант, |
цементаз |
убов, |
|
|
|
|
|
|
усиливаетвсасывание |
подкожные |
|
|
|
|
|
|
|
железа,необходим |
кровотечения( |
|
|
|
|
|
|
|
длякатаболизма |
питехии) |
|
|
|
|
|
|
|
тирозина. |
|
|
|
|
|
|
|
|
|
|
|
ВитаминРвитамин( |
|
|
|
|
|
Биологическое |
Гиповитаминоз |
|
проницаемости,рутин) |
|
|
|
|
действиесвязано |
витаминаРпохож |
|
|
|
|
|
|
|
|
аскорбиновой |
нагиповитами ноз |
|
|
|
|
|
|
|
кислотой. |
аскорбиновой |
|
|
|
|
|
|
|
Регулирует |
кислоты. |
|
|
|
|
|
|
|
проницаемостьстенок |
|
|
|
|
|
|
Антивитамины |
|
|
||
Этовещества,которыенарушаютфункциивитаминовмогутвызвасостояниеь |
|
|
|
|
|
|||
авитаминозадажепридостаточномобеспеченииорганизвита.Какпрм,инамивило |
|
|
|
|
|
|||
антивитамиблокируютактивцентферментовны. ы |
|
|
|
|
|
|
|
|
Существует двегруппыантивит: структурные1) аналогивитаминов; вещ2), ества |
|
|
|
|||||
являющиесяструктурныантивитаминааналогамивитам.Пр меромновпервойгруппы |
|
|
|
|
|
|||
являетсягидразизоникотиновойкислотыд |
|
|
–антивитаминпирид.Ковтгруппеоксинарой |
|
|
|||
относится,нап |
ример,тиаминаза |
–фе,расщепляющийментвитаминВ |
1. |
|
|
|||
|
|
Глава5ВВЕДЕНИЕ. БИОЭНЕРГЕТИКУ |
|
|
|
|||
Метаболизмобмен(веществ) |
|
|
— этос вокупнохимическихреакций, ть |
|
протекающихв |
|||
клеткоргсмоментанизмахпоступленияпищевыхвеществдообразоваконечнияых |
|
|
|
|
|
|||
продуктовбмена. |
|
|
|
|
|
|
|
|
Функцииметаболизма |
: |
|
|
|
|
|
|
|
▪cнабжклетокхимическойниеэнергие;
▪ |
превращениемолекулпищистроительныеблоки |
–низкомолекулярные |
24

органическиесо единенияамин( , окиносахариды,спирт,жирныелокислоты);
▪сборкаизэтихблоковкомпонентовклеткибе( ,липидовков,нуклеинкисл); отвых
▪синтезразрушенспециализированныхб ологическихмолекулнапример( ,гема,
холина).
Метаболическийпуть |
— |
этоп следоватхимичпреевльностьскихеществаращений. |
|
|
Метаболическиепутимногоэтапны,взаимо,регулируемыскоординированы, вязаны |
|
|||
пространстве.Онибываютлинейныинтезнапр( ,распадмергликогена,гликолиз, |
|
|
||
окислежиркислот)нцыхклическим |
|
ицикл( трикарбоновыхкислот,орнитиновыйцикл): |
|
|
E1 E2 |
E3 E4 |
E5 |
— примерлинейнометаболическогопути, деS |
—исходный |
S → A → B → C → D → P |
||||
субстрат,Р |
—конечныйпродукт,А,В,С, D |
—метабпр( омежуточныелитыпродукты),Е |
1-5 - |
|
ферменты. |
|
|
|
|
Ферменфермент( ),коопыскоростьыееделяютвсегопроцессацелом,называются ключевымирегуляторными( )Онкатализируют. необрреакции, тимыечетютвертичную структуру,инаихктивносвлияюнизкомолекулярныетэффекторыь.
Двестор оныметаболизма:
1.Анаболизм — процесссинтезасложныхвеществизболеепростых,идущий
затратойэнергииввидеАТФ.
2.Катаболизм —процессрасщеплениясложныхмолекулдоболеепростых,идущий выделенэнерг. иеми
Анаболизмкатаболизмтесно |
|
|
|
|
взаимосвязаны: |
|
|
|
|
||||
|
Пищевыевещества |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Метаболиты |
|
|
|
|
|||||
Катаболизм |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Энергия |
Анаболизм |
|
|
|||||||
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Образоваконечныхие |
|
|
|
Функциональная активность |
|
|
Синтез |
||||||
продуктовбмена |
|
|
|
(актраиввеществныйспорт, |
|
|
|
структурнофункцио- |
|||||
(углекислогогазаводы, |
|
|
|
|
|
мышечнработ, ая |
|
|
|
нальныхкомпонентов |
|||
мочевина) |
|
|
|
|
теплопродукциядр.) |
|
|
|
клетки |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 5.1 Общаясхемаобменавеществиэнергии.
Обменвеществсостоитизтрехэтапов: |
|
|
1)поступ лениевеществорганизм; |
|
|
2)метаболизм,илипромежуточныйоб; ен |
|
|
3)выделконпрениечныходуктовбмена |
|
|
Реакциикатаболизмасопровождаютсявыделенэнергэкзе( иемигонические),кции |
|
|
еёиспольсвяреакцзаноованиеанаболфизямиактивностьюзмаолгическойрганиз |
ма |
|
(эндереакциигонические). |
|
|
Прямпреохимическойбразованэнергисубстрэнергиюматовкроэргическихсвязей |
|
|
АТФневозм.Этотпрразбитцессжнонадвестадии: |
|
|
1 |
2 |
|
Окислениесубстратов |
%%→химическаяэнергия |
%%%%%%→АТФ |
|
Макроэргическиесоединения |
|
Этоорганическиесоединения,которыемакроэргическиееютсвязи,то тьвязи,пр |
|
|
гидролитичекоторыхмрасщеплениивы вболеебождается30кДж/моль |
|
(иликкал7/моль) |
25
энергии.Макрсвязьобозначаеэргическаяволинией, стойся |
|
|
знакомтильда« ». |
|||
|
Кчислумакроэргсоедиотнчосятсяуклеозидтрифосфатыенийских, |
|
|
|||
нуклеозиддифосфаты,креатинфосфат, 1,3 |
-дифосфог,ацетилицерат |
-КоАфосфоенолпируват |
||||
другие. |
|
|
|
|
|
|
|
Ведущаябиолросредигическаяльвсехмакроэргсоединенийпринадлежитчских |
|
АТФ. |
|||
|
|
|
|
|
|
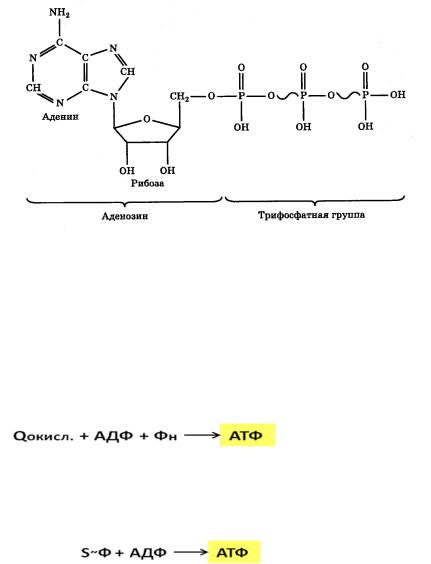
АТФсодержитве |
|
|
|
|
|
|
макроэргическиесвязи:между |
|
|
|
|
|
|
первымивторым,атакже |
|
|
|
|
|
|
междувтоирыметьим |
|
|
|
|
|
|
остатфосфорнойкамиислоты. |
|
|
|
|
|
|
АТФиспоклеткамиьзуется |
|
|
|
|
|
|
дляпроцебиосинтезасов |
|
|
|
|
|
|
(анаболическиереакции), |
|
|
|
|
|
|
активацмногихмолекули |
|
|
|
|
|
|
(глюкоза,глицерол), |
|
|
|
|
|
|
выполнениямеханической |
|
|
|
|
|
|
работы,первечерезществноса |
|
|
|
|
|
|
мембраны. |
|
|
|
|
СинтезАТФ |
|
|
|
СиАТФназываетсятезфосфорилированием: |
|
|
|||
|
АДФ+Н |
3РО4 =АТФ+Н |
2О. |
|
|
|
|
Дляэтойреакциитребуетсяменее32кДж/мольэнергии. |
|
|
|
||
|
АТФобразуетсявклеткедвумпут: ми |
окислительногофосфорилирования |
|
|
||
I. |
Спомощью |
: |
|
|||
|
Q –этоэнергияокислениясубстрата. |
|
|
|
||
|
Окислительноефосфорилирование |
–этосинтезАТФизАДФфосфорнойкислоты |
, |
|||
которыйпроисходитзасчетэнергии |
|
трансэлектпомитохондриальнойтаонов |
||||
дыхатецепи.Этоглавньной |
|
ыйпутьсинтезаАТФваэробныхусловиях. |
|
|
||
II. |
Спомощью |
субстратногофосфорилирования: |
|
|
||
ВслучаесубстратногофосфорилирдлясинтезаАТФиспэнергияованияльзуетсягидролиза макроэргическойсвязисубстрата,кислороднетребуется.Реакциисубстратного фосфорилированиямогутбытьлокализованынетолькомитохондриях,ноцитоплазме.
Витаминыкоферме,участвующобменэнергетичтыеском ПроизводныевитаминаРРВ(
никотинамидадениндинуклеотидНАД +
5)НАДФ, :
НАДН+ |
+ |
|
26
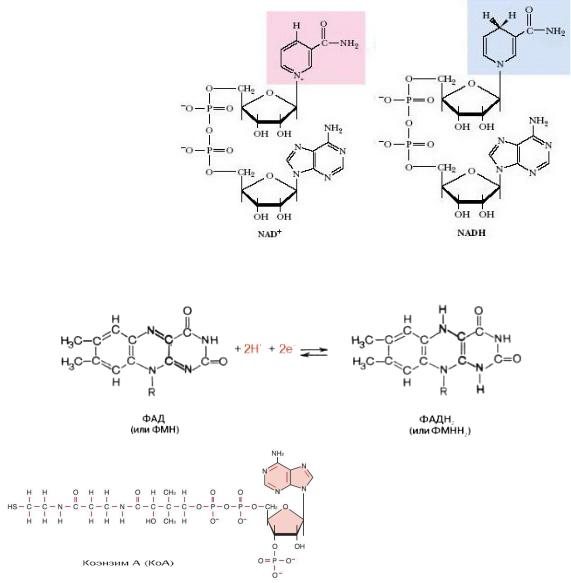
ПроизводныевитаминаВ |
2: флавинмононуклеотид,флавинадениндинуклеотидФМН( , |
ФАД): |
|
Производноепантотеновойкислотывитамина(
В3) –коэнзимАкофермент( А):
|
|
|
Тканевоедыхание.Окислительное |
|
|
фосфорилирование |
|
||
Процесс окислительногофосфорилирования |
|
тесносвязан( пряжен) |
окислительно- |
|
восстановительнымиреакциямиОВР( |
),аименнос |
реаокисленияцией |
водорода |
|
кислдоводыродом |
— тканевымдыханием. |
Реакцияобразованияводы |
in vitro в(пробирке) |
|
сопровождаодномоментнымвыдоколотсяление230кДжмоль/ энергииописываетсякак реакциявзрывагремучегогаза.Вживойклеткетакойпутьрмодинаневозмож, иченски
поэтомуокислениеводоводырода in vivo в(организме)характ ризует сядвумяважными особенностями.
Во-первых,газообразныйводородклеткахнеобразуется.Онвходитсоставсубстратови |
|
|
|||
отделяетсянихпутем |
|
дегидрирования.Ферменты,которыекаталэтреакции,зируют |
— |
||
дегидрогеназыДГ(). |
Этодвухкомпоферменентныеты |
;ониделятсяна |
пиридиновыеПДГ(), |
||
которыевкачествекоферментаиспользуютпроизводныевитаминаРР |
|
— НАД+ иНАДФ +, и |
|||
флавиновые, |
которыевкачествекоферментаиспользуютпроизводныевитаминаВ |
|
2 — ФМНи |
||
ФАД. |
ВходеОВРсубстратыокисляются,коферментыв |
осстанавливаются. |
|||
Во-вторых,выделенпостепенноэнепргоиисх, дит,рциямидлячегопр цесс |
|
дыхательнойцепи. |
|||
окисленияводородаосуществляетсянестадийколькоучастиемферментов |
|
||||
Восстансубстр,повленнляющиестаатомыддыхателорода |
|
ьнойцепи,это |
|||
небольшиемолекулыкарбоновые( кислоты,кетокаминокислоты, др.)Основн. ми |
|
|
|||
27

поставщикамивосстановленныхсубстратовявляются |
|
центральныеметаболическиепути. |
|
Тканевоедыхание |
—этопроцесспередачиатомовводородапротонов( и |
элек)отронов |
|
органичесубстратанакипофеклогомитохондриальнойментамоддыхательнойцепис |
|
|
|
образоэндогеннводы,аниемсопрвысвобождениемвождающийсяэнергии,заключеннойв |
|
|
|
субс.Приэтомрате60%высвобождэнергиирасходуетсятеплопющейся |
родукцию,а40% |
- |
|
насинтезАТФпомеханизмуокислительногофосфорилирования. |
|
|
|
Комцепионерэлектроновентыоса |
|
локализовавовнутремембранеитохондрийнейы |
|
||
(ВММ)Водород. отсубстпе( рдонороввичныхатов)вводитсядыхател |
|
|
ьнуюцепьспомощью |
||
НАД-завиФАДсимых |
-зависимыхденидрогеназ. |
|
|
||
Системутканевогодыханияможнопредввидеставитьхпятиферментныхмыкомплесов: |
|
|
Q-цитохром c-редуктаза; 4) |
||
1)НАДН |
-Ко Q-редуктаза; сукцинат2) |
–Ко Q-редуктаза; Ко3) |
|||
цитохром а –оксидаза; |
5)протоннаяАТФ |
-аза. |
|
|
|
Рольтакихпереносчикэленакислтронвэтихкомплексахвродвыполняют: |
|
|
|
||
▪ |
актиформывитаминаныеВ |
|
2 — ФМНиФАД |
(присоэлеипротоныктроныдиняют); |
|
▪ |
атомыжели всоставедиза |
|
цитохромов; |
|
|
▪железосерныебелки (FeS-белки);цитохромыжелезосерныебелкипереносяттолько
электроны.ЖелезобелкиассоциированыерныесФМН,ФАДцитохромом |
b. |
▪жирораствперенэлектроновипсчикимый,отсв перемещающийсябднов
мембране, |
— убихинонКо( |
|
Q). |
|
|
|
|
||
Цельработы |
дыхательной |
цепи:провестиреакцисленияводородаюкислородом |
|
|
|||||
образоэндогеннойводы.анием |
|
|
|
|
|
|
|
||
Принципработы |
|
дыхательнойцепи:разделениепотоковпротоновэл ,ктронов |
|
|
|
||||
поступающихизматри.Элепередаютсяксатронынаконечныйакцептор |
|
|
|
|
|
—кислпрот; одны |
|||
выбрасываютсявмитохондмежмембприальноеостранствоММП( ). ное |
|
|
|
редокс- |
|||||
Местотогоилииногопереносчикавдыхательнойце ределяетсявеличиной |
|
|
|
|
|||||
потенциала. |
Всереакциивдыхательнойцепинаправленыпотермодинамическойлес нице |
|
H·Н +)ккислороду,имеющему |
||||||
компссамымонентатрицтел |
|
|
ьнымредокс |
-потенциаломНАД( |
|||||
самыйположительныйредокс |
|
|
-потенциал. |
|
|
|
|
||
Редокс-потенциалЕ( |
о!)численэлектрондвижущейраве силеВольтах,возникающей |
|
|
||||||
междурастворамиокислителявосстако( новиценМ1, телярации |
°С)Чемотрицательнее. редокс |
|
|
|
|||||
рН=темп7,0, |
|
ература25 |
|
-потенциалсистемы, вышеее |
|
||||
способностьотдаваэлек роны |
|
|
(восстановители) |
.Чемположительнеередокс |
-потенциал,тем |
||||
вышеспособновеществаприэлектроныдинятьть |
|
|
|
|
(окислители). |
|
|||
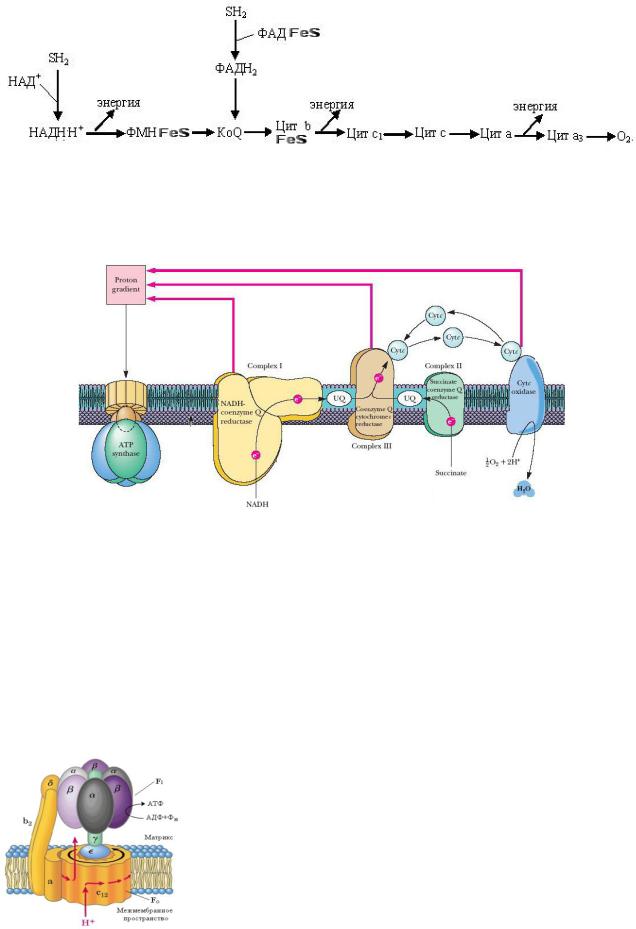
Перенэлектроновпдыхательнойсцепиосуществляследующейпосл :тсядовательности
28
|
Комплексыдыхательнойцепи |
|
|
|
КомплексΙ: |
НАДН-убихинонКо( |
Q)-оксидоредуктазаилиНАДН( |
-дегилрогеназа) |
. |
ПринэлектроныипрмаетотНАДН· |
|
+;протонывыбрасываются |
межмембранное |
|
пространство,электроныпередаютсянауб,ихкоэнзимл нон |
Q |
|
|
|
(Ко Q). |
|
|
|
|
Рис.5Дыхательная.2. цепь
КомплексΙΙ : сукцинат-убихинон(Ко Q)-оксидоредуктазаили(сукцинатдегидрогеназа) .
Принэлектроныипрмаетотсубстратовматрипередаетихнаксеубихинон.
Убихинон (Ко Q) —этолипофимолекула,хинон, егкоьнаяперепомембране,щается принимаетэлектроныотΙΙΙкомплексовдыхатцепильнойэлектроныредает наΙΙΙкомплекс.
Цитохромы b, c1 , c,входящиесоставдыхательнойцепи,представляютсобой железосодебелки,простетичг которыхуппажащиегемомскаядставлена.Цитохромы могутпереноситолькоэлектрзасчетатьжелезаоманысперемвалентностью, ной входящегосоставгемма:
|
|
Fe3+ +ē↔ |
Fe2+. |
|
|
|
|
КомплексШ: |
убихинон(Ко |
Q)-цитохромс |
-оксидоредуктазаили( |
QH2-дегидрогеназа). |
|||
|
|
Переносэлектроныубинацхитохромна |
|
|
|
с. |
|
|
|
Одноврзасчетэн,высвободившейсяменноргиипри |
|
|
|
||
|
|
переносе,изматриксав |
|
межмембпространствоное |
|
||
|
|
перенпр.отонысятся |
|
|
|
|
|
|
|
Комплекс IV:цитохромс |
-оксидаза. |
Переноситэлектроны |
|||
|
|
сцитохрома снепосредснакислород.Цитвенноохромы |
|
аи а3, |
|||
|
|
помиатожелезамо,с вдержататомымеди,поэтотму |
|
|
|
|
|
|
|
комплексодн существляетвременнопо |
|
|
|
лное |
|
|
|
(четырехэле)восстановмолекулыкистрон. орноиеда |
|
|
|
||
|
|
Энергияпереносаэлектриспнаоперекачиваниельзуетсянов |
|
|
|
||
межмембпространствооепротонов.
29
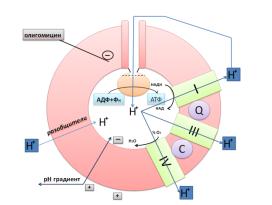
Vкомплексом внутреннеймембраныитохондрийявляетсяфермент,осуществляющий |
|
|
+- АТФ-аза) . |
|
||
реакциюсинтезаАТ |
Ф, - АТФ-синтазаили(протоннаяАТФ |
|
-азаН( |
|
||
Этотферментативныйкомплекссостоитиздвухчастей: |
|
|
|
|
||
Fо (о –олиг),комицинторыйвстроенмембранупроееизыасквозь. ает |
|
|
F1,- поформе |
|||
напомшляпкугрибадвналиручкуетрнуюиобращенвматриксмитохондрии.В |
|
|
|
|
||
изолированномвиде |
|
F1 неможетсинАТФезировать,номожпровг дролизить |
|
|
|
|
АДФифосфата. |
|
|
|
|
|
|
РеакциясинтезаАТФ,которуюпроводит |
|
Vкомп,являетсяекс |
|
окислительным |
|
|
фосфорилированием. |
|
|
|
|
|
|
Биохимикидолгоискалпромакроэргическиеежуточныесоедин,кот бырыеглиния |
|
|
|
|
||
служитьпосредникамимеждупроцесстканевогодыханиякислительм |
|
|
ным |
|
||
фосфорил.Английскийб охимикрованием |
|
П.Митчелл |
предп,чтсинтезоАТФложил |
V |
||
комплекВММсопряженсостояниембымэтойембраны,сформулировал |
|
|
|
|
||
хемиоосмотическуютеорию |
окислительногофосфорилированияНобелевская( премия1978г.). |
|
|
|
|
|
|
|
Рис. 5.4 СтроениеАТФ |
-азы |
|
||
|
|
Оснпостулатывные |
|
хемиоосмотической |
|
|
|
|
теории: |
|
|
|
|
▪внутренняямитохондмембриальнаяана
(ВММ)непроницаемадляионов,частностидля Н+ иОН -;
|
|
▪ |
засчетэнетранспогииэлектртаонов |
|
|
|
через I, IIIи IVкомплексыдыхательнойцепииз |
||
|
|
матриксавыкачиваютсяпротоны; |
|
|
▪ |
вознмембранеикающий |
электрохимпотенциалЭХП() ческий |
иесть |
|
промежуточформазапасаниэнергии; ая |
|
|
|
|
▪ |
возвт(ращениенслокац)протоновматрмитохондриичерезксяпротонныйканал |
|
|
|
VкомплексазасчетЭХПявляетдвижущейсилойинтезаяАТФ. |
|
|
|
|
Дальнейшиеисследования( |
Дж.Уокер ,П.Бойер |
,Нобелевскаяпремия1997г.подтвердили) |
|
|
предположенияП.Митчелла.Имипоказано,чтоэнергиядвиженияпротоиспользуетсяаов |
|
|
||
измеконенияактивногоформациицентраАТФ |
-син,чстоазыпровождаетсясинтезомАТФ, |
|
||
затемеговысво.Обождениемра |
зовавшийсяАТФпомощью |
транслоказыперемещаетсяв |
||
цитозоль.ВответнаэтоматриксмитохондриипоступаютАДФфосфат. |
|
|
|
|
Энергетическийэффектбиологическогоокисления
Источникамимакроэргсоединенявляютсяуглеводыч,скихпидыбелкий.Путиих преобразонеприводятк ысвобождениюанийодинаковыхколичествАТФ.
ДлясинтезаодноймолекулыАТФнеобхзатратитьоколодимо32кДж/ энергииль.Для |
|
|
|
||
этогодостаточявляетсяразностьпотенцмеждуйокиивосстановителемовслителемне |
|
|
|
||
менее0,26В.В.П. |
|
Скустановиллачев, акихучастковдыхательнойцепитр.Они |
пунктамисопряжениятканевогодыхания |
|
|
соответствуют I, IIIи IVкомплексаминазваны |
|
||||
окислительногофосфорилирования. |
|
|
|
||
ПерваямолекулаАТФсинтезивовремяпереносаэлу оттсякНАронов |
|
ДН+ |
+ к |
||
флавопротеинууровень( |
Iдыхательногокомплекса),вторая |
|
–припереносеэлекотронов |
|
|
восстанцитохромавленного |
bнацитохром |
с уровень( |
IIIдыхательногокомплекса),третья |
|
|
молекулаАТФсинтезируеприпереносеэлекотцитохромасяронов |
|
анакислуровень( род |
IV |
||
дыхательногокомпл)Им. вэтихучасткахнноксадыхательнойцеписуществуетнаибольшая |
|
|
|
||
разницаредокс |
-потенц,иколэнергииаловчест,высвопритранспортебождаемой |
|
|
|
|
30
