
- •57. Антигенпрезентирующие клетки
- •58. Медиаторы иммунного ответа
- •59. Последовательность событий в ходе иммунного ответа при экзогенных антигенах
- •60. Последовательность событий в ходе иммунного ответа при эндогенных антигенах
- •61. Иммунный ответ: стадии и основные «участники». Передача сигналов с Toll-рецепторов и инициация иммунного ответа.
- •Передача сигнала с толл-рецепторов tir домен
- •Активация и передача сигнала
- •62. Главный комплекс гистосовместимости (система hla): антигены hla-I и hla-II классов, их функции.
- •63. Иммунологическая память и иммунологическая толерантность.
- •66. Цитотоксический т-клеточный иммунный ответ.
- •67. Воспалительный т-клеточный иммунный ответ.
- •69. Эффекторные механизмы иммунитета: антителозависимый (гуморальный) и опосредованный клетками (клеточный). – смотреть предыдущие вопросы про ио и иммунитет
- •70. Антителозависимая клеточная цитотоксичность (азкт)
- •Альтернативный путь
- •Лектиновый путь
- •72. Антителонезависимая клеточноопосредованная цитотоксичность
- •73. Реликтовые свойства антител.
- •74. Реакция бласттрансформации.
- •75. Реакция торможения миграции лейкоцитов.
- •76. Супрессия (торможение) иммунного ответа. Механизмы супрессии лимфоцитов и лейкоцитов.
- •80. Иммунологически привелегированные ткани.
- •81. Апоптоз как иммунный механизм выбраковки клеток.
- •82. Особенности противоопухолевого иммунитета.
- •83. Иммунный статус: понятие и характеристика. Тесты первого и второго уровня определения иммунного статуса.
59. Последовательность событий в ходе иммунного ответа при экзогенных антигенах
экзоантигены( транзиторные бактерии, грибы, простйешие, гельминты, АГ-химич токсинов, АГ-орг) Процессинг в лизосомах. Шапероны ответств за особую укладку белка, они рядом с мнс(когда мнс в инакт сост, шаперон занимает желобок и наблюд за иммунолог девственност мнс) -МНС2 Поглощ эндоцитозом в эндосому, там гидролиз АГ и высвобожд эпитопа.
1 Фаза: АГ поступает в орг, нач афф фаза(1) у всех одинаков
2.Фаза –эфферентая фаза
о этап- подготовит TLR(толл-подобные рецепторы) взаимод с этим АГ распознает его, связыв своим доменом (TIR) белок (IRAK4 и myD88 -адапторный белок).Их связыв привод к акт IKK-киназы (освобождает белок NF-KB от IRB). Этот белок поступ в ядро, где акт гены, ответств за синтез цитокинов , АПК-клеткой и синтез CD80 И СD86, кот выходят на поверх кл АПК. Происход обрз эндоспоры и аг наход в нем, происх лизис ферментами лизосомы и он гидролиз на фрагменты: в этот же момент на эпс происходит синтез МНС-2 и после синтеза, желобок закрывается ii-цепью. Затем МНС 2 поступ в эндосому, расщепление ii цепи при помощи лизосом-ферментов, желобок открыв, он связыв АГ и МНС2 с АГ- выходят на поверх мембраны. Экспрессирует АГ.
1 этап – двойного связыв( АПК кл с экспрессир МНС2 +аг дает распознать TH0( он наивный, недифферин)ТН0 приближ к АПК кл и взаим с этой клетк через 3 стимула:а)ТСR рецепт и BCR рец – связыв с комплек МНС2+АГ. Б) Под дейст цитокинов просходит 2 стимул к тh0 в)от корецепторов -сд-80 связыв с рецеторами ТH0( СД28 И С152) . если сд152 экспресс больше сд28 до сд80 связыв с сд152 и тогда идет по гуморал (тh2) . если с152 меньше сд28 то по клеточн (th1). Если больше ИЛ-12 то клеточн, ИЛ4 то гуморал. (ИЛ-цитокины)
2 этап -активация лимфоцитов данного клона
3 этап- клональная экспансия
4 этап-финальная дифф лимф клона
5 этап – деструкция тканей- выведение продуктов распада
60. Последовательность событий в ходе иммунного ответа при эндогенных антигенах
Подготовил этап (экспрессия) для эндоАГ --расщепл в протеосоме . в итоге осовобод эпитопы с помощью белков Тэйп1, 2 поступ в эпс. Одновременно там идёт синтез мнс1 Однако Его желобок тоже закрыт АГ попадает и грув открывается Выставление комплекса на поверхность Для вирусов только в дендритных клетках
1 этап – двойного связыв( АПК кл с экспрессир МНС2 +аг дает распознать TH0( он наивный, недифферин)ТН0 приближ к АПК кл и взаим с этой клетк через 3 стимула:а)ТСR рецепт и BCR рец – связыв с комплек МНС2+АГ. Б) Под дейст цитокинов просходит 2 стимул к тh0 в)от корецепторов -сд-80 связыв с рецеторами ТH0( СД28 И С152) . если сд152 экспресс больше сд28 до сд80 связыв с сд152 и тогда идет по гуморал (тh2) . если с152 меньше сд28 то по клеточн (th1). Если больше ИЛ-12 то клеточн, ИЛ4 то гуморал. (ИЛ-цитокины)
2 этап -активация лимфоцитов данного клона
3 этап- клональная экспансия
4 этап-финальная дифф лимф клона
5 этап – деструкция тканей- выведение продуктов распада
61. Иммунный ответ: стадии и основные «участники». Передача сигналов с Toll-рецепторов и инициация иммунного ответа.
В начальных стадиях иммунного ответа участвуют, по крайней мере, три вида клеток: макрофаг (или дендритная клетка), Т- и В-лимфоцит. В целом все клетки, вовлеченные в этот процесс,
могут быть разделены, как указывалось выше, на антигенпредставляющие, регуляторные, эффекторные и клетки памяти. Имеются 2 магистральных пути иммунного ответа:
1. Клеточный иммунный ответ (T-клеточный).
2. Гуморальный иммунный ответ (в-клеточный).
Первый из них регулируется Т-хелперами типа 1 (Th1) и приводит к формированию эффекторных CD4+ T-клеток воспаления и цитотоксических CD8+ T-лимфоцитов, а также соответствующих им Т-клеток памяти.
Второй путь регулируется Т-хелперами типа 2 (Th2) и заканчивается образованием плазматических клеток (продуцентов антител) и В-лимфоцитов памяти. Переключение на синтез некоторых изотипов антител частично контролируется Th1. За исключением скрытого индуктивного периода иммунный ответ в среднем продолжается около трех недель с максимальным напряжением на 1-й неделе.
Можно выделить несколько основных стадий иммунного ответа
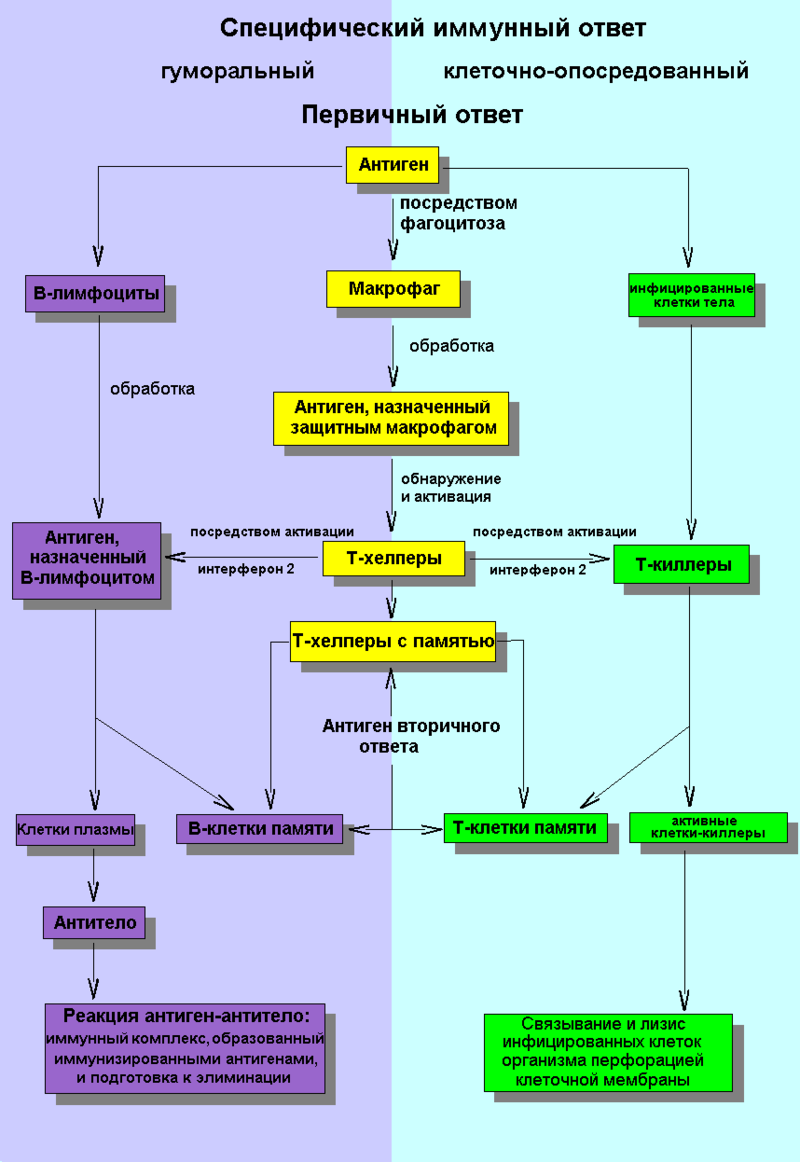
1. Эндоцитоз антигена, его процессинг (обработка) и загрузка на молекулы HLA I или HLA II для презентации лимфоцитам.
2. Распознавание комплекса антигенный пептид/HLA I или антигенный пептид/HLA II и других стимулов.
3. Сигнальная трансдукция и активация лимфоцитов.
4. Клональная экспансия (пролиферация) лимфоцитов.
5. Созревание эффекторных лимфоцитов и клеток памяти.
6. Эффекторная активность (деструкция антигена).
Первая стадия иммунного ответа (эндоцитоз, процессинг и презентация антигена). Антигенпредставляющая клетка (макрофаг, дендритная клетка или В-лимфоцит) сталкивается с нативным антигеном и поглощает его. Макрофаги фагоцитируют главным образом патогены, для которых характерно внутриклеточное паразитирование (вирусы, бактерии, грибы, простейшие и др.); дендритные клетки пиноцитируют вирусы; В-клетки интернализируют различные токсины.
Следующее событие, процессинг, представляет собой ферментативный катализ макромолекулы антигена внутри антигенпредставляющей клетки. В результате процессинга происходит высвобождение доминирующей антигенной детерминанты (иммуноактивного пептида или суперантигена), который загружается на желобки собственных молекул HLA I или HLA II и выводится на поверхность клетки для представления лимфоцитам. В зависимости от происхождения антигена выделяют два пути процессинга.
Экзогенные антигены презентируются в комплексе с молекулами HLA II «наивным» CD4+ T-клеткам (путь, опосредуемый HLA II).
Огачала эти антигены поглощаются и фрагментируются с помощью протеолитических ферментов в эндосомах (лизосомах). В то же самое время молекулы HLA II, связанные с шаперонами (калнексином и инвариантной цепью Ii), синтезируются и собираются в эндоплазматическом ретикулуме. Ii-цепь необходима для защиты желобка молекулы HLA вплоть до того момента, пока не будет загружен антигенный пептид. Затем комплекс HLA II/Ii-цепь транспортируется через аппарат Гольджи в эндосомы, где Ii-цепь теряется, а роль по защите желобка начинают выполнять дополнительные молекулы HLA-DM и, вероятно, HLA-DO. Наконец, антигенный пептид загружается на желобок молекулы HLA II, и этот комплекс экспрессируется на поверхности клетки.
Эндогенные или внутриклеточно расположенные антигены микробного происхождения загружаются на молекулы HLA I (путь, опосредуемый HLA I) для представления «наивным» CD8+ T-клеткам. Сначала, в отличие от экзогенных антигенов, такие цитоплазматические антигены перемещаются в цитозоль, где они расщепляются в крупном протеолитическом комплексе - протеасоме. После этого антигенный пептид транспортируется через «туннель» молекул TAP-1/TAP-2 в эндоплазматический ретикулум. Одновременно здесь происходит сборка молекулы HLA I, желобок которой (по аналогии с Ii-цепью у HLA II) находится «под защитой» шаперонов (сначала калнексина, затем кальретикулина), а укладка всей молекулы HLA I в последующем стабилизируется дополнительными молекулами (тапазином и др.). После загрузки антигенного пептида на желобок HLA I этот комплекс транспортируется на поверхность клетки.
Небелковые антигены загружаются на не-HLA-антигенпредстав- ляющие молекулы CD1.
В целом макрофаги и В-клетки вовлечены, соответственно, в Т-клеточный или гуморальный иммунный ответ по пути, опосредованному HLA II, а дендритные клетки двух типов способны к перекрестной презентации. Дендритная клетка типа 1 осуществляет процессинг эндогенных антигенов по пути с HLA I для запуска Т-клеточного ответа, а дендритная клетка типа 2 процессирует экзогенные антигены по пути с HLA II и включает В-клеточный ответ.
Вторая стадия иммунного ответа (распознавание антигена) протекает в течение нескольких часов. Однако при нарушениях клеточной миграции и межклеточных взаимодействий она может быть более длительной. Возможно, это приводит к замедлению всего иммунного ответа на патоген. Клиническими проявлениями этой стадии являются повышение температуры тела, мышечная слабость, снижение аппетита и сонливость. По большей части они обусловлены системными эффектами цитокинов (см. ниже).
Для того чтобы мог стартовать специфический иммунный ответ на конкретный антиген, необходимо, чтобы Т- и В-лимфоциты соответствующего клона встретились с антигенпредставляющей клеткой. Некоторые антигены бактерий (T-независимые антигены) распознаются с помощью BCR B-клеток и не требуют помощи со стороны Т-хелперов. Большинство нативных антигенов (так называемых T-зависимых антигенов) полностью распознаются «наивными» CD4+ Th1 и CD8+ T-клетками (для включения Т-клеточного ответа или пути Th1), а также «нaивными» CD4+ Th2 (для включения гуморального ответа или пути Th2). Интересно, что для прайминга CD8+ Т-клеток необходимо участие CD4+ Th1.
Третья стадия (сигнальная трансдукция и активация лимфоцитов). Во время распознавания лимфоциты воспринимают три типа обязательных сигналов, один специфический и два неспецифических:
1. Aнтигенный пептид/HLA I или антигенный пептид/HLA II.
2. Цитокины.
3. Костимулирующие молекулы.
Антигенный пептид, загружаемый на HLA I или HLA II в результате процессинга, служит специфическим сигналом. Это одновременное «двойное» распознавание «своего» (белков HLA) и «несвоего» (антигена) было открыто нобелевскими лауреатами (1996) P.C. Doherty (Австралия, США) и R.M. Zinkernagel (Швейцария) и оказалось довольно универсальным явлением. Секретируемые цитокины и экспрессируемые костимулирующие молекулы являются двумя обязательными неспецифическими сигналами. Более того, для обеспечения надежного физического контакта клеток необходимо также взаимодействие таких адгезивных молекул, как LFA-1, ICAM-1, ICAM-2, ICAM-3.
Цитокины играют одну из ключевых ролей в неспецифической регуляции иммунного ответа. Т- и В-лимфоциты получают цитокиновые сигналы от антигенпредставляющих клеток, NK-клеток, тучных клеток и др. Обратный сигнал от лимфоцитов, например секретируемый IFN-γ, способствует реэкспрессии HLA I/HLA II на антигенпредставляющих клетках. Цитокины, действующие на ранних стадиях иммунного ответа, могут быть разделены на две группы в зависимости от его направления:
1. Th1-цитокины: IL-2, IL-12, IL-18, IFN-γ, TNF-α/β (для пути Т-хелперов типа 1).
2. Th2-цитокины: IL-4, IL-13 (для пути Т-хелперов типа 2). Однако на следующих стадиях иммунного ответа (клональная экспансия, созревание эффекторов, переключение синтеза изотипов антител) в процесс вовлекаются другие цитокины.
Активация клеток является результатом сигнальной трансдукции, которая осуществляется серией сложных внутриклеточных реакций. После распознавания первоначально происходит активация связанных с корецепторами и молекулами CD3 (на Т-клетках) или CD79 (на В-клетках) тирозинкиназ нескольких семейств (Lck, Fyn, Blk, Btk, Lyn, Zap70, Syk и др.), затем через посредничество адаптерных белков включаются сигнальные пути. Один из них связан с активацией фосфолипазы Cγ, образованием инозитолтрифосфата и диацилглицерола, активацией протеинкиназы С и мобилизацией внутриклеточного Ca2+, с транскрипцией гена IL-2. Данный цитокин является ключевым ростовым фактором для лимфоцитов в иммунном ответе. Второй сигнальный путь связан с обменом арахидоновой кислоты и приводит к транскрипции генов структурных белков, необходимых для осуществления митозов клеток.
Четвертая (клональная экспансия лимфоцитов) и пятая (созревание эффекторных лимфоцитов и клеток памяти) стадии иммунного ответа. Клональная экспансия представляет собой пролиферацию активированных лимфоцитов, которая протекает в периферических органах иммунной системы. Пролиферирующие В-лимфоциты образуют вторичные фолликулы в лимфатических узлах (центробластная стадия), при этом размножение клеток регулируется рядом цитокинов: IL-2, IL-4, IL-5, IL-6, IL-10, IL-13, IL-14, IFN-γ, TNF и др. В последующем центробласты начинают превращаться в центроциты, которые мигрируют на периферию фолликулов (центроцитарная стадия). В этот момент клетки вступают в период соматических гипермутаций, который является своеобразным способом селекции нужной специфичности BCR. Происходит позитивный отбор клеток с высокоспецифичным BCR и негативный отбор В-лимфоцитов с низкоспецифичным рецептором. В процессе созревания В-клетки претерпевают морфологические изменения (плазмобласт (иммунобласт) - проплазмоцит (лимфоплазмоидная клетка) - плазмоцит) и мигрируют в костный мозг и MALT для синтеза антител различных классов. Синтез ранних антител (IgM) регистрируется уже к концу первых суток клинического инфекционного эпизода, а высокоспецифических IgG - на 5-7 сутки.
Клональная экспансия и созревание Т-клеток протекают в паракортикальных зонах лимфатических узлов и периартериолярных пространствах селезенки. Распознавшие антиген клетки вступают в пролиферацию и превращаются в лимфобласты. Клоны CD8+ T-клеток нарастают быстро, а клоны CD4+ Т-лимфоцитов - более медленно. В целом, клональная экспансия и дифференцировка регулируются разными цитокинами (IL-2, IL-7, IL-9, IL-12, IL-15, IFN-γ, TNF и др.) и адгезивными молекулами. В процессе дифференцировки значительно изменяется фенотип Т-лимфоцитов, но, в отличие от В-лимфоцитов, они не меняются морфологически.
Характерным клиническим эквивалентом стадий клональной экспансии и дифференцировки является увеличение периферических лимфатических узлов, миндалин, видимых лимфатических фолликулов и селезенки. Можно наблюдать эти симптомы при респираторной, урогенитальной или значительной системной инфекциях.
В процессе иммунного ответа наряду с эффекторными клетками формируются Т- и В-клетки памяти. В отличие от эффекторных лимфоцитов с небольшими сроками жизни, клетки памяти остаются жизнеспособными в течение длительного времени (пожизненно). Существуют CD4+ и CD8+ T-клетки памяти, В-клетки памяти и долгоживущие плазматические клетки. В отличие от наивных Т-лимфоцитов Т-клетки памяти характеризуются фенотипом CD45RO+, CD44hi, быстрым HLA-независимым циклом и способностью секретировать большие количества цитокинов. Долгоживущие плазматические клетки обеспечивают дополнительный механизм поддержания синтеза иммуноглобулинов без дополнительной антигенной стимуляции в течение 1,5 лет.
Вторичный иммунный ответ протекает в ускоренном режиме за счет клеток памяти. Появление IgM в сыворотке крови часто указывает на «свежую» инфекцию или реактивацию персистирующего патогена, а синтез IgG соответствует наличию иммунной памяти к однажды перенесенной инфекции. При таком ускоренном синтезе IgG клинические проявления инфекционной болезни обычно отсутствуют.
Шестая стадия иммунного ответа (эффекторная активность). Конечной стадией как гуморального, так и клеточного иммунного ответа является деструкция антигена, которая осуществляется с привлечением неспецифических факторов врожденного иммунитета. Известны следующие эффекторные механизмы деструкции антигена.
