
3885
.pdfТолстые клеточные стенки бактерий не позволяют белкурецептору вместе с присоединившимся к нему вирусом погружаться в цитоплазму, как это происходит при инфицировании клеток животных. Поэтому бактериофаг вводит полый стержень в клетку и выталкивает через него ДНК (или РНК), находящуюся в его головке. Геном бактериофага попадает в цитоплазму, а капсид остается снаружи. В цитоплазме бактериальной клетки начинаются репликация генома бактериофага, синтез его белков и формирование капсида. Через определенный промежуток времени бактериальная клетка гибнет, и зрелые фаговые частицы выходят в окружающую среду.
Вопросы и задания для самоконтроля
1.Строение и размножение вирусов.
2.Имеют ли вирусы клеточное строение?
3.Какие вирусы называются бактериофагами?
4.Строение и размножение бактериофага.
5.Какие организмы относятся к прокариотам?
6.Строение бактерий.
7.Чем представлен генетический аппарат в бактериальной клетке?
8.Строение и типы плазмид.
9.Кто и в каком году создал клеточную теорию?
10.Основные положения клеточной теории.
11.Строение эукариотической клетки по современным данным.
12.Строение и функции мембранных органоидов.
13.Строение и функции немембранных органоидов.
14.Какие органоиды эукариотической клетки содержат ДНК?
15.Строение ядра.
16.Химический состав, строение и функции хромосом.
17.Сходство и различие в строении растительной и животной клеток.
18.Сходство и различие в строении клеток прокариот и эукариот.
ЛАБОРАТОРНАЯ РАБОТА №2
Приготовление и описание микропрепаратов клеток растений Цель: рассмотреть клетки различных организмов и их тканей под
микроскопом (вспомнив при этом основные приемы работы с микроскопом), вспомнить основные части, видимые в микроскоп и сравнить строение клеток растительных, грибных и животных организмов.
Оборудование: микроскопы, чашка Петри, пинцет, предметное стекло, р-р йода, луковица, лист бегонии.
Ход работы:
-приготовьте микропрепараты: а) – клеток кожицы лука, б) – клеток ткани листа бегонии
-рассмотрите под микроскопом микропрепараты клеток.
11
-зарисуйте увиденные клетки. Подпишите их основные части, видимые в микроскоп.
-сравните строение клеток. Сделайте вывод о сложности их строения в связи с тем, в состав какой ткани клетки входят.
-сделайте вывод, опираясь на имеющиеся у вас знания, в соответствии с целью работы.
ЛАБОРАТОРНАЯ РАБОТА №3
Исследование химического состава витаминных препаратов: Качественные реакции на витамины.
Общие сведения.
Интенсивного роста и развития, высокой продуктивности и хорошо выраженного конституционального иммунитета удается добиться при оптимальном обеспечении организма животных витаминами: β-каротином, парааминобензойной кислотой, витамином U, витамином Е. Показано, что введение повышенных доз витамина А в рацион коров способствует стабилизации в молоке фракционного состава казеина, сывороточных белков и устойчивости казеинкальцийфосфатного комплекса. Целесообразным оказалось использование повышенных доз витамина Е при тепловых стрессах при выращивании бройлеров. Комплекс фолиевой и аскорбиновой кислот повышает продуктивность свиноматок, нормализует обменные процессы, стимулирует естественные защитные силы организма, а также инициирует многоплодие. Двойная норма витаминов В12 и фолиевой кислоты оказывает положительное влияние на сперматогенез птицы, увеличивает объем и общее количество спермиев в эякуляте, что способствует повышению оплодотворяемости яиц и процента вывода цыплят. Более высоких показателей продуктивности и естественной резистентности животных можно добиться при комплексном использовании витамина С и протосубтилина Г3х, витамина U и смеси ферментных препаратов пектофоетидина П10х и протосубтилина Г3х, витамина К4 и цеолита, витамина В12 и кобальта.
Производство витаминов.
Биотехнологическим путем производят витамин А, D, В2, В12, С и др. Каротиноиды (предшественники витамина А) синтезируются пигментными микроорганизмами из рода Fusarium, Pseudomonas, Sarcina др. Всего известно около 500 каротиноидов, которые продуцируются бактериями, дрожжами и мицелиальными грибами. Они находятся в клеточной мембране микроорганизмов в виде сложных эфиров и гликозидов
или в свободном состоянии – в липидных гранулах цитоплазмы.
В основе витамина D лежит скелет эргостерина, который находится в клеточных мембранах эукариот. Так, пекарские или пивные дрожжи содержат 0,2-11 % эргостерина. Под влиянием УФО эргостерин
12
трансформируется в витамин D2, который легко переходит в D3. Продуцентами эргостерина также являются аспергиллы и пенициллы. В них содержится 1,2 - 2,2 % эргостерина. Облученные сухие дрожжи используют в животноводстве. В нихсодержится не менее 46% сырого белка, незаменимые аминокислоты (лизин, метионин, триптофан.) и 5000 МЕ витамина D2 /г.
Витамин В2 (рибофлавин) продуцируется бактериями, дрожжами и нитчатыми грибами. В настоящее время получают до 0,5 г и более рибофлавина в 1 л среды.
Витамин С синтезируют все растения и животные, кроме обезьян и морских свинок, а также человека. Микроорганизмы витамин С не синтезируют и в нем не нуждаются.
Аскорбиновую кислоту получают химико-ферментативным способом. Так, некоторые виды уксуснокислых бактерий образуют полупродукт аскорбиновой кислоты – L-сорбозу. Затем проводят химическую стадию. В результате получается 2-кето-L-гулоновая кислота. Ее подвергают энолизации и трансформируют в L-аскорбиновую кислоту. L-сорбозу также получают ферментацией Gluconobacter oxydans на средах, содержащих сорбат, кукурузный или дрожжевой экстракт при интенсивной аэрации. Выход L-сорбозы составляет 98 % за 2 суток. Культивирование проводят в периодическом или непрерывном режиме.
Витамин В12 (цианкобаламин) продуцируют пропионовые бактерии – Propionibacterium var. Shermanii. На ацетобутиловой и спиртовой бардах с добавлением кобальта и метанола получают кормовой препарат, который содержит витамин В12 и другие ростовые факторы. Здесь биообъектом является смешанная культура метаногенных бактерий.
ЦЕЛЬ: сформировать навык исследования химического состава ветеринарных витаминных препаратов (на примере кормовых дрожжей).
Оборудование:
1.Газовая горелка.
2.Пробирки.
3.Пипетки.
4.Стеклянная палочка.
Реактивы:
1.Эфир.
2.Анилиновый реактив (15 частей анилина и 1 часть концентрированной соляной кислоты).
3.Концентрированная соляная кислота.
4.Цинк металлический.
5.5% раствор сульфата меди.
6.5% раствор хлорида железа (III).
7.20% раствор серной кислота.
13

Ход анализа
Предварительно в химическую пробирку помещают 8 г кормовых дрожжей и, проверив, что в лаборатории погашены все горелки и нет включенных электроплиток, добавляют 2-4 мл эфира для разрушения клеточных оболочек. Содержимое пробирки растирают стеклянной палочкой. Эфир разрушает оболочки дрожжевых клеток.
Витамин D. К 2 мл полученной из дрожжей массы прибавляют 1-2 капли анилинового реактива, перемешивают и нагревают. Появляется красно-бурое окрашивание.
Витамин В2. К 2 мл гидролизата дрожжей добавляют 0,5 мл концентрированной соляной кислоты и небольшой кусочек металлического цинка. Начинается бурное выделение пузырьков водорода, жидкость постепенно окрашивается в красный цвет, затем окраска бледнеет.
Кислота никотиновая. К 3 мл теплого гидролизата дрожжей приливают 1 мл 5% раствора сульфата меди. Выпадает осадок синего цвета.
Витамин В6. К 1 мл гидролизата дрожжей прибавляют 2 капли 5% раствора хлорида железа (111), появляется красное окрашивание, исчезающее при добавлении 20% серной кислоты.
СПИСОК ЛИТЕРАТУРЫ 1. Общая биотехнология: методические указания к лабораторным работам /
сост.: В.А. Блинов, С.Н. Буршина. – Саратов: «РИК «Полиграфия Поволжья»,
2004. – С. 17-20, 72-75.
ЛАБОРАТОРНАЯ РАБОТА №4
Качественная идентификация антибиотиков различных групп Основные сведения
В настоящее время известно примерно 6000 антибиотиков, их синтез существляется микробными клетками. Шесть родов грибов производят около 1000 различных антибиотиков, в т.ч. цефалоспорины и пенициллины. Два рода бактерий синтезируют 500 антибиотиков, три рода актиномицетов – около 3000 антибиотиков. Новые формы антибиотиков стараются получать не путем биосинтеза новых веществ, а путем химической или биотехнологической трансформации уже известных антибиотиков.
По биологическому действию антибиотики делятся на:
–к ним относятся: а) угнетающие рост
грамположительных бактерий (пенициллин, цефалоспорин, эритромицин, олеандомицин, карбомицин и др.); б) угнетающие рост грамотрицательных бактерий (тетрациклин, неомицин,
стрептомицин, полимиксин, грамицидин и др.); в) обладающие противотуберкулезным действием (стрептомицин, биомицин, циклосерин и др.);
– нистатин, гризеофульвин,
леворин, кандицидин и др.;
14
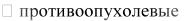
– актиномицин, митомицин С и др.
Селекция продуцентов антибиотиков.
Антибиотики продуцируются в результате совместного действия 10-30 генов. Высокопродуктивные штаммы пенициллина и тетрациклина были получены в результате последовательных циклов мутагенеза и селекции. Сначала обнаружили спонтанный мутант, производивший 60 мг/л пенициллина, затем из большого числа колоний был выделен суперпродуцент с выходом пенициллина 150 мг/л. После рентгеновского облучения получен штамм, производящий 300 мг/л пенициллина, после ультрафиолетового облучения выделили штамм, который давал 550 мг/л пенициллина. После обработки ипритом был получен штамм, который производил 7 г/л пенициллина. Позднее выявили продуцент, который производил 20 г/л пенициллина. Это в 10000 раз превышал исходный выход.
Основы технологии получения антибиотиков.
В1940 году А. Флеминг впервые получили пенициллин из культуральной жидкости в аморфном, а затем – в кристаллическом виде.
Антибиотики относятся ко вторичным метаболитам (идиолитам). Микроорганизмы, которые производят вторичные метаболиты, сначала проходят стадию быстрого роста, или тропофазу. Во время нее синтез вторичных метаболитов незначителен. Затем, по мере истощения одного или нескольких необходимых питательных веществ в культуральной среде микроорганизмы переходят в идиофазу. В этот период и синтезируется вторичные метаболиты. Большинство микроорганизмов в тропофазе чувствительны к собственным антибиотикам. Поэтому при культивировании микроорганизмов, продуцирующих антибиотики, процесс как можно быстрее переводят в идиофазу. Например, ядром пенициллинов является 6- аминопенициллановая кислота (6-АПК). Ее используют для получения полусинтетических пенициллинов. Обычно 6-АПК получают микробиологически из бензилпенициллина (пенициллин G ) при помощи адсорбированной на бентоните пенициллинамидазы. Продуцентами являются E. coli или B. megatherium. Такой иммобилизованный фермент используют для получения новых антибиотиков из группы цефалоспоринов.
Внастоящее время с помощью Penicillium notatum или P. сhrysogenum
производят полусинтетические антибиотики – β-лактамы.
Многие антибиотики получают методом глубинной ферментации. Например, интенсивный синтез пенициллина начинается при большом количестве биомассы мицелия полном использовании глюкозы и молочной кислоты в среде и при рН ≈ 7. Бензилпенициллановая кислота синтезируется из L-цистина, фенилуксусной кислоты, диметилпировиноградной кислоты. При составлении питательных сред надо учитывать, что для синтеза пенициллина лимитирующим фактором является глюкоза, а при синтезе других антибиотиков – фосфаты.
15
Атиномицеты способны расти и продуцировать антибиотики на многих средах, содержащих белки (соевая мука, рыбная мука, белок клейковины пшеницы и др.) или крахмал. Каждый продуцент имеет свои особенности. Например, при культивировании Str. erythreus в питательную среду добавляют пропиловый спирт, как предшественник антибиотика эритромицина.
Опыт 1 КАЧЕСТВЕННАЯ ИДЕНТИФИКАЦИЯ АНТИБИОТИКОВ
ЦЕЛЬ: сформировать навык проведения качественной идентификации антибиотиков.
Оборудование:
1.Газовая горелка.
2.Пробирки.
3.Пипетки. Реактивы:
1.1 н раствор гидроксиламина.
2.1 н, 10% и 20% растворы гидроксида натрия.
3.Ледяная уксусная кислота.
4.Концентрированная серная кислота.
5.Концентрированная соляная кислоты.
6.Концентрированная азотная кислота.
7.15% раствор соляной кислоты.
8.Бутанол.
9.5% раствор хлорида железа (III).
10.5% сульфата (нитрата) меди.
11.5% раствор хлорида бария.
12.1% раствор нитрита натрия.
13.Щелочной раствор бета-нафтола.
14.Реактив Несслера.
15.Реактив Фелинга.
Опыт 2 КАЧЕСТВЕННЫЕ РЕАКЦИИ НА АНТИБИОТИКИ ГРУППЫ
ПЕНИЦИЛЛИНА
Ход анализа
Гидроксамовая реакция. В две пробирки помещают по 0,01 г бензилпенициллина, приливают 1 каплю раствора, состоящего из 1 мл 1н раствора гидроксиламина гидрохлорида и 0,3 мл 1н раствора гидроксида натрия. Через 2-3 мин к смеси добавляют 1 каплю ледяной уксусной кислоты, тщательно перемешивают. Затем добавляют в первую пробирку 1 каплю 5% раствора хлорида железа (111). Образуется красно-фиолетовое окрашивание.
16
Во вторую пробирку прибавляют 1 каплю 5% раствора нитрата (сульфата) меди – образуется зеленое окрашивание.
Реакция обнаружения серы. К 0,01 г бензилпенициллина прибавляют 2-3 мл концентрированной азотной кислоты и кипятят под тягой в течение 2-3 мин. По охлаждении прибавляют 0,5 мл 5% раствора хлорида бария. Выпадает белый осадок.
Реакция на первичные ароматические амины. Около 0,01 г
бензилпенициллина растворяют в 2 мл воды, прибавляют 0,5 мл 15% соляной кислоты, 0,5 мл 1% раствора нитрита натрия. Полученный раствор хорошо перемешивают и прибавляют 1 мл щелочного раствора бета-нафтола. Появляется вишнево-красное окрашивание.
Опыт 3
КАЧЕСТВЕННЫЕ РЕАКЦИИ НА АНТИБИОТИКИ ГРУППЫ СТРЕПТОМИЦИНА
Ход анализа
Растворяют около 0,05 г стрептомицина сульфата в воде и прибавляют по каплям реактив Несслера. Появляется бурое окрашивание вследствие выпадения металлической ртути;
-растворяют около 0,05 г стрептомицина в 1 мл воды и прибавляют 0,5 мл реактива Фелинга, нагревают. Появляется красное окрашивание вследствие образования оксида меди (1);
- нагревают около 0,05 г стрептомицина с 1,5-2,0 мл 10% раствора гидроксида натрия. Идет выделение аммиака, который можно обнаружить по изменению окраски индикаторной бумаги.
Опыт 4
КАЧЕСТВЕННЫЕ РЕАКЦИИ НА АНТИБИОТИКИ ГРУППЫ ТЕТРАЦИКЛИНА
Ход анализа
Реакция изомеризации: под действием гидроксида натрия. 0,01 г тетрациклина растворяют в 2 мл 10% раствора гидроксида натрия. Появляется коричневое окрашивание. Нагревают в кипящей водяной бане в течение 1-2 мин – появляется синяя флюоресценция, наблюдаемая в УФ свете.
Реакция образования ангидротетрациклина. 0,01 г стрептомицина растворяют в 2 мл концентрированной соляной кислоты и нагревают на кипящей водяной бане в течение 2-3 мин. Тетрациклин дает желто-зеленую флюоресценцию, наблюдаемую в УФ свете.
17
Реакция с концентрированной серной кислотой. К 1-2 мг стрептомицина прибавляют 2 мл концентрированной серной кислоты. Появляется фиолетовое окрашивание.
Реакция с хлоридом железа (III). 0,01 г стрептомицина растворяют в 2 мл концентрированной соляной кислоты и нагревают на кипящей водяной бане в течение 2-3 мин. Тетрациклин дает желто-зеленую флюоресценцию, наблюдаемую в УФ свете.
Опыт 5
КАЧЕСТВЕННЫЕ РЕАКЦИИ НА АНТИБИОТИКИ ГРУППЫ ЛЕВОМИЦЕТИНА
Ход анализа
Реакция с гидроксидом натрия. 0,1 г левомицетина растворяют при нагревании на огне газовой горелки в 5 мл 20% раствора гидроксида натрия. При этом появляется желтое, затем красно-оранжевое окрашивание, усиливающееся при кипячении раствора, выпадает осадок кирпичнокрасного цвета, обусловленный образованием азобензойной кислоты. Кроме того, ощущается запах аммиака (из амидной группы).
Реакция комплексообразования. К 0,01 г левомицетина прибавляют 3
капли 5% раствора сульфата меди и 0,5 мл 1н раствора гидроксида натрия. Через 1 мин взбалтывают с 1 мл бутанола. Слой бутанола окрашивается в сине-фиолетовый цвет.
СПИСОК ЛИТЕРАТУРЫ
1.Общая биотехнология: методические указания к лабораторным работам / сост.: В.А. Блинов, С.Н. Буршина. – Саратов: «РИК «Полиграфия Поволжья», 2004. – С. 72-75.
2.Биологические препараты. Сельское хозяйство. Экология: Практика применения / ООО «ЭМ-Кооперация» / сост.: Костенко Т.А., Костенко В.К.; под. ред. П.А. Кожевина. – Саранск: ГУП РМ «Республиканская типография «Красный Октябрь», 2008. – 296 с. – ISBN 978-5-7493- 1236-2
3.Биотехнология: реальность и перспективы в сельском хозяйстве: Материалы Международной научно-практической конференции (К 100-летию СГАУ имени Н.И. Вавилова). – Саратов: Издательство
«КУБиК», 2013. – 286 с. – ISBN 978-5-91818-278-1
4.Блинов, В.А. Общая биотехнология: Курс лекций. В 2-х частях. Ч. 2. – Саратов: ФГОУ
5.ВПО «Саратовский СГАУ», 2004. – 144 с. – ISBN 5-7011-0436-2
Вопросы для самоконтроля
18
1) Какие ветеринарные препараты получают биотехнологическим путем?
2) Классификация антибиотиков по биологическому действию.
3)Селекция продуцентов антибиотиков (на примере получения пенициллина).
4)Основы технологии получения антибиотиков.
ЛАБОРАТОРНАЯ РАБОТА №5
Выявление источников мутагенов в окружающей среде (косвенно) и оценка возможных последствий их влияния на организм.
Цель: научиться определять источники мутагенов в быту. Оборудование: карта вводной теории, упаковки (пакет из-под молока,
сухариков, сока), упаковки косметической продукции (крем для рук, шампунь, дезодорант), таблица кодов пищевых добавок.
Ход работы.
Вводная теория.
В 60-е и 70-е годы в нашей стране были созданы методические руководства по оценке потенциальной мутагенной опасности промышленных загрязнителей, пестицидов, правда, большая часть их получила правовую основу позже. Однако при определении этой опасности помимо установления предельно допустимых концентраций химических веществ в питьевой воде, атмосферном воздухе и воздухе рабочей зоны, в пищевых продуктах необходимо помнить и о так называемых отдаленных последствиях, т.е. изучать мутагенную, канцерогенную, тератогенную активности этих соединений. Помимо тригалометанов, которые были обнаружены еще в 1974 г., к настоящему времени в питьевой воде выявили немало других соединений, которые обладают мутагенной и канцерогенной активностью. Есть мутагены в воде плавательных бассейнов, в сточных водах (промышленных и бытовых), а также в тканях рыб и гидробионтов, населяющих загрязненные водоемы. Ясно, что в организм человека мутагены могут поступать не только с питьевой водой, но и с пищевыми продуктами. Тестирование продуктов питания на мутагенность привело к выявлению многих мутагенов: природных ингредиентов (флавоноиды, фураны, гидразины), пищевых контаминантов (пестициды, микотоксины) и мутагенных соединений, образующихся в процессе приготовления пищи. Этот список можно продолжить. Стало очевидным, что нельзя ограничиваться изучением мутагенных свойств отдельных веществ. Необходимо оценивать суммарное загрязнение всех компонентов окружающей среды. Была создана и в значительной степени стандартизирована методическая база исследований, разработана
методология |
мониторинга |
загрязнения |
окружающей |
среды |
|
|
|
|
19 |

генотоксикантами, причем такого рода работы ведутся не только за рубежом, но и в нашей стране.
Задание 1. Рассмотрите внимательно этикетку предложенного вам продовольственного товара. Какие вещества входят в состав продукта? Есть ли в составе вещества, занесѐнные в список пищевых добавок?
Сделайте вывод о качестве продукта и степени опасности для человека.
Задание 2. Рассмотрите внимательно этикетку предложенного вам непродовольственного товара. Какие вещества входят в состав продукции? Есть ли в составе вещества, занесѐнные в список канцерогенов?
Сделайте вывод о качестве продукта и степени опасности для человека.
Приложение к лабораторной работе
Здесь представлены особо вредные, опасные и запрещѐнные законом пищевые добавки группы Е (данные по сведениям министерства здравоохранения Российской Федерации):
Е 102; Е 104; Е 110; Е 120; Е 121; Е 122; Е 123; Е 124; Е 127; Е 128; Е 129; Е 131; Е 132; Е 133; Е 142; Е 151; Е 153; Е 154; Е 155; Е 173; Е 174; Е 175; Е 180; Е 214; Е 215; Е 216; Е 217; Е 219; Е 226; Е 227; Е 230; Е 231; Е 233; Е 236; Е 237; Е 238; Е 239; Е 240; Е 249 ... Е 252; Е 296; Е 320; Е 321; Е 620; Е 621; Е 627; Е 631; Е 635; Е 924 а-b; Е 926; Е 951; Е 952; Е 954; Е 957.
Специалисты Роспотребнадзора так же не рекомендуют и считают опасными ещѐ группу добавок:
Е102, Е110, Е120, Е124, Е127, Е129, Е155, Е180, Е201, Е220, Е222, Е223, Е224, Е228, Е233, Е242, Е270, Е400, Е401, Е402, Е403, Е404, Е405,
Е501, Е502, Е503, Е620, Е636 и Е637. В список очень опасных занесены Е123,
Е510, Е513 и Е527.
Однако по неизвестным причинам эти добавки не запрещены и по сей день. Подозрительными названы добавки Е104, Е122, Е141, Е150, Е171,
Е173, Е241 и Е477.
Список вредных консервантов г руппы - "Е" и последствия от их применения
E 102 |
опасен |
|
|
E 103 |
запрещѐн |
|
|
E 104 |
подозрителен |
|
|
E 105 |
запрещѐн |
|
|
E 110 |
опасный |
|
|
E 111 |
запрещѐн |
|
|
E 120 |
опасен |
|
|
E 121 |
запрещѐн |
|
|
E 122 |
подозрителен |
|
|
E 123 |
очень опасен, запрещѐн |
20
