
Пищевая Биохимия / Рогожин В.В., Рогожина Т.В. Биохимия сельскохозяйственной продукции
.pdf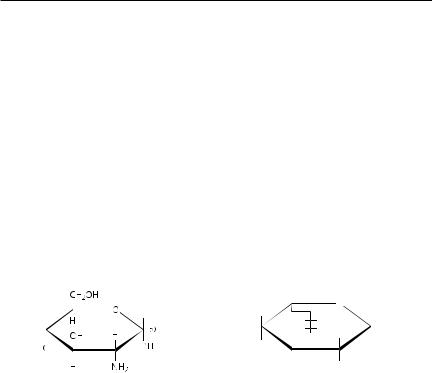
18.1. Химический состав молока
18.1.2. Белки молока
К основным белкам молока относят четыре электрофоретически разделимые фракции казеинов, сывороточные белки (β-лактоглобулин, α-лак- тальбумин), альбумин сыворотки крови, иммуноглобулины, β-микрогло- булин, лактоферрин, церулоплазмин. Казеина содержится в молоке около 80% от общего количества белка, тогда как β-лактоглобулина — 7…12%, α-лактальбумина — 2…5%, сывороточного альбумина — 0,8…1,4%.
Казеин. По структуре казеин является фосфопротеидом, обладает способностью к самопроизвольному формированию мицелл в присутствии ионов кальция, цитратов и фосфатов. Известны четыре типа казеина: αs1-, αs2-, β-, χ-казеин, которых в молоке соответственно 38, 10, 39 и 13 % от суммарного количества казеинов. Казеины отличаются между собой по молекулярной массе, количеству фосфорной кислоты в них, а χ-ка- зеин — еще и содержанием углеводов, представленных глюкозамином и сиаловыми кислотами.
|
|
|
|
|
H |
|
|
|
|
C |
|
|
|
|
|
O |
OH |
|
|
|
|
|
|
|
||
H3 |
|
CO NH |
H |
OH |
||||
|
|
|
||||||
|
|
|
|
|
|
H |
OH |
|
|
|
|
|
|
H |
|
CH2OH H |
COOH |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
OH |
H |
|
|
Глюкозамин |
|
|
|
|
Сиаловая кислота |
|
||
В молоке около 95% казеина образуют мицеллы глобулярной формы, размер которых составляет 150…200 нм, и только 5% казеина находится в виде мономерных форм, полимеров фракций казеина и субмицелл. Каждая мицелла содержит в себе все виды казеина и состоит из 7000…8000 полипептидных цепей, соединенных между собой ионами Са2+. На периферии мицелл расположен χ-казеин, выполняющий роль защитного коллоида.
Особое внимание следует уделить строению χ-казеина. Этот белок состоит из нескольких компонентов, главный из которых не содержит углеводы, тогда как в структуре других компонентов содержатся олигосахариды. Сложность формирования вторичной структуры χ-казеина обусловлена наличием у него 32% α-спирали, 31% параллельной и 24% антипараллельной β-структуры. Причем спирализация полипептидной цепи χ-казеина происходит вблизи участка связывания химозина (реннина).
Фермент реннин (сычужный фермент), который добавляется к молоку при изготовлении сыров, отщепляет от χ-казеина гликопептид, после чего нарушается структура мицелл и происходит створаживание молока. Причиной створаживания является то, что χ-казеин, потеряв под дейс-
383

Глава 18. Биохимия молока
твием фермента гидрофильный гликопротеид, образует нерастворимые соли с ионами Са2+ даже в нейтральной среде, чего не происходит при нативном состоянии белка в молоке. Тогда как растворимые αs1-, αs2- и β- казеины подвергаются гидролитическому расщеплению под действием плазмина молока.
Казеин характеризуется высокой биологической ценностью благодаря содержанию в его составе полного набора аминокислот. В казеине содержится от 0,1 до 1% фосфора, связанного сложноэфирной связью с остатками серина, входящими в молекулу белка. С казеином соединен кальций. Все это обусловливает высокие питательные качества казеина для человека. Синтез казеина осуществляется в молочной железе из доставляемых в нее кровью аминокислот и фосфатов. Для этой же цели в железе используются и сывороточные альбумины, которые вначале гидролизуются до аминокислот, а потом вовлекаются в процессы биосинтеза белка.
β-Лактоглобулин. После осаждения казеина (при подкислении молока или под действием реннина) остается сыворотка, содержащая набор белков, среди которых содержится β-лактоглобулин. Он относится к группе альбуминов, так как способен растворяться в растворе (NH4)2SO4 и характеризуется высоким содержанием SH-групп. β-Лактоглобулин состоит из двух полипептидных цепей с молекулярной массой 18,3 кДа, которые при температуре выше 30 °С способны распадаться на мономерные формы. Дальнейшее нагревание приводит к агрегации субъединиц, соединенных между собой дисульфидными связями. В целом β-лактоглобулин имеет две дисульфидные связи между остатками цистеина в положении 66 и 160, 106 и 119 и одну свободную сульфгидрильную группу в положении 13. При нагревании молока до 70 °С и выше часть сульфгидрильных групп отщепляется в виде сероводорода, что придает кипяченному молоку специфический запах. Нагревание молока также сопровождается изменением пространственной структуры сывороточных белков, в результате чего возникают дополнительные дисульфидные связи, при этом молекулы белка денатурируют. β-Лактоглобулин придает молоку определенные физико-химические свойства. Так, в денатурированном состоянии этот белок адсорбируется на мицеллах казеина, предохраняя молоко от свертывания при сгущении. В денатурированном состоянии β-лактоглобулин препятствует створаживанию молока, поэтому молоко, предназначенное для получения творога, нельзя перегревать.
α-Лактальбумин. Белок относится к гликопротеидам, состоит из одной полипептидной цепи с молекулярной массой 16,5 кДа и изоэлектрической точкой 5,1. Входит совместно с галактозилтрансферазой в состав лактозосинтазы. В стабилизации третичной структуры белковой молекулы α-лактальбумина принимают участие ионы кальция, поэтому α-лакталь- бумин денатурирует только при температурах выше 65 °С.
384

18.1. Химический состав молока
Альбумин сыворотки крови (сывороточный альбумин). В молоке содержится сывороточный альбумин — белок глобулярной структуры с молекулярной массой 66 кДа. Он мало чем отличается от аналогичного белка крови, т. е. его синтез происходит не в молочной железе, а в других органах животных.
Церулоплазмин и лактоферрин. Они являются соответственно медь-
ижелезосодержащими белками молока. Оба белка предназначены для накопления и переноса ионов меди и железа, адсорбируя их на поверхности белковой глобулы. Как специализированные переносчики они способны обеспечить поступление ионов меди и железа в организм детенышей, ликвидируя таким образом недостаток этих ионов в растущем организме. Однако между собой церулоплазмин и лактоферрин различаются по молекулярной массе — 151 и 76,5 кДа соответственно.
Очищенный церулоплазмин имеет голубую окраску за счет высокого содержания меди (8 атомов меди на молекулу белка); катализирует реакции оксидазного окисления аскорбиновой кислоты, гидрохинона, катехолов и п-фенилендиамина. Оптимум активности церулоплазмина приходится на рН 5,6…6,0. Ингибиторами фермента являются цианид и азид, а активаторами — Fe2+. Содержание церулоплазмина в молоке составляет менее 1 мг/кг.
Лактоферрин содержит в своем составе углеводы, являясь гликопротеидом. Синтез лактоферрина происходит в клетках молочной железы. В молоке КРС содержится 20…350 мг/кг лактоферрина. При этом его концентрация может возрастать в молозиве и стародойном молоке в десятки
иболее раз.
18.1.3. Ферменты молока
В молоке присутствуют ферменты глутатионпероксидаза, каталаза, липаза, щелочная фосфатаза и др. Глутатионпероксидаза представлена в организме животных в нескольких формах (GPX–I, GPX–II, GPX–III и GPX–IV). Глутатионпероксидаза GPX–I эукариот является селенсодержащим белком, катализирующим следующую реакцию:
2Г-SH + Н2О2 → Г-S-S-Г + 2Н2О,
где Г-SH и Г-S-S-Г — восстановленная и окисленная формы глутатиона.
Другой формой глутатионпероксидазы служит GPX–II, которая катализирует реакцию окисления глутатиона при участии гидроперекисей липидов:
2Г-SH + ROOН → Г-S-S-Г + ROН + Н2О,
где R — алкильный радикал (обычно фосфолипид).
В последнее время обнаружена новая форма глутатионпероксидазы GPX–IV, по специфичности действия тождественная GPX–II, но отлича-
385

Глава 18. Биохимия молока
ющаяся от нее строением первичной структуры полипептидной цепочки. Возрастание пероксидазной активности в молоке может наблюдаться при воспалительных процессах в молочной железе.
В молоке содержится незначительное количество каталазы. Фермент катализирует реакции разложения (диспропорционирования) перекиси водорода на воду и кислород.
Н2О2 → Н2О + О2
Совместно с пероксидазой и СОД каталаза входит в состав антиоксидантной системы животных. Возрастание активности фермента отмечается у новотельных и стародойных коров. Особенно высокая активность фермента проявляется при заболеваниях вымени у коров (маститах).
Липаза, обнаруженная в молоке, катализирует реакции гидролиза сложноэфирных связей, расщепляя триглицериды на глицерин и жирные кислоты. Высокое содержание липазы наблюдается в зимнем молоке по сравнению с летним. Отмечается возрастание активности липазы к концу лактации, что сказывается на качестве молока (прогорклое молоко). Липаза может адсорбироваться на поверхности жировых шариков, вызывая порчу масла, подвергшегося плесневению. Под действием липаз сыры, созревающие при участии плесени, приобретают специфичный вкус.
Щелочная фосфатаза катализирует в щелочной среде реакции гидролиза ортофосфорных эфиров. В действии фермента проявляются свойства гидролазы (1) при отщеплении фосфата от субстрата и трансферазы, когда осуществляется перенос фосфата на молекулу акцептора (глюкоза) (2).
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1) |
R |
|
|
O P |
|
|
|
O + H2O |
|
|
|
R |
|
|
OH + HO |
|
P |
|
|
|
O |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
R′ |
|
|
|
|
O |
|
|
|
|
O |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
HO |
|
|
|
|
|
|
O + R′ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
2) |
P |
|
|
|
|
OH |
|
|
|
|
|
O |
|
P |
|
|
|
O + H2O |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|||||||||||||||||||
Максимальная активность фермента проявляется при рН 9,0…10,0. Высокое содержание фермента отмечено в лактирующей молочной железе. По своей природе щелочная фосфатаза относится к мембранным ферментам и поэтому участвует в механизмах переноса фосфора через клеточные мембраны, являясь компонентом системы активного транспорта. Кроме того, фермент принимает активное участие в процессах кальцификации костной ткани, поэтому его много в сыворотке крови, откуда щелочная фосфатаза поступает при активном кровоснабжении в молочную железу.
386

18.1. Химический состав молока
Ферменты попадают в молоко из крови или являются составными частями отторгающихся клеток секреторного эпителия. Поэтому высокая активность щелочной фосфатазы в молоке может свидетельствовать о заболеваниях печени и костной системы. Щелочная фосфатаза в молоке может быть и микробного происхождения. Поэтому высокая активность фермента может свидетельствовать о низком санитарном качестве молока.
18.1.4. Углеводы молока
Основным углеводом молока является дисахарид лактоза, или молочный сахар, которого содержится 4,5…5,0 %. Кроме того, в молоке может быть до 0,2 % галактозы и 0,01…0,1 % глюкозы. В незначительных количествах в молоке присутствуют и другие олигосахариды: трисахариды, тетрасахариды, пентасахариды, гексасахариды и др.
18.1.5. Липиды молока
Жирные кислоты молока могут частично синтезироваться в молочной железе, а частично поступают из крови. Содержание нейтральных липидов
вмолоке может колебаться в пределах 2,8…4,5%. При этом содержание моно- и диглицеридов в молоке составляет 80%, т. е. всего 1,2…2,6%.
Фосфатидилхолин и фосфатидилэтаноламин являются основными фосфолипидами молока, содержание которых составляет более 60% всех фосфолипидов. При этом основная часть фосфолипидов молока входит
всостав оболочек жировых шариков (60…70 %).
Общее содержание фосфолипидов в молоке и молочных продуктах может составлять (в %): 0,02…0,06 в молоке, 0,15…0,19 в сливках, 0,016…0,028
вобезжиренном молоке, 0,36…0,38 в масле, 0,14…0,23 в пахте. При гомогенизации 5…15% фосфолипидов может перейти в раствор, тогда как при сепарировании молока 60…70% фосфолипидов переходят в сливки, а при сбивании сливок (при производстве масла) 50…65% фосфолипидов переходят в пахту.
Основным стерином молока является холестерин, который входит
всостав жировых шариков. Содержание стеринов в молоке может достигать 0,010…0,014 % и обычно составляет 0,2…0,4 % от общего количества липидов.
Биологически активные вещества липидной природы, представляющие собой оксигенированные производные полиненасыщенных жирных кислот, содержащие в углеводородной цепи пятичленные циклы, называются простагландинами. В молоке содержатся низкие концентрации простагландинов. Однако их высокое содержание в крови определяет сильное регуляторное действие на секрецию молочной железы.
387

Глава 18. Биохимия молока
18.1.6. Витамины молока
В молоке коров содержится более 23 витаминов. Основными источниками витаминов для животных являются травянистые растения, и только часть из них синтезируется микрофлорой рубца. На содержание витаминов в молоке оказывает влияние рацион кормления, физиологическое состояние, вид и порода животного и время года. Кроме того, на содержание витаминов в молоке могут влиять условия хранения и транспортировки продукции, а также воздействие различных физических факторов (низкая и высокая температура, УФ излучение и др.).
Особенно высокое содержание в молоке отмечено следующих витаминов: А, В1, В2, В12 и С.Тиамин преимущественно синтезируется микрофлорой рубца и поступает с кормом животных. В молоке содержание витамина В1 может доходить до 0,8…1,2 мг/кг. Содержание рибофлавина
вмолоке зависит от времени года и может колебаться в пределах 1,0… 2,9 мг/кг. Витамин имеет желтую окраску и при значительных количествах
вмолоке может обусловливать окраску молочной сыворотки. В молозиве
витамина В2 содержится в 3…4 раза больше, чем в молоке. Пантотеновая кислота поступает в организм животных из зеленых растений, а также может быть синтезирована дрожжами и микрофлорой желудочно-кишечно- го тракта животных. Входит в состав КоА и в молоке может содержаться
впределах 2,1…3,8 мг/кг. Содержание В4 в молоке очень низкое и может достигать только 0,2…0,6 мг/кг.
Никотиновая кислота и ее амид могут присутствовать в молоке как в свободном виде, так и в составе коферментов (НАД+ и НАДФ+). При этом
содержание витаминов РР и В5 в молоке может составлять соответственно 1,0…1,2 и 0,8…1,8 мг/кг. Витамин В6 присутствует в молоке в виде восстановленных и окисленных форм (пиридоксол и пиридоксаль), а также их фосфорных эфиров (фосфопиридоксол и фосфопиридоксаль). Общее
содержание витамина В6 и его производных в молоке может определяться в пределах 0,2…1,7 мг/кг. Причем осенью витамина в молоке бывает больше, чем зимой и летом.
Фолиевая кислота совместно с витамином В12 участвует в реакциях метилирования в качестве кофермента. Содержание в молоке фолиевой
кислоты и витамина В12 может составлять соответственно 0,04…2,6 и 2,3… 5,9 мг/кг. Аскорбиновая кислота активно участвует в окислительно-восста- новительных реакциях, протекающих в организме животных. Кроме того, витамин в водной среде может быстро окисляться кислородом воздуха. Реакция окисления витамина С ускоряется в присутствии ионов железа и меди, а также света и высокой температуры. В свежем молоке витамина С может содержаться 3,8…25,2 мг/кг.
388

18.1. Химический состав молока
Биотин активно используется в метаболических процессах дрожжей, молочных бактерий и в животном организме в качестве кофермента карбоксилаз. В молоке отмечает низкое содержание витамина Н, которое может составлять 0,03…0,05 мг/кг. Липоевая кислота входит в состав ферментов пируват- и кетоглутаратдегидрогеназных комплексов в качестве простетической группы, участвуя в реакциях окислительного декарбоксилирования α-кетокислот (пировиноградной и α-кетоглутаровой). В молоке липоевой кислоты содержится 0,02…0,05 мг/кг.
Вмолоке содержится до 0,3 мг/кг витамина В7. Концентрация каротина в молоке зависит от рациона питания, времени года, вида и породы животного. При этом в летний период, когда в кормлении животных преобладает зеленая растительная масса, содержание каротина в молоке составляет 0,5…0,95 мг/кг, а зимой — 0,03…0,18 мг/кг. Высокие концентрации каротина оказывают влияние на окраску масла. Физические воздействия (пастеризация, стерилизация, УФ и видимый свет) могут разрушать каротин, понижая его содержание в молоке и молочных про-
дуктах. В состав витаминов группы А входят несколько соединений (А1, А2 и А3). В молоке преимущественно присутствует витамин А1 (ретинол), содержание которого может колебаться в пределах от 0,08 до 1,0 мг/кг. Количество ретинола в молоке может возрастать в первые месяцы лактации и понижаться к концу лактации. В молозиве содержание ретинола может составлять 0,6…12 мг/кг. Наиболее богато каротинами и витамином А молоко в летний период, когда в питании животных преобладают зеленые корма. Молочные продукты, вырабатываемые в этот период, содержат в 5…6 раз больше каротиноидов, чем в зимнее время.
Вмолоке могут содержаться практически все формы витамина
D. Однако в количественном соотношении преобладает витамин D3. Содержание витамина в молоке очень сильно зависит от времени года и в среднем может колебаться в пределах от 0,5 до 1,5 мкг/кг. Летом обыч-
но витамина D3 может быть в 5…8 раз больше, чем зимой. На содержание витамина влияет УФ облучение животных, которое способствует его возрастанию.
Токоферолы в молоке представлены в группе из нескольких соединений (α-, β-, γ-, δ-токоферол). Однако среди них в молоке преобладает α- токоферол, содержание которого может варьироваться от 0,2 до 1,9 мг/кг. Витамин входит в состав соединений, обладающих антиоксидантным действием. Поэтому высокие концентрации токоферола в молочных продуктах будут обеспечивать их защиту от действия свободных радикалов при длительном хранении. Витамин K синтезируется преимущественно микрофлорой кишечника животных и в молоке поэтому содержится в очень малых концентрациях (30…40 мкг/кг).
389

Глава 18. Биохимия молока
18.1.7. Элементный состав молока
В молоке содержится более 30 макро- и микроэлементов, которые присутствуют в свободном виде или в составе белков и биологически активных соединений. Молоко богато содержанием таких макроэлементов, как Na+, K+, Ca2+, Cl–, P+5, Mg2+. Тогда как микроэлементный состав молока представлен ионами Zn2+, Si+4, Fe3+, Al3+, F–, B+3, Sn2+, Br–, Cu2+, Mn2+, Mo2+, Pb2+, I–, As3+, Se2+, Cr3+, Ni2+, Cd2+, Hg2+, Co2+ (см. табл. 18.1). При этом их действие в клетках и тканях животных проявляется только в составе белков
ибиологически активных соединений. Так, например, Na+ и K+ участвуют в создании трансмембранного потенциала, активизации Na+/K+-АТФазы. Содержание ионов калия в молоке может составлять 126…170, а ионов натрия — 36…78 мг%. Основная роль ионов калия и натрия в молоке сводится к регулированию содержания ионизированной формы кальция, который принимает основное участие в формировании и стабилизации мицелл казеина.
Mg2+ активирует АТФ-азу мышц, участвует в действии АТФ зависимых ферментов (глюкоза-6-фосфатдегидрогеназа, пируваткиназа, гексокиназа
идр.). В молоке содержится 12…14 мг% ионов магния, которые принимают участие в формировании мицелл казеина.
Fe2+ в организме животных участвует в действии гемоглобина, миоглобина, трансферрина, ферритина. Fe3+ входит в состав цитохромов и гемсодержащих ферментов (пероксидаза, каталаза, цитохром с пероксидаза, глутатионпероксидаза), белка молока лактоферрина.
Фосфор (P) является составной частью фосфорной кислоты, которая входит в состав нуклеотидов, моно-, ди- и нуклеозидтрифосфатов (АТФ, ГТФ, ЦТФ, УТФ) и нуклеиновых кислот (ДНК, РНК), коферментов (НАД, НАДФ, ФАД, ФМН, КоА) и др. Кроме того, фосфор входит в состав казеинаткальцийфосфатных комплексов молока.
Ионы хлора (Cl–) обеспечивают в организме животных поддержание трансмембранного потенциала, используются слизистой кишечника для секреции соляной кислоты. В молоке содержится от 100 до 120 мг% ионов хлора.
Ионы меди, цинка, кобальта, молибдена, марганца, а также фтора, йода и брома присутствуют в молоке в микроколичествах (см. табл. 18.1). При этом эти ионы входят в состав функционально важных ферментов
ибиологически активных соединений. Так, например, Cu2+ входит в состав цитохромоксидазы, пластоцианина, тирозиназы, уратоксидазы, полифенолоксидазы, белка крови церулоплазмина, участвует в процессе эритропоэза. Содержание ионов меди в молоке может достигать 0,013…0,014 мг%. Zn2+ входит в состав карбоангидразы, карбоксиполипептидазы, лактатдегидрогеназы, глутаматдегидрогеназы. В молоке содержится 0,3…0,5 мг%
390

18.2. Физико-химические свойства молока
ионов цинка. Cr3+ активирует фосфоглюкомутазу и трипсин. Mn2+ активирует АТФ зависимые ферменты. В молоке содержится 0,004…0,008 мг% ионов марганца. I– входит в состав гормонов щитовидной железы (тироксин, трийодтиронин), которые оказывают регуляторное действие на функционирование молочной железы.
Ca2+ в организме животных необходим для формирования костной ткани, проведения нервного импульса, активирует VIII фактор свертываемости крови, участвует в мышечном сокращении, стабилизирует белки. Содержание кальция в молоке составляет 114…130 мг%. Около 20% всего количества ионов кальция принимают участие в формировании мицелл казеина. Остальная часть их находится в растворе в виде солей фосфорной и лимонной кислот. Основное количество Са2+ поступает в организм животного в виде солей фосфорной кислоты (см. также гл. 7). Всасывание ионов Са2+ происходит главным образом в проксимальных участках тонкого отдела кишечника. Причем наиболее активно процесс всасывания кальция наблюдается у растущего организма, а также при беременности и лактации.
18.2. ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА МОЛОКА
Общая, или титруемая, кислотность молока определяется содержанием
вего составе карбоновых кислот, лимонной кислоты, солей, аминокислот, белков. Накопление в молоке молочной кислоты свидетельствует об активной деятельности молочнокислых бактерий, использующих молочный сахар в реакциях брожения. Общая кислотность молока выражается
вградусах Тернера (°Т) или для масла в градусах Кеттстофера (°К). При этом один градус Тернера соответствует объему 0,1 М водного раствора гидроксида натрия, необходимого для нейтрализации 100 г исследуемого продукта. Один градус Кеттстофера соответствует объему 0,1 М водного раствора гидроксида натрия, необходимого для нейтрализации 5 г сливочного масла или его жировой фазы, умноженному на два. Кислотность свежевыдоенного коровьего молока колеблется в пределах 16…18 °Т.
Вотличие от общей кислотности, активная кислотность молока определяется приборами (рН-метрами), в основе работы которых положен потенциометрический метод (рН — это отрицательный логарифм концентрации ионов водорода. См. также п. 17.1.10). Присутствие в молоке аминокислот, белков, карбоновых кислот и аминосодержащих соединений обеспечивает постоянство рН молока и его буферную емкость. рН свежего коровьего молока 6,2…6,9.
Плотность молока КРС зависит от содержания липидов и СОМО. Плотность коровьего молока может колебаться в пределах 1,029…1,032 г/см3. Плотность обезжиренного молока 1,033…1,035 г/см3. Плотность оленьего
391

Глава 18. Биохимия молока
молока 1,048 г/см3. Добавление к молоку воды приводит к понижению плотности молока.
Молоко имеет осмотическое давление, которое по величине близко к осмотическому давлению крови и зависит от содержания в молоке углеводов и солей.
Вмолоке содержатся различные ионы, которые и будут определять величину электропроводности. Возрастание электропроводности отмечается при болезни животного, а понижение ее возможно при разбавлении молока водой.
Вязкость молока обусловлена взаимодействиями частиц молока при их перемещении относительно друг друга. Вязкость молока больше вязкости воды и зависит от содержания белков, липидов и солей. С повышением температуры вязкость молока понижается, но может возрастать с увеличением
вмолоке липидов и СОМО. Скисание молока сопровождается повышением вязкости молока. Предел колебания вязкости молока от 1,6 до 2,1.
Поверхностное натяжение молока ниже воды, что обусловлено присутствием в молоке молекул белка и жировых шариков.
Вмолоке животных присутствуют следующие газы: углекислый газ, кислород, азот. При этом молоко в молочной железе коровы может содержать
до 10% СО2 от всего объема. Во время доения количество углекислого газа снижается до 4…5% вследствие вспенивания молока в подойнике. После
доения концентрация СО2 снижается в течение нескольких часов до 3%. Свертываемость — способность компонентов молока свертываться под действием сычужного фермента в определенных условиях среды. Имеет значение при производстве сыра и является оценочным критерием молока на сыропригодность. Продолжительность свертывания молока зависит от его кислотности и температуры среды. В диапазоне низких и высоких температур отмечается понижение свертываемости компонентов молока за счет того, что при низких температурах понижается активность сычужного фермента, а высокие температуры (более 65 °С) приводят к его денатурации, сопровождаемой утратой нативной структуры белковой глобулы. Оптимальной для свертывания молока считается температура 40…42 °С. Продолжительность свертывания молока увеличивается с возрастанием его кислотности. Свертываемость молока и качество сгустка
напрямую зависят от условий кормления и содержания животных.
18.3. БАКТЕРИЦИДНЫЕ СВОЙСТВА МОЛОКА
Свеженадоенное молоко содержит вещества, придающие молоку бактерицидные свойства, т. е. способность препятствовать размножению бактерий. Среди группы соединений, обладающих бактерицидным дейс-
392
