
Федеральное агентство по образованию
Государственное образовательное учреждение
высшего профессионального образования
Санкт-Петербургский государственный университет низкотемпературных и пищевых технологий

Факультет пищевых технологий
Кафедра технологии мясных, рыбных продуктов и консервирования холодом
Холодильная технология пищевых продуктов: биохимические и физико-химические основы
Методические указания к лабораторной работе "Действие замораживания на содержание витамина С в растительных продуктах" для студентов всех форм обучения по специальности 260504 очной и заочной форм обучения
Санкт-Петербург
2010
УДК 551.571+725.35
Колодязная В.С., Кипрушкина Е.И. Холодильная технология пищевых продуктов: Методические указания к лабораторной работе "Действие замораживания на содержание витамина С в растительных продуктах" для студентов специальности 260504 очной и заочной форм обучения
. – СПб: СПбГУНиПТ, 2010.. – 11с.
Изложены теоретические положения и метод определения витамина С в растительных продуктах при холодильной обработке.
Рецензент:
Проф., д.х.н. Нечипоренко А. П.
Рекомендованы к изданию советом факультета пищевых технологий
© Санкт-Петербургский государственный
университет низкотемпературных
и пищевых технологий, 2010
ТЕОРЕТИЧЕСКИЕ ПОЛОЖЕНИЯ
Проблема сохранения высокого качества продуктов растительного происхождения при холодильной обработке, содержании в охлаждённом и замороженном состоянии сводится не только к тому, чтобы они не утратили своих органолептических свойств, но и к максимальному ограничению потерь микрокомпонентов, особенно витаминов.
Наибольшим изменениям при замораживании и хранении растительных продуктов подвергается витамин С.
Аскорбиновая кислота, обладая высокой биологической активностью и лабильностью под воздействием различных внешних факторов, может служить одним из показателей качества, критерием оценки биологической ценности и оптимизации технологических условий холодильной обработки и продолжительности хранения.
Витамин С рассматривается как один из самых необходимых компонентов для жизнедеятельности организма человека. Под влиянием витамина С снижается проницаемость сосудистой оболочки, повышается её эластичность и прочность. Недостаточность витамина С в организме может привести к развитию атеросклероза и других болезней. Суточная потребность человека в этом витамине составляет в среднем 50 – 60мг.
Основным источником витамина С являются овощи и фрукты.
Аскорбиновая кислота является окисленным производным шестиуглеродного спирта сорбита (продукты восстановления глюкозы).
Существуют различные формы аскорбиновой кислоты: восстановленная (АК), обратимо окисленная дегидроаскорбиновая кислота (ДАК), связанная (аскорбиген) и инертная–дикетогулоновая кислота (ДКГК).
Под витамином С в растительных продуктах понимают физиологически активные формы АК и ДАК.
Окисление аскорбиновой кислоты катализируется различными оксидазами (аскорбинатоксидазой, фенолоксидазой, пероксидазой), а также химическими процессами, происходящими особенно интенсивно в щелочной среде. В связи с этим потери витамина С при хранении замороженных овощей больше, чем при хранении замороженных плодов.
Кислоты являются стабилизаторами, обеспечивающими более длительное сохранение аскорбиновой кислоты в растворах.
Аскорбиновая кислота участвует в процессах метаболизма плодов и овощей, а окислительно-восстановительные превращения её играют важную роль в биологических реакциях, протекающих с участием транспортёра электронов.
Превращения аскорбиновой кислоты при замораживании и хранении плодов и овощей сводятся к её окислению до ДАК и затем до 2,3-дикетогулоновой кислоты по схеме:

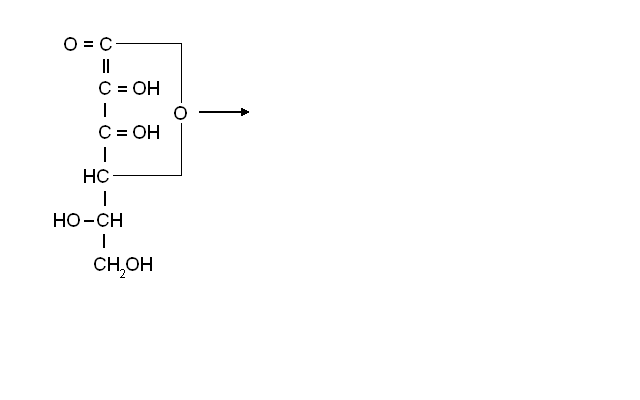
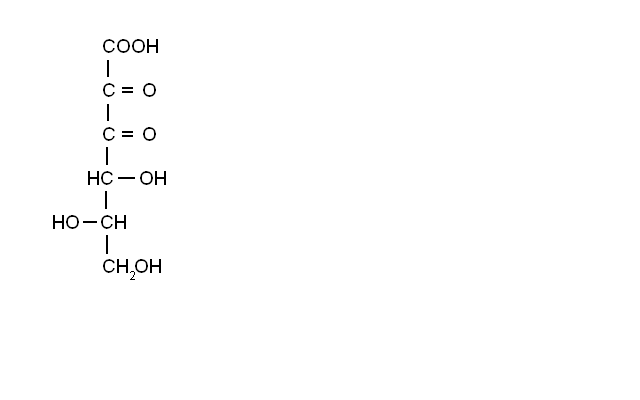
L-аскорбиновая L-дегидроаскорбиновая L-2,3-дикетогулоновая
кислота кислота кислота
2,3-дикетогулоновая кислота при дальнейшем окислении переходит в щавелевую и треноновую кислоты.
Известно, что увеличение количества аскорбиновой кислоты происходит в результате гидролиза аскорбигена, в меньшей мере – за счёт восстановления дегидроаскорбиновой кислоты, а уменьшение количества восстановленной аскорбиновой кислоты вызвано её окислением. Поэтому изменение количества аскорбиновой кислоты в плодах и овощах под воздействием внешних факторов, в том числе температуры и продолжительности хранения, может служить показателем физиологического состояния растительного организма и его биологической ценности.
ЦЕЛЬ РАБОТЫ
Целью настоящей работы является определение количественного изменения содержания восстановленной формы аскорбиновой кислоты в растительных продуктах в зависимости от условий обработки.
Определение аскорбиновой кислоты основано на способности обратимо окисляться и восстанавливаться благодаря наличию в её молекуле диэнольной группировки. Специфичным индикатором для определения аскорбиновой кислоты является 2,6-дихлорфенолиндофенол – соединение, обладающее способностью изменять окраску в зависимости от рН среды.
Химический метод определения аскорбиновой кислоты несовершенен. Основной недостаток этого метода состоит в том, что им можно определять только L-аскорбиновую кислоту в бесцветных или слабоокрашенных растворах.
Для определения содержания витамина С в яблоках, картофеле, капусте этот метод вполне приемлем, так как вытяжки из этих продуктов получаются бесцветные или с очень слабым зеленовато-жёлтым оттенком.
Следует отметить, что L-аскорбиновая кислота на воздухе очень быстро переходит в L-дегидроаскорбиновую кислоту.
При взятии навески растительной ткани необходимо как можно быстрее инактивировать действие фермента аскорбатоксидазы, который под действием кислорода воздуха легко окисляет восстановленную форму аскорбиновой кислоты.
Для инактивации этого фермента можно использовать 2 %-ный раствор метафосфорной кислоты (лучший стабилизатор витамина С), 1 %-ный раствор соляной кислоты или смесь 1 %-ных растворов соляной и щавелевой кислот.
Приборы и материалы, необходимые для выполнения работы
Весы технические …………………………………………………1
Колба мерная 100 мл …………………………………………...... 1
Колба круглая плоскодонная 100 мл ………………………….... 1
Колба коническая 50 мл ………………………............................ 1
Стаканчик 100 мл ………………………………………………… 1
Стаканчик 50 мл ………………………………………………... .. 1
Цилиндр мерный 20 мл ………………………………………….. 1
Пипетка 10 мл ………………………………………………….... 1
Микробюретка (пипетка) 5 мл …………………………………. 1
Ступка с пестиком ………………………………………………. 1
Палочка стеклянная ……………………………………………... 1
Пробник диаметром 5-7 мм …………………………………….. 1
Воронка ………………………………………………………….. 2
Пробка на мерную колбу ……………………………………….. 1
Бумага фильтровальная ………………………………………….
Песок прокалённый ………………………………………………
Вода дистиллированная ………………………………………….
Смесь 4 %-ных растворов метафосфорной и соляной кислот… 40 мл
0,001 %-ный раствор 2,6-дихлорфенолиндофенола……………. 40 мл
Объект исследования: продукт растительного происхождения.
Порядок выполнения работы
Студенты разделяются на группы:
- одна группа определяет содержание витамина С в свежих плодах;
- вторая – после бланширования;
- третья – после замораживания (температура замораживания задаётся преподавателем).
Приготовление раствора краски Тильманса
Раствор индикатора – 2,6-дихлорфенолиндофенола (краска Тильманса) приготавливается растворением 200 мг краски в 1 л дистиллированной воды, затем раствор фильтруется и к нему добавляется несколько кристалликов NaHCO3. Титр полученного раствора устанавливается по кристаллической аскорбиновой кислоте. Раствор краски неустойчив и его титр определяется непосредственно перед опытом.
Определение титра индикатора
Около 1-1,5 мг аскорбиновой кислоты растворяют в 50 мл 2 %-ной серной или лучше метафосфорной кислоты. Пять миллилитров этого раствора титруют краской из микробюретки. Затем такой же объём раствора аскорбиновой кислоты титруют из другой микробюретки 0,001%-ым раствором KJO3 (0,03568 KJO3, высушенного в течение 2 ч при 102оС в 1л воды) с добавлением перед титрованием нескольких кристаллов (не больше 0,10 г) KJ и пяти капель 1%-ного раствора крахмала. Расчёт титра краски по аскорбиновой кислоте производят по следующей формуле, исходя из того, что 1 мл 0,001н йода (йодата) эквивалентен 0,088 мг аскорбиновой кислоты, мг:

где а – 0,001н KJO3, мл;
б – объём раствора краски, мл.
Таким образом определяется, какому количеству (в миллиграммах) аскорбиновой кислоты соответствует 1 мл краски.
Порядок выполнения работы
Яблоки для всех анализов выбираются одинаковые по размеру, окраске и форме.
В стаканчик на 100 мл мерным цилиндром приливается 20 мл 2 %-ного раствора метафосфорной кислоты или 1 %-ного раствора соляной кислоты. Затем стаканчик с содержимым взвешивается на технических весах, масса а записывается. После этого из трёх свежих яблок пробником берётся проба массой примерно 15 г.
При взятии проб из яблок следует учитывать, что аскорбиновая кислота располагается в плодах неравномерно: в кожице её в 6 раз больше, чем в сердцевине. Поэтому среднюю пробу желательно составлять так, чтобы в ней всегда было одно и то же соотношение всех частей плода (кожицы, сердцевины и т.д.). Для этой цели используются специальные пробники. Пробником может служить любая металлическая трубка с поршнями из нержавеющего материала диаметром от 0,5 до 0,7 см.
Проба выталкивается из пробника поршнем непосредственно в стаканчик со смесью кислот и взвешивается ( в ). Определяется масса пробы:
![]()
где в – масса стаканчика со смесью кислот и пробой.
Всё содержимое стаканчика переносят в ступку и растирают пробу с небольшим количеством песка. Затем переносят содержимое ступки в колбу на 100 мл или в мерный цилиндр на 100 мл.
Ступку тщательно обмывают раствором кислоты, затем водой. Обмывающие жидкости смывают в ту же мерную колбу или цилиндр и доводят до метки. После этого колбу энергично встряхивают в течение 3-5 мин; если же проба перенесена в цилиндр, то в течение 3-5 мин её энергично помешивают стеклянной палочкой.
После перемешивания вытяжку фильтруют через складчатый фильтр. Из фильтрата берётся 10 мл прозрачной и почти бесцветной вытяжки в стаканчик на 50 мл и титруется из микробюретки стандартизированным раствором 2,6-дихлорфенолиндофенола до появления стойкого слабо-розового окрашивания, не исчезающего в течение одной минуты. Титрование повторяется не менее 3 раз.
В табл.1 вписывается количество краски С, пошедшее на титрование.
Параллельно проводится контрольный опыт. В мерную колбу на 100 мл наливают 20 мл смеси соляной и щавелевой кислот и доводят до метки. Затем берут 10 мл испытуемого раствора в коническую колбу на 50 мл и титруют краской Тильманса до появления слабо-розового окрашивания, записывают количество 2,6-дихлорфенолиндофенола, затраченного на титрование при контрольном опыте Со.
Определение аскорбиновой кислоты аналогично проводят в яблоках, подвергнутых холодильной обработке. Полученные результаты записывают в табл. 1.
Таблица 1
|
Состояние плода |
а, г |
в, г |
g, г |
С, мл |
Со, мл |
|
Свежий плод
|
|
|
|
|
|
|
Бланшированный плод |
|
|
|
|
|
|
Замороженный плод |
|
|
|
|
|
Обработка результатов эксперимента
Расчёт содержания аскорбиновой кислоты в 100 г яблок проводится по следующей формуле:

где x – количество аскорбиновой кислоты в 100 г яблок, мг;
С-Со – количество раствора 2,6-дихлорфенолиндофенола, затраченного на титрование вытяжки за вычетом поправки на контрольный опыт, мл;
Т – титр раствора 2,6-дихлорфенолиндофенола по аскорбиновой кислоте, мг;
е – общее количество вытяжки, полученное при добавлении к навеске экстрагирующей жидкости, мл;
0,088 – количество миллиграммов аскорбиновой кислоты, соответствующее 1 мл 0,001н раствора 2,6-дихлорфенолиндофенола;
h – количество вытяжки, взятой непосредственно для титрования, мл;
g – навеска, г.
Выводы
В заключение работы делаются выводы о количественном содержании аскорбиновой кислоты в яблоках в зависимости от холодильной обработки. Совместно студентами всех подгрупп обсуждаются полученные результаты и составляется отчёт.
Оформление работы
Отчёт по работе должен содержать:
-
Теоретические предпосылки.
-
Цель работы и её краткое содержание.
-
Краткий ход проведения анализа.
-
Таблицу опытных данных.
-
Выводы по результатам работы.
Список литературы
-
Большаков С.А. Холодильная техника и технология продуктов питания. - М.: ,2003 - 304с.
-
Щербаков В.Г. и др. Биохимия растений. - СПб.: Гиорд, 2003. – 440с.
-
Досон Р. И др. Справочник биохимика. – М.: 43-60 Мир, 2001. – 544с.
Колодязная Валентина Степановна
Кипрушкина Елена Ивановна
ХОЛОДИЛЬНАЯ ТЕХНОЛОГИЯ ПИЩЕВЫХ ПРОДУКТОВ
Методические указания к лабораторной работе "Действие замораживания на содержание витамина С в растительных продуктах" для студентов специальности 260504 «Технология консервов и пищеконцентратов»
Редактор
Корректор
Компьютерная верстка
Директор ИПЦ
Подписано в печать . .09. Формат 60×84 1/16.
Печать офсетная. Усл. печ. л. . Печ. л. . Уч.-изд. л.
Тираж экз. Заказ № С
________________________________________________________________
СПбГУНиПТ. 191002, Санкт-Петербург, ул.Ломоносова, 9
ИПЦ СПбГУНиПТ. 191002, Санкт-Петербург, ул.Ломоносова, 9
