
Pain Pathophysiology
.pdf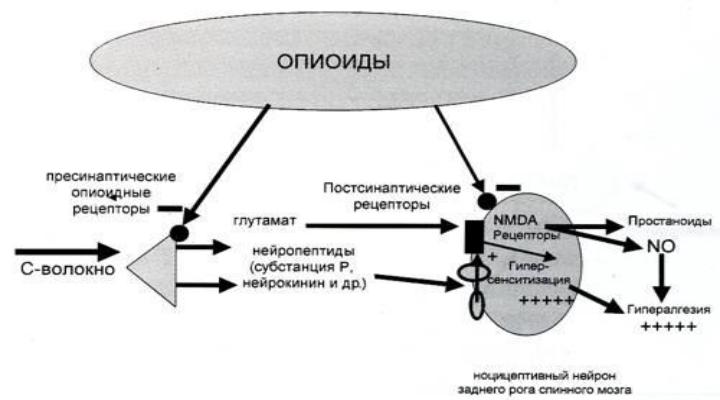
Механизм действия опиоидов
Закрытие потенциал-зависимых Ca2+ каналов в пресинаптическом нейроне приводит к уменьшению выброса возбуждающих аминокислот – глутамата и аспартатата, уменьшая взаимодействие с NMDA-рецепторами, а активация К+ каналов в постсинаптическом нейроне приводит к гиперполяризации мембраны, что уменьшает чувствительность
нейрона к возбуждающим нейромедиаторам.
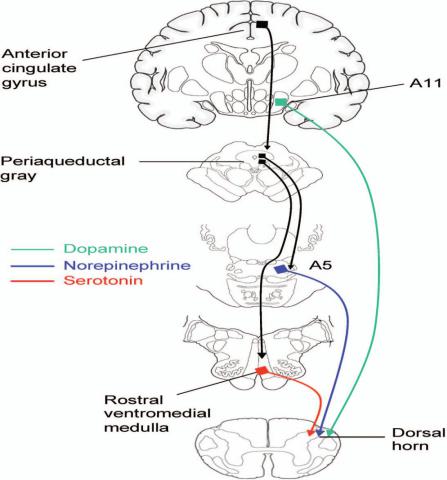
Моноаминергическая нисходящая модулирующая система
•Серотонинергическая система:передняя поясная извилина - околоводопроводное серое вещество (каудальный отдел среднего мозга) - locus coeruleus покрышки моста (А5) - гигантоклеточные ядра шва продолговатого мозга к задним рогам спинного мозга
•Дофаминергические и адренергические пути: вентромедиальные ядра гипоталамуса
(А11) - locus caeruleus (А5) - к задним рогам спинного мозга
Роль опиоидергической и моноаминергической систем в модуляции боли
•При острой ноцицептивной боли модуляция в большей степени связана с
опиоидергической системой
•Хроническая боль, связанная с нейропатическим компонентом, ведет к
редукции опиоидергического ответа в силу его истощения (опиоидная
толерантность). Модулирующую роль начинает играть
моноаминергическая система
•На уровне заднего рога спинного мозга серотонин, норэпинефрин, дофамин оказывают антиноцицептивное действие за счет торможения высвобождения
нейротрансмиттеров из первичных афферентных нейронов влиянием на
пресинаптические 5-HT1B, 2, и D2/D3 тормозные рецепторы
•Опосредованное действие. Динорфин, взаимодействующий со вставочными нейронами на уровне клеток заднего рога спинного мозга, стмиулирует высвобождение GABA, ведущей к гиперполяризации II ноцицептивного нейрона ЗРСМ
•Интернейроны могут опосредовать модулирующий эффект моноаминов. Например норэпинефрин может оказывать антиноцицептивное действие через возбуждающие постсинаптические альфа1-рецепторы, расположенные на GABA-ергических вставочных нейронах. Серотонинергические волокна заканчиваются наингибиторных вставочных нейронах задних рогов спинного
мозга, реализующие свой антиноцептивный тормозный эффект
высвобождением опиоидов на пре- (С-волокна) и постсинаптическом (II нейрон) уровнях
Роль GABA (гамма-аминомасляная кислота ) в поддержании гомеостаза между активирующей и ингибирующей активностью ЦНС
•Действие GABA на глутаминергические афферентные терминали ингибирует
высвобождение субстанции Р, предотвращая избыточное возбуждение
ноцицептивных нейронов
•Активация GABA-рецепторов нейрона ведет к массивному поступлению Cl и его гиперполяризации с нарушением дальнейшего возбуждения нейрона
•Периферического повреждение нейрона (волокна) ведет к разрастанию клеток микроглии, высвобождающие нейротрофический фактор, способствующий разрастанию АТФ-стимулированных P2X4-рецепторов Взаимодействие GABA c данными рецепторами приводят не к тормозной гиперполяризации а возбуждению клетки, что лежит в основе формирования стойкой нейропатической боли (феномен sprouting). Из тормозного нейротрансмиттера GABA становится возбуждающим
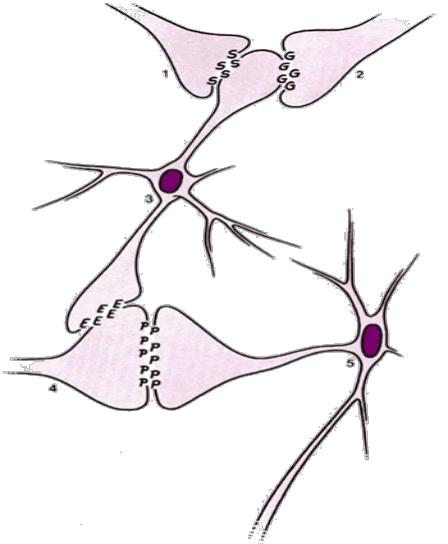
механизм ингибирования активации болевых нейронов посредством энкефалинсекреторных интернейронов (желатинозная субстанция)
•1.Нисходящий ингибиторный нейрон из области околоводопроводного серого вещества.
•2.Большой А-β нейрон
•3.Энкефалинэргический интернейрон в желатинозной субстанции
•4.Ноцицептор (А-δ и С-волокно)
•5.Нейрон второго порядка, ведущий к спинно-таламическому пути
•G = гамма -аминобутиратная кислота
•S = 5-гидрокситриптами или норэпинефрин
•E = энкефалин
•P = нейротрансмиттер боли («Субстанция Р»)
•гидрокситриптамин (5НТ, серотонин) и норэпинефрин также модулируют высвобождение болевых нейротрансмиттеров в ЖС путем активации нисходящих ингибиторных путей
•Неврологическая активность в больших А
волокнах в том же сегменте может также подавлять ответ на повреждающие стимулы в ЖС (так называемое закрытие ворот), которые, как полагают, обусловлены высвобождением ГАМК
Теория воротного контроля (Melzak R. и
Wall P.D., 1965 )
•На нейроны желатинозной субстанции оказывают влияние нисходящие пути от таламуса, неноцицептивными воздействиями с афферентных А - волокон, ноцицептивными воздействиями с афферентных А - волокон
•Это ведет к затруднению проведения ноцицептивной импульсации через желатинозную субстанцию и уменьшению мощности потока импульсов, который пройдя через таламус и, достигнув коры, формирует ощущение боли.
•Если повышается активность С-волокон, то проведение возбуждения через желатинозную субстанцию облегчается.
•Теория воротного контроля боли объясняет, почему неболевые стимулы могут подавлять ответы нейронов заднего рога спинного мозга, передающих в мозг
информацию о болевых стимулах – например при сдавлении поврежденного участка конечности, когда возбуждаются афферентные А - волокона
•В рамках данной теории можно объяснить высокую эффективность превентивно использованных анальгетиков по сравнению с теми же анальгетиками и в тех же дозах, но примененных у больного во время наибольшей выраженности болевого синдрома.
Заключение
•Проведение боли в организме имеет несколько уровней
•Периферический уровень соответствует зоне повреждения тканей, детекторами которой являются периферические ноцицепторы
•После передачи импульсов с Аδ- и С- волокон к нейронам ЗРСМ боль достигает
сегментарного и центрального уровней
•На нейроны заднего рога спинного мозга проецируется множество активирующих и тормозных, восходящих и нисходящих влияний, каждое из которых влияет на уровень болевого возбуждения
•Выделение вещества Р, брадикинина, гистаминаи других БАВ усиливают
ноцицептивную импульсацию, а катехоламины, серотонин, энкефалины,
эндорфины – угнетают
•Можно заключить, что имеется постоянное взаимодействие ноцицептивных и антиноцицептивных механизмов, что, в конечном счете, формирует порог болевой чувствительности и его функциональные колебания
Список литературы
•Ананьева Л.П., Балабанова Р.М. Лечение анальгетиками центрального действия хронического болевого синдрома при заболеваниях костно-мышечной системы // Consilium-medicum Том 3/N 9/2001
•Ананьева Л. П. Симптоматическая терапия боли при ревматических заболеваниях // Терапия боли в ревматологии.— 2002.— Т. 4, № 8.
•Буров, Н. Е. Анальгезия послеоперационного периода / Н. Е. Буров // Рус. мед. журн. - 2003. – N 21. - C. 1172-1177. (http://www.medlinks.ru)
•Вальдман А.В., Игнатов Ю.Д. Центральные механизмы боли. – Л.: Наука, 1976. – 191 с.
•Вейн А.М., Авруцкий М.Я. Боль и обезболивание. – М.: Медицина, 1997. – 279 c.
•Вознесенский А. Г., www.volgadmin.ru, Клиническая фармакология нестероидных противовоспалительных средств
•Вознесенский А.Г., Клиническая фармакология нестероидных противовоспалительных средств // Кафедра клинической фармакологии Волгоградской медицинской академии
(www.volgadmin.ru).

Список литературы
•Гельфанд, Б. Р. Послеоперационная анальгезия / Гельфанд Б. Р.,. Кириенко П. А,. Черниенко Л. Ю // Рус. мед. журн. - 2003. – N 12. - C. 707-713.
•Гнездилов А. Фантомно-болевой синдром,// Конспект врача (приложение к изданию "Медицинская газета") (Москва) , N017 15.3.2002, www.webground.su
•Горобец Е.С. Подходы к современному послеоперационному обезболиванию// ХИРУРГИЯПРИЛОЖЕНИЕ К CONSILIUM MEDICUM Том 09-N 1-2007.mht,
•Горобец Е.С.,.Гаряев Р.В, О проблеме послеоперационного обезболивания и перспективах его совершенствования // Consilium-medicum Том 08/N 7/2006 .
•Дмитриев А.В. Вегетативные реакции ноцицептивного генеза и некоторые механизмы их формирования // Нейрофармакологические аспекты боли. – Л., 1982. – С. 108-127.
•Игнатов Ю.Д., Зайцев А.А. Современные аспекты терапии боли: опиаты // Качественная клиническая практика. – 2001. – № 2. – C. 2-13
•Калюжный Л.В., Голанов Е.В. Центральные механизмы контроля болевой чувствительности // Успехи физиол. наук. – 1980. – № 3. – С. 85-115.
•Кукушкин Л.М., В.К.Решетняк, Механизмы патологический боли, http://www.rusanesth.com

Список литературы
•Кукушкин М.Л., Неврогенные болевые синдромы: патофизиология, особенности клинической картины, принципы терапии// Consilium-medicum Том 07/N 2/2005
•Кукушкин М.Л., Иванова А.Г., Овечкин А.М. и др Неврогенные болевые синдромы: патофизиология, особенности клинической картины, принципы терапии.// Анестезиол. и реаниматол.1996; 4: 39-42
•Кукушкин М.Л., Патогеническое обоснование принципов лечения соматогенных болевых синдромов, 2005 г. medtema.ru
•Кукушкин М.Л., Решетняк В.К. Механизмы возникновения острой боли и хронических болевых синдромов //Materia Medica. 1997. Т. 3. * 15. С. 5- 21; (www.medbiol.ru)
•Лебедева Р.Н., Никода В.В. Фармакотерапия острой боли. – М.: Аир-Арт, 1998. – 184 с.
•Лебедева Р.Н., Никода В.В., Нестероидные противовоспалительные и другие ненаркотические анальгетики в лечении острой боли (www.medlibrary.ru)
•Кукушкин М. Л., Журнал "Боль" № 1, 2003 г., (http://www.painstudy.ru)
•Малрой М.., Местная анестезия. – М. БИНОМ., Лаборатория знаний, 2005 – 301 с.
•Михайлович В.А., Игнатов Ю.Д. Болевой синдром. – Л.: Медицина, 1990. – 330 c.
•Морган Д.Э., Михаил М.С. Клиническая анестезиология: Пер. с англ. – С.Пб.: БИНОМ – Невский диалект, 1998. – кн. 1. – 430 с.
•Овечкин A.M., Гнездилов А.В., Кукушкин М.Л. Предупреждающая аналгезия. Мультимодальный подход к профилактике послеоперационной боли // Материалы VII Всероссийского съезда анестезиологов и реаниматологов. – СПб., 2000.– C. 62-64.
