
- •1.Ацетилен и синтезы на его основе
- •2.Производство ацетилена из карбида кальция
- •3.Теор основы получения ацетилена из углеводородного сырья
- •4. Производство ацетилена окислительным пиролизом метана Лекции
- •5.Синтез-газ и производство органически продуктов на его основе
- •6.Теоретические основы получение синтез газа из высокоуглеродистых материалов и ув. (большой)
- •7. Получение синтез газа окислительной конверсией метана.
- •8.Теоретические основы процессов алкилирования.
- •9.Алкилирование ароматических соединений олефинами
- •10.Сравнительная оценка алкилирования бензола на катализаторах
- •11.Производство этил бензола и изопропилбензола.(схему).Слайды как допол-е
- •12.Зеленая химия.
- •14.Применение ионных жидкостей .
- •15.Ресурсоэнергосберегающие и энергосберегающие технологии в нп и нх.
- •16.Технологии переработки полимерных отходов (еще сократить) не все способы писать
- •17. Проблемы экологичности нефтеперерабатывающих предприятий.
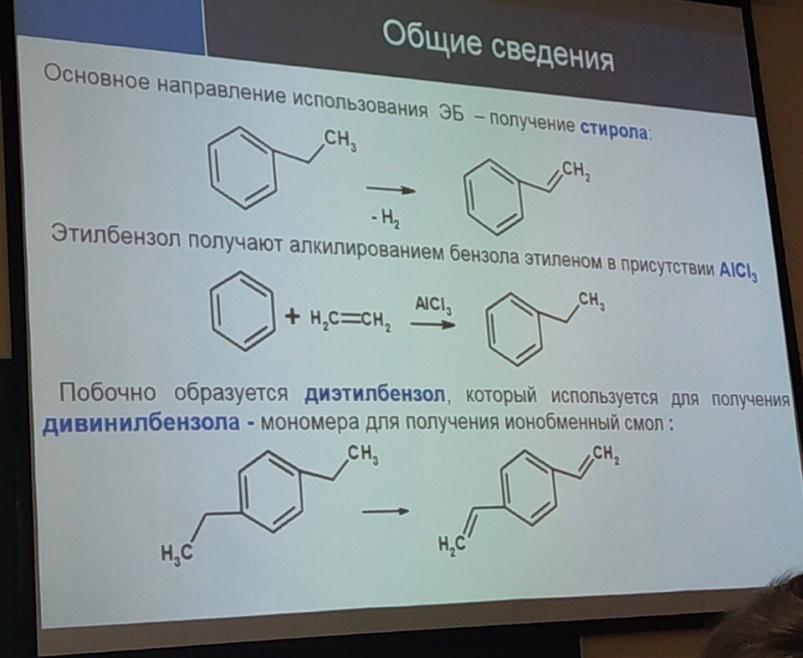
11.Производство этил бензола и изопропилбензола.(схему).Слайды как допол-е



12.Зеленая химия.
Зеленая химия - новый подход к сокращению или полному отказу от использования опасных и токсичных химических веществ.
Цель– отбор исходных материалов и схем процессов, которые вообще исключает использование вредных веществ на самых начальных стадиях планирования и осуществления химических процессов.
пути синтеза.
1.использование катализатора, который снижает энергетический барьер реакции. 2. использование локальных источников энергии для активации молекул позволяющих снизить затраты энергии.
3.использование биомассы вместо нефти
выделяют 4 основных Принципа «зеленой химии».
1 лучше предотвратить образование загрязнений, чем потом от них избавляться.
2. эффективность химических реакций .Синтез веществ следует планировать так, чтобы максимальное количество исходных материалов вошло в конечный продукт, а число отходов уменьшилось.
3. энергия. Стремиться минимизировать энергетические затраты, (химические процессы следует проводить по возможности при низких температурах и давлениях.) Подбор подходящих катализаторов.
4. безопасность химических производств. Вещества и процессы следует выбирать так, чтобы несчастных случаев –стало меньше.
Сверхкритическим флюидом (СКФ) называют состояние вещества, при котором исчезает различие между фазами. Любое вещество, находящееся при температуре и давлении выше критической точки, является сверхкритической жидкостью. В критической точке две фазы, жидкая и газовая, становятся неразличимы.
Вещества в ск состоянии могут применяться в качестве заменителей органических растворителей (сверхкритическая вода и сверхкритический диоксид углерода)
Одно из наиболее важных свойств сверхкритического состояния — это способность к растворению веществ. Изменяя температуру или давление флюида, можно менять его свойства в широком диапазоне Так, можно получить флюид, по свойствам близкий либо к жидкости, либо к газу.
Сверхкритическая область начинается в критической точке , которая характеризуется непременно двумя параметрами — температурой и давлением. Понижение либо температуры, либо давления ниже критического выводит вещество из сверхкритического состояния.
В критической точке плотность жидкости и её насыщенного пара становятся равны, а поверхностное натяжение ( термодинамическая характеристика поверхности раздела двух фаз) жидкости падает до нуля, поэтому исчезает граница раздела фаз жидкость-пар.
14.Применение ионных жидкостей .
«Ионные жидкости» -вещества, которые являются жидкостями при температуре ниже 100 °С и состоят из органических катионов и разнообразных анионов (например, 1,3-диалкилимидазолия)
Ионные жидкости относятся к так называемым «зелёным растворителям», которые соответствуют принципам зелёной химии.
Ионные жидкости в твёрдом состоянии представляют собой порошки либо воскообразные субстанции белого, либо желтоватого цвета. В жидком состоянии бесцветны, либо с желтоватым оттенком, который обусловлен небольшим количеством примесей.
Перспективно использование ионных жидкостей в качестве катализаторов и реакционных сред в синтезе органических, металлорганических и высокомолекулярных соединений; электролитов в электрохимическом синтезе, химических источниках тока и процессах электроосаждения металлов и сплавов; эффективных и экологически чистых растворителей.
Из-за их высокой стоимости ионные жидкости вряд ли найдут широкое применение в многотоннажных процессах
Ионные жидкости состоят из объемных органических катионов и органических или неорганических анионов. Несимметричность строения, а также пространственная изолированность зарядов препятствует организации кристаллической структуры и обусловливает ионный характер жидкой фазы.
СВОЙСТВА ИОННЫХ ЖИДКОСТЕЙ
1)широкий интервал жидкого состояния (>300 °C) и низкая температура плавления(Тпл<100 °C);
2)высокая удельная электропроводность;
3)хорошая растворяющая способность по отношению к разнообразным органическим, неорганическим, металлоорганическим соединениям и полимерам природного и синтетического происхождения;
4)нелетучесть, возможность многократного использования;
5)негорючесть, невзрывоопасность, нетоксичность;
6)каталитическая активность, обуславливающая повышение селективности органических реакций и выхода целевого продукта;
7)безграничные возможности в направленном синтезе ионных жидкостей с заданными свойствами.
ПРИМЕНЕНИЕ иж
Наиболее значимые перспективные ионные жидкости как каталитические среды в катализе и органическом синтезе:
алкилирование и ацетилирование; олигомеризация и димеризация олефинов; реакции образования С–С-связей; карбонилирование и гидроформилирование; гидрирование; галогенирование; окисление органических соединений; изомеризация различных ув.
Ионные жидкости в синтезе полимеров:
Одним из свойств ИЖ является способность пластифицировать различные полимеры, что позволяет получать композиционные материалы с улучшенными физ. и мех. характеристиками.
По физическим характеристикам полимеры, пластифицированные ИЖ, сопоставимы с полимерами, пластифицированными традиционными пластификаторами (например, диоктифталатом) , но являются более термически стабильными.
Кроме того, ИЖ снижают горючесть полимеров, что позволяет применять их в качестве огнезащитного состава
Применение ИЖ в алкилировании:
ИЖ используется в качестве катализатора алкилирования для получения высокооктановых моторных топлив в качестве альтернативы традиционным фтористоводородной или серной кислотам.
Этот жидкий катализатор имеет малое давление насыщенных паров и может регенерироваться непосредственно на объекте, а значит, оказывает меньшее воздействие на окружающую среду, чем кислоты.
