
- •Лекция 9-10
- •Тема 3.2. Кинетика процесса электрохимической коррозии металлов Зависимость скорости коррозии от внутренних и внешних факторов
- •Влияние концентрации водородных ионов
- •Влияние состава и концентрации солей в растворе
- •Влияние скорости движения коррозионной среды
- •Влияние температуры
- •Влияние давления
Влияние температуры
С повышением температуры скорость коррозии в электролитах увеличивается. Увеличение скорости коррозии объясняется падением омического сопротивления электролитов при повышении температуры, возрастанием скорости диффузии, интенсификацией анодных и катодных процессов. Таким образом, все факторы изменяются в сторону усиления коррозионных пар.
При растворении металлов в неокислительных кислотах температурная зависимость скорости коррозии описывается уравнением Аррениуса
К = А . е–B/T , (38)
где А и В – постоянные;
е – основание натуральных логарифмов;
T – абсолютнаятемпература.
После логарифмирования это уравнение имеет вид:
lnK = lnA – B/T, (39)
то есть логарифм скорости коррозии изменяется линейно с величиной, обратной абсолютной температуре.
Для случаев коррозии с кислородной деполяризацией наблюдается более сложная зависимость изменения скорости коррозии с повышением температуры. С повышением температуры скорость коррозии в начале увеличивается за счет ускорения диффузии кислорода и уменьшения перенапряжения ионизации кислорода. Однако при дальнейшем повышении температуры скорость коррозии может снижаться. Это явление связано с уменьшением растворимости кислорода или появлением защитных свойств у продуктов коррозии.
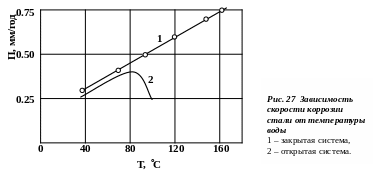
Уменьшение скорости коррозии вследствие понижения концентрации кислорода в растворе особенно характерно для коррозии железа в воде в открытой системе. Вода в открытой системе при комнатной температуре содержит в 1 л. около 6 см3 растворенного кислорода, а при 98оС – около 0,2 см3/л; содержание же кислорода в воде, находящейся в закрытой системе, практически не меняется. Вследствие этого скорость коррозии железа в воде изменяется при повышении температуры различно в зависимости от того, закрыта или открыта система.
Как видно из рис.27, в первом случае при повышении температуры скорость коррозии непрерывно увеличивается. Во втором случае до 80оС наблюдается усиление коррозии, но при более высокой температуре, вследствие уменьшения содержания кислорода в растворе, скорость коррозии уменьшается.
Помимо прямого влияния температуры установленным является факт влияния теплопередачи на коррозию металлов как в активном, так и пассивном состояниях. Действие тепловых потоков на скорость коррозии металлов является сложным и определяется природой коррозионной системы. Передача тепла от металла к раствору или в обратном направлении не просто изменяет температуру в коррозионной зоне, но влияет на массоперенос в жидкости, а в связи с этим на механизм и кинетические закономерности коррозионного процесса и состав фазовой границы.
Причиной интенсификации коррозии в неизотермических условиях считается повышение концентрации кислорода у корродирующей поверхности, омываемой более холодной жидкостью.
При кинетическом контроле в кислой среде теплопередача от жидкости к металлу усиливает коррозию металла, а при обратном направлении теплового потока – уменьшает. Приведенные эффекты объясняются влиянием теплопереноса на структуру и состав двойного электрического слоя, а также на механизм процесса. Например, в растворе 1N Na2SO4 (рН=2) изменяется порядок реакции по гидроксил- и сульфат-ионам. При тепловой нагрузке 19 – 58 кВт/м2 теплопередача приводит к усилению коррозии углеродистой стали в водных растворах при любом характере деполяризации – водородной и кислородной.
Увеличение скорости коррозии на 2 – 3 порядка при теплопередаче наблюдается при неполном погружении в раствор за счет усиления процессов испарения – конденсации и появления зон повышенной коррозионной агрессивности в системе “металл-раствор”.
На коррозионном поведении неизотермических систем может проявляться термогальваническая коррозия из-за наличия температурного градиента по сечению металла.
Кроме того, на теплопередающей поверхности интенсифицируются процессы кристаллизации трудно растворимых солевых систем из-за изменения физико-химических свойств растворенных в воде компонентов. Самым распространенным видом солеотложения является карбонат кальция из-за взаимных превращений диссоциированных форм карбонатно-кальциевой основы воды. Повышение температуры, теплопередача, солеотложения способствуют развитию неравномерной, как правило, язвенной коррозии.
