
Задание № 1.
Дополните
1. Неорганические макротела, состоящие из атомов одного и того же химического элемента, называются…
2. Изменение концентрации одного из реагирующих веществ или продуктов реакции в единицу времени в…, называется скоростью гомогенной реакции.
3. Вещество, в узлах кристаллической решетки которого находятся сложные частицы, способные к самостоятельному существованию при переходе вещества в расплавленное или растворенное состояние, называется ...
4. Процесс отдачи электронов атомом, молекулой или ионом, приводящий к повышению степени окисления, называется…
5. Протон – частица, несущая единичный … заряд
6. Число молей растворенного вещества, содержащихся в 1 дм3 раствора, называется …
Выберите правильный ответ
7. Окислительно-восстановительную двойственность проявляет вещество:
1) Na2S; 2) KMnO4, 3) NaNO2, 4) KClO4.
8. Элемент с электронной конфигурацией атома 1s22s22p63s23p64s23d104p5 :
1) Mn; 2) Se; 3) Br; 4) Kr.
9. При возрастании температуры от 298 оК до 338 оК скорость реакции при температурном коэффициенте Вант-Гоффа, равном 2
1) увеличится в 2 раза; 2) не изменится; 3) увеличится в 8 раз; 4) увеличится в 16 раз.
10. При н. у. 1 л любого газа содержит:
1)
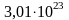 молекул;
2)
молекул;
2)
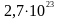 молекул;
молекул;
3)
 молекул;
4)
молекул;
4)
 молекул.
молекул.
11. Для комплексного соединения К2[MoF8] заряд комплексного иона, координационное число и степень окисления комплексообразователя имеют значения:
–1, 8, +7; 2) –2, 1, +6; 3) –2, 8, +6; 4) +2, 9, –6
12. Молярная масса вещества равна, если 0,75 г его в парообразном состоянии занимает объем 400 мл при 87 оС и давлении 96,8 кПа:
14; 2) 5,8; 3) 58; 4) 24.
13. Мольная концентрация раствора, содержащего сульфат алюминия массой 8 г в
воде массой 25 г, равна (плотность раствора принять равной единице)
0,52; 2) 0,71; 3) 0,65; 4) 0,48.
14. В реакции Сl2 + H2S + Н2O = НСl + Н2SO4 сумма коэффициентов равна:
1) 14; 2) 15; 3) 16; 4) 18
15. Масса меди, которая выделится при электролизе водного раствора сульфата меди(II) при силе тока 4 А в течение 1 часа, равна
1) 2,37 г; 2) 1, 34 г; 3) 4,78 г; 4) 3,25 г.
Задание № 2
Дополните
1. Отношение количества растворенного вещества (n1) к суммарному количеству всех компонентов раствора, то есть n1 + n2 (где n2 –количество растворителя), называется…
2.Величина, равная отношению средней массы молекулы естественного изотопического состава вещества к 1/12 массы 12С, называется…
3. Скорость химической реакции при постоянной температуре пропорциональна произведению концентраций реагирующих веществ в степени их стехиометрических коэффициентов – это формулировка закона…
4. Число лигандов в комплексном соединении, окружающих центральный ион, называется …
5. Элемент, находящийся в своей высшей степени окисления, в окислительно-восстановительных реакциях может выступать только …
6. Сумма всех протонов и нейтронов в ядре называется …
Выберите правильный ответ
7. При повышении давления в 5 раз скорость реакции образования йодоводорода из простых веществ возрастет:
1) в 5 раз; 2) в 10 раз; 3) в 25 раз; 4) в 125 раз.
8. Массовая доля раствора равна, если он получен смешением растворов массами 200 и 250 г с массовыми долями 10 и 40 % соответственно
1) 25,4 %; 2) 26,7 %; 3) 31,3 %; 4) 27,5 %.
9. Объем (н.у.) водорода, образующегося при прохождении тока 3 А в течение 1 часа через раствор KNO3, равен
1) 1,25 дм3; 2) 0,61 дм3; 3) 2,24 дм3; 4) 0,56 дм3.
10. Относительная плотность углекислого газа по воздуху составляет:
22; 2) 2,2; 3) 1,52; 4) 1,11.
11. Для комплексного соединения Na[Ag(NO2)2] заряд комплексного иона, координационное число и степень окисления комплексообразователя имеют значения:
+1, 2, –1; 2) +1, 1, –1; 3) –1, 2, +1; 4) –1, 1, –3
12. Из нитрата металла массой 1,1 г получили хлорид этого металла массой 0,93 г. Эквивалентная масса металла составляет:
109,5 г/моль; 2) 219 г/моль; 3) 108 г/моль; 4) 40 г/моль.
13. При электролизе водного раствора сульфата натрия на катоде протекает процесс:
1) 2H2O - 4e O2 + 4H+; 2) 2Na+ + 2e Na2O; 3) 2H2O + 2e H2 + 2OH-; 4) 2H+ + 2e H2O.
14) Число нейтронов в ядре изотопа 17О равно
1) 17; 2) 7; 3) 9; 4) 8
15) В реакции 2Pb(NO3)2 = 2PbO + 4NO2↑ + O2↑ окислителем является:
1) Pb(NO3)2; 2) PbO; 3) NO2; 4) O2
