
FTF 4 semestr / 10 - 11
.pdf
21
Лекция №3. Диены.
Алкадиенами называются ненасыщенные углеводороды, содержащие две двойные связи. Общая формула алкадиенов СnH2n-2. Изомерия диенов, подобна алкенам, обусловлена как строением углеводородного скелета, так и положением двойных связей. По этому признаку различают три типа диенов:
1.H2C-CH-(CH2)n-CH=CH2, n 1 - изолированные, в молекулах двойные связи разделены одним и более sp3-гибридизованными атомами углерода. Строение кратных связей в изолированных диенах практически не отличается от обычных алкенов. Их реакции ничем не отличаются от реакций алкенов с той лишь разницей, что в реакции могут вступать одна или две связи.
Пример: CH2=CH-CH2-CH2-CH=CH2 - гексадиен-1,5.
2.CH2=C=CH2 - кумулированные (1,2-диены), в молекулах которых двойные связи непосредственно примыкают друг к другу. Пример: CH2=C=CH2 - аллен (пропадиен). В кумулированных диенах орбитали двух π-связей расположены во взаимно перпендикулярных плоскостях. Центральный атом углерода находится в состоянии sp-гибридизации. Кумулированные диены менее стабильны, чем диены с сопряженными и изолированными кратными связями. При нагревании в щелочной среде они перегруппировываются в алкины.
3.CH2=CH-CH=CH2 - сопряженные (1,3 –диены), в молекулах которых двойные связи разделены одной одинарной связью. По своим химическим свойствам несколько отличаются от алкенов и важны с практической точки зрения.
Пример:
CH3
H2C
 CH2 H2C
CH2 H2C
 CH2
CH2
бутадиен-1,3 |
2-метилбутадиен-1,3 |
(дивинил) |
(изопрен) |
Изопреновый фрагмент часто встречается в структурах природных соединений (изопреноиды). Молекулы β-каротина, витамина А, холестерина содержат изопреновые фрагменты.
Наибольшее практическое значение имеют сопряженные диены, и именно они будут рассмотрены. 1,3-Диены отличаются рядом особенностей в своем химическом поведении, которое обусловлено их электронным строением.
CH2 CH CH CH2
В молекуле бутадиена-1,3 между атомами углерода имеются три σ-связи, образованные sр2-электронами, и две π-связи, образованные четырьмя р- электронам. При этом происходит перекрывание всех четырех р-орбиталей, т.е

22
образуется единое облако р-электронов, которое находится в плоскости, перпендикулярной плоскости σ-связей. Это взаимодействие двух π-связей получило название эффекта сопряжения.
В этом случае отдельные пары π-электронов не закреплены за определенными связями, а распределены (делокализованы) по всей молекуле.
Максимальная электронная плотность сосредоточена на атомах С1 и С2, С3 и С4 (рисунок), меньшая — между С2 и С3. Атомы С2 и С3, кроме σ-связи, как бы дополнительно связаны между собой. Вследствие взаимодействия сопряженных связей происходит выравнивание межъядерных расстояний. Длина связей между С1 и С2, С3 и С4 0,136 нм (длина С=С 0,134 им), длина связи С2 и С3 0,146 пм (длина С-С 0,154 пм).
Диены с сопряженной системой двойных связей более энергетически выгодны (более стабильны). Внутренняя энергия 1,3-диенов на 16,7 кДж/моль ниже по сравнению с соединениями с тем же числом атомов углерода и двойных связей, у которых этот эффект отсутствует. Все эти особенности строения 1,3-диенов и определяют их свойства.
р-Орбитали нескольких атомов могут перекрываться друг с другом, образуя общую π-электронную систему. Такой особый вид взаимного влияния атомов называется сопряжением.
Сопряжение - это образование в молекуле единого делокализованного электронного облака в результате перекрывания негибридизованных p-орбиталей.
Возможно два типа сопряжения:
а) π,π-сопряжение - делокализованные МО могут принадлежать двум или более π-связям.
H2C |
|
H2C |
|
|
CH3 |
H2C |
CH |
H2C |
N |
|
|
||||||||
CH2 |
|
|
CH2 |
||||||
|
|
|
|
|
|
||||
бутадиен-1,3 |
2-метилбутадиен-1,3 |
винилацетилен |
акрилонитрил |
||||||
(дивинил) |
(изопрен) |
|
|
|
|
||||
б) р,π- сопряжение-в сопряжении могут участвовать π-связи и соседний атом с р-орбиталью.

23
CH2=CH-Cl 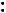

 CH2-CH=Cl
CH2-CH=Cl 
CH-CH-Cl
Метод резонанса - это описание молекулы с помощью нескольких формул (резонансных структур), при этом истинные структуры являются суперпозицией приведенных резонансных структур.
Сопряжение приводит к тому, что в молекуле другие длины связей (стремление к выравниванию). Молекулы с делокализованными связями имеют по сравнению с молекулами с изолированными связями, энергию.
Химические свойства.
Сопряженные диены - ненасыщенные соединения, для них характерны реакции электрофильного присоединения. Диены не только присоединяют различные вещества по одной из двойных связей (1,2-положению), но и по крайним атомам сопряженной системы 1,4-положению с перемещением двойной связи. Соотношение между ними в значительной степени зависит от условий эксперимента.
1.Присоединение галогенов. (Cl2, Br2; F2 - разрушает молекулу; I2 - дает неустойчивый аддукт).
H2C CH CH CH2 |
Br2 |
Br-CH2 CH CH CH2-Br |
|
Br-CH2 |
|
CH CH CH2 |
|
|
|||||
|
|
|||||
|
|
|
|
|
|
|
|
|
1,4-дибромбутен-2 |
|
Br 3,4-дибромбутен-1 |
||
Соотношение 1,2- и 1,4-продуктов зависит от строения диенового углеводорода, природы галогена и условий реакции. Термодинамически 1,4- аддукт более выгоден и поэтому преобладает. Выход продукта 1,4-присоединения возрастает при повышении температуры и при переходе от хлора к йоду.
2.Гидрогалогенирование. В реакциях присоединения НХ (НСl, НВr) действуют те же закономерности, что рассматривались выше.
H2C CH CH CH2 HBr 
 CH3 CH CH CH2 CH3 CH CH CH2
CH3 CH CH CH2 CH3 CH CH CH2
|
|
|
|
|
|
|
Br |
|
|
||||
|
|
|
CH3 |
CH CH CH2 |
|
CH3 CH CH CH2-Br |
|
|
|
||||
|
|
|
Br |
|
|
|
|
|
|
1,2-присоединение |
|
1,4-присоединение |
|

24
3. Гидрирование.
|
|
|
|
|
в момент выделения |
||
|
|
|
H2 Ni |
H2C CH CH CH2 |
H |
CH3 CH CH CH3 |
|
CH CH CH CH |
|
|
|||||
|
|
||||||
3 |
2 |
2 |
3 |
|
|
|
|
(сначала 1,2; 1,4; далее алканы) |
|
|
(1,4) |
||||
Для сравнения рассмотрим подобные реакции для диена с изолированными двойными связями.
|
|
HCl |
|
H3C |
CH CH2 CH2 CH CH2 |
|
|
|
|
||
|
|
|
|||
H2C CH CH2 CH2 CH CH2 |
|
|
|
Cl |
|
|
Br2 |
|
|
1 продукт |
|
|
|
|
H2C CH CH2 CH2 CH CH2 |
||
|
|
|
|
||
Br Br
4. Полимеризация.
Важнейшее свойство. Для диенов с сопряженными двойными связями особенно характерна способность под действием различных катализаторов (AlCl3, TiCl4 + (C2H5)3Al) или света, особенно УФ, а иногда и самопроизвольно полимеризоваться с образованием ВМС. Число мономерных звеньев изменяется от 2 до десятков тысяч.
Порядок соединения отдельных полимерных звеньев в принципе может быть:
|
|
1,4-1,4 |
H2C CH CH CH2 n |
|||
|
|
|
||||
|
|
1,2-1,2 |
||||
n H C CH CH CH |
|
CH |
CH |
|
||
|
|
n |
||||
|
||||||
2 |
2 |
|
2 |
|
||
|
|
|
|
|
CH=CH2 |
|
|
|
1,2-1,4 |
CH2 |
CH CH2-CH=CH-CH2 |
||
|
|
|
||||
|
|
|
|
|
|
n |
|
|
|
|
CH=CH2 |
||
В случае применения определенных катализаторов (TiCl4+Al(C2H5)3 - Циглера-Натто можно получить продукт полимеризации по положению 1,4-, причем с определенной конфигурацией цепей, а именно цис- (цис-конфигурацию имеет натуральный каучук). Макромолекулы натурального каучука имеют спиралевидную структуру цепи из-за того, что изопреновые звенья в них изогнуты, что создает пространственные препятствия упорядоченному расположению цепей. В каучуке длинные молекулы скручены в спутанные друг с другом спирали. При растяжении каучука спирали растягиваются, а при снятии растяжения они снова скручиваются.
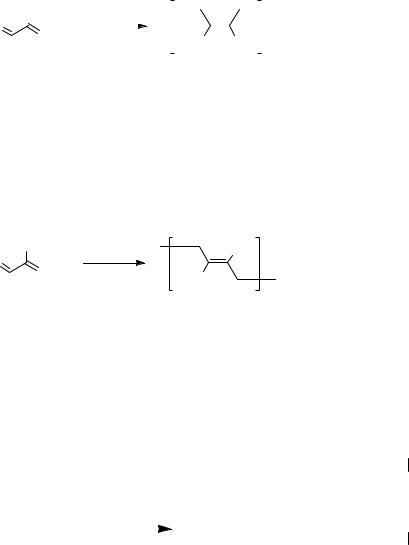
25
n H2C |
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C H |
|
n |
|||||||||
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
цис-1,4-полиизопрен |
||||||||||||
В природе существует другой полимер изопрена гуттаперча (транс- конфигурация), получаемая из сока деревьев семейства сапотовых. Гуттаперча обладает стержнеобразной структурой цепи из-за выпрямленности изопреновых звеньев (цепи с транс-конфигурацией двойных связей могут располагаться одна вдоль другой), - твердый, но хрупкий (плотно упакована полимерная цепь в объеме вещества).
n H2C |
CH3 |
|
H |
CH2 |
|
|
|
|
H3C |
n |
|
|
|
транс-1,4-полиизопрен
Натуральный каучук имеют немногие страны (получают из каучуконосных растений - гевеи). Остальные либо покупают натуральный каучук, либо заменяют его синтетическим. Большое значение имеют каучуки, которые получают при совместной полимеризации (сополимеризации) дивинила со стиролом (шинный каучук), а также с акрилонитрилом.
H2C CH CH CH2 + CH2=CH-C6H5  CH2-CH CH-CH2-CH2-CH
CH2-CH CH-CH2-CH2-CH
стирол |
|
бутадиенстирольный каучук C H |
|
|
6 |
5 |
|
H2C CH CH CH2 + CH2=CH-CN |
|
CH2-CH CH-CH2-CH2-CH |
|
|
|||
|
|
CN |
|
|
|
обладает масло- и бензоустойчивостью |
|
Каучук пластичный материал. Для того чтобы придать ему прочность, износоустойчивость, эластичность, стойкость к изменениям температуры, к действию растворителей его подвергают вулканизации нагреванием с серой или её соединениями (вулканизатор) в смеси с наполнителями (сажа, каолин, окись цинка, антиоксиданты и др.) В процессе вулканизации происходит «сшивание» линейных молекул каучука в ещё более крупные сетчатые (трёхмерные) молекулы и получается резина. Каучук и изделия из вулканизированного каучука (резины) играют огромную роль в технике и быту.
Методы получения важнейших диенов.
Способы получения углеводородов ряда дивинила в большинстве случаев не отличаются от способов получения алкенов. Только соответствующие реакции необходимо проводить дважды или в качестве исходного вещества применять соединения, уже содержащие двойную связь.

26
1.Дегидрирование. Дивинил, изопрен получают в промышленности из бутанобутиленовых или изопентан-изопентеновых фракций нефти.
CH CH CH CH |
|
+ CH -CH=CH-CH Cr2O3 Al2 |
O3 |
H C CH CH CH |
|
+ 3 H |
|
|||||||||||||||||||||||||
|
3 |
2 |
|
|
3 |
|
|
|
|
3 |
|
|
|
|
3 600-680 C |
|
2 |
|
|
|
2 |
|
2 |
|||||||||
|
|
|
бутано-бутиленовая фракция |
|
|
|
|
кат,t |
|
|
|
|
|
|
|
|
||||||||||||||||
CH CH CH CH CH C CH CH |
|
CH C CH CH |
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
3 |
|
|
|
|
|
|
3 |
|
|
2 |
|
|
|
2 3 |
-H2 |
|
2 |
|
|
|
2 |
|
|||||||||
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
CH3 |
|
CH3 |
изопрен |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
2. |
Гидрирование винилацетилена (над Fe, осторожно). |
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
HC CH |
|
|
|
|
|
|
|
H2 |
|
|
|
|
|
|
|
|
|||||||||
|
|
HC CH |
|
|
|
|
|
|
|
H2C CH C CH |
|
H2C CH CH CH2 |
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
CuCl2 |
|
Fe |
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
винилацетилен |
|
|
|
|
|
|
|
|
||||||||||||||||
3. |
Синтез дивинила по Лебедеву С.В. 1932 г. (выход невысок) |
|
|
|
|
|
||||||||||||||||||||||||||
2 C H OH |
MgO,ZnO |
|
|
H C CH CH CH + 2 H O + H |
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
2 |
|
|
|
|
|
|
|||||||||||||||||||||||
|
2 |
5 |
|
400-500 C |
2 |
|
|
|
2 |
|
2 |
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3CH2OH |
|
|
|
|
|
|
|
H3C |
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
-H2 |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
2 H3C C |
|
|
|
|
H3C |
H C |
|
|
|
O +H2 |
CH3-CH-CH2-CH2-OH |
|
|
|
дивинил |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
C |
C |
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
OH |
H |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
4. Дегидратация гликолей.
HO-CH2 CH2 CH2 CH2-OH H3PO4 H2C CH CH CH2
бутандиол-1,4
NaPO3
-H2O
5. Дегидрогалогенирование диагалогеналканов.
Cl-CH2 CH2 CH2 CH2-Cl |
|
2 KOH |
H2C CH CH CH2 |
+ 2 KCl + 2 H2O |
||
|
|
|
||||
спирт, t |
||||||
|
|
|
||||
