
- •Материаловедение
- •Рецензент:
- •Определение твёрдости материалов. Исследование влияния содержания углерода на твердость стали (Практическая работа)
- •Метод Бринелля
- •Метод Роквелла
- •1 Кристаллическая структура тел
- •2.7.5 Объяснить наличие зональной ликвации в строении стального слитка.
- •3 Макроструктурный и микроструктурный методы исследования металлов и сплавов (Практическая работа)
- •Макроанализ по виду излома
- •Макроанализ по макрошлифам
- •Выявление волокнистости
- •Выявление ликвации серы
- •Микроструктурный анализ
- •4 Построение диаграммы Sn–Pb с помощью метода термического анализа (Лабораторная работа)
- •5 Диаграммы двойных сплавов и их анализ
- •Углеродистых сталей и белого чугуна (Лабораторная работа)
- •Кривая охлаждения железа
- •Анализ диаграммы Fe – ц
- •Углеродистые стали
- •Белые чугуны
- •7 Структуры и свойства cepыx, ковких и высокопрочных чугунов (Практическая работа)
- •Серый чугун
- •Ковкий чугун
- •8 Закалка углеродистой стали. Влияние различных факторов на результаты закалки (Лабораторная работа)
- •Выбор температуры наг рева стали при закалке
- •Выбор времени нагрева и выдержки
- •Определение скорости охлаждения
- •9 Влияние температуры отпуска закаленной
- •10 Цементация стали
- •Термообработка после цементации
- •11 Микроструктура и свойства легированных сталей
- •Конструкционные легированные стали
- •Микроструктура конструкционных сталей
- •Инструментальные стали
- •12 Микроструктура цветных металлов и их сплавов (Лабораторная работа)
- •Медь и её сплавы
- •Материаловедение (Часть1) Практикум по лабораторным и практическим работам
- •350044, Г. Краснодар, ул. Калинина,13
1 Кристаллическая структура тел
(Лабораторная работа)
1.1 Цель работы
Изучить законы кристаллизации металлов и их сплавов.
2.2 Задание
2.2.1 Изучить справочные данные. Ознакомиться с устройством и работой прибо-ров, используемых в работе.
2.2.2 Провести эксперимент.
2.2.3 Написать отчёт.
2.3 Оборудование и материалы на рабочем месте
2.3.1 Биологический микроскоп.
2.3.2 Стеклянные пластинки.
2.3.3 Растворы NaCl различной концентрации.
2.3.4 Плакаты.
2.3.5 Излом слитка сурьмы.
2.4 План выполнения работы
2.4.1 Объяснить с помощью второго закона термодинамики механизм процесса кристаллизации.
2.4.2 Изобразить график изменения свободной энергии металла в зависимости от температуры нагрева.
2.4.3 Изобразить график зависимости образования числа центров (Ч.Ц.) и скорости роста кристаллов (С.К.) от изменения степени переохлаждения Т и объяснить, как Т влияет на величину зерна.
2.4.4 Зарисовать схему структуры капель насыщенного и ненасыщенного растворов NaCl и объяснить наблюдаемые различия.
2.4.5 Изобразить схему стального слитка и объяснить наличие его зональной ликвации.
2.4.6 Изобразить схему дендритного строения излома слитка сурьмы.
2.5 Справочные данные
Все металлы и металлические сплавы в твердом состоянии имеют кристаллическое строение, т.е. образуют кристаллическую решетку. В кристаллической решетке атомы за-нимают определенные места в пространстве, положение их упорядочено.
На основе многолетних исследований Д.К.Чернов установил, что процесс кристал-
13
лизации состоит из двух стадий:
– образование центров кристаллизации (зародышей);
– рост кристаллов вокруг этих центров.
Основной причиной и движущей силой процесса кристаллизации по закону термо-динамики является стремление вещества к наименьшему запасу свободной энергии, т.е.,
если свободная энергия жидкого металла |
G |
ж меньше свободной энергии выпавших кри- |
|
||
|
|
||||
сталлов |
G |
т в , то жидкое состояние – более устойчиво, идет процесс плавления. На рисун- |
|
||
|
|
||||
ке 2.1 представлена зависимость изменения |
G ж и G т в от температуры нагрева. |
|
|||

Рисунок 2.1 – Изменение запаса свободной энергии в зависимости
от температуры нагрева
Для развития процесса кристаллизации необходимо создать такие условия, при кото-рых свободная энергия твердой фазы будет меньше, чем у жидкой. Это наблюдается при переохлаждении сплава на величину Т, называемую степенью переохлаждения. Степень переохлаждения зависит от чистоты металла (чем чище сплав, тем больше Т), от скоро-сти охлаждения (чем она выше, тем больше Т).
где
0
кр
-
Т Т 0 Т кр ,
(2.1)
– теоретическая температура плавления;
– фактическая температура кристаллизации.
Степень переохлаждения влияет на образование числа центров кристаллизации (Ч.Ц.), на скорость роста зёрен (С.К.) и, как результат, на величину зерна в сплаве. Исследовани-ями установлено, что характер изменения параметров Ч.Ц. и С.К. в зависимости от степе-ни переохлаждения Т подчиняется закону нормального распределения. При равновесной температуре плавления ( Т 0 ), когда Т = 0 (рис. 2.2.), Ч.Ц. = 0 и С.К. = 0 процесс кристал-лизации не происходит.
14
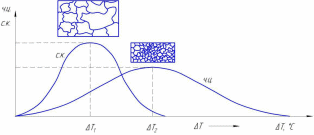
Рисунок 2.2 – Изменение Ч.Ц. и С.К. от степени переохлаждения
Если жидкий сплав переохладить на величину Т1 то число центров (Ч.Ц. – за-родышей) – невелико, а скорость роста кристаллов – максимальна, в сплаве получается крупнозернистая структура.
При степени переохлаждения Т2 число центров значительно выше, идёт массо-вая кристаллизация в итоге сплав приобретает мелкозернистую структуру. Схема за-рождения и роста кристаллов показана на рисунке 2.3.

Рисунок 2.3 – Схема зарождения и роста кристаллов, образование зёрен
Сначала кристаллы растут правильной формы, но на последней стадии в местах их соприкосновения правильная внешняя форма нарушается. Получившиеся кристаллы неправильной форма называются зернами.
Механизм зарождения зерна и процесс кристаллизации металлов очень сходны с процессами, протекающими при кристаллизации раствора солей. Так как жидкости про-зрачны, то можно пронаблюдать и изучить механизм зарождения кристаллов в них, по-явление осей первого, затем второго порядка и использовать эту информацию при рас-смотрении процесса кристаллизации в металлах и их сплавах. Для исследования исполь-зуют растворы солей NaCl 2 , хлористого аммония NH 4 Cl различной концентрации.
Обычно кристаллизация капли раствора соли начинается у краев, т.к. раствори-тель здесь испаряется быстрее, раствор перенасыщается. Это способствует зарождению большого числа центров кристаллизации и получению мелкого зерна.
растворе малой концентрации в следующей зоне испарение воды замедляется, зародышей образуется немного, и оси первого порядка растут большие, направление их
15
роста – от края к центру. В центральной части направление осей хаотично, в целом по-лучается крупнозернистая структура (рисунок 2.4 а).
Если рассматривать кристаллизацию перенасыщенного раствора, то можно наблюдать, как в капле сразу образуется много зародышей по всей площади. Оси пер-вого порядка не успевают вырасти, как процесс кристаллизации уже заканчивается. Получается мелкозернистая структура (рисунок 2.4 б).

Рисунок 2.4 – Схема строения капли: а – ненасыщенного раствора,
б – перенасыщенного раствора
Из вышесказанного можно сделать вывод, что, создавая искусственные центры кристаллизации, меняя скорость охлаждения, можно регулировать величину зерна в металлических сплавах.
Строение стального слитка по Д.К. Чернову
производственных условиях сталь заливается в вертикальную чугунную форму (изложницу) с холодными стенками. Рассматривая сечение стального слитка, Д.К. Чер-нов выявил, что кристаллическое строение его меняется как по высоте, так и от перифе-рии к центру. В отливке образуются три структурные зоны (рисунок 2.5).
Там, где жидкий сплав контактирует с изложницей, степень переохлаждения ве-лика, следовательно, в этой зоне образуется много зародышей и получается мелкозерни-стая структура (зона 1). В следующей зоне 2 охлаждение идет медленнее, Ч.Ц. уменьша-ется, рост осей первого порядка идет в направлении противоположном отводу тепла.
На них формируются оси второго порядка, т.е. образуются столбчатые кристаллы, напоминающие форму дерева – «дендриты» (дендрон – по-гречески дерево). В неболь-ших отливках в металлические формы при заливке перегретого металла зона столбчатых кристаллов может занять все сечение вплоть до центра, это нежелательно.
Скорость охлаждения центральной части замедляется, что характеризуется
уменьшением величины Т. Теплоотвод в разные стороны слитка – почти одинаков. Все это способствует образованию крупных зерен с различной ориентацией осей кристаллов (зона 3).
В верхней части слитка из–за усадки металла образуется усадочная раковина 4. В нижней (донной) части слитка собираются примеси. Перед обработкой давлением ниж-нюю и верхнюю часть с усадочной раковиной отделяют и отправляют на переплав.
При рассмотрении сечения стального слитка обнаруживается явление зональной ликвации (ликвация – неоднородность).
16

Рисунок 2.5 – Схема строения стального слитка спокойной стали
2.6 Содержание отчёта
отчёт следует записать: цель работы, записать законы кристаллизации, зари-совать структуры капель насыщенного и ненасыщенного растворов NaCl, стального слитка, схему дендритного строения излома слитка сурьмы, выводы.
2.7 Вопросы для контроля
2.7.1 Объяснить механизм зарождения и роста кристаллов.
2.7.2 Объяснить механизм процесса кристаллизации, применяя второй закон термодинамики.
2.7.3 Как зависят Ч.Ц. и С.К. от степени переохлаждения Т?
2.7.4 Описать механизм кристаллизации насыщенного и ненасыщенного растворов соли.
