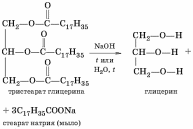
- •Аминокислоты с неполярными r-группами
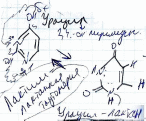
- •Отличия днк и рнк
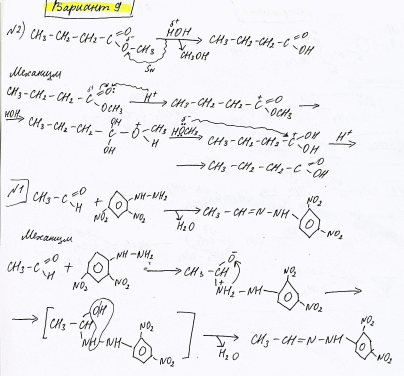
- •2) Образование гидразона этаналя
- •Вариант 3
- •Билет 4
- •Фруктаны, маннаны, Пектиновые вещества – пищевые волокна фруктов, овощей
- •Пептиды:
- •6) Представление о желчных кислотах и их функциях:
- •Вариант 7
- •Вариант 8
- •Роль пептидов в организме:
- •Физико-хим свойства нк:
- •Вариант 9
- •Билет 10
- •3) Ф изи ко -х имич ес кие с во йст ва бел ко в
- •Роль белков в организме
- •2)Гидролиз никотинамида
Вариант 9
Структурная организация белковой молекулы
Первичная структура
Это последовательность (порядок чередования) аминокислот в полипептидной цепи
Связи, стабилизирующие эту структуру – пептидные
Форма – зигзагообразная цепь
Вторичная структура
Это регулярное (закономерное) расположение полипептидной цепи в пространстве
Связи, стабилизирующие эту структуру – водородные между пептидными группами
Форма: α-спираль или β-складчатый лист или спираль коллагена
Тетичная структура
Это дальнейший специфический способ укладки полипептидной цепи в пространстве
Связи, стабилизирующие эту структуру – водородные между боковыми R-группами аминокислот (это отличает третичную структуру от вторичной)
–Ионные
–Гидрофобные взаимодействия
–Дисульфидные (наиболее прочные)
Форма – клубок (глобула) или нить (фибрилла).
Четвертичная структура
Некоторые белки собираются в олигомерный комплекс из нескольких субъединиц (протомеров) с помощью
нековалентных связей.
Пространственное расположение субъединиц в олигомерном белке – это и есть 4-ая структура. Субъединичная (или четвертичная) структура очень важна для аллостерической регуляции ферментов, а также регуляции экспрессии генов.
Конформация – это форма молекулы, определяемая ее вторичной и третичной структурой. Не является жесткой и зависит от наличия кофакторов в окруж. среде.
Домен – фрагмент ПП-цепи, сходный по своим свойствам с самостоятельным глобулярным белком. Домен автономен, но вместе с другими доменами в данном белке нацелен на
выполнение одной задачи.

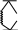 HO
*
H O
HO
*
H O
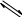
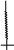 O CH
O CH
H
H * OH
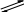
 O
H
O
H
фуранозный цикл
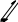

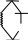 H OH
H OH
O
 HO H
HO H
*
O H * OH
пиранозный цикл
5) Мальтоза относится к дисахаридам типа гликозидо-глюкоз и составлена из двух остатков а-D- глюкопиранозы, соединенных гликозидной связью в положениях 1,4. Связь такого типа называют а-1,4- гликозидной связью. Мальтозу получают при гидролитическом расщеплении крахмала с помощью специфического фермента, которым очень богаты прорастающие зерна ячменя
6) Липиды – это гидрофобные органические соединения природного происхождения, не растворяются в воде, но растворяются в органических растворителях (спирт, эфир, бензол, толуол и т.д.).
Биологическая классификация(основана на функциях липидов):
Липиды делятся на: жиры (энергетическая ф-ция), липоиды (мембранная), биологически активные вещества
(регуляторная).
Липиды делятся на:
Омыляемые (содержат сложно-эфирную связь): они в свою очередь делятся на простые и сложные
Простые (два компонента)- жиры, стериды, воски, твины
Сложные (более двух компонентов) – фосфодипиды (содержат ФК) и гликолипиды (не содержат ФК, но содержат У).
Неомыляемые (не содержат сложно-эфирную связь).
Билет 10
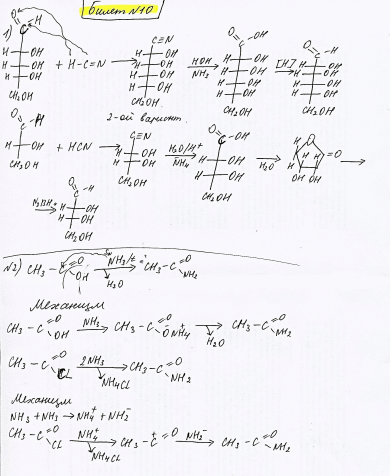
3) Ф изи ко -х имич ес кие с во йст ва бел ко в
Набухаемость (ограниченная и неограниченная)
Растворимость в воде (касается только тех белков, у которых на поверхность выступают гидрофильные группы)
Осаждаемость (или коагуляция) Электрофоретическая подвижность Буферное действие
Лиофилизация Изоэлектрическая точка
Оса ждение бел ко в
Высаливание – осаждение без нарушения структуры белка: путём отнятия гидратной оболочки и
 нейтрализации
заряда
на
поверхности
с
помощью
солей
щелочных
и
щелочно-земельных
металлов,
а
также
сернокислого
аммония
нейтрализации
заряда
на
поверхности
с
помощью
солей
щелочных
и
щелочно-земельных
металлов,
а
также
сернокислого
аммония
Денатурация – разрушение всех структур белка, кроме первичной.
Денатурирующие факторы:
высокие температуры
УФ и ионизирующее излучение
встряска
кислоты и щелочи
соли тяжелых металлов
спирт, ацетон при длительном воздействии