
- •Содержание
- •Примерный тематический план практических занятий
- •1 Основные понятия и определения термодинамики. Идеальный газ
- •1.1 Примеры решения задач
- •1.2 Задачи для самостоятельного решения
- •2 Анализ процессов идеальных газов
- •2.1 Примеры решения задач
- •2.2 Задачи для самостоятельного решения
- •3 Второй закон термодинамики
- •4 Реальные газы и пары
- •4.1 Примеры решения задач
- •4.2 Задачи для самостоятельного решения
- •5 Течение, истечение и нагнетание газов и паров
- •5.1 Примеры решения задач
- •5.2 Задачи для самостоятельного решения
- •6 Газовые циклы
- •6.1 Примеры решения задач
- •6.2 Задачи для самостоятельного решения
- •7 Паровые циклы
- •7.1 Примеры решения задач
- •7.2 Задачи для самостоятельного решения
- •8 Теплопроводность, закон Фурье. Теплопровоность плоских и цилиндрических стенок
- •8.1.Примеры решения задач
- •8.2 Задачи для самостоятельного решения
- •9 Подобие и моделирование процессов конвективного теплообмена
- •9.1 Примеры решения задач
- •9.2 Задачи для самостоятельного решения
- •10 Теплоотдача при свободном движении жидкости
- •10.1 Примеры решения задач
- •10.2 Задачи для самостоятельного решения
- •11 Теплообмен при вынужденном движении
- •11.1 Примеры решения задач
- •11.2 Задачи для самостоятельного решения
- •12 Теплообмен излучением
- •12.1 Примеры решения задач
- •12.2 Задачи для самостоятельного решения
- •13 Сложный теплооб мен
- •13.1 Примеры решения задач
- •13.2 Задачи для самостоятельного решения
- •14 Теплообменные аппараты
- •14.1 Примеры решения задач
- •14.2 Задачи для самостоятельного решения
- •Список использованной и рекомендуемой литературы
1.2 Задачи для самостоятельного решения
Задача 1.2.1 Определить абсолютное давление в паровом котле, если манометр показывает 0,25 МПа, а атмосферное давление по ртутному барометру составляет 700 мм рт. ст. при температуре 20 °С.
Ответ:
![]() =
0,343 МПа.
=
0,343 МПа.
Задача 1.2.2 В баллоне емкостью 60 л находится водород при давлении 5 МПа в температуре 30 °С. Определить массу газа в баллоне.
Ответ:
![]() = 0,24 кг.
= 0,24 кг.
Задача 1.2.3 Масса воздуха, заключенного между крышкой цилиндра и поршнем компрессора, равна 0,5 кг. Диаметр цилиндра 0,5 м, давление и температура внутри цилиндра 0,35 МПа и 400 К соответственно. При неизменном давлении движущийся без трения поршень перемещается на 20 см.
Определить начальное расстояние поршня от крышки цилиндра и температуру в цилиндре после перемещения поршня.
Ответ:
Х=0,64 м;
![]() =
495 К;
=
495 К;
![]() 305
К.
305
К.
Задача 1.2.4
Объемный состав сухих продуктов сгорания
органического топлива следующий:
![]() 12,3 % ;
12,3 % ;
![]() 7,2 %;
7,2 %;
![]() = 80,5 %.
= 80,5 %.
Найти молярную массу к газовую постоянную смеси, а также плотность и удельный объем продуктов сгорания при давлении 100 кПа и температуре 800 °С
Ответ:
![]() 30,3
кг/кмоль;
=
274 кДж/кг-К;
30,3
кг/кмоль;
=
274 кДж/кг-К;
![]() =0,34
кг/м3
;
=0,34
кг/м3
;
![]() 2,94 м3/кг.
2,94 м3/кг.
Задача 1.2.5
Объемные доли компонентов влажного
воздуха: кислорода
21 %, азота
![]() - 78,1 % ; водяного пара
- 78,1 % ; водяного пара
![]() - 0,9 %. Определить массовые доли,
парциальные давления компонентов
воздуха при давлении смеси 0,1 МПа, газовую
постоянную воздуха и его плотность
при нормальных условиях.
- 0,9 %. Определить массовые доли,
парциальные давления компонентов
воздуха при давлении смеси 0,1 МПа, газовую
постоянную воздуха и его плотность
при нормальных условиях.
Ответ:![]() ;
;![]() ;
;![]() ;
;![]() кПа;
кПа;
![]() кПа;
кПа;![]() кПа;
=
289 кДж/кг·К;
кПа;
=
289 кДж/кг·К;![]() кг/м3
кг/м3
Задача 1.2.6 Какое
количество теплоты необходимо подвести
к воздуху в закрытом сосуде объемом
![]() м3,
если начальная температура t1
=100 оС
, давление
м3,
если начальная температура t1
=100 оС
, давление
![]() =
300 кПа, а конечная температура t2
=500 оС?
Определить также массу воздуха и конечное
давление. Зависимость теплоемкости от
температуры считать нелинейной.
=
300 кПа, а конечная температура t2
=500 оС?
Определить также массу воздуха и конечное
давление. Зависимость теплоемкости от
температуры считать нелинейной.
Ответ:
![]() = 1,4 кг;
= 1,4 кг;
![]() =
412 кДж;
=
412 кДж;
![]() = 623 кПа.
= 623 кПа.
2 Анализ процессов идеальных газов
2.1 Примеры решения задач
Задача
2.1.1 Воздух
массой 10 кг расширяется изотермически
при
![]() оС
от
начального давления
=
800 кПа
до конечного объема
оС
от
начального давления
=
800 кПа
до конечного объема
![]() = 5 м3.
Определить
начальный объем, конечное давление,
работу расширения, теплоту процесса,
изменение энтропии, энтальпии и внутренней
энергии.
= 5 м3.
Определить
начальный объем, конечное давление,
работу расширения, теплоту процесса,
изменение энтропии, энтальпии и внутренней
энергии.
Решение. Начальный объем определяем из уравнения состояния для кг газа:
![]() м3.
м3.
Конечное давление определяем из соотношения параметров в изотермическом процессе:
![]() , (2.1)
, (2.1)
тогда:
![]() кПа
кПа
Работу расширения в изотермическом процессе определяем по формуле:
![]() . (2.2)
. (2.2)
После подстановки данных имеем:
![]() кДж.
кДж.
В
изотермическом процессе вся теплота
расходуется на совершение работы,
поэтому в данном случае
![]() кДж.
кДж.
Изменение энтропии в изотермическом процессе находим по формуле:
![]() , (2.3)
, (2.3)
тогда
![]() кДж/кг·К.
кДж/кг·К.
Энтальпия
и внутренняя энергия идеального газа
в изотермическом процессе не изменяются,
таким образом,
![]() и
и
![]() .
.
Ответ:
![]() м3;
м3;
![]() кПа;
кДж;
кПа;
кДж;
![]() кДж/кг·К;
и
.
кДж/кг·К;
и
.
Задача 2.1.2 В изохорном процессе температура газа массой m с начальным давлением p1 изменяется от t1 до t2. Затем газ адиабатно расширяется.
Определить температуру, давление, удельный объем в конце адиабатного расширения и суммарную работу процессов, если температуры рабочего тела в точках один и три равны. Представить процессы в vр- и sT-диаграммах.
Дано: m = 2,0 кг, p1 =0,1 МПа, t1 = 19оС, t2 =66оС, ср = 1,0458 кДж/кг∙К,
газ-кислород,
![]() =259,8
кДж/кг∙К.
=259,8
кДж/кг∙К.
Решение
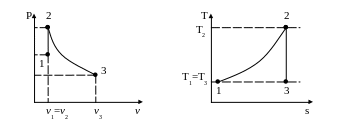
Определим параметры в точках 1-3.
Точка 1.
![]() ;
;
![]()
![]() м3/кг;
м3/кг;
Точка 2.
![]() К.
К.
![]() =0,63
м3/кг;
=0,63
м3/кг;
![]() .
.
Точка 3.
![]() К.
К.
 ;
;
![]() - показатель адиабаты
- показатель адиабаты

![]() кДж/кг∙К.
кДж/кг∙К.
![]() .
.
 кПа
кПа
Суммарная работа процессов:
![]()
![]() т.к
т.к
![]() .
.
В адиабатном процессе 2-3:
![]() ;
;
![]() кДж/кг.
кДж/кг.
![]() кДж/кг.
кДж/кг.
![]() кДж.
кДж.
Ответ:
![]() К;
К;
![]() кПа;
кПа;
![]() 31,3
кДж/кг;
31,3
кДж/кг;
![]() кДж.
кДж.
