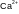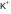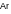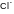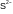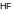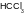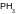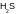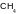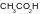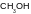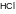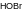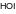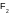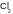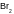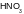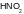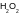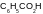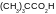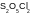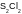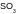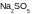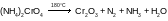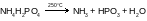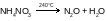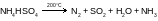9кл олимп17
.docxЗадания I этапа республиканской олимпиады по химии
2017/2018
9 класс
Часть А. Тестовое задание (Выберите 1 правильный ответ)
1. Тот факт, что почти вся масса атома сосредоточена в ядре, установил:
Эйнштейн
Дальтон
Бор
Резерфорд
Беккерель
2. Расположите следующие типы радиации в порядке увеличения их проникающей способности:
α,γ,β
β,α,γ
α,β,γ
β,γ,α
γ,β,α
3. Частица с наибольшим радиусом:
A |
|
B |
|
C |
|
D |
|
E |
|
4. Какое вещество образует наиболее прочные водородные связи:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5. Какое выражение концентрации соответствует 0,01 % (по массе) раствору глюкозы:
1,0 ppb
100 ppm
10 ppt
1,1 ppt
1,0 %
6. Наибольшую электрическую проводимость имеет 0,001 М раствор:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7. Наиболее сильная кислота Бренстеда в водном растворе:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8. Соединения, используемые в качестве первичных стандартов, обладают большой эквивалентной массой, т.к.:
такие соединения, как правило, легче очистить
такие соединения обычно гигроскопичны
реагируют, как правило, в стехиометрии 1:1
большие соединения содержат, как правило, меньше воды на поверхности
ошибка взвешивания минимальна
9. Увеличение температуры кипения является результатом увеличения от фтора к иоду:
|
°С |
|
-187,9 |
|
-34,0 |
|
+58,5 |
|
+184,5 |
ионных связей
силы ковалентных связей
сродства к электрону
сил Ван-дер-Ваальса
ядерного квадрупольного момента
10. Верно для элемента ксенон:
не образует химических соединений
существует в виде двухатомных молекул
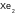
первый потенциал ионизации меньше чем для Na
имеет большое число органометаллических соединений
образует соединения с некоторыми электроотрицательными элементами
11. Залежи, богатые бором, появились на Земле при осаждении из водного раствора. Форма существования бора в них:
элементная форма
сульфид
оксид или гидроксид
диборан
нитрид бора
12. Взаимодействие диоксида азота с водой приводит к:
|
|
только
|
|
|
только
|
|
|
и
|
|
|
и
|
|
|
и
|
13. Наиболее сильная кислота из приведенных:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
14. Соотнесите название сплава и его качественный состав:
|
|
дуралюмин |
|
Cu, Sn |
|
|
латунь |
|
Cu, Zn |
|
|
мельхиор |
|
Cu, Al |
|
|
нихром |
|
Cu, Ni |
|
|
оловянная бронза |
|
Cr, Ni |
15. Соотнесите степень окисления серы и формулу соединения, в состав которого она входит:
|
|
-2 |
|
|
|
|
+1 |
|
|
|
|
+2 |
|
|
|
|
+4 |
|
|
|
|
+6 |
|
|
|
|
|
|
Часть Б. Практическое задание
Задание 1
Для описания газообразного состояния вещества используется уравнение состояния – зависимость давления от температуры и объема. Одним из таких уравнений является уравнение состояния идеального газа (уравнение Менделеева-Клапейрона):
 ,
,
где
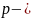 давление;
давление;
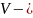 объем;
объем;
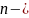 химическое
количество, моль;
химическое
количество, моль;
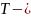 абсолютная
температура, К (T(К)=
tºС+273,15);
абсолютная
температура, К (T(К)=
tºС+273,15);
 универсальная
газовая постоянная (
универсальная
газовая постоянная ( ).
).
исходя из приведенного выше уравнения состояния, установите верные утверждения:
при постоянном давлении изменение объема газа прямо пропорционально температуре
при постоянном давлении изменение объема газа обратно пропорционально температуре
при постоянной температуре объем данного количества газа обратно пропорционален давлению, под которым он находится
при постоянной температуре объем данного количества газа прямо пропорционален давлению, под которым он находится
установите, во сколько раз изменится объем газа при увеличении температуры с 20ºС до 100 ºС, если одновременно уменьшить давление в 2 раза;
газовая смесь состоит из метана ( ) и пропана (
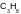 ).
Отношение числа атомов углерода и
водорода равно 9:28. Рассчитайте плотность
(г/л) данной газовой смеси при 20 ºС и
давлении 101325 Па.
).
Отношение числа атомов углерода и
водорода равно 9:28. Рассчитайте плотность
(г/л) данной газовой смеси при 20 ºС и
давлении 101325 Па.
Задание 2
Из 140 г образца, содержащего 64,0 % серы по массе, было получено 600 г кристаллогидрата состава Na2SO4 · xH2O. Выход кристаллогидрата составил 80,0 % от теоретически возможного.
установите точную формулу кристаллогидрата и приведите его название;
в дистиллированной воде растворили 5,36 г данного кристаллогидрата. От полученного раствора, объемом 100 мл, отобрали аликвоту 40,0 мл и в ней дополнительно растворили 0,67 г кристаллогидрата. Рассчитайте массу осадка, которая образуется при добавлении к полученному раствору избытка хлорида стронция.
Задание 3
Дана
смесь калиевых солей:
 .
В данной смеси содержится (элементный
состав) 4,29 г калия, 0,16 г водорода и 4,0 г
кислорода.
.
В данной смеси содержится (элементный
состав) 4,29 г калия, 0,16 г водорода и 4,0 г
кислорода.
приведите структурные формулы кислот, соответствующие каждой соли и названия солей;
рассчитайте массу смеси и массовые доли каждой соли в ней.
Задание 4
Ниже приведены схемы реакций разложения солей аммония.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
укажите название каждой соли;
расставьте коэффициенты в каждом случае.
9 КЛАСС
ПРАКТИЧЕСКИЙ ТУР
Материалы и оборудование:
№ |
наименование |
количество |
1 |
пронумерованные пробирки с растворами |
4 |
2 |
чистые пробирки |
4 |
3 |
стеклянная палочка |
1 |
4 |
промывалка с дистиллированной водой |
1 (на 4 человека) |
5 |
химический стакан (500 мл) |
1 (на 4 человека) |
Примечание: 4 и 5 в случае отсутствия раковины в аудитории
ЗАДАНИЕ
В пронумерованных пробирках содержатся 10 %-ные водные растворы следующих веществ:
хлорид бария
сульфат меди (II)
хлорид натрия
карбонат натрия
Используя только выданные Вам растворы, установите содержимое каждой из пробирок.
Приведите схему определения и уравнения химических реакций, с указанием аналитических эффектов (цвет, осадок, etc).