
- •Пм 02. «Эксплуатация нефтегазопромыслового оборудования»
- •21.02.01 «Разработка и эксплуатация нефтяных и газовых месторождений»
- •Содержание
- •Мдк 02.01 Эксплуатация нефтегазопромыслового оборудования
- •Термодинамика. Методические указания к выполнению контрольной работы.
- •Задачи 11 –20
- •Задачи 21-30
- •Задачи 31-40
- •Задачи 41-50
- •Примеры решения задач
- •Задача № 1
- •Задача №2
- •Задача №3
- •Задача №4
- •Задача №5
- •Задачи № 22 и 27
- •Задачи № 23 и 28
- •Задачи № 24 и 29
- •Задача № 25 и 30
- •Задачи №31-40
- •Задачи № 41-50
- •Приложения
- •2. Контрольная работа № 2
- •Техническая механика.
- •Методические указания
- •К выполнению контрольной работы.
- •Задачи для контрольной работы 3
- •3. Контрольная работа № 3
- •Нефтегазопромысловое оборудование.
- •Методические указания для выполнения контрольной работы № 3.
- •Общие указания к выполнению контрольной работы
- •4. Контрольная работа № 4 Нефтегазопромысловое оборудование.
- •Общие указания к выполнению контрольной работы.
- •5.Контрольная работа № 5
- •Оборудование прс
- •Методические указания к выполнению
- •Контрольной работы
- •Задача №1 Выбор агрегата для ремонта скважин оборудованных шсну
- •Задача №2
- •Задача №3 Выбор оснастки талевой системы при проведении ловильных работ
- •Контрольные вопросы
- •6.Контрольная работа № 6 Электрооборудование промыслов. Методические указания к выполнению контрольной работы
- •Контрольные задания и типовые задачи с решениями Задача 1
- •Задача 2.
- •Выбор варианта
- •Контрольные задания по двигателям постоянного тока Таблица 2
- •Задача 1.
- •Задача 2.
Примеры решения задач
Пример №1
0,5 м3 сернистого газа (SO2) при начальном давлении 0,2 МПа и начальной температуре 27oС, адиабатно сжимается до давления 2 Мпа. Считая зависимость теплоемкости от температуры линейной, определить конечную температуру, конечный объем, изменение внутренней энергии газа и работу затраченную на сжатие.
Д ано:
V1=
0,5 м3
ано:
V1=
0,5 м3
Р1 = 0.2 Мпа
t1 =27 C
P2 = 2 Мпа
Газ- S02
 T2-
?; V2
-
?
T2-
?; V2
-
?
U- ? L- ?
Решение:
1.Определяем удельную газовую постоянную серниcтого газа (SO2)
![]()
2.Из уравнения состояния идеального газа : P1* V 1= M*R*T1
определяем массу газа участвующего в процессе
M=P1*V 1/R*T1=0 .2* 106 * 0 5/129 .9* 300= 2.5 кг.
3.Для адиабатного процесса справедливо соотношение;
![]()
Здесь к = 1.3. коэффициент Пуассона для 3-х атомных газов, откуда
определяем конечную температуру газа
Т2 =Т1*(Р1/ Р2) к -1/к =300* (2 /0.2)1..3-1/1..3.=513 К
t2 =513-273= 240 0 C
4. По таблице приложения (1) интерполируя, определяем истинные удельные, изохорные массовые теплоемкости SO2 при t1 = 27 C и t 2= 240 C
![]() ;
;
![]()
5. Определяем среднюю удельную изохорную, массовую теплоемкость сернистого газа в процессе
![]()
6.Определяем изменение внутренней энергии в адиабатном ( впрочем как и во всех других элементарных процессах)
![]() U=
Cv
cp*
(T2
- T1)*
М= 0.501* (513-300)*
2.5 = 266.78 кДж
U=
Cv
cp*
(T2
- T1)*
М= 0.501* (513-300)*
2.5 = 266.78 кДж
7. Из соотношения давления и объема в адиабатном процессе
(Р1/Р2)=(V2/V1)к ;
определяем конечный объем газа :
V2 =V1* (Р1/Р2)1/к =0.5*(0.2/2)1/1.3 = 0.0831 м3 ;
или для проверки определим конечный объем из уравнения состояния:
Р2* V2= М*R*Т2.
V2=М*R*T2/Р2=2.5* 129.9* 513 /2*106 =0.0832 м3
Расхождение результатов составляет всего 0.0001,что допустимо.
8.Определим работу, совершенную в процессе:
L=
(R/K-1)*(T1-T2)*
М=
(129.9/1.3.-1)*
(300-513)*2.5=230572.5
Дж
![]() -230.6 кДж знак (-)в результате, показывает,
что работа была затрачена.
-230.6 кДж знак (-)в результате, показывает,
что работа была затрачена.
Ответ:T2=513 K, V2=0.0831 м3, U=266.78 кДж, L=230.6 кДж
Пример № 2
Какое количество теплоты необходимо затратить. чтобы нагреть 2 м3 воздуха при постоянном давлении Р=0.2 Мпа от 1000 С до 5000 С?. Какую работу при этом совершит воздух? Теплоемкость воздуха считать постоянной
Дано: V1=2м2 Р= 0.2 Мпа t1= 100C t2= 500C Р=const Решение: 1.Определяем удельную газовую постоянную воздуха:
R=8314/ 2.Из уравнения состояния:Р* V1=M* R* T1 определяем массу воздуха, участвующего в процессе М=Р*V1 / R*T1=0.2*106*2 / 286.7*373=3.7.кг 3.Работа,совершенная газом в изобарном процессе,определяется по формуле:L=R*(Т2-T1)*M= 286,7*(773-373)*3.7=424316 Дж 4.Т.к. по условию задачи теплоемкость можно считать постоянной, то определим ее по уравнению Майера. Изохорная массовая удельная теплоемкость воздуха: Cv=R/(K-1) , где K=1.4.- коэффиент Пуассона в данном случае для 2-х атомных газов, т. к воздух представляет собой смесь в основном 2-х атомных газов N2 и О2. Т.к. по определению коэффициент Пуассона К = Ср/Сv то изобарная массовая удельная теплоемкость воздуха Ср=К*Сv=K* R/(K-1)= 1.4*286.7/(1.4-1)=1003,45 Дж/ кг*к 5.Тепло, подведенное к газу в изобарном процессе: Q=Cp*(T2-T1)*M=(1003/45)*(773-373)*3.7=1485106 Дж Ответ: Q= 1485,1 кДж L= 424.3 кДж |
Пример № 3
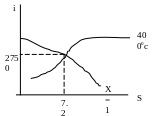
Определить энтальпию и энтропию сухого насыщенного газа при температуре 400 0С
Дано: t= 400C X= 1 I -? S- ? Решение: Задача решается при помощи i- S диаграммы. Точка характеризующая заданное состояние пара находится на пересечении изотермы 400 0С и линии сухости х=0. Опустив из этой точки перпендикуляры на оси , i и S считываем результаты i = 2750 к/Дж/кг; S =7.2 кДж/кг |
Пример № 4
Водяной пар имеет давление 0.2. Мпа и сухость Х=0.85. Какое количество тепла следует затратить, чтобы 7 кг этого пара нагреть до 800 0 С, при постоянном давлении. Какова при этом будет плотность пара?
Дано: t2 = 800 С P=0.2. Мпа Х1 = 0.85 М =7 кг Q-? й ?
|
Решение: Начальное состояние пара характеризуется точкой 1, на пересечении изобары 0.2. Мпа и линии сухости Х=0.85. Опустив из этой точки перпендикуляр на ось i. Определяем удельную энтальпию начального состояния пара i1 = 2400 кДж/кг. Окончание процесса подвода тепла будет характеризоваться точкой 2 на пересечении изобары 0.2 Мпа (процесс изобарный ) и изотермы 8000 С. Опустив из точки 2 перпендикуляра на ось i . Находим удельную энтальпию пара в конечном состоянии i2 = 3550 к Дж/кг. Определяем количество затраченного тепла Q=(i2- i1)*M= (3550-2400)*=8050 к/Дж/кг
Д |
Пример № 5
Для
идеального цикла поршневого двигателя
внутреннего сгорания с подводом тепла
при V
= const,
определить параметры рабочего тела в
характерных точках, полученную работу,
термический К.П.Д., количество подведенной
и отведенной теплоты, если известно:
P1=
0.1 MПа,
t1=20
С, =
3.6. ,
![]() =3.33
=3.33
Рабочим телом считать воздух. Теплоемкость считать постоянной.
t1= 20 С P1= 0.1. МПа = 3.6. = 3.33 газ- воздух Решение: Схематично Р-U диаграмма предложенного в задании цикла будет иметь вид:
|
На схеме процессы: 1-2- адиабатное сжатие рабочего тела 2-3- изохорный подвод тепла, 3-4 – адиабатное расширение, 4-1 –изохорный отвод тепла.
Расчет ведем для 1 кг. воздуха
1.Определяем параметры состояния в характерных точках
Точка 1. Р1 = Мпа; t1=20C- по уловию задачи. Из уравнения состояния
P1*V1 = R*T1 определяем удельный объем V1=R* T1/ P1 здесь
R=8314/ =8314/29= 287 Дж/кг*к, Т1 =20+273= 293 К
U2= 287*293/0.1*106=0.84 кг/м3
Точка 2.Т.к. степень сжатия = V1/V2=3/6,то V2= V1/ =0.84/3.6=0.233 м3/ кг
Для адиабатного процесса 1-2 соотношения между температурами и объемами:
Т2 /Т1= ( v1 / v 2) К-1; где К- коэффициент Пуассона для 2-х атомных газов
( воздух- это смесь в основном 2-х атомных газов)
Откуда температура Т2=Т1* ( v 1 / v2)К-1= 293* (0.84/0.233) 1,4-1= 489 К
.t2 = 489.273= 216С
Из уравня состояния Р2* V2 =R*T2 определим давление
Р2= R*T2/V2=287*489/0.233=600000 Па= 0.6 Мпа
Точка 3. Удельный объем v 3 = v2= 0.233 м3/ кг- процесс 2-3 изохорный. Степень повышения давления = P3/ P2 – по определению. Откуда давление Р3= *Р2=3.33*0.6 = 2 Мпа
Для изохорного процесса 2-3 соотношение между давлениями и температурами:
Р3/Р2 =Т3/Т2., откуда Т3 =Т2* Р3/ Р2 =Т2* =489*3.33= 1628 К;
t 3=1628 –273=1355 C
Точка 4.Удельный объем v4 = v1 =0/84 м3/кг - процесс 4-1 изохорный. В адиабатном процессе 3-4 справедливо соотношение Т4 =Т3* (v 3 / v4) К-1; откуда
Т4 =Т3*( v3/ v4) К-1= Т3* ( v2 /v1)К-1 =Т3*(1/) К-1 =1628/3.6 0.4 =976 К
В изохорном процессе 4-1 справедливо соотношение
Р4/Р1 =Т4 /Т1; откуда Р4=Р1*Т4 /Т1 =0.1*97/6/293=0.33 Мпа
2.Количество подведенного тепла в изохорном процессе 2-3 q1 = Cv*(Т3-Т 2)
здесь: Сv – изохорная массовая удельная теплоемкость
Сv = R/(K-1)= 287/(1/4-1)= 717.5 Дж/кг*к; q1= 717.5*(1628-489) = 82500 Дж/кг
3.Количество отведенного тепла в изохорном процессе 4-1
q2=Cv*(T 4-T1)=717.5*(976-293)=495000Дж/кг= 495 кДж/кг
4.Работа,
полученная в цикле:
![]() = q
1
–q
2
= 825-495 = 330 Кдж
= q
1
–q
2
= 825-495 = 330 Кдж
5.К.П.Д.
цикла (термический)
![]() q1
=330/825 = 0.4
q1
=330/825 = 0.4
Для проверки определим К.П.Д. по другой формуле:
![]() к-1)
= 1- (1/3.61.4.-1)=0.4
к-1)
= 1- (1/3.61.4.-1)=0.4
Пример № 6
Кирпичная стенка имеет толщину 40 см. Одна поверхность стенки имеет температуру 20 С, другая – 20 С. Принимая коэффициент теплопроводности стенки = 0.6 Вт/м* к. Определить плотность теплового потока в стенке и термическое сопротивление стенки.
Дано:
t1 = 20C
t 2 = -20 C
![]() 0.6
Вт/м*
к
0.6
Вт/м*
к
![]() 40
см.
40
см.
Решение:
Для решения используем закон теплопроводности (Фурье) т.е плотность теплового потока
q
=
*
(t
1
–t
2)/![]() =0.6*(20-(-20))/0.4=60
(Вт/м2)
=0.6*(20-(-20))/0.4=60
(Вт/м2)
Термическое
сопротивление стенки R=
![]() 0/667
(м2к/Вт)
0/667
(м2к/Вт)
В качестве проверки определим
q=(t1 - t2)/ R = (20 –(20))/0.667=60 ( Вт/м2)
м2 к/Вт
q- ? R- ?
Пример № 7
Поверхность стенки площадью 4 м2 омывается водой с температурой 70 0С. Определить тепловой поток от воды к поверхности стенки, если последняя имеет температуру 680С. Коэффициент теплоотдачи от воды к стенке принять = 90 Вт/м2*к
Дано: t1= 200C 90 Вт/м2*к t2 =68 0C F= 4м2
|
Решение:
Согласно
закону теплоотдачи (Ньютона-Рихмана)
тепловой поток Q= |
Q-?
Пример № 8
Трехслойная стенка разделяет потоки дымовых газов и воды. Температура дымовых газов 750 0 С, температура воды 900С. Толщина каждого слоя стенки
![]() 5мм;
2
= 3 мм;
3
= 10 мм.
5мм;
2
= 3 мм;
3
= 10 мм.
Коэффициенты теплопроводности каждого слоя соответственно: 1 =0.8 Вт/м*к; 2=40 Вт/м* к ; 3= 0.5 Вт/м*к. Коэффициент теплоотдачи от газов к поверхности стенки 1 =500 Вт/м2*к, от поверхности стенки к воде 2 =900 Вт/м2*к. Расчетная поверхность теплопередачи составляет 2 м2. Определить тепловой поток от газов к стенке.

Дано: t1= 750 0C t2=900 C 1=5мм 1=0.8 Вт/м* к 2 =3 мм 2=40Вт/м*к 3 =10 мм 3=0.5 Вт/м*к 1 =500 Вт/м2* к 2=900 Вт/м2* к
|
Решение: 1.Определим термическое сопротивление стенки R=R1+R2+R3= 1/ 1 + 2/ 3+ 3/ 3; R=0.005/08+0.003/40+0.01/05=0.263(м2* к/Вт) 2Определим коэффициент теплопередачи К=1/(1/ 1 +R +1/ 2)= 1/(1.500+0.0263+1.900)= 34( Вт/м2к) 3. Тепловой поток : Q = К*(t1- t 2)* F= 34* (750-90)*2=44880 Вт |
Q - ?
Пример № 9
Малосернистый мазут М-100 имеет следующий элементарный состав в расчете на рабочую массу:
С р =85.2% ;Н р =10.2%; О р =0.4%; N р =0.4%; S рR%= 0,5%; Ар =0,3%; wp=3%
Определить элементарный состав мазута в расчете на сухую массу
Решение:
1.Определяем пересчетный коэффициент для пересчета рабочей массы топлива в сухую
К=100/(100-wp) =100/(100-3)=1.031
2.Определяем элементарный состав топлива в расчете на сухую массу.
С =К* Ср =1.031*85.2= 87.84%
Нс =К* Нр =1.031*10.2=10.52%
Ос =К* Ор =1.031* 0.4= 0.41%
Nc= К* N p=1.031*0.4 =0.41%
Sc=К*Sp %=1.031*0.5.= 0.54%
Ас =К*А р =1.031*0.3= 0.31%
Проверка: Сс+Нс+Ос+Nс+Sс+Ас= 87.84+10.52+0.41+0.54+ 0.31 =100.02%
Отклонение составляет 0.02% что в пределах округлений
Пример № 10
Определить теоретический удельный расход воздуха для сжигания 1 кг топлива. Элементарный состав топлива в расчете на рабочую массу принять по условию примера № 9
Решение:
Теоретический удельный расход воздуха определяется по формуле:
L т = 0.115* Ср +0.345*Нр +0.043*( Sр – Oр ) =
= 0.115*85.2 +0.345*10.2+0.043*(0.5-0.4)=13.4 кг/кг
Таблица к выбору задач контрольной работы
Последняя цифра шифра |
|||||||||||
Предпоследняя цифра шифра |
|
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
0 |
1.11 |
2.12 |
3.13. |
4.14 |
5.15 |
6.16 |
7.17 |
8.18 |
9.19 |
10.20 |
|
|
21.32 |
22.33 |
23.34 |
24.35 |
25.36 |
26.37 |
27.32 |
39.28 |
29.40 |
30.31 |
|
|
43.51 |
44.52 |
45.53 |
46.54 |
47.55 |
48.56 |
49.57 |
50.58 |
41.59 |
42.60 |
|
1 |
2.12 |
3.13. |
4.14 |
5.15 |
6.16 |
7.17 |
8.18 |
9.19 |
10.20 |
1.11 |
|
|
23.31 |
24.32 |
25.33 |
26.34 |
27.35 |
28.36 |
29.37 |
30.38 |
21.39 |
22.40 |
|
|
42.70 |
43.69 |
44.68 |
45.67 |
46.66 |
47.65 |
48.64 |
49.63 |
50.62 |
41.61 |
|
2 |
3.14 |
4.15 |
5.16 |
6.17 |
7.18 |
8.19 |
9.20 |
10.11 |
1.12 |
2.13 |
|
|
22.33 |
23.34 |
24.35 |
25.36 |
26.37 |
27.38 |
28.39 |
29.40 |
30.31 |
21.32 |
|
|
41.71 |
42.72 |
43.75 |
44.74 |
45.75 |
46.76 |
47.77 |
48.78 |
49.79 |
50.80 |
|
3 |
4.13 |
5.14 |
6.15 |
7.16 |
8.17 |
9.18 |
10.19 |
1.20 |
2.11 |
3.12 |
|
|
25.35 |
26.36 |
27.37 |
28.38 |
29.39 |
30.40 |
21.31 |
22.32 |
23.33 |
24.34 |
|
|
44.60 |
45.59 |
46.58 |
47.57 |
48.56 |
49.55 |
50.54 |
41.53 |
42.52 |
43.51 |
|
4 |
5.16 |
6.17 |
7.18 |
8.19 |
9.20 |
10.11 |
1.12 |
2.13 |
3.14 |
4.15 |
|
|
24.34 |
25.35 |
26.36 |
27.37 |
28.38 |
29.39 |
30.40 |
21.31 |
22.32 |
23.33 |
|
|
45.61 |
46.62 |
47.63 |
48.64 |
49.65 |
50.66 |
41.67 |
42.68 |
43.69 |
44.70 |
|
5 |
6.15 |
7.16 |
8.17 |
9.18 |
10.19 |
1.20 |
2.11 |
3.12 |
4.13 |
5.14 |
|
|
27.36 |
28.37 |
29.38 |
30.39 |
21.40 |
22.31 |
23.32 |
24.33 |
25.34 |
26.35 |
|
|
48.80 |
49.79 |
50.78 |
41.77 |
42.72 |
43.75 |
44.74 |
45.73 |
46.72 |
47.71 |
|
6 |
7.18 |
8.19 |
9.20 |
10.11 |
1.13 |
2.12 |
3.14 |
4.16 |
5.15 |
6.17 |
|
|
26.35 |
27.36 |
28.37 |
29.38 |
30.39 |
21.40 |
22.31 |
23.32 |
24.33 |
25.34 |
|
|
47.51 |
48.52 |
49.53 |
50.54 |
41.55 |
42.56 |
43.57 |
44.58 |
45.59 |
46.60 |
|
7 |
8.17 |
9.18 |
10.19 |
1.20 |
2.11 |
3.12 |
4.13 |
5.14 |
6.15 |
7.16 |
|
|
28.37 |
29.38 |
30.39 |
21.40 |
22.31 |
23.32 |
24.33 |
25.34 |
26.35 |
27.36 |
|
|
46.70 |
47.69 |
48.68 |
49.67 |
50.66 |
41.65 |
42.64 |
43.63 |
44.62 |
45.61 |
|
8 |
9.18 |
10.12 |
1.13 |
2.11 |
3.15 |
4.14 |
5.17 |
6.16 |
7.19 |
8.18 |
|
|
30.39 |
21.40 |
22.31 |
23.32 |
24.33 |
25.34 |
26.35 |
27.36 |
28.37 |
29.38 |
|
|
49.71 |
50.72 |
41.73 |
42.74 |
43.75 |
44.76 |
45.77 |
46.78 |
47.79 |
48.80 |
|
9 |
10.20 |
1.19 |
2.11 |
3.12 |
4.13 |
5.14 |
6.15 |
7.16 |
8.17 |
9.18 |
|
|
29.38 |
30.39 |
21.40 |
22.31 |
23.32 |
24.33 |
25.34 |
26.35 |
27.36 |
28.37 |
|
|
50.60 |
41.59 |
42.58 |
43.57 |
44.56 |
45.55 |
46.54 |
47.53 |
48.52 |
49.51 |
|

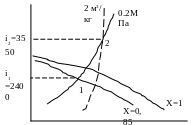 ля
определения плотности пара в конечном
состоянии выясним, какая пунктирная
линия проходит через точку 2.Это будет
величина удельного объема V=
2м3/кг.
Следовательно, плотность пара P=
1/V
= ½=0.5. кг/м3
ля
определения плотности пара в конечном
состоянии выясним, какая пунктирная
линия проходит через точку 2.Это будет
величина удельного объема V=
2м3/кг.
Следовательно, плотность пара P=
1/V
= ½=0.5. кг/м3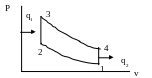 Дано:
Дано: