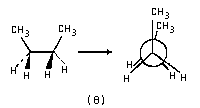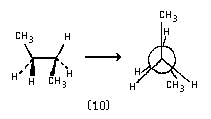- •I. Элементы симметрии.
- •Центр симметрии (центр инверсии),I
- •Плоскость симметрии
- •Простая ось симметрии n-го порядка Cn
- •Зеркально-поворотная ось симметрии n - ого порядка Sn.
- •П. Способы изображения пространственного строения молекул
- •1. Клиновидная проекция.
- •2.Конформации. Формулы Ньюмена.
- •Ш. Хиральность. Молекулы с одним асимметрическим атомом.
- •1. Энантиомеры. Асимметрический атом
- •2.Абсолютная конфигурация
- •3.Проекционные формулы Фишера
- •1.Принципы r,s-номенклатуры
- •2.Определение порядка старшинства сложных заместителей при асимметрическом атоме
- •V.Оптическая активность. Рацематы.
- •VI.Молекулы с двумя асимметрическими атомами. Диастереомеры.
- •VII Относительная конфигурация. Эритро-трео-обозначения.
- •VIII Методы Разделения энантиомеров.
- •Метод Пастера.
- •Расщепление через диастереомерные соли .
- •Биохимический метод.
- •IX. Стереоизомерия алкенов.
- •X. Дополнительные сведения. 1.Особенности изображения циклических молекул
- •2.Конформационная энантиомерия
- •3. Проекции Фишера и для молекул с тремя и более асимметрическими атомами.
- •Амино и гидроксикислоты
- •5.Хиральные молекулы без асимметрических атомов
- •6.К правилу последовательности в r,s - номенклатуре.
2.Конформации. Формулы Ньюмена.
Атомы углерода в алканах находятся в sp3 -гибридном состоянии. Следовательно, связь С-С образуется за счёт перекрывания двух sp3 гибридных орбиталей вдоль их общей оси:

Характерная особенность ![]() связи
- ее аксиальная (осевая) симметрия. При
повороте вокруг оси симметрии С
на
любой угол, изображенный на рисунке
фрагмент молекулы совпадает сам с собой.
Следствие аксиальной симметрии
связи
- возможность вращения групп групп СН3 в
молекуле этана друг относительно друга.
При этом не изменяется степень перекрывания
двух sp3-гибридных орбиталей, то
есть не нарушается
связь
С-С. Описанное вращение действительно
происходит (за счет энергии теплового
движения молекул).
связи
- ее аксиальная (осевая) симметрия. При
повороте вокруг оси симметрии С
на
любой угол, изображенный на рисунке
фрагмент молекулы совпадает сам с собой.
Следствие аксиальной симметрии
связи
- возможность вращения групп групп СН3 в
молекуле этана друг относительно друга.
При этом не изменяется степень перекрывания
двух sp3-гибридных орбиталей, то
есть не нарушается
связь
С-С. Описанное вращение действительно
происходит (за счет энергии теплового
движения молекул).
Рассмотрим молекулу этана (2). Повернем в ней правую СН3- группу относительно левой - на 60° (один из атомов водорода выделен):

Формы молекулы этана (2) и (4) представляют собой лишь две из бесконечно большого числа всевозможных форм , возникающих при вращении одной из СН3-групп относительно другой. Эти формы, различающиеся взаимным расположением атомов в молекуле, называются конформациями.
КОНФОРМАЦИЯМИ называются различные геометрические (пространственные) формы, которые молекула может принимать в результате вращения вокруг простых связей и других внутримолекулярных движений, проходящих без разрыва химических связей. |
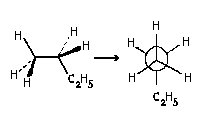
Для изображения конформации удобны проекции, предложенные в 1955 г. М.Ньюменом. Посмотрим на молекулу этана вдоль оси C-C-связи со стороны одной из метильных групп. При этом задний атом углерода закроется "передним" ("передние" атомы Н выделены):

Мы получим еще одну проекцию (5) молекулы этана на плоскость. Изобразим в этой проекции удаленный от нас атом углерода окружностью, а близкий к нам атом углерода - точкой пересечения его связей. Тогда все связи С-Н мы можем нарисовать сплошными линиями, и проекция (5) преобразуется в (6):
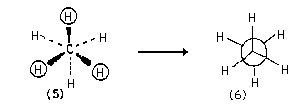
Проекция (6) и является формулой Ньюмена молекулы этана в конформации (2).
При попытке изобразить формулу Ньюмена, соответствующую конформации (4), мы столкнемся с тем, что "передние" атомы водорода заслоняют "задние". Для того, чтобы в формуле Ньюмена были видны все атомы водорода, слегка повернем "задний" атом углерода относительно "переднего" так, что бы атомы водорода, связанные с ним, выглядывали из-за "передних":
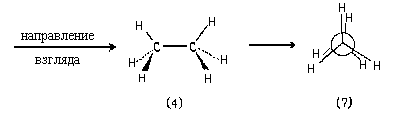
В конформации, изображеннойй формулой
(7), атомы водорода "передней"
и, "задней" CH3-групп расположены
ближе друг к другу, чем в конформации,
соответствующей формуле (6). Поэтому
отталкивание между электронами "передних"
и "задних" связей С-Н в случае (7)
сильнее, чем в случае (6). Принято говорить,
что в конформации (7) имеется напряжение.
Энергия отталкивания электронов двух
связей С-Н зависит от величины двугранного
угла ![]() :
:
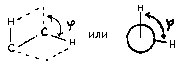
Этот угол называется торсионным (torsion angle) - угол кручения (англ.), а напряжение, зависящее от величины угла f - торсионным напряжением. Для молекулы этана зависимость энергии напряжения от величины торсионного угла выглядит следующим образом:
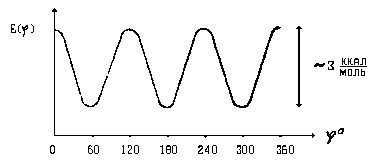
Максимумы на этой кривой соотвотствуют конформации (С7), которая называется заслоненной. Минимум соответствует конформации (6), которая называется заторможенной.
Если в молекуле есть несколько -связей С-С с различным окружением, то формулы Ньюмена изображают относительно каждой такой связи. Так, формулы Ньюмена для молекулы бутана, можно построить относительно связи С1-С2 и относительно связи С2-С3 :
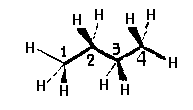
Проекции относительно связи С3-С4будут идентичны проекциям, построенным относительно связи С1-С2так как окружение этих связей одинаково. Формулы Ньюмена изображают обычно для таких конформаций молекул, у которых значения торсионного угла кратны 60°.
Проекция относительно связи С1-С2:
|
|
заторможенная конформация |
заслоненная конформация |
Проекции относительно связи С2-С3:
|
|
Заслоненная, или цисоидная конформация |
скошенная, или гош-конформация |
|
|
частично заслоненная конформация |
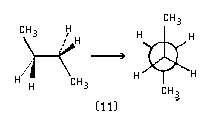
заторможенная, или трансоидная конформация |
При рассмотрения молекулы бутана вдоль связи С2-С3 помимо упомянутых выше заслоненной и заторможенной конформаций, появились еще две конформации (9) и (10). Им также соответствуют минимумы и максимумы на кривой зависимости энергии напряжения от величины торсионного угла (угол отсчитывается от заслоненной кокформации 8):
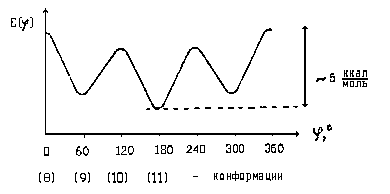
О частично заслоненной и гош-конформации имеет смысл говорить только тогда, когда у каждого из атомов углерода, образующих данную С-С-связь, по крайней мере, один из заместителей отличен от двух других. Поэтому об этих конформациях не идет речь в случае молекулы этана., а также бутана при рассмотрении его вдоль связи С1-С2.
Разница в энергиях напряжения заслоненной (8) и заторможенной (II) конформации бутана значительно превышает разницу в энергиях аналогичных конформаций молекулы этана (5 и 3 ккал/моль, соответственно). Такое различие вызвано тем, что CH3-группы по размерам больше атомов водорода. Поэтому CH3-группам молекулы бутана сложнее расположиться рядом (конформация 8), чем двум атомам водорода молекулы этана (конформация 7).
Поскольку молекула в разных конформациях обладает разной энергией, при данной температуре имеется различная заселенность конформаций. Заселенными оказываются конформации, отвечающие минимумам энергии. Такие конформации называются конформерами (в более строгом определении комформера говорится о множестве близких конформаций в окрестностях потенциального минимума). Конформации, отвечающие максимумам энергии, не заселены. Их следует рассматривать как переходные состояния в процессе превращения одного конформера в другой. Во многих случаях наиболее заселенной оказывается заторможенная конформация, в которой торсионное напряжение минимально, например:
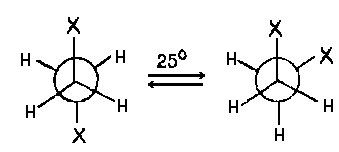
заторможенная гош
X- СН3 |
66% |
34% |
X- CI |
70% |
30% |
X- Вг |
89% |
11% |
Но в ряде случаев в силу дополнительных внутримолекулярных взаимодействий более заселенной может оказаться гош-конформация.
|
|
|