
- •Патофизиология Учебник
- •Минск 2015
- •Предисловие
- •Список сокращений
- •Авторский коллектив
- •Введение
- •Предмет, задачи, методы и разделы патофизиологии
- •Краткая историческая справка развития патофизиологии
- •Часть I. Общая нозология
- •Глава 1. Общее учение о болезни
- •1.1. Здоровье и болезнь
- •Принципы классификации болезней
- •Периоды развития болезни
- •1.2. Патологические и защитно-приспособительные реакции организма
- •Адаптация и компенсация
- •Структурные основы и механизмы компенсации
- •Глава 2. Общая этиология
- •Глава 3. Общий патогенез
- •Глава 4. Роль реактивности организма в развитии патологии
- •Виды реактивности и их характеристика
- •Взаимоотношение между реактивностью и резистентностью
- •Эволюция реактивности и резистентности
- •Факторы, снижающие неспецифическую резистентность организма. Пути и методы её повышения и укрепления
- •Глава 5. Конституция человека и ее роль в развитии патологии
- •О трактовке понятия «конституция»
- •Конституция человека и патология
- •Диатезы
- •Глава 6. Роль наследственности в патологии
- •6.1 Понятие о врожденной и наследственной патологии
- •6.2 Классификация наследственных форм патологии
- •6.3 Этиология и патогенез наследственных форм патологии. Мутации, их виды. Антимутагенез
- •Механизмы действия антимутагенов
- •6.4. Генные болезни. Этиология, классификация, патогенез, клинические проявления
- •Патогенез генных болезней
- •6.5 Хромосомные болезни. Этиология, классификация, патогенез, клинические проявления
- •Клинико-цитогенетическая характеристика синдромов, связанных с числовыми аномалиями аутосом
- •Клинико-цитогенетическая характеристика синдромов, связанных со структурными перестройками хромосом
- •6.6 Методы профилактики наследственной патологии и принципы ее терапии
- •Глава 7. Особенности патологии внутриутробного развития организма
- •7.1. Общая этиология и патогенез. Основные проявления патологии внутриутробного развития
- •Факторы, оказывающие патогенное воздействие на материнский организм и плод
- •Общий патогенез и основные проявления патологии внутриутробного развития
- •7.2 Профилактика внутриутробных повреждений
- •Глава 8. Роль возраста в развитии патологии
- •8.1. Старение. Причины и механизмы старения
- •Общие закономерности процесса старения
- •Виды старения, факторы, влияющие на его темп
- •Причины и механизмы старения. Изменения в организме при старении
- •Изменения в организме при старении
- •Изменения на системном уровне
- •Старение и болезни
- •8.2 Особенности течения и проявления болезни в пожилом и старческом возрасте
- •8.3 Прогерия. Пути увеличения продолжительности жизни
- •Пути увеличения продолжительности жизни
- •Глава 9. Патофизиология иммунной системы
- •9.1. Общая характеристика иммунологической реактивности и закономерности ее нарушений
- •Общие закономерности нарушений иммунологической реактивности
- •9.2 Иммунодефициты и принципы их терапии
- •Общие принципы терапии иммунодефицитов
- •9.3. Аллергия. Типы аллергических реакций и принципы их терапии
- •Значение наследственной предрасположенности
- •Принципы терапии аллергии
- •Патологическая толерантность
- •Реакция «трансплантат против хозяина»
- •9.4 Аутоиммунные заболевания и принципы их терапии
- •Теория расстройства иммунологической регуляции
- •Теория нарушения идиотип-антиидиотипических взаимодействий
- •Принципы терапии аутоиммунных заболеваний
- •Глава 10. Патофизиология клетки
- •10.1 Причины нарушения функционирования и повреждения клетки
- •10.2 Общие механизмы и основные проявления повреждения клетки
- •Основные проявления повреждения клетки
- •Специфические и неспецифические изменения при повреждении клеток
- •10.3 Механизмы компенсации при повреждении
- •10.4 Типы клеточной гибели в организме
- •Механизм и стадии апоптоза
- •Возможности терапевтического регулирования аппоптоза
- •10.5 Общие реакции организма на повреждение
- •10.5.1 Ответ острой фазы
- •10.5.2 Шок: виды, патогенез, клинические проявления
- •10.5.3 Коллапс: виды, патогенез, клинические проявления
- •10.5.4 Кома: виды, патогенез, клинические проявления
- •10.6 Принципы повышения устойчивости клеток к действию повреждающих факторов и патогенетической терапии
- •Глава 11. Патогенное влияние факторов окружающей среды на организм человека
- •11.1 Повреждающее действие электрического тока
- •11.1.1 Особенности электрического тока как повреждающего фактора. Факторы определяющие тяжесть электротравмы
- •Факторы, определяющие тяжесть электротравмы
- •11.1.2. Патогенез, проявления и последствия действия электрического тока
- •Поражения от разрядов атмосферного электричества (молнии)
- •11.1.3 Принципы профилактики, оказание первой медицинской помощи и терапии при электротравме
- •11.2. Повреждающее действие ионизирующих излучений
- •11.2.1. Общая характеристика. Патогенез лучевых повреждений
- •Патогенез лучевых повреждений
- •11.2.2 Лучевая болезнь человека: острая и хроническая лучевая болезнь
- •Защитно-приспособительные реакции и процессы восстановления в облученном организме
- •11.2.3. Отдалённые последствия лучевого воздействия
- •11.2.4 Принципы профилактики и терапии лучевых повреждений
- •11.3 Патогенное влияние температурного фактора на организм
- •11.3.1 Общее перегревание организма (гипертермия)
- •11.3.2 Общее переохлаждение организма (гипотермия)
- •Принципы терапии и профилактики гипотермических состояний
- •Глава 12. Смерть и принципы оживления организма
- •12.1. Общая характеристика смерти
- •12.2. Оживление организма
- •12.3. Постреанимационная болезнь
- •Глава 13. Лечебные принципы в медицине. Их научные основы
- •13.1. Краткая характеристика становления и формирования научной клинической медицины
- •13.2. Современные принципы терапии в медицине
- •13.3. Общая стратегия современной терапии
- •Часть II. Типовые патологические процессы
- •Глава 14. Патофизиология регионального кровообращения и микроциркуляции
- •14.1 Артериальная гиперемия: виды, причины, механизмы развития, проявления
- •14.2 Венозная гиперемия: причины, механизмы развития, проявления
- •14.3. Ишемия: причины, механизмы развития, проявления
- •14.4 Стаз: виды, причины, механизмы развития, проявления
- •14.5 Тромбоз и эмболия как факторы нарушения регионального кровообращения
- •14.5.1 Тромбоз: причины, механизмы, виды тромбов
- •14.5.2 Эмболия: виды, причины, механизмы развития
- •14.6 Расстройства микроциркуляции: формы нарушений, причины, механизмы развития
- •14.7 Принципы терапии расстройств регионального кровообращения и микроциркуляции
- •Глава 15. Воспаление
- •15.1. Определение понятия и общая характеристика
- •15.2. Общая этиология и основные клинические проявления
- •Основные клинические признаки
- •15.3. Общий патогенез
- •Сосудистые реакции. Экссудация плазмы, эмиграция форменных элементов крови и фагоцитоз
- •Просвет капилляра
- •Псевлоподия лейкоцита
- •Пролиферация и исходы воспаления
- •Роль нервной, эндокринной и иммунной систем в патогенезе воспаления
- •15.4. Течение воспаления. Острое и хроническое воспаление
- •15.5. Виды воспаления
- •15.6. Теории воспаления
- •15.7. Значение воспаления для организма
- •15.8. Принципы терапии воспаления
- •Глава 16. Лихорадка
- •16.1. Определение понятия и общая характеристика
- •16.2. Общая этиология
- •16.3. Общий патогенез
- •Стадии лихорадки. Изменение теплообмена
- •Изменения обмена веществ и функций внутренних органов при лихорадке
- •16.4. Разновидности лихорадки. Типы температурных кривых
- •Гипертермии, имеющие черты сходства с лихорадкой
- •16.5. Биологическое значение лихорадки. Пиротерапия
- •16.6. Принципы жаропонижающей терапии
- •Глава 17. Инфекционный процесс
- •17.1. Определение понятия. Основные виды инфекционного процесса
- •Основные виды инфекционного процесса
- •Факторы защиты микроорганизмов
- •17.3. Общий патогенез
- •Механизмы защиты макроорганизма
- •Периоды течения инфекционного процесса
- •17.4. Принципы терапии инфекционного процесса и инфекционной болезни
- •Глава 18. Типовые нарушения обмена веществ
- •18.1. Нарушения белкового, углеводного и липидного обмена
- •18.1.1. Нарушения обмена белков
- •18.1.2. Нарушение обмена нуклеиновых кислот
- •18.1.3. Нарушения обмена углеводов
- •Клинические проявления гипергликемии
- •Гексоземии
- •18.1.4. Нарушение обмена липидов
- •Нарушение межуточного обмена липидов
- •18.1.5 Сахарный диабет
- •Сахарный диабет 1 типа
- •Сахарный диабет 2 типа
- •18.1.6. Принципы коррекции и терапии нарушений белкового, углеводного и липидного обмена
- •18.1.7. Алиментарная недостаточность. Голодание
- •Лечение голоданием
- •18.2. Нарушения водно-электролитного обмена
- •18.2.1. Общая характеристика водно-электролитного обмена
- •18.2.2. Типовые формы нарушения водного и электролитного обмена, их коррекция
- •18.2.3. Отеки: классификация, этиология и патогенез, принципы терапии
- •Последствия отека для организма
- •Принципы терапии отеков
- •18.3. Нарушения кислотно-основного состояния организма
- •18.3.1. Механизмы поддержания кислотно-основного состояния организма
- •Физиологические механизмы поддержания кос
- •Показатели кос организма и их значение
- •Классификация нарушений кос организма
- •Критерии оценки нарушений кислотно-основного состояния организма
- •18.3.2 . Ацидозы и алкалозы: причины, механизмы развития и компенсации, принципы их коррекции
- •Сдвиги и компенсаторные реакции при нарушениях кос
- •Глава 19. Гипоксия
- •19.1. Определение понятия и общая характеристика
- •19.2. Общая этиология
- •19.3. Общий патогенез
- •Механизмы гипоксического некробиоза
- •19.4. Компенсаторно-приспособительные реакции организма при гипоксии
- •19.5. Принципы профилактики и терапии гипоксических состояний
- •Глава 20. Опухоли
- •20.1. Определение понятия, виды опухолей и их характеристика
- •Классификация опухолей
- •Биологические особенности злокачественных опухолей
- •Методы экспериментальной онкологии
- •20.2. Этиология опухолей
- •20.3. Молекулярно-генетические механизмы канцерогенеза
- •20.4. Взаимодействие опухоли и организма. Маркеры злокачественного роста. Антибластомная резистентность
- •Маркеры опухоли, антибластомная резистентность
- •20.5. Предраковые состояния
- •20.6. Принципы профилактики и терапии опухолей
- •Часть ш. Патофизиология органов и систем
- •Глава 21 Патофизиология системы крови
- •21.1 Введение
- •21.2 Патофизиология системы эритрона
- •21.2.1 Критерии оценки нарушений в системе эритрона
- •21.2.2. Типовые формы патологии и реактивных изменений системы эритрона
- •21.2.2.1 Эритроцитозы. Виды. Общая характеристика. Принципы терапии
- •21.2.2.2 Анемии. Виды. Общая характеристика. Принципы терапии
- •21.3 Патофизиология системы лейкона
- •21.3.1 Качественные и количественные изменения лейкоцитов
- •21.3.2 Типовые формы нарушений в системе лейкона
- •21.3.2.1 Лейкоцитозы и их характеристика
- •21.3.2.2 Лейкопении и их характеристика. Агранулоцитоз. Панмиелофтиз
- •21.3.2.3 Лейкемоидные реакции и их характеристика
- •21.3.2.4 Типовые изменения лейкоцитарной формулы
- •21.3.3 Принципы терапии патологии белой крови
- •21.4. Гемобластозы. Лейкозы
- •21.4.1. Общая характеристика, принципы классификации
- •Принципы классификации лейкозов
- •Отдельные виды хронических лимфолейкозов
- •21.4.2. Острые лейкозы. Особенности течения и патогенеза клинических проявлений острых лейкозов
- •21.4.2.1. Острые миелоидные лейкозы
- •21.4.2.2. Острые лимфоидные лейкозы
- •21.4.3. Хронические лейкозы
- •21.4.3.1. Хронический миелоидный лейкоз
- •21.4.3.2. Хронический лимфоидный лейкоз
- •21.4.4. Принципы терапии лейкозов
- •21.5. Патофизиология тромбоцитов
- •21.5.1. Тромбоцитозы. Общая характеристика, принципы терапии
- •21.5.2. Тромбоцитопении. Общая характеристика, принципы терапии
- •21.5.3. Тромбоцитопатии. Общая характеристика, принципы терапии
- •Принципы терапии тромбоцитопатии
- •21.6. Нарушения гемостаза
- •21.6.1 Сосудисто-тромбоцитарный гемостаз, его нарушения
- •21.6.1.1 Тромботический – тромбофилический синдром
- •21.6.2 Коагуляционный гемостаз, его нарушения
- •21.6.2.1 Геморрагический синдром
- •Нарушения гемостаза сосудистого (вазопатии) и смешанного генеза
- •Приобретенные коагулопатии
- •21.6.4. Принципы терапии нарушения гемостаза
- •21.7. Нарушения общего объема крови и соотношения форменных элементов и плазмы крови
- •21.7.1. Общая характеристика нарушений объема крови
- •21.7.2 Кровопотеря: причины, механизмы развития, проявления и принципы терапии
- •Принципы терапии кровопотери
- •Глава 22. Патофизиология сердечно-сосудистой системы
- •22.1. Недостаточность кровообращения
- •22.2. Сердечная недостаточность
- •Симптомы застоя крови в малом и большом кругах кровообращения
- •22.2.1 Острая левожелудочковая недостаточность
- •22.2.2 Острая правожелудочковая недостаточность
- •22.2.3 Ишемическая болезнь сердца
- •22.2.3.1 Коронарная недостаточность
- •22.2.3.2 Инфаркт миокарда
- •22.2.3.3. Принципы терапии коронарной недостаточности
- •22.2.4 Хроническая сердечная недостаточность
- •22.2.5. Механизмы компенсации сниженной сократительной функции сердца
- •22.2.6. Принципы терапии сердечной недостаточности
- •22.3. Нарушения ритма сердца (аритмии)
- •22.3.1. Общая характеристика, этиология и патогенез аритмий
- •22.3.2 Аритмии, возникающие в результате нарушения автоматизма
- •22.3.3. Аритмии, возникающие в результате нарушений проводимости
- •22.3.4. Аритмии, возникающие в результате сочетанных нарушений возбудимости и проводимости миокарда
- •22.3.5. Принципы терапии нарушений ритма сердца
- •22.4. Нарушения регуляции сосудистого тонуса и системного артериального давления Расстройства сосудистого тонуса
- •Нарушения регуляции уровня системного артериального давления
- •22.4.1. Артериальные гипертензии: виды, их характеристика и принципы терапии
- •Нейрогенные артериальные гипертензии
- •Эндокринные артериальные гипертензии
- •Почечные артериальные гипертензии
- •Метаболические (органно-ишемические) артериальные гипертензии.
- •Эссенциальная артериальная гипертензия
- •Стадии развития артериальной гипертензии
- •Классификация стадий артериальной гипертензии по поражению органов-мишеней (воз, 1999)
- •Основные порочные круги при артериальной гипертензии
- •Факторы, стабилизирующие высокий уровень артериального давления при артериальной гипертензии
- •Симптоматические артериальные гипертензии
- •Принципы терапии артериальной гипертензии
- •22.4.2 Артериальные гипотензии: виды, их характеристика и принципы терапии
- •Острая артериальная гипотензия
- •Хроническая артериальная гипотензия
- •Принципы коррекции артериальных гипотензий
- •22.5. Нарушения мозгового кровообращения
- •22.5.1 Общая характеристика мозгового кровообращения и механизмов его регуляции
- •Патологические реакции артерий мозга
- •22.5.2. Расстройства мозгового кровообращения
- •22.5.3. Принципы терапии расстройств мозгового кровообращения
- •Глава 23. Патофизиология системы внешнего дыхания
- •23.1. Общая характеристика расстройств внешнего дыхания
- •23.2 Нарушения вентиляции легких
- •23.2.1 Обструктивные нарушения дыхания
- •23.2.2 Рестриктивные нарушения дыхания
- •Проявления гиповентиляции
- •23.3 Нарушения кровообращения в легких
- •Легочная гипо- и гипертензия
- •23.4 Нарушения вентиляционно-перфузионных отношений
- •23.5. Нарушения диффузии газов через альвеолярно-капиллярные мембраны
- •23.6. Нарушения ритма дыхательных движений
- •23.7. Недостаточность внешнего дыхания
- •23.8. Респираторный дистресс-синдром
- •23.9. Нарушения недыхательных функций легких
- •23.10. Принципы профилактики и терапии патологии внешнего дыхания
- •Глава 24. Патофизиология системы пищеварения
- •24.1. Общая этиология расстройств пищеварения
- •24.2. Нарушения пищеварения в полости рта
- •Дисфагия
- •24.3. Нарушения пищеварения в желудке
- •24.3.1. Расстройства моторной функции желудка
- •24.3.2. Расстройства секреторной функции желудка
- •24.3.3. Расстройства всасывания в желудке
- •24.3.4. Нарушения барьерной и защитной функции желудка
- •24.4. Язва желудка и 12-перстной кишки
- •Факторы защиты слизистой оболочки желудка
- •Факторы, повреждающие слизистую оболочку желудка
- •Факторы риска ульцерогенеза:
- •Нейроэндокринная регуляция
- •24.5. Расстройства пищеварения в кишечнике
- •24.5.1. Энтеропатии (энтериты): виды, механизмы развития, проявления
- •24.5.2. Колиты: виды, механизмы развития, проявления
- •24.6. Принципы профилактики и терапии основных расстройств системы пищеварения
- •Глава 25. Патофизиология печени
- •25.1 Общая характеристика патологии печени
- •25.2. Печеночная недостаточность
- •25.3 Основные синдромы при патологии печени
- •25.3.1 Синдром желтухи
- •25.3.2 Синдром холестаза
- •25.3.3 Синдром нарушенного питания
- •25.3.4 Геморрагический синдром
- •25.3.5 Портальная гипертензия
- •25.3.6. Гепато-эндокринный, гепато-ренальный синдромы, синдром гепато-церебральной недостаточности
- •25.3.7 Печеночная кома
- •Клинико-биохимические печеночные синдромы
- •25.4 Принципы профилактики и терапии патологии печени
- •Глава 26. Патофизиология почек
- •26.1. Общая характеристика патологических процессов в почках
- •Виды почечной патологии по их происхождению
- •Основные клинические проявления патологии почек
- •26.2. Основные механизмы нарушений экскреторной функции почек
- •26.2.1. Нарушения клубочковой фильтрации
- •26.2.2. Нарушения канальцевой реабсорбции, экскреции и секреции
- •26.3. Почечные синдромы
- •Изменение количества мочи (диуреза)
- •Изменения относительной (удельной) плотности мочи
- •Изменения качественного состава мочи
- •Изменения ритма мочеиспускания
- •26.4. Внепочечные синдромы Отеки
- •Артериальная гипертензия
- •Нарушения гемокоагуляции
- •26.5. Типовые формы патологии почек. Гломерулопатии
- •26.5.1. Нефриты
- •26.5.1.1. Острый диффузный гломерулонефрит
- •26.5.1.2. Хронический диффузный гломерулонефрит
- •26.5.2. Пиелонефрит
- •26.5.3. Нефротический синдром (нефроз)
- •26.5.4. Почечная недостаточность
- •26.5.4.1. Острая почечная недостаточность
- •26.5.4.2. Хроническая почечная недостаточность
- •26.5.5. Почечно-каменная болезнь (нефролитиаз)
- •26.6. Принципы терапии патологии почек
- •Глава 27. Патофизиология эндокринной системы
- •27.1. Общая характеристика эндокринной системы и механизмов ее регуляции
- •Эндокринные железы и их гормоны
- •27.2. Эндокринопатии: виды, принципы классификации
- •27.3 Общая этиология и патогенез эндокринных расстройств
- •Парциальная гипофункция гипоталамо-гипофизарной системы
- •27.4.1.2. Гиперфункция гипоталамо-гипофизарной системы
- •27.4.2. Нарушения гипоталамо-нейрогипофизарной системы
- •27.4.3. Нарушения функции надпочечников
- •27.4.3.1. Надпочечниковая недостаточность
- •Хроническая недостаточность коры надпочечников
- •27.4.3.2. Гиперфункция коры надпочечников Гиперфункция клубочковой зоны коры надпочечников
- •Первичный гиперальдостеронизм (синдром Конна)
- •Гиперфункция пучковой зоны коры надпочечников
- •Гиперфункция сетчатой зоны коры надпочечников
- •27.4.3.3 Гиперфункция мозгового вещества надпочечников
- •27.4.4 Нарушения функций щитовидной железы
- •27.4.4.1 Гипотиреоидные состояния организма
- •27.4.4.2 Гипертиреоидные состояния организма
- •Диффузный токсический зоб (болезнь Грейвса-фон-Базедова)
- •27.4.5 Нарушения функций паращитовидных желез
- •27.4.5.1 Гипопаратиреоидные состояния
- •27.4.5.2 Гиперпаратиреоидные состояния
- •27.4.6 Нарушения функции половых желез
- •27.4.6.1 Нарушения полового развития и половой функции у лиц мужского пола
- •27.4.6.2 Нарушения полового развития и половой функции у лиц женского пола
- •27.5. Принципы терапии эндокринных расстройств
- •Глава 28. Патофизиология нервной системы
- •28.1. Общая этиология нарушений деятельности нервной системы
- •28.2 Общий патогенез нарушений деятельности нервной системы
- •28.2.1 Патология нейрона
- •28.2.2 Типовые патологические процессы в нервной системе
- •28.2.3 Расстройства интегративной деятельности нервной системы
- •28.3 Нейрогенные расстройства чувствительности
- •28.4 Боль: виды, причины, механизмы формирования. Основы обезболивания
- •28.5. Нейрогенные расстройства локомоторных функций
- •Типовые формы нейрогенных расстройств локомоторной функции
- •28.6. Нейрогенные расстройства трофики
- •28.7. Нарушения функции вегетативной нервной системы
- •28.8. Нарушения высшей нервной деятельности
- •28.9 Следовые реакции и их роль в патологии нервной системы
- •Исходы патологических процессов в нервной системе
- •28.10 Принципы терапии нервных расстройств
22.2.6. Принципы терапии сердечной недостаточности
Этиотропная терапия при сердечной недостаточности направлена на прекращение или ослабление действия патогенного фактора. Патогенетическая терапия направлена на разрыв ведущих и второстепенных звеньев патогенеза сердечной недостаточности.
При лечении миокардиальной формы сердечной недостаточности необходимо:
уменьшить степень нарушения энергообеспечения кардиомиоцитов (антигипоксанты; антиоксиданты, коронародилататоры);
защитить мембраны и ферменты кардиомиоцитов (антиоксиданты, препараты с мембранопротекторным действием);
уменьшить степень дисбаланса ионов и жидкости в миокарде (регуляторы транспорта ионов через мембраны, калийсберегающие диуретики, блокаторы кальциевых каналов и др.);
корригировать адрено- и холинергические влияния на сердце, его адренохолинореактивные свойства (симпатолитики, адреноблокаторы, адреномиметики) при достаточном резерве (холиномиметики).
Для лечения сердечной недостаточности при перегрузке следует снизить нагрузку на сердце путем:
уменьшения постнагрузки (снижения тонуса резистивных сосудов), то есть использование вазодилататоров, α-адреноблокаторов, адренолитиков;
уменьшения преднагрузки (снижение возврата венозной крови к сердцу), то есть использование венозных вазодилататоров, мочегонных;
снижения «инотропизма» (применение симпатолитиков, β-адре-ноблокаторов, ганглиоблокаторов).
Симптоматическая терапия обеспечивает уменьшение проявления ряда симптомов заболевания, усугубляющих общее состояние болезни. С этой целью применяют седативные, анальгетические средства и т.д.
22.3. Нарушения ритма сердца (аритмии)
22.3.1. Общая характеристика, этиология и патогенез аритмий
Аритмии (от греч. а – не, rhytmos – теку, ритм) – типовая форма патологии сердца, характеризующаяся нарушением частоты и периодичности генерации импульсов возбуждения и (или) последовательности возбуждения предсердий и желудочков.
Возникновение аритмий чаще всего ассоциируется с наличием органического заболевания сердца различной этиологии – ишемией, воспалением, дегенеративными изменениями, токсическим поражением. Однако их регистрируют также у лиц с практически здоровым сердцем, у которых с помощью современных методов исследования не выявляют какой-либо патологии. Установлено, что возникновение аритмий учащается параллельно увеличению возраста пациентов. В связи с этим в общей популяции определяется наличие взаимосвязи между распространённостью ИБС и частотой нарушений ритма сердца. Наиболее часто аритмии сердца наблюдаются при коронарной недостаточности. Так, в остром периоде инфаркта миокарда аритмии регистрируются у 95-100% пациентов.
Этиология. Аритмии являются следствием нарушения автоматизма, возбудимости и проводимости миокарда, или их комбинаций. Основными причинами аритмий являются:
патология, приводящая к повреждению миокарда (ИБС, пороки сердца, ревматизм, миокардиты, кардиомиопатии, механическая травма, опухоли и др.);
функциональные нарушения нейрогуморальной регуляции сердца (стресс, неврозы, дисфункция вегетативной нервной системы и др.);
врождённые аномалии и особенности проводящей системы сердца (например, наличие дополнительных проводящих путей);
нарушения водно-электролитного баланса и КОС.
гормональные нарушения (эндокринные заболевания, изменение гормонального статуса при физиологических и патологических состояниях);
токсическое повреждение миокарда (алкоголь, никотин и др.), в том числе обусловленное действием лекарственных средств (например, антиаритмические лекарственные средства потенциально способны вызвать нарушение ритма из-за изменения ионного гомеостаза миокарда).
Патогенез. Согласно современным представлениям, в основе возникновения аритмий лежат нарушения образования или проведения импульса (ПД). Однако чаще всего аритмии возникают при участии обоих механизмов (рис. 31).
Нарушения образования импульса. Нарушение образования импульса может быть обусловлено нарушением автоматизма и повышением возбудимости кардиомиоцитов (рис. 33).

Рисунок 33. Патогенез сердечных аритмий
Автоматизм (автоматия) – способность кардиомиоцитов спонтанно генерировать ПД. Способностью к автоматизму обладают все атипичные кардиомиоциты (клетки проводящей системы сердца), но не обладают рабочие кардиомиоциты (клетки сократительного миокарда).
Возбудимость – свойство клеток возбудимых тканей воспринимать действие раздражителя и реагировать на него реакцией возбуждения. Возбудимость сердечной мышцы выражается в способности генерировать ПД в ответ на раздражение.
В норме автоматизм проявляет только синоатриальный узел (СА-узел, узел Киса-Флека), являющийся номотопным (т.е. нормально расположенным) водителем ритма. Частота генерации импульсов клетками СА-узла в покое у взрослого человека составляет 60-90 в мин. СА-узел называется истинным водителем ритма, или пейсмекером 1-го порядка (от англ. pacemaker – водитель ритма). Остальные структуры проводящей системы сердца (атриовентрикулярный узел, пучок Гиса, ножки пучка Гиса, волокна Пуркинье), также способны спонтанно генерировать импульсы, однако собственная частота разрядов клеток этих отделов мала. Она тем ниже, чем дальше от пейсмекера 1-го порядка расположены клетки (градиент автоматии). Благодаря этому в нормальных условиях ПД в этих клетках проводящей системы сердца возникает в результате прихода возбуждения от более часто разряжающихся верхних отделов (клетки СА-узла), и их собственный автоматизм «не успевает» проявиться.
Таким образом, нижележащие структуры проводящей системы сердца проявляют автоматизм лишь при нарушении поступления импульсов от СА-узла, и поэтому называются латентными (скрытыми, потенциальными) водителями ритма.
Изменения нормального автоматизма. Как известно, в основе процесса автоматизма лежит медленная спонтанная диастолическая деполяризация (рис. 34), постепенно уменьшающая мембранный потенциал до критического уровня (порог возбуждения), с которого начинается быстрая деполяризация мембраны (фаза 0 потенциала действия).

Рисунок 34. Потенциал действия: А – рабочий (типичный) кардиомиоцит; Б – клетка синоатриального узла (атипичный кардиомиоцит): 0 – фаза быстрой деполяризации; 1 – фаза ранней быстрой реполяризации; 2 – фаза медленной реполяризации (фаза «плато»); 3 – фаза быстрой реполяризации; 4 – фаза потенциала покоя; 5 – порог возбуждения.
Изменения нормального автоматизма сердца приводят к возникновению синусовых аритмий. На продолжительность спонтанной диастолической деполяризации и, следовательно, частоту генерации импульсов клетками СА-узла оказывают влияние следующие факторы:
– скорость спонтанной диастолической деполяризации. При её возрастании порог возбуждения достигается быстрее и происходит учащение синусового ритма (тахикардия). Замедление спонтанной диастолической деполяризации, ведёт к замедлению синусового ритма (брадикардия);
– величина потенциала покоя клеток СА-узла. Если величина потенциала покоя становится более отрицательной (например, в результате гиперполяризации мембраны при действии АХ), требуется больше времени для достижения порога возбуждения (при условии, что скорость спонтанной диастолической деполяризации остаётся неизменной), возникает брадикардия. Если потенциал покоя клеток СА-узла становится менее отрицательным, соответственно требуется меньше времени для достижения порога возбуждения, развивается тахикардия;
– величина порога возбуждения. Более отрицательное значение величины порога возбуждения клеток СА-узла способствует учащению синусового ритма, а менее отрицательное значение – урежению синусового ритма. Возможны и различные комбинации трёх основных электрофизиологических механизмов, регулирующих автоматизм СА-узла.
Аномальный автоматизм. В норме ритм сердечных сокращений задают клетки СА-узла – истинные водители ритма (пейсмекеры 1-го порядка). Все остальные клетки проводящей системы сердца разряжаются, как и рабочий миокард, под действием распространяющегося возбуждения. Потенциал действия в них возникает под влиянием токов от возбуждённых участков миокарда до того, как в результате их собственной медленной спонтанной диастолической деполяризации их мембранный потенциал достигнет порога возбуждения.
Аномальный автоматизм – это появление пейсмекерной активности в клетках сердца, не являющихся в норме водителями сердечного ритма (т.е. они становятся водителями ритма сердца вместо клеток СА-узла).
Если по той или иной причине возбуждение СА-узла не возникает либо не может перейти на предсердие вследствие нарушения проводимости, роль водителя ритма берёт на себя атриовентрикулярный узел (АВ-узел, узел Ашоффа-Тавара) – пейсмекер 2-го порядка (частота генерации импульсов 40-60 в мин). Если проведение возбуждения от предсердий к желудочкам полностью нарушено, то желудочки сокращаются в ритме пейсмекера 3-го порядка (частота генерации импульсов менее 40 в мин), расположенного в проводящей системе желудочков.
СА-узел называют номотопным (нормально расположенным) водителем ритма, а очаги возбуждения в остальных отделах проводящей системы сердца – гетеротопными (ненормально расположенными). Эктопический водитель ритма – источник сердечных импульсов, расположенный в любом месте миокарда помимо СА-узла.
Сокращение сердца, вызванное импульсом из гетеротопного очага возбуждения, называют замещающим, а последовательность сокращений – замещающим ритмом. Такие ритмы выполняют защитную функцию, поддерживая относительно высокую ЧСС при выраженном замедлении импульсации из СА-узла.
Гетеротопные очаги возбуждения могут определять ЧСС в случае, если их скорость генерации импульсов (соответственно, частота) будет больше, чем у СА-узла. Например, на фоне высокой концентрации КА может усиливаться автоматизм клеток нижележащих отделов проводящей системы сердца, и если частота их деполяризации оказывается больше частоты генерации импульсов клетками СА-узла, это приводит к появлению эктопического ритма (например, экстрасистолия). Такие эктопические ритмы могут возникать при ишемии миокарда, гипоксии, при электролитных нарушениях и т.д. При поражении миокарда (например, ишемии и др.) рабочие кардиомиоциты могут приобретать патологическую способность к автоматизму. Если скорость спонтанной диастолической деполяризации таких кардиомиоцитов превышает частоту генерации импульсов клетками СА-узла, то эти клетки устанавливают собственную частоту сокращений сердца, становясь эктопическим водителем ритма.
Повышение возбудимости кардиомиоцитов наиболее часто обусловливает возникновение аритмий по механизму триггерной активности (наведённой, пусковой, от англ. trigger – спусковой крючок). Электрофизиологической основой триггерной активности (триггерного автоматизма) являются ранние и поздние постдеполяризации (рис. 35).
Р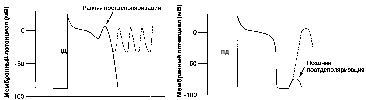 анняя
постдеполяризация
– это
преждевременная деполяризация
кардиомиоцитов, которая появляется в
фазу реполяризации, когда потенциал
мембраны ещё не достиг величины потенциала
покоя (рис.
35). Условиями возникновения ранних
постдеполяризаций являются: удлинение
фазы реполяризации потенциала действия
и брадикардия.
анняя
постдеполяризация
– это
преждевременная деполяризация
кардиомиоцитов, которая появляется в
фазу реполяризации, когда потенциал
мембраны ещё не достиг величины потенциала
покоя (рис.
35). Условиями возникновения ранних
постдеполяризаций являются: удлинение
фазы реполяризации потенциала действия
и брадикардия.
Рисунок 35. Потенциал действия: триггерная активность.
При замедлении реполяризации и соответственно увеличении общей продолжительности потенциала действия может возникнуть преждевременная спонтанная деполяризация в тот момент, когда процесс реполяризации ещё не завершился. При уменьшении частоты основного ритма сердца (брадикардии) происходит постепенное возрастание амплитуды ранних надпороговых колебаний мембранного потенциала, что при достижении величины порога возбуждения может вызывать образование нового потенциала действия ещё до завершения исходного.
Этот преждевременный потенциал действия рассматривается как триггерный (наведённый), поскольку он обязан своим возникновением ранней постдеполяризации, исходящей от основного потенциала действия. В свою очередь, второй (наведённый) потенциал действия за счёт своей ранней постдеполяризации может вызвать третий, тоже триггерный потенциал действия и т.д.
Если источник триггерной активности находится в желудочках, то может развиться желудочковая экстрасистолия или полиморфная (пароксизмальная) желудочковая тахикардия (желудочковая тахикардия типа «пируэт» – torsade de pointes). Электрокардиографическая картина полиморфной желудочковой тахикардии представлена на рисунке 36 – желудочковые комплексы как бы «вьются» вокруг изоэлектрической оси (здесь и далее ЭКГ приведены во II-м стандартном отведении, скорость записи 25 мм/с).

Рисунок 36. Полиморфная желудочковая тахикардия (torsade de pointes).
Возникновению ранних постдеполяризаций способствуют гиперкатехоламинемия, гипокалиемия, ацидоз, ишемия.
Поздняя постдеполяризация – это преждевременная деполяризация кардиомиоцитов, которая появляется сразу после завершения фазы реполяризации, т.е. когда электрический заряд мембраны соответствует потенциалу покоя (рис. 35).
Подпороговые колебания мембранного потенциала, которые в норме могут присутствовать, но никогда себя не проявляют, при патологических состояниях, сопровождающихся увеличением внутриклеточной концентрации Са2+ в кардиомиоцитах, могут возрастать по амплитуде, достигая порога возбуждения (рис. 34). Повышение внутриклеточной концентрации Са2+ вызывает активацию неселективных ионных каналов, обеспечивающих усиленное поступление катионов (главным образом Na+) из внеклеточной среды в кардиомиоцит. В результате отрицательный заряд внутренней поверхности мембраны уменьшается, достигая величины порога возбуждения, вследствие чего возникает серия преждевременных потенциалов действия. Поздние постдеполяризации могут возникать при инфаркте миокарда, под действием сердечных гликозидов, КА.
Нарушения проведения импульса. Проводимость – способность кардиомиоцитов проводить импульсы возбуждения. Существует три основных типа нарушений проводимости: замедление или блокада проведения; повторный вход импульса (механизм re-entry); сверхнормальное проведение.
Замедление или блокада проведения импульса. Распространение импульса возбуждения блокируется, если он достигает участка миокарда, неспособного к возбуждению. Чаще всего проведение импульса нарушается, если он достигает кардиомиоцитов, находящихся в рефрактерной фазе. В этом случае говорят о функциональной блокаде. Распространение следующего импульса возбуждения при этом может не нарушаться. Блокада, вызванная барьером в виде рубцовой ткани, замещающей кардиомиоциты, называется фиксированной блокадой проведения импульса.
Причиной замедления проведения импульса возбуждения или его блокады нередко бывает снижение количества потенциалзависимых Na+-каналов клеток, которым в норме присуще свойство быстрой деполяризации (например, рабочие кардиомиоциты, волокна Пуркинье). Существует прямая зависимость между количеством фунциональноактивных потенциалзависимых Na+-каналов и величиной потенциала покоя. Так, при уменьшении мембранного потенциала покоя рабочего кардиомиоцита до уровня -50 мВ (в норме -90 мВ) инактивируется около половины всех Na+-каналов. В этом случае возбуждение и проведение импульса становятся невозможными (например, в зоне ишемии миокарда).
В определенных случаях даже при значительном уменьшении потенциала покоя проведение импульса возбуждения, правда, существенно замедленное, сохраняется. Такое проведение осуществляется «медленными» Са2+-каналами и «медленными» Na+-каналами, которые устойчивы к снижению потенциала покоя (рис. 37).

Рисунок 37. Влияние острой ишемии миокарда на потенциал действия рабочего (типичного) кардиомиоцита: А – нормальный потенциал действия; Б – «медленный» потенциал действия.
В рабочих кардиомиоцитах имеются только «быстрые» Na+-каналы, но в условиях ишемии миокарда одна половина этих каналов инактивируется, а другая половина может превратиться в аномальные «медленные» Na+-каналы. Таким образом, «быстрые» клетки превращаются в «медленные» кардиомиоциты, при прохождении через которые импульс возбуждения может замедлить свое распространение или блокироваться.
Повторный вход импульса (механизм re-entry). Этим термином обозначают явление, при котором электрический импульс, совершая движение по замкнутому кругу (петле, кольцу), возвращается к месту своего возникновения (circus movement). Различают macro re-entry (макрориентри) и micro re-entry (микрориентри). При таком делении учитывают размеры круга (петли), в которой осуществляется повторный вход импульса.
В норме импульсы из СА-узла строго упорядоченно распространяются по сердцу, вызывая деполяризацию всех волокон миокарда, после чего затухают. Каждый участок миокарда и проводящей системы деполяризуются под действием одного импульса только один раз (в силу рефрактерности кардиомиоцитов).
Для развития механизма re-entry необходимы следующие условия:
существование 2-х каналов проведения импульса, разделенных между собой функционально или анатомически;
односторонняя блокада проведения импульса в одном из каналов;
наличие потенциально замкнутой петли движения импульса (например, в местах разветвления волокон проводящей системы, зонах контактов окончаний волокон Пуркинье с кардиомиоцитами);
замедление проведения импульса по цепи re-entry (замедление скорости проведения импульса, так что ни в одной точке петли волна возбуждения не встречается с зоной рефрактерности).
Соблюдение этих условий возможно в том случае, если соседние клетки миокарда будут различаться по скорости проведения импульсов и продолжительности рефрактерного периода (например, функционально гетерогенный участок при ишемии миокарда).
На рисунке 38 показано распространение волны возбуждения в норме. Импульс достигает точки «х» и далее следует по двум параллельным путям (α и β) в нижележащие отделы проводящей системы. Скорость проведения и рефрактерность путей α и β одинаковы, поэтому две волны возбуждения одновременно приходят в дистальный участок проводящей системы, где гасят друг друга (затухание импульса).

Рисунок 38. Проведение импульса в норме (конечные волокна Пуркинье).
На рисунке 39 показано, что происходит, если проведение импульса по одному из путей блокировано. В этом случае прохождение импульса возбуждения из верхних в нижние отделы проводящей системы возможно только по пути α (рис. 39А). Распространяясь, импульс может достигнуть конечной точки пути β («у»). Если проводимость дистальных отделов пути β тоже нарушена, то импульс продолжает распространяться в нижележащие участки. Однако иногда импульс способен проводиться по пути β ретроградно (вверх), и это явление – одно из обязательных условий реализации механизма re-entry (рис. 39Б).


А
Б
Рисунок 39. Механизм повторного входа импульса (re-entry). Односторонняя блокада.
Нарушение, при котором импульс распространяется по проводящим путям только ретроградно, называют односторонней блокадой. Односторонняя блокада проведения импульса наблюдается в участках миокарда, где соседние клетки имеют разный рефрактерный период (например, при ишемии миокарда). Импульс, распространяющийся ретроградно по пути β, может вновь достигнуть точки «х». Если в этот момент путь α находится в фазе реполяризации, то повторная волна возбуждения затухает в точке «х» (рис. 39Б).
Если скорость ретроградного проведения импульса по пути β меньше, чем в норме, то в этом случае время, за которое повторная волна возбуждения проводится по пути β, достаточно для полной реполяризации пути α (рис. 40). Достигнув точки «х», импульс вновь активирует путь α, замыкая круг, по которому постоянно циркулирует волна возбуждения. Этот круг может существовать неопределенно долгое время, при этом каждое прохождение импульса активирует дистальные отделы проводящей системы, после чего волна возбуждения распространяется по всему миокарду, вызывая тахиаритмии.

Рисунок 40. Механизм повторного входа импульса (re-entry).
Замедление ретроградного проведения импульса
Таким образом, сущность механизма re-entry заключается в том, что импульс повторно входит в участок миокарда или проводящей системы, что создаёт циркуляцию волны возбуждения.
Сверхнормальное проведение возникает в случае, если импульс возбуждения из СА-узла быстрее достигает желудочков по дополнительным путям предсердно-желудочкового проведения. К таким путям относятся: пучок Кента (правый и левый), Джеймса и некоторые другие. Правый пучок Кента соединяет правое предсердие с правой ножкой пучка Гиса, а левый пучок – левое предсердие с левой ножкой пучка Гиса. Пучок Джеймса соединяет предсердия с нижней частью АВ-узла. По этим дополнительным проводящим путям импульсы возбуждения из СА-узла достигают части желудочков раньше импульсов, которые идут обычным путём через АВ-узел. Это приводит к преждевременной активации части желудочков, другая их часть возбуждается позже импульсами, проходящими через АВ-узел. При этом происходит взаимное наложение проводимых импульсов возбуждения и возникает тахиаритмия (например, синдром Вольфа-Паркинсона-Уайта).
