
- •Тематический план
- •Введение
- •Занятие № 1
- •1. Тема: Анализ качества лекарственных средств из группы алкалоидов с экзоциклическим атомом азота и алкалоидов, производных пурина, а также их синтетических аналогов
- •3. Целевые задачи:
- •Физико-химические свойства алкалоидов
- •Методы выделения алкалоидов из растительного сырья
- •Методы разделения алкалоидов
- •Принципы установления строения алкалоидов
- •Классификация алкалоидов
- •Методы идентификации алкалоидов
- •Методы количественного определения алкалоидов
- •Аспекты создания синтетических лекарственных средств на основе модификации «структуры-лидера» из группы природных алкалоидов
- •4. План и организационная структура занятия:
- •5. Задание для самоподготовки студентов:
- •Учебные вопросы для самоподготовки студентов
- •5.3. Проработать тестовые задания:
- •5.4. Ситуационные задания:
- •5.5. Задачи:
- •Литература
- •6. Лабораторная работа
- •7. Наглядные пособия, технические средства обучения и контроля:
- •Занятие № 2
- •1. Тема: Анализ качества лекарственных средств из группы алкалоидов, производных имидазола, пирролизидина, индола и их синтетических аналогов
- •3. Целевые задачи:
- •4. План и организационная структура занятия:
- •5. Задание для самоподготовки студентов:
- •Учебные вопросы для самоподготовки студентов
- •5.3. Проработать тестовые задания:
- •5.4. Ситуационные задания:
- •5.5. Задачи:
- •Литература
- •6. Лабораторная работа
- •7. Наглядные пособия, технические средства обучения и контроля:
- •Занятие № 3
- •1. Тема: Анализ качества лекарственных средств из группы алкалоидов, производных хинолина, изохинолина и их синтетических аналогов
- •3. Целевые задачи:
- •4. План и организационная структура занятия:
- •5. Задание для самоподготовки студентов:
- •Учебные вопросы для самоподготовки студентов
- •5.3. Проработать тестовые задания:
- •5.4. Ситуационные задания:
- •5.5. Задачи:
- •Литература
- •6. Лабораторная работа
- •7. Наглядные пособия, технические средства обучения и контроля:
- •Занятие № 4
- •1. Тема: Анализ качества лекарственных средств из группы алкалоидов, производных тропана, хинолизина, хинолизидина и их синтетических аналогов
- •3. Целевые задачи:
- •4. План и организационная структура занятия:
- •5. Задание для самоподготовки студентов:
- •Учебные вопросы для самоподготовки студентов
- •5.3. Проработать тестовые задания:
- •5.4. Ситуационные задания:
- •5.5. Задачи:
- •Литература
- •6. Лабораторная работа
- •7. Наглядные пособия, технические средства обучения и контроля:
- •Занятие № 5
- •1. Тема: Анализ качества лекарственных средств из группы алкалоидов, производных морфинана и их синтетических аналогов
- •3. Целевые задачи:
- •4. План и организационная структура занятия:
- •5. Задание для самоподготовки студентов:
- •Учебные вопросы для самоподготовки студентов
- •5.3. Проработать тестовые задания:
- •5.4. Ситуационные задания:
- •5.5. Задачи:
- •Литература
- •6. Лабораторная работа
- •7. Наглядные пособия, технические средства обучения и контроля:
- •Занятие № 6
- •1. Тема: Итоговое занятие по теории и практике по теме: «Анализ качества лекарственных средств из группы алкалоидов и их синтетических аналогов по действию»
- •3. Целевые задачи:
- •4. План и организационная структура занятия:
- •5. Задание для самоподготовки студентов к итоговому занятию
- •5.1. Контрольные вопросы
- •5.3. Проработать тестовые задания:
- •5.4. Ситуационные задания:
- •5.5. Задачи:
- •Литература
Аспекты создания синтетических лекарственных средств на основе модификации «структуры-лидера» из группы природных алкалоидов
В 1879 году В.К. Анреп впервые обнаружил анестезирующие свойства алкалоида кокаина и предложил использовать его в медицинской практике для местного обезболивания. Однако кокаин имел ряд недостатков, значительно ограничивающих его применение. Основной из них – привыкание к препарату (развитие кокаинизма). Кроме того, кокаин достаточно токсичен и вызывает ряд побочных явлений. Например, он повышает внутриглазное давление, поэтому при глаукоме применение его как анестетика исключается. Все эти факты обусловили необходимость замены кокаина синтетическими аналогами по действию.
Последующее изучение структуры, физиологического действия кокаина, его аналогов и продуктов распада привело исследователей к выводу, что анестезирующее действие этих соединений обусловлено наличием в составе их молекул остатка бензойной кислоты, связанной сложноэфирной связью с азотсодержащей основной группой. Таким образом, в структуре кокаина была выявлена «анестезиофорная группа», которая и отвечает за анестезирующий эффект кокаина (выделена рамкой):
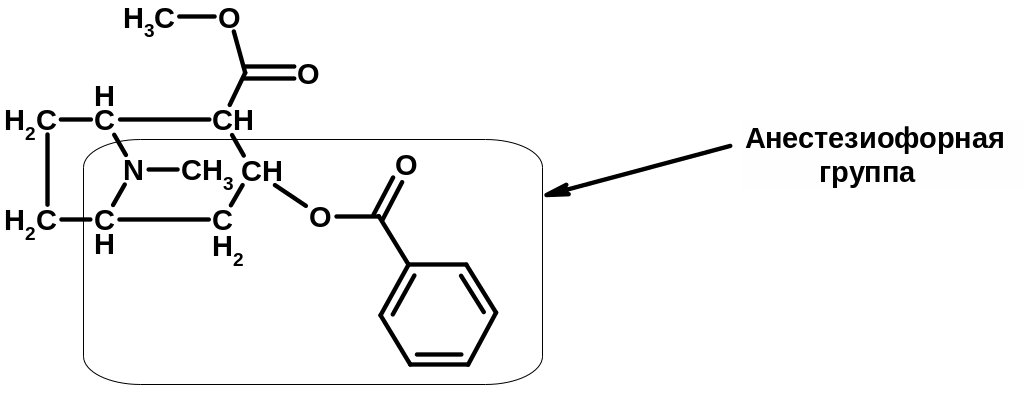
Как можно заметить, анестезиофорная группа гипотетически является структурным эквивалентом бензойной кислоты, эстерифицированной метиламинопропиловым спиртом. Поэтому дальнейший поиск синтетических анестетиков проводился в ряду сложных эфиров бензойной кислоты. Исследования показали, что эфиры бензойной кислоты, хотя и обладают сильным анестезирующим действием, превосходящим действие кокаина, но вызывают сильное раздражение. Последующая модификация структуры данной группы соединений позволила установить, что несравнимо лучшими качествами обладают эфиры п-аминобензойной кислоты. Это привело к созданию таких лекарственных средств как анестезин, новокаин, дикаин, инкаин и др.
После дальнейшего изучения и систематизации исследований по созданию местных анестетиков, структуру анестезиофорной группы в общем виде можно представить следующим образом:
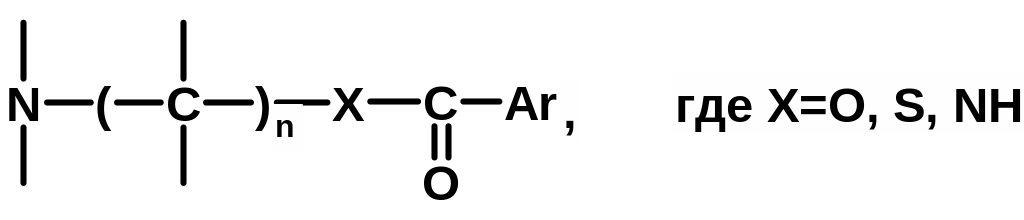
Таким образом, выяснение данной закономерности стало предпосылкой и основой для получения большой группы анестезирующих веществ, которые нашли широкое применение в медицинской практике.
При рассмотрении подходов к созданию лекарственных средств путем модификации «структуры-лидера» из группы природных алкалоидов, привлекают внимание анальгетические препараты, полученные на основе алкалоида морфина с сохранением элементов его структуры или ее упрощением. Этот принцип позволил получить ряд препаратов, различающихся по силе и продолжительности болеутоляющего действия, быстроте и степени развития привыкания, пристрастия и других побочных эффектов.
Так, группа важнейших анальгетиков, производных пиперидина, берет свое начало с 1940-х годов, когда на основе изучения взаимосвязи «структура-действие» в ряду морфинановых алкалоидов и идеи упрощения их структуры, был синтезирован промедол. Данный анальгетик по химическому строению может рассматриваться как аналог фенил-N-метилпиперидиновой части молекулы морфина, видоизмененное изображение формулы которого для наглядности приведено ниже в сравнении с формулой промедола (в виде оснований):
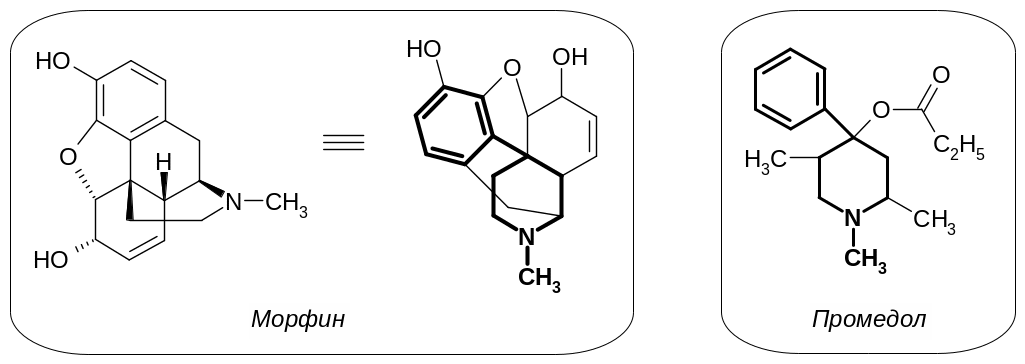
В дальнейшем, обнаружение анальгетической активности у большой серии производных 4-фенилпиперидина (промедол, фентанил, просидол и др.), привело к формулированию правила Беккета-Кейзи, которое оказалось, несмотря на некоторую упрощенность, полезным на определенном этапе создания наркотических анальгетиков. В соответствии с этим правилом, для моделирования и конструирования потенциального наркотического анальгетика (взаимодействующего с опиатными рецепторами) необходимо, во-первых, наличие четвертичного атома углерода и ароматического кольца при этом атоме. Во-вторых, необходимо наличие третичного атома азота на расстоянии, эквивалентном двум атомам углерода в sp3-гибридизации от указанного четвертичного атома углерода:

По последним данным, ароматическое кольцо возле четвертичного атома углерода может быть заменено на пиперидиновый цикл (пиритрамид), фениламинную группу (фентанил, ремифентанил), замещенные бензола и др. Важно также, что расширение шестичленного пиперидинового кольца до семичленного (эгогептазин) или сужение гетероцикла до пирролидинового (пролидин), а также его замена на фенил (эстоцин) или циклогексан (трамадол) не приводят к снижению анальгетической активности. Кроме того, вышеупомянутое правило соблюдается не только в случае алоксикарбонильного заместителя (см. R) при четвертичном атоме углерода, но и если данный заместитель будет замен на гидроксильную, ацилоксильную, амидную, алкильную и другие функциональные группы.
