
- •Конспект лекций
- •Лекция 1 Энерготехнологическая переработка низкосортных топлив
- •1 Формирование исходных знаний
- •2 Изучение нового материала
- •3 Анализ
- •4 Применение новых опорных знаний
- •5 Синтез
- •6 Формирование аналогов опорного знания мысленными образами
- •1 Формирование исходных знаний
- •2 Изучение нового материала
- •3 Анализ
- •4 Применение новых опорных знаний
- •5 Синтез
- •6 Формирование аналогов опорного знания мысленными образами
- •1 Формирование исходных знаний
- •2 Изучение нового материала
- •3 Анализ
- •Применение новых опорных знаний
- •5Синтез
- •6 Формирование аналогов опорного знания мысленными образами
- •1 Формирование исходных знаний
- •2 Изучение нового материала
- •3 Анализ
- •4 Применение новых опорных знаний
- •6 Формирование аналогов опорного знания мысленными образами
- •1 Формирование исходных знаний
- •2 Изучение нового материала
- •3 Анализ
- •4 Применение новых опорных знаний
- •5 Синтез
- •Формирование аналогов опорного знания мысленными образами
- •1Формирование исходных знаний
- •2 Изучение нового материала
- •3 Анализ
- •4 Применение новых опорных знаний
- •5 Синтез
- •6 Формирование аналогов опорного знания мысленными образами
- •1 Формирование исходных знаний
- •2 Изучение нового материала
- •3 Анализ
- •4 Применение новых опорных знаний
- •5 Синтез
- •6 Формирование аналогов опорного знания мысленными образами
- •Лекция 8 « Регенеративный подогрев питательной воды»
- •1 Формирование исходных знаний
- •2 Изучение нового материала
- •3 Анализ
- •4 Применение новых опорных знаний
- •5 Синтез
- •6 Формирование аналогов опорного знания мысленными образами
- •2 Изучение нового материала
- •3 Анализ
- •4 Применение новых опорных знаний
- •5 Синтез
- •1 Формирование исходных знаний
- •2 Изучение нового материала
- •3 Анализ
- •4 Применение новых опорных знаний
- •5 Синтез
- •6 Формирование аналогов опорного знания мысленными образами
- •1 Формирование исходных знании
- •2 Изучение нового материала
- •3 Анализ
- •4 Применение новых опорных знании
- •5 Синтез
- •6 Формирование аналогов опорного знания мысленными образами
3 Анализ
Коксовый газ – содержит пары, коксовые смолы, пары бензольных углеводородов, аммиак, сероводород, нафталин, пары воды, водород, метан, этилен и его гомологи, угарный и углекислый газы, азот. Доля коксохимических продуктов в сырьевой базе промышленности основного органического синтеза составляет около 50%, а таких важных продуктов, как бензол, достигает 80%, нафталин и крезолы – 100%. Цветная металлургия является потребителем малозольного пекового кокса и связующего, получаемых из каменноугольной смолы. Коксы используются для приготовления анодной массы, применяемой при выплавке алюминия. На 1 т получаемого алюминия расходуется примерно 450 кг малозольного кокса и около 150 кг связующего. Для получения 1 т алюминия надо израсходовать 1 т пека или скоксовать около 70 т угля [8].
Коксохимическая промышленность поставляет сельскому хозяйству ценное удобрение – сульфат аммония. На базе водорода коксового газа и азота кислородных станций металлургических комбинатов производятся самые дешевые азотистые удобрения. Водород является составной частью коксового газа, получаемого в значительном количестве при коксовании углей. Азот и кислород – составные части воздуха. Кислород нужен для интенсификации металлургических процессов. Азот кислородных станций может рационально использоваться в упомянутом комплексе, сочетающем черную металлургию и химическую промышленность.
Химические продукты коксования используются для производства химических средств защиты растений и животных. Более 20 наименований продуктов и препаратов для нужд сельского хозяйства поставляет коксохимия.
Для газификации используют торф, полукокс, низкосортные угли. В результате газификации получают генераторные газы. Водород 16% угарный газ 10% метан. Метанол является основой для получения высокооктановых добавок к моторному топливу, так же как и водород, он является экологически перспективным видом топлива взамен бензина, также в быту для освещения и – отопления помещений [8].
4 Применение новых опорных знаний
Для одного и того же топлива количества минеральных примесей и влажность могут изменяться в зависимости его добычи, транспортировки и хранения. В связи с этим для удобства сравнительной оценки теплотехнических свойств различных сортов топлива введены условные понятия сухой, горючей и органической массы топлива.
Произведем перерасчет расчет горючей массы угля на рабочую массу топлива [9], имеющего следующее горючей массе: Cг=76,8%; Нг=5,6%; Sг=0,9%; Ог=14,7%; Nг=2%; Содержание золы – Ас = 16,0%; Содержание влаги – Wр = 9,0%
Состав рабочего топлива:
Ар = Ас ⋅ (100 – W р )/100 = 16 ⋅ (100 – 9,0)/100 = 14,6%
Ср = Сг ⋅ [100 – (Ар + W р )]/100 = 86,0 ⋅ [100 – (14,6 + 9,0)]/100 = 65,7%
Hр = Hг ⋅ [100 – (Ар + W р )]/100 = 5,0 ⋅ [100 – (14,6 + 9,0)]/100 = 3,8%
Ор = Ог ⋅ [100 – (Ар + W р )]/100 = 6,3 ⋅ [100 – (14,6 + 9,0)]/100 = 4,8%
Nр = Nг ⋅ [100 – (Ар + W р )]/100 = 2,0 ⋅ [100 – (14,6 + 9,0)]/100 = 1,5%
Sр = Sг ⋅ [100 – (Ар + W р ]/100) = 0,7 ⋅ [100 – (14,6 + 9,0)]/100 = 0,6%
где W p – влага в рабочем топливе, %;
А р – зольность топлива, %;
S р – количество летучей серы, %;
С р – количество углерода, %;
Н р – количество водорода, %;
N р – количество азота, %;
О р – количество кислорода, %.
Проверка: суммарный элементарный состав топлива на рабочую массу:
 Ар
+Ср+Hр
+Ор
+Sр
+W
p
=14,6+65,7+3,8+4,8+1,5+0,6+9=100%
Ар
+Ср+Hр
+Ор
+Sр
+W
p
=14,6+65,7+3,8+4,8+1,5+0,6+9=100%
По составу рабочей массы топлива вычисляют по формуле Менделеева [7] низшую теплоту сгорания, кДж/кг:
 ,
(2.1)
,
(2.1)
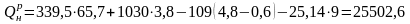 кДж/кг
кДж/кг
