
- •Методика розв’язування розрахункових задач
- •1. Введення. Актуальність і мета обраної теми 3
- •2. Типи розрахункових задач. 4
- •3. Висновки 19
- •4. Список використаних джерел 20
- •Введення. Актуальність і мета обраної теми
- •2. Типи розрахункових задач.
- •2.1. Обчислення масової частки елемента в складі речовини за її хімічною формулою
- •2.2. Обчислення числа атомів (молекул) у певній кількості речовини
- •2.3. Обчислення маси речовини за відомою кількістю і кількості речовини за відомою масою
- •2.4. Обчислення маси, об’єму та кількості речовини за рівнянням реакції
- •2.5. Обчислення, пов’язані з молярним об’ємом
- •2.6. Обчислення, пов’язані з відносною густиною газів
- •2.7. Обчислення на застосування закону об’ємних відношень газів
- •2.8. Обчислення за термохімічними рівняннями реакцій
- •2.9. Обчислення з використанням понять, пов’язаних з розчинами
- •2.10. Розв’язування задач на домішки
- •2.11. Обчислення, пов’язані з масовою та об’ємною частками виходу продукту реакцій
- •2.12. Обчислення за хімічним рівнянням, якщо одна з реагуючих речовин дана в надлишку
- •2.13. Знаходження молекулярної формули газоподібної речовини за масовими частками елементів і відносною густиною за іншим газом
- •2.14. Встановлення молекулярної формули речовини за продуктами згоряння
- •3. Висновки
- •4. Список використаних джерел
2.10. Розв’язування задач на домішки
Домішки не вступають в реакцію і не дають продукту реакції. Масова частка домішок w(дом) обчислюється за формулою:
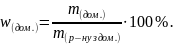
Об’ємна частка домішок:
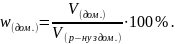
Задача. Обчисліть масу кальцій оксиду, яку можна одержати внаслідок термічного розкладу вапняку масою 500 г, який містить 8 % домішок.
Д ано:
Розв’язання
ано:
Розв’язання
Обчислюємо масу кальцій карбонату в 500 г вапняку.
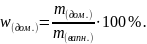
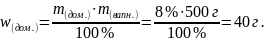
m(CaCO3) = m(вапн.) - m(дом.) = 500г - 40г = 460г.
2. Знаходимо масу кальцій оксиду, яка утвориться в результаті реакції.
460 г Xг
СаСO3 = СаО + СO2.
n=1моль n=1моль
m=100г m=56г
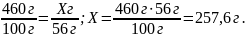
Відповідь: m(CaO) = 257,6г.
Задачі для самостійного розв’язування
1. Який об’єм водню виділиться внаслідок взаємодії розчину сульфатної кислоти з алюмінієм масою 12г, масова частка домішок у якому 10%?
2. Який об’єм кисню витратиться на спалювання сірки масою 10 г, масова частка домішок у якій становить 4%?
3. Який об’єм кисню витратиться на окиснсння сульфур (IV) оксиду об’ємом 27 л, об’ємна частка домішок у якому 20%?
2.11. Обчислення, пов’язані з масовою та об’ємною частками виходу продукту реакцій
За рівнянням реакції обчислюється лише теоретичний вихід. Практичний вихід завжди менший від теоретичного через неповний перебіг реакції та втрати. Вихід продукту обчислюється за формулами:
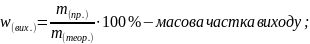
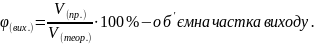
Задача. Під час нагрівання калій нітрату масою 30,3 г зібрали 3 л кисню. Обчисліть об’ємну частку виходу.
Д ано:
Розв’язання
ано:
Розв’язання
Обчислюємо об’єм кисню, який може віділитися теоретично:
30,3 г Xл
2KNO3 = 2KNO2 + O2 .
n=2моль n=1моль
m=2•101г V=22,4л
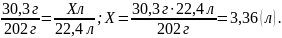
2. Знаходимо об’ємну частку виходу кисню.
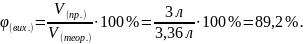
Відповідь:
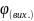 (O
2 ) = 89,2%.
(O
2 ) = 89,2%.
Задачі для самостійного розв’язування
1. З азоту масою 56 кг було синтезовано аміак масою 48 кг. Знайдіть масову частку виходу аміаку від теоретично можливого.
2. Який об’єм аміаку можна синтезувати з азоту масою 112 кг, якщо об’ємна частка виходу аміаку становить 90 % від теоретичного?
3. Який об’єм водню витратиться на добування аміаку масою 70 г, що становить 78 % від теоретично можливого?
2.12. Обчислення за хімічним рівнянням, якщо одна з реагуючих речовин дана в надлишку
Алгоритм розв’язку задач за цим способом:
1. Записуємо скорочену умову задачі.
2. Визначаємо речовину, яка перебуває в недостачі, обчислюємо кількості вихідних речовин за умовою задачі.
3. Записуємо хімічне рівняння реакції, складаємо мольні відношення вихідних речовин та порівнюємо отримані результати.
4. Розрахунки проводимо за речовиною, що перебуває в недостачі.
Задача. Обчисліть об’єм водню, що утвориться в результаті взаємодії цинку масою 13 г із сульфатною кислотою масою 20 г.
Д ано:
Розв’язання
ано:
Розв’язання
13 г 20г Xл
Zn + H2SO4 = ZnSO4 + H2
n=1моль n=1моль n=1моль
m=65г m=98г V=22,4л
1. Знаходимо вихідну речовину. Позначаємо одну з відомих величин через Y. Нехай m(H2SO4) = Y(г).
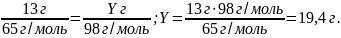
Оскільки з 13 г Zn може повністю прореагувати 19,4 г H2SO4, то кислота дана в надлишку, цинк — у недостачі, а отже, є вихідною речовиною.
2. Визначаємо, який об’єм водню виділиться.

Відповідь: V(H2) = 4,48(л).
Задачі для самостійного розв’язування
1. До розчину, що містить натрій ортофосфат масою 20 г, додали кальцій хлорид масою 22,2 г. Яка маса осаду утвориться при цьому?
2. Яку масу сульфур діоксиду можна одержати із сірки масою 10 г і кисню об’ємом 5,6 л (н.у.)?
3. Яку масу алюміній сульфіду можна одержати під час сплавлення 8,1 г алюмінію з 9,6 г сірки? Яка речовина і з якою масою не прореагує?
