
- •Основные классы неорганических соединений. Номенклатура. Характерные свойства.
- •Модели строения атома. Модель атома по Бору. Постулаты Бора. Квантовые числа n, l, m, s. Количество и разновидность электронных орбиталей.
- •Строение электронной оболочки многоэлектронных атомов. Электронные и электронные графические формулы атомов элементов (на примере хлора и марганца в основном и возбужденном состоянии).
- •Принцип минимума энергии. Правила Клечковского. Их применение. Принцип Паули. Правило Хунда (Гунда). Валентные электроны.
- •Энергия ионизации и сродство к электрону. Электроотрицательность как характеристика свойств элемента. Строение ядра атома. Понятие об изотопах и радиоактивности.
- •Химическая связь и способы её образования. Донорно-акцепторная, ионная связь. Водородная связь, её особенности.
- •Ковалентная связь (простая, кратная, Сигма (σ)-, пи (π)-связи , полярность связи, направленность). Гибридизация электронных орбиталей, геометрическая конфигурация молекул.
- •Основы термодинамики химических реакций: термодинамические функции (энтальпия, энтропия, свободная энергия Гиббса). Теплота образования.
- •Азотистая и азотная кислоты и их соли
- •Азотная кислота
- •Физические свойства
- •Химические свойства
- •Применение
- •Особенности строения фтора.
- •Химические свойства.
- •Особенности химических свойств фтора.
- •Особенности строения.
- •Межгалоидные соединения.
- •Химические свойства.
Понятия: моль; эквивалент. Основные стехиометрические и газовые законы (закон сохранения массы, эквивалентов, кратных отношений, закон Бойля-Мариотта, закон Гей-Люссака, закон Авогадро). Уравнения Клапейрона, Менделеева-Клапейрона. Парциальное давление газа в смеси. Закон парциальных давлений.
Моль (русское обозначение: моль; международное: mol; устаревшее название грамм-молекула (по отношению к количеству молекул); от лат. moles — количество, масса, счётное множество) — единица измерения количества вещества в Международной системе единиц (СИ), одна из семи основных единиц СИ.
Моль принят в качестве основной единицы СИ XIV Генеральной конференцией по мерам и весам (ГКМВ) в 1971 году.
Моль есть количество вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде-12 массой 0,012 кг. При применении моля структурные элементы должны быть специфицированы и могут быть атомами, молекулами, ионами, электронами и другими частицами или специфицированными группами частиц.
Эквивалент вещества или Эквивалент — это реальная или условная частица, которая может присоединять, высвобождать или другим способом быть эквивалентна катиону водорода в кислотно-основных (ионообменных) химических реакциях или электрону в окислительно-восстановительных реакциях.
Закон сохранения массы:
Закон сохранения массы — закон физики, согласно которому масса физической системы сохраняется при всех природных и искусственных процессах.
В метафизической форме, согласно которой вещество несотворимо и неуничтожимо, этот закон известен с древнейших времён. Позднее появилась количественная формулировка, согласно которой мерой количества вещества является вес (с конца XVII века — масса).
С точки зрения классической механики и химии, сохраняются общая масса закрытой физической системы, равная сумме масс компонентов этой системы (то есть масса считается аддитивной). Этот закон с большой точностью верен в области применимости ньютоновской механики и химии, так как релятивистские поправки в этих случаях пренебрежимо малы.
В современной физике концепция и свойства массы существенно пересмотрены. Масса более не является мерой количества вещества, а закон сохранения массы тесно связан с законом сохранения внутренней энергии системы. В отличие от классической модели, сохраняется масса только изолированной физической системы, то есть при отсутствии энергообмена с внешней средой. Не сохраняется сумма масс компонентов системы (масса неаддитивна). Например, при радиоактивном распаде в изолированной системе, состоящей из вещества и радиации, совокупная масса вещества уменьшается, но масса системы сохраняется, несмотря на то что масса радиации может быть нулевая.
Закон эквивалентов:
все вещества реагируют и образуются в эквивалентных отношениях.
формула, выражающая Закон эквивалентов: m1Э2=m2Э1
Закон кратных отношений:
Если два элемента образуют между собой несколько молекулярных соединений, то масса одного элемента, приходящаяся на одну и ту же массу другого, относятся между собой как небольшие целые числа.
Закон Бойля-Мариотта:
Закон Бойля-Мариотта отражает взаимосвязь между давлением р и объемом V определенного количества газа при постоянной температуре: при постоянной температуре давление, производимое данной массой газа, обратно пропорционально объему газа:
pV = const.
Другими словами, при переходе газа из состояния с параметрами р1 и V1 в состояние с параметрами р2 и V2 (при Т, п = const) выполняется условие:
p1V1=p2V2.
Закон Гей-Люссака:
Закон Гей-Люссака связывает объем газа V с его температурой Т (при р = const): при постоянном давлении объем газа изменяется прямо пропорционально абсолютной температуре:
![]()
При расчетах обычно используется соотношение
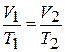
показывающее постоянство отношения объема к температуре при переходе из состояния 1 в состояние 2.
Закон Авогадро:
Закон Авогадро — закон, согласно которому в равных объёмах различных газов, взятых при одинаковых температурах и давлениях, содержится одно и то же число молекул.
Уравнение Клапейрона: !!!!!
Уравнение Менделеева-Клапейрона:
Парциальное давление газа в смеси:
Парциальное давление— давление отдельно взятого компонента газовой смеси. Общее давление газовой смеси является суммой парциальных давлений её компонентов.
Парциальное давление газа, растворённого в жидкости, является парциальным давлением того газа, который образовался бы в фазе газообразования в состоянии равновесия с жидкостью при той же температуре. Парциальное давление газа измеряется как термодинамическая активность молекул газа. Газы всегда будут вытекать из области с высоким парциальным давлением в область с более низким давлением; и чем больше разница, тем быстрее будет поток. Газы растворяются, диффундируют и реагируют соответственно их парциальному давлению и не обязательно зависимы от концентрации в газовой смеси.
Закон парциальных давлений:
Парциальное давление идеального газа в смеси равно давлению, которое будет оказываться, если бы он занимал тот же объём, что и вся смесь газов, при той же температуре. Причина этого в том, что между молекулами идеального газа не действуют силы притяжения или отталкивания, их соударения между собой и со стенками сосуда абсолютно упруги, а время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями. Реально существующие газы очень близко подходят к этому идеалу. Следствием этого является то, что общее давление смеси идеальных газов равно сумме парциальных давлений каждого газа в смеси, как это формулирует закон Дальтона[3]. Например, дана смесь идеального газа из азота (N2), водорода (H2) и аммиака (NH3):
P = P N2 + PH2 + PNH3, где:
P = общему давлению в газовой смеси
PN2 = парциальному давлению азота (N2)
PH2 = парциальному давлению водорода (H2)
PNH3 = парциальному давлению аммиака (NH3)
Основные классы неорганических соединений. Номенклатура. Характерные свойства.
Основными классами неорганических соединений являются оксиды, кислоты, соли и основания.
Оксиды представляют собой соединения элементов с кислородом. Оксиды подразделяют на солеобразующие и несолеобразующие. Солеобразующие оксиды делят на основные (образуют соли с кислотами), кислотные (образуют соли с основаниями) и амфотерные (образуют соли как с кислотами, так и с основаниями). Основным оксидам отвечают основания, кислотным – кислоты, а амфотерным – гидраты, которые проявляют как кислотные, так и амфотерные свойства. Кислотные оксиды представляют собой ангидриды кислот (SO2 – серный ангидрид, N2O5 – азотный ангидрид).
Примеры: N2O, NO – несолеобразующие оксиды; SO3, SiO2 – кислотные оксиды; СаО, МgО – основные оксиды и т.д.
В настоящее время общепринятой является международная номенклатура оксидов. Согласно международной номенклатуре в названии оксида указывается валентность элемента: СuO и Cu2O – оксиды меди [II] и [III] соответственно. Существует также русская номенклатура, согласно которой окисью называется единственно возможный оксид элемента, в остальных случаях название дается в соответствии с числом атомов кислорода. Оксиды, в которых элемент проявляет низшую валентность, называются закисями.
Примеры: MgO – окись магния; NiO – одноокись никеля; Ni2O3 – полутораокись никеля; Сu2О – полуокись меди.
Пероксиды (перекиси) металлов являются солями перекиси водорода Н2О2 и лишь формально относятся к оксидам. Приставка пер в названии соединений обычно указывает на принадлежность соединения к перекисным, но существуют исключения: соли кислот НMnO4 (перманганаты) и НСlO4 (перхлораты) перекисными не являются, а приставка пер в названии этих соединений указывает на максимальную насыщенность соединений кислородом.
Гидроксиды (основания) классифицируют по их силе (сильные – все щелочи кроме NH4OH и слабые), а также по растворимости в воде (растворимые – щелочи и нерастворимые). Важнейшими щелочами являются КОН (едкое кали) и NaOH (едкий натр).
В состав кислот входит водород, способный замещаться металлом, а также кислотный остаток. Коэффициент х, отвечающий количеству атомов водорода, а, следовательно, равный валентности кислотного остатка, называют основностью кислоты. Кислоты классифицируют по их силе (H2SO4, HNO3 – сильные кислоты; HCN – слабая кислота), на кислородсодержащие (H2SO4, HNO3) и бескислородные (HCN, HI); а также по основности (х) – HCN – одноосновная кислота, H2SO3 – двухосновная кислота, H3РO4 – трехосновная кислота. Важнейшим свойством кислот является их способность образовывать соли с основаниями. Названия кислот образуют от того элемента, которым образована кислота, при этом названия бескислородных кислот оканчивается словом водород (HCN –циановодород или синильная кислота). Названия кислородсодержащих кислот образуют от того элемента, которым образована кислота, с добавлением слова кислота (H3AsO4 – мышьяковая кислота, H2CrO4 – хромовая кислота). В случаях, когда один элемент образует несколько кислот различие между кислотами проявляют в окончаниях названий (на ная или овая оканчиваются названия тех кислот, в которых элемент проявляет наивысшую валентность; на истая или овистая оканчиваются названия тех кислот, в которых элемент проявляет валентность ниже максимальной).
Примеры: HNO3 – азотная кислота, а HNO2 – азотистая кислота; H3AsO4 – мышьяковая кислота, а H3AsO3 – мышьяковистая кислота.
Одному и тому же оксиду могут соответствовать несколько кислот, при этом наиболее богатая водой форма имеет в названии приставку орто, а наименее богатая – мета (ортофосфорная кислота H3РO4 – на одну молекулу ангидрида Р2О5 приходится три молекулы воды; метафосфорная кислота HРO3 – на одну молекулу ангидрида Р2О5 приходится одна молекула воды). Следует также учитывать и то, что ряд кислот имеют исторически сложившиеся названия.
Соли являются продуктом замещения водорода в кислоте на металл или гидроксогрупп в основании на кислотный остаток. Нормальные (средние) соли получаются при полном замещении; кислые – при неполном замещении водорода кислоты на металл; основные – при неполном замещении гидроксогрупп основания на кислотный остаток. Кислая соль может быть образована только кислотой, основность которой 2 и более, а основная – металлом, заряд которого 2 и более.
Примеры: NaHS, KHCO3 – кислые соли (гидросульфид натрия и гидрокарбонат натрия); MgOHCl, CaOHCl – основные соли (хлориды гидроксо магния и кальция); NaCl, CuS – нормальные соли (хлорид натрия и сульфид меди).
