
- •Растворы электролитов и ионные равновесия Учебно-практическое пособие
- •1. Электролитическая диссоциация
- •1.1. Механизм электролитической диссоциации ионных веществ
- •1.2. Механизм электролитической диссоциации сильно полярных веществ в сильнополярных растворителях
- •1.3. Растворы электролитов
- •1.4. Степень и константа электролитической диссоциации
- •2. Равновесие в растворах слабых электролитов
- •Константы диссоциации некоторых слабых электролитов в водных растворах при 25 0с
- •2.1. Влияние общего иона и противоиона на равновесие
- •2.2. Взаимосвязь константы и степени электролитической диссоциации
- •3. Особенности растворов сильных электролитов. Ионная сила раствора
- •Коэффициенты активности ионов
- •4. Электролитическая диссоциация и ионное произведение воды
- •5. Водородный и гидроксильный показатели
- •Водородный показатель
- •Кислотность некоторых природных жидкостей
- •Методы определения рН растворов
- •Кислотно-основные индикаторы
- •6. Буферные растворы
- •7. Равновесия в растворах коодинационных (комплексных) соединений
- •8. Произведение растворимости и образование осадков
- •8.1. Произведение растворимости
- •8.2. Образование осадков
- •Произведение растворимости (пр) и растворимость при 25 0с некоторых малорастворимых веществ
- •9. Физико–химические основы водно–электролитного баланса в организме
- •Баланс электролитов в организме
Коэффициенты активности ионов
Ионная сила раствора |
Заряд иона – z |
||
± 1 |
± 2 |
± 3 |
|
0,05 |
0,84 |
0,50 |
0,21 |
0,1 |
0,81 |
0,44 |
0,16 |
0,2 |
0,80 |
0,41 |
0,14 |
0,3 |
0,81 |
0,42 |
0,14 |
0,4 |
0,82 |
0,45 |
0,17 |
0,5 |
0,84 |
0,50 |
0,21 |
* * *
В биологических системах широко распространены межионные взаимодействия, которые сильно зависят от ионной силы растворов, что прежде всего сказывается на значениях констант диссоциации ионогенных* групп биологических субстратов, так как они определяются активностями ионов, а не их концентрациями. Незначительное увеличение ионной силы раствора вызывает изменение степени ионизированности белков или нуклеиновых кислот, вследствие чего меняется их конформация, а следовательно, и биологические функции. Поэтому при использовании растворов электролитов в биологических экспериментах крайне необходимо, чтобы их ионная сила была равна ионной силе соответствующей биологической системы. Так, ионная сила плазмы крови человека равна 0,15 моль/л, поэтому физиологический раствор – простейший заменитель плазмы крови – должен иметь соответствующую концентрацию NaCl (0,15 моль/л, или 0,9 %).
Таким образом, ионная сила биологических систем, обусловленная содержанием в них сильных электролитов, влияет не только на химическую активность ионов, но и на биологическую функцию белков и нуклеиновых кислот, содержащихся в этих системах, что имеет большое значение в практической медицине.
При значительном увеличении ионной силы раствора в нём уменьшается количество свободной воды, не участвующей в гидратации ионов. Другими словами, уменьшается активность воды, участвующей в процессе гидратации растворённых частиц. Это обстоятельство чрезвычайно важно для биологических систем, так как оно приводит к дегидратации природных полиэлектролитов (белков и нуклеиновых кислот), в результате чего вначале изменяется их конформация, а затем происходит даже их высаливание**, то есть выделение белков и нуклеиновых кислот из этих растворов.
Влияние ионной силы раствора на растворимость полиэлектролитов имеет большое значение при проведении биохимического эксперимента. Добавление к биологическим жидкостям солей позволяет не только выделить белки и нуклеиновые кислоты, но и фракционировать их по молекулярной массе. При постепенном увеличении ионной силы раствора из него вначале выделяются полиэлектролиты с большей молекулярной массой и меньшей гидрофильностью. Для выделения полиэлектролитов с меньшей молекулярной массой и с большей гидрофильностью требуется создать в растворе более высокую ионную силу.
При выделении природных полимеров из биологических сред наибольшее высаливающее действие проявляют анионы солей, так как структура их гидратной оболочки ближе к структуре гидратной оболочки белков и нуклеиновых кислот, чем катионов. Чем больше заряд аниона и меньше его размер, тем сильнее он гидратируется и тем выше его дегидратирующая способность по отношению к полиэлектролитам. По высаливающему действию анионы могут быть расположены в следующий ряд:
I– < Br– < Сl– NО3– SO42– C2O42–*
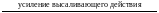
В практике для выделения белков обычно используют сульфат аммония (NH4)2SO4. Например, для выделения из крови фибриногена (М = 340 000) требуется ионная сила 2,9, гемоглобина (М = 64 450) – 5,8, а миоглобина (М = 17 800) – 9,6.
