
- •Термодинамикалық жүйе және жұмыс денесі. Термодинамикалық параметрлер және күй теңдеуі.
- •1 Моль газ үшін Менделеев-Клапейрон теңдеуі
- •Тепе-теңдік күй және процесс.
- •Ішкі энергия күй функциясы ретінде.
- •Термодинамикадағы жұмыс. Жылу.
- •Термодинамиканың бірінші бастамасының теңдеуі.
- •Жылусыйымдылық түсінігі. Ағындар үшін термодинамиканың бірінші бастамасы. Ағындар жұмысының түрлері.
- •Идеал газдардың термодинамикалық процестері .
- •Идеал газ заңдары
- •Идеал газдар қоспасы
- •Идеал газдың негізгі термодинамикалық процестері, процестердің жұмысы және жылуы, идеал газ күйіндегі заттың калориялық қасиетінің өзгеруін анықтау.
- •Термодинамиканың екінші бастамасы
- •Қайтымды Карно циклі, жылулық пәк
- •Карно теоремасы. Еркін қайтымды цикл, энтропияны күй функциясы ретінде түсіну
- •Еркін қайтымды цикл
- •Қайтымды және қайтымсыз процестердегі энтропияның өзгеруі
- •Оқшауланған термодинамикалық жүйенің тепе-теңдік шарты
- •Күйдің термодинамикалық ықтималдығы
- •Вандер-Ваальс изотермасы және теңдеуі.
- •Нақты заттардың рT-, рv-диаграммасы, күй теңдеуі мен жылулық коэффициенттер және кестелер.
- •Сәулелік ағындардың қасиеті және сәуле бөлетін денелер жүйесінің геометриялық
Термодинамикалық жүйе және жұмыс денесі. Термодинамикалық параметрлер және күй теңдеуі.
Термодинамикалық жүйе деп бір бірімен және жүйені қоршаған сыртқы денелермен (сыртқы ортамен) механикалық және жылулық әрекеттестікте болатын материалдық денелер жиынтығын айтамыз. Жүйеге кірмейтін денелерді қоршаған орта деп атайды. Жүйені қоршаған ортадан бақылайтын қабықпен бөледі. Жалпы тұрғыдан алғанда жүйе ортамен затпен де алмасуы мүмкін. Мұндай жүйені ашық деп атайды. Егер зат жүйенің шекарасы арқылы өтпейтін болса, онда жүйе жабық деп аталады. Қоршаған ортамен жылу алмасу мүмкіндігі жоқ жүйені жылу изоляцияланған немесе адиабаталық деп атайды. Қоршаған ортамен энергиямен де, затпен де алмаспайтын жүйені оңашаланған жүйе деп атайды. Жылуды жұмысқа немесе жұмысты жылуға түрлендіруді іске асыратын жұмысшы дене қарапайым термодинамикалық жүйе бола алады. Мысалы іштен жанатын қозғағышта жұмысшы дене ретінде карбюраторда дайындалған ауа мен бензин буынан тұратын жанғыш қоспа қолданылады.
Жүйенің
қасиеттерін сипаттайтын шамаларды
термодинамикалық параметрлер деп
атайды. Негізгі термодинамикалық күй
параметрлері р,v және Т бір бірімен
өзара байланыста болып, мынадай
математикалық теңдеу арқылы анықталады:
F(v,p,T)=0. Қысым жұмысшы дене молекулаларының
ыдыс бетімен әрекеттесуінің нәтижесімен
түсіндіріледі. МКТ бойынша қысым мына
қатынаспен анықталады
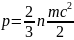 .
Бірліктердің халықаралық жүйесінде
қысым паскальмен өлшенеді. Қысымды
манометрдің, барометрдің, вакуумметрдің
көмегімен өлшенеді. Температура дененің
қызғандығының немес қызбағандығының
дәрежесін сипаттайтын физикалық шама.
МКТ бойынша температура молекулалардың
жылулық қозғалысының интенсивтілігін
сипаттайтын шама. БХЖ бойынша
температураның өлшем бірлігі Кельвин.
Меншікті көлем- зат массасы бірлігінің
көлемі. Егер массасы М біртекті дене
көлемде V
орналасса,
онда анықтама бойынша
.
Бірліктердің халықаралық жүйесінде
қысым паскальмен өлшенеді. Қысымды
манометрдің, барометрдің, вакуумметрдің
көмегімен өлшенеді. Температура дененің
қызғандығының немес қызбағандығының
дәрежесін сипаттайтын физикалық шама.
МКТ бойынша температура молекулалардың
жылулық қозғалысының интенсивтілігін
сипаттайтын шама. БХЖ бойынша
температураның өлшем бірлігі Кельвин.
Меншікті көлем- зат массасы бірлігінің
көлемі. Егер массасы М біртекті дене
көлемде V
орналасса,
онда анықтама бойынша
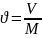 .
БХЖ бойынша меншікті көлемнің өлшем
бірлігі м3/кг.
.
БХЖ бойынша меншікті көлемнің өлшем
бірлігі м3/кг.
Тепе
теңдіктегі термодинамикалық жүйенің
күй параметрлерінің арасында функционалдық
байланыс бар. Осындай байланысты күй
теңдеуі деп атайды. Қарапайым жүйелердің
меншікті көлемі, температурасы және
қысымы термиялық күй теңдеуімен
байланысқанын тәжірибе көрсетті
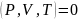 .
Күй теңдеуін басқаша жазуға болады:
.
Күй теңдеуін басқаша жазуға болады:
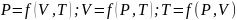
Газдың
еркін массасы М үшін күй теңдеуі
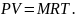
1 Моль газ үшін Менделеев-Клапейрон теңдеуі
Ван-дер-Ваальс
теңдеуі:
 .
.
Тепе-теңдік күй және процесс.
Егер термодинамикалық параметрлердің бәрі уақыт өткен сайын өзгермесе және жүйе нүктелерінің бәрінде бірдей болса, онда жүйенің мұндай күйін тепе-теңдік күй деп атайды. Егер жүйенің әр түрлі нүктелерінің арасында температураның, қысымның және басқа параметрлердің айырымдары болса, онда жүйе тепе-теңдік емес күйде деп түсіну керек. Тепе-тең процесс – термодинамикалық жүйенің бір тепе-тең күйден екінші күйге шексіз баяу ауысуы. Мұндай кезде жүйенің кез келген кезеңдегі физикалық күйінің тепе-тең күйден шексіз аз айырмашылығы ғана болады. Тепе-тең процесс кезінде жүйедегі тепе-теңдік, жүйенің физикалық параметрлерінде болатын өзгерістерге қарағанда, әлдеқайда жылдам орнайды. Кез келген тепе- тең процесс – қайтымды процесс. Тепе-тең процесс термодинамикада үлкен рөл атқарады. Өйткені, құрамына тепе-тең процесс енетін термодинамикалық циклдер ғана ең көп жұмыс өндіреді. “ Тепе-тең процесс” терминін неміс математигі К.Каратеодори (1873 – 1950) ұсынған (1909).
Термодинамиканың негізгі заңдары.
Термодинамика - физика ғылымындағы жылудың жұмыс және басқа энергия түрлерімен арадағы қарым-қатынасын зерттейтін тармағы.
Термодинамиканың
бірінші бастамасы — термодинамикалық
жүйелер
үшін энергияның
сақталу заңы;
бұл заң бойынша жүйеге берілетін жылу
оның ішкі энергиясын өзгертуге
және жүйенің сыртқы күштерге қарсы
жұмысына жұмсалады.
![]()
Термодинамиканың екінші бастамасы) — статистикалық нысандардың (мысалы, атомбеидардың, молекулалардың) үлкен санынан тұратын жүйелердің өз бетінше ықтималдығы аздау күйден ықтималдығы молырақ күйге ауысу процесін сипаттайтын табиғаттың түбегейлі заңы.
Термодинамиканың үшінші бастамасы — абсолюттік нөлге жуық температура маңында, реакцияның жылу эффектісі мен максимал жұмыстысипаттайтын қисық сызықтар өзара бірігіп кетеді, ал олардың ортақ жанамасы температуа осіне параллель болады дейтін, химиялық реакцияларға тән эксперименттік нәтижелерді қорытындылаудан туатын постулат.
Термодинамиканың бірінші бастамасы .
Термодинамиканың бірінші бастамасы — термодинамикалық жүйелер үшін энергияның сақталу заңы; бұл заң бойынша жүйеге берілетін жылу оның ішкі энергиясын өзгертуге және жүйенің сыртқы күштерге қарсы жұмысына жұмсалады.
Дене
күйінің барлық энергиясы -
микроскопиялық қозғалысының толық
түріндегі сыртқы кинетикалық
энергиясы Ек және
салмақ күші өрісі, электрлі немесе
магнит өрісі жағдайындағы потенциалды
энергия Еn,
сонымен қатар, дене бөлшектерінің
құрамдық әрекеттері мен қозғалу
энергиясын жасаушы ішкі энергия U
қосындыларынан тұрады:
![]()
Сыртқы
ортамен әрекеттестігі жоқ болғандағы
кезінде (dQ=0 және dL=0), формуладағы dU=0,
яғни жүйе энергиясы өзгеріссіз сақталады.
Жүйелер қатнасының жекеленген жылулығы
үшін, ондағы dQ=0 екені белгілі.![]()
