Глава 7. Механизмы транспорта ксенобиотиков
Физиологическая активность ксенобиотиков, как мы видим, в значительной степени зависит от способности взаимодействовать с клеточными мембранами; не менее важное значение имеет их способность проникать внутрь клетки.
При рассмотрении основных механизмов переноса веществ через биологические мембраны различают пассивный (простая и облегченная диффузия) и активный (выполняемый молекулярными машинами (АТФазы), редокс-цепями и осуществляемый за счет сопряжения электрохимических градиентов переносимых веществ) транспорт.
7.1. Пассивный транспорт
При простой диффузии ксенобиотики проходят через мембрану в результате случайного молекулярного движения, и величина потока линейно зависит от концентрации и коэффициента проницаемости мембраны для данного вещества.
Биологические мембраны, как известно, представляют собой мозаичную структуру, состоящую из липидов, структурных белков, белков-ферментов и других компонентов. «Сердцевина» мембраны представляет собой в основном гидрофобную область, поэтому неполярные вещества сравнительно легко проникают в клетки. Гидрофобные группы способствуют увеличению проникающей способности, полярные – ее уменьшению.
Так, например, пропиловый спирт проникает в эритроциты в 3 раза быстрее, бутиловый в 10 раз быстрее, чем этиловый. С другой стороны, проникающая способность бутанола резко уменьшается при введении в его молекулу дополнительных полярных ОН-групп.
Различие в проницаемости зависит от скорости диффузии через мембрану, причем уменьшение скорости диффузии для разветвленной углеводородной цепи обусловлено стерическими факторами. Проницаемость неэлектролитов зависит также и от липидного состава мембраны.
В качестве количественного параметра проникновения любого вещества в клетку вводится коэффициент проницаемости. В этом случае скорость переноса определяют с помощью закона Фика:
1 dS (Cн – Cв)
–– ––– = –DKр –––––––––, (7.1)
A dt x
где D – коэффициент диффузии; А – площадь поверхности; Cн, Cв – концентрация снаружи и внутри соответственно; Кр – коэффициент распределения, представляющий отношение концентрации растворенного вещества в мембране к концентрации вне мембраны; x – расстояние, преодолеваемое соединением при прохождении через мембрану.
Так как молекуле, возможно, приходится преодолевать путь x, не обязательно равный толщине мембраны, то этот путь трудно измерить непосредственно. Коэффициент распределения обычно определяют, используя в качестве липидной фазы оливковое масло, а не истинные липиды, что вводит некоторую неопределенность в величину К. Зависимость D от x также неизвестна ни для какой мембраны. Поэтому Р = DKр/x (коэффициент проницаемости) является единственной измеряемой величиной, характеризующей мембрану и переносимое растворенное вещество, которую легко вычислить, используя выражение:
dS/dt = PA(Cн – Cв) , (7.2)
где размерность Р – длина в единицу времени (т. е. скорость), см/с.
Во всех случаях прохождения растворенных веществ через плазматическую мембрану обнаруживается тесная связь между проницаемостью и коэффициентом распределения для системы масло–вода. Чем выше липофильность вещества, тем выше коэффициент распределения.
Для различных веществ способность проникать через мембрану определяется, как уже отмечалось, и коэффициентом распределения. Отношение концентраций какого-либо вещества, состоящего из простых молекул, в двух находящихся в равновесии фазах имеет постоянное значение и называется константой распределения Кр:
Кр = С2/С1, (7.3)
где С1 – водная фаза, С2 – неводная фаза (масло, липид).
Это соотношение получено в предположении, что в системе нет заметных взаимодействий между молекулами растворенного вещества или сильных специфических взаимодействий между растворенным веществом и растворителем, которые могли бы повлиять на процесс распределения.
Коэффициент распределения некоторого вещества зависит от способности его молекул к образованию водородных связей. Кроме того, для соединений с одинаковым коэффициентом распределения в системе липид–вода скорость диффузии через мембрану может значительно варьировать в зависимости от пространственной структуры молекул.
Пассивный перенос – это движение вещества по градиенту электрохимического потенциала без затраты энергии, т. е. движущей силой пассивного транспорта веществ служит градиент электрохимического потенциала. Электрохимический потенциал () характеризуется свободной энергией некоторого вещества j.
Химический потенциал, так же как и другие виды потенциальной энергии, является относительной величиной, т. е. он определяется каким-то условным уровнем энергии (вводится константа аддитивности или стандартный член *):
j = j* + RTlnCj + ZjF. (7.4)
В случае переноса через мембрану незаряженных частиц уравнение (5.4) упрощается и химический потенциал вещества можно выразить как функцию его концентрации (точнее активности):
j = j* + RTlnCj . (7.5)
Здесь j – энергия на единицу количества вещества (Дж/моль); Cj – концентрация вещества; Zj – заряд; – электрический потенциал; R – газовая постоянная; Т – абсолютная температура.
Фактор RT, на который умножается величина lnCj, необходим для перевода активности в единицы энергии на 1 моль.
Если рассмотреть систему в состоянии равновесия, когда электрохимический потенциал вещества одинаков по обеим сторонам мембраны, то:
jв = jн . (7.6)
В этом случае нет градиента электрохимического потенциала и никакая движущая сила не действует на переносимый ксенобиотик; он проходит в результате беспорядочного теплового движения, но при этом два противоположно направленных потока сбалансированы. В этом случае
RTlnCjн + ZjFн = RTlnCjв + ZjFв , (7.7)
и соотношение для разности электрических потенциалов (р = в–н) будет иметь вид:
RT Cjн
р = ln . (7.8)
ZjF Cjв
Величину р называют потенциалом Нернста. Экспериментально измерив мембранный потенциал и концентрацию ионов по обе стороны мембраны, на основании выражения (7.8) можно предсказать направление пассивного переноса ксенобиотика.
Проницаемость мембран для некоторых малых молекул оказывается более высокой, чем это можно было бы ожидать на основании данных об их растворимости в липидах. В частности, хорошо проникают через мембраны такие гидрофильные вещества, как глицерин, мочевина и др., радиус молекул которых не превышает 0,3 нм. Предполагают, что эти молекулы проходят через особые участки мембраны, так называемые «поры» (каналы). Аналогично считают, что заряженные частицы (ионы) движутся через ионные каналы.
Через ионные каналы осуществляется не только транспорт веществ, они также непосредственно участвуют в передаче сигнала возбудимым клеткам (генерация потенциала действия). Существуют хемовозбудимые (рецепторы ацетилхолина, -АМК, глутамата, глицина и др.) и электровозбудимые (натриевые, калиевые, хлорные и др.) каналы.
Довольно подробно изучены ацетилхолиновый, натриевый и другие каналы мембран различных клеток. Схематическое строение одиночного ионного канала представлено на рис. 7.1.
|
Рис. 7.1. Схема строения потенциалуправляемого ионного канала |
Канал – это белковая макромолекула, субъединицы которой образуют в мембране пору через бислой липидов. В поре имеется узкий селективный фильтр вблизи наружной поверхности мембраны и воротное устройство вблизи ее внутренней поверхности. Пространство между селективным фильтром и воротами получило название туннеля. Сенсор напряжения, расположенный в липидном слое, управляет открытием ворот под влиянием внутримембранного поля. Расширенные части канала у наружной и внутренней поверхности образуют устья (или вестибюли).
Облегченная диффузия. Вещества, нерастворимые в липидах, с размером молекулы более 0,3–0,4 нм, не диффундируют через мембраны. Так, шестиатомные спирты с диаметром молекул 0,42 нм не проникают в большинство клеток. Однако глюкоза и некоторые другие моносахариды с такими же размерами молекул, как правило, хорошо проникают в клетку. Для объяснения высокой проницаемости клеточных мембран по отношению к сахарам, аминокислотам и некоторым другим соединениям была выдвинута концепция «переносчиков», связывающихся с транспортируемым веществом и таким образом «облегчающих» их прохождение через мембрану. Такая облегченная диффузия происходит по градиенту концентрации без затрат энергии и относится к пассивному транспорту.
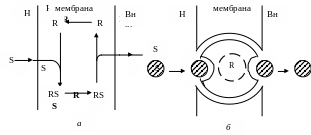
В основе механизма облегченной диффузии лежит обратимое соединение транспортируемого вещества со специфическим переносчиком, и образующийся комплекс вещество–переносчик диффундирует внутри мембраны от наружной поверхности к внутренней, где комплекс диссоциирует с высвобождением вещества внутрь клетки. Свободный же переносчик диффундирует назад к наружной поверхности мембраны, где соединяется с новой молекулой вещества, и цикл повторяется (рис. 7.2, а, б).
|
Рис. 7.2. Схема транспорта веществ с участием подвижного (а) и фиксированного (б) переносчиков |
Развивается также тетрамерная модель облегченного переноса. Согласно этой модели транспорт осуществляется не в результате присоединения переносимого субстрата к подвижному переносчику, а путем «внутреннего» переноса субстрата через белковый тетрамер, встроенный в мембрану (фиксированный переносчик). Тетрамер состоит из симметрично расположенных субъединиц, две из которых характеризуются высоким сродством к субстрату, а две – низким. Тетрамер может существовать в одной из двух энергетически эквивалентных конформаций, переход между которыми происходит только в том случае, когда молекула субстрата присоединяется к одной из субъединиц. Этот конформационный переход и является непосредственной причиной переноса субстрата через мембрану (рис. 7.2, б).
Можно отметить ряд характерных отличий между облегченной и простой диффузией.
1. При простой диффузии поток вещества пропорционален внешней концентрации и все время возрастает с увеличением последней. При облегченной диффузии кривая, описывающая поток веществ через мембрану, стремится к насыщению при концентрациях, обеспечивающих связывание всех молекул переносчика.
2. Наличие специфических переносчиков, взаимодействующих с веществами определенного строения, обусловливает резко выраженную зависимость проникающей способности вещества от его химической структуры и, в частности, от пространственной конфигурации его молекул.
3. Облегченная диффузия, в отличие от простой, может ингибироваться некоторыми соединениями (иногда в весьма малых концентрациях), которые блокируют переносчик.
Процесс переноса веществ через мембраны с помощью переносчика описывается в рамках кинетики Михаэлиса – Ментен (рис. 7.3).
|
Рис. 7.3. Соотношение между концентрацией растворенного вещества в наружной среде и скоростью поступления внутрь (кинетика Михаэлиса–Ментен) |
Скорость переноса пропорциональна концентрации вещества в интервале низких концентраций, а затем снижается по мере ее роста и в конце концов приближается к максимуму (происходит насыщение) (рис. 7.3.), поток вещества, например, внутрь клетки Фjв, в этом случае описывается соотношением:
С![]() Ф
Ф![]()
Фjвн = , (7.9)
Кj
+ С![]()
где Ф – максимальная скорость переноса; j-ксенобиотика; Кj – константа, характеризующая сродство вещества к переносчику; С – концентрация веществ в наружной среде.
При Кj = Сj поток становится равен половине максимального потока. Поэтому и графическое определение константы сводится к определению полумаксимальной величины потока и экстраполяции на точки пересечения оси абсцисс (см. рис. 7.3): чем ниже величина Кj, тем выше сродство транспортируемого вещества к переносчику.
В плазматических мембранах многих животных клеток существуют, как минимум, пять различных белков-переносчиков аминокислот, которые действуют как системы симпорта, перенося одновременно ионы Na+, причем каждый из этих белков специфичен для группы родственных аминокислот. Градиент концентрации Na+ может также приводить в действие системы антипорта. Например, в оплодотворенном яйце морского ежа значительное повышение внутриклеточного рН активирует синтез белков и ДНК; это изменение рН вызывается потоком Н+ из клетки, возникающим благодаря потоку Na+ в клетку.
У бактерий и растительных клеток большинство систем активного транспорта, приводящихся в действие ионными градиентами, используют в качестве котранспортируемого ион Н+, а не Na+. Например, хорошо изучен трансмембранный белок-переносчик лактозы (пермеаза или М-белок), функционирующий в бактериальной мембране. Белок состоит из одной полипептидной цепи (30 000 дальтон) и осуществляет Н+-зависимый симпорт: с каждой транспортируемой в клетку молекулой лактозы переносится один протон. Не исключено и наличие переносчиков определенных видов ксенобиотиков.
Для регуляции переноса веществ используются ионофоры. Ионофоры – это небольшие гидрофобные молекулы, которые растворяются в липидных бислоях и повышают их проницаемость для ионов. Большинство ионофоров синтезируется микроорганизмами (вероятно, в качестве биологического оружия против своих конкурентов); некоторые из них используются как антибиотики. Ионофоры широко применяются для повышения проницаемости мембран по отношению к определенным ионам. Существуют два класса ионофоров – подвижные переносчики ионов и каналообразующие ионофоры. Ионофоры обоих типов действуют, экранируя заряд транспортируемого иона так, чтобы последний мог пройти гидрофобную внутреннюю область липидного бислоя. Поскольку ионофоры не связаны ни с каким источником энергии, они лишь позволяют ионам двигаться по электрохимическим градиентам.
Примером каналообразующего ионофора является грамицидин А. Он представляет собой линейный пептид, состоящий из 15 аминокислот; все они имеют гидрофобные боковые цепи. Вероятно, в бислое две молекулы грамицидина объединяются и образуют трансмембранный канал, позволяющий моновалентным катионам передвигаться по электрохимическим градиентам. При наличии большого электрохимического градиента грамицидин А может пропустить 2107 катионов в расчете на один открытый канал за 1 с, что в 1000 раз больше, чем может перенести за это же время одна молекула подвижного переносчика.
В расчете на один открытый канал за 1 с, что в 1000 раз больше, чем может перенести за это же время одна молекула подвижного переносчика.
Подвижный переносчик (ионофор) валиномицин осуществляет перенос ионов калия через мембраны. Он представляет собой полимер и имеет кольцеобразную структуру. Наружная гидрофобная часть его молекулы состоит из боковых цепей валина и контактирует с углеводородной сердцевиной липидного бислоя. Во внутренней полярной области как раз может поместиться один ион калия ( рис. 7.4).

Валиномицин переносит ионы калия по его электрохимическому градиенту ; он захватывает этот ион с одной стороны мембраны, диффундирует с ним через бислой и высвобождает на его на другой стороне. Такой перенос совершается в обоих направлениях, поэтому суммарный эффект будет иметь место только в том случае, если при движении переносчика в каком-то одном направлении с ним будет связываться больше ионов калия, чем при движении в другом.